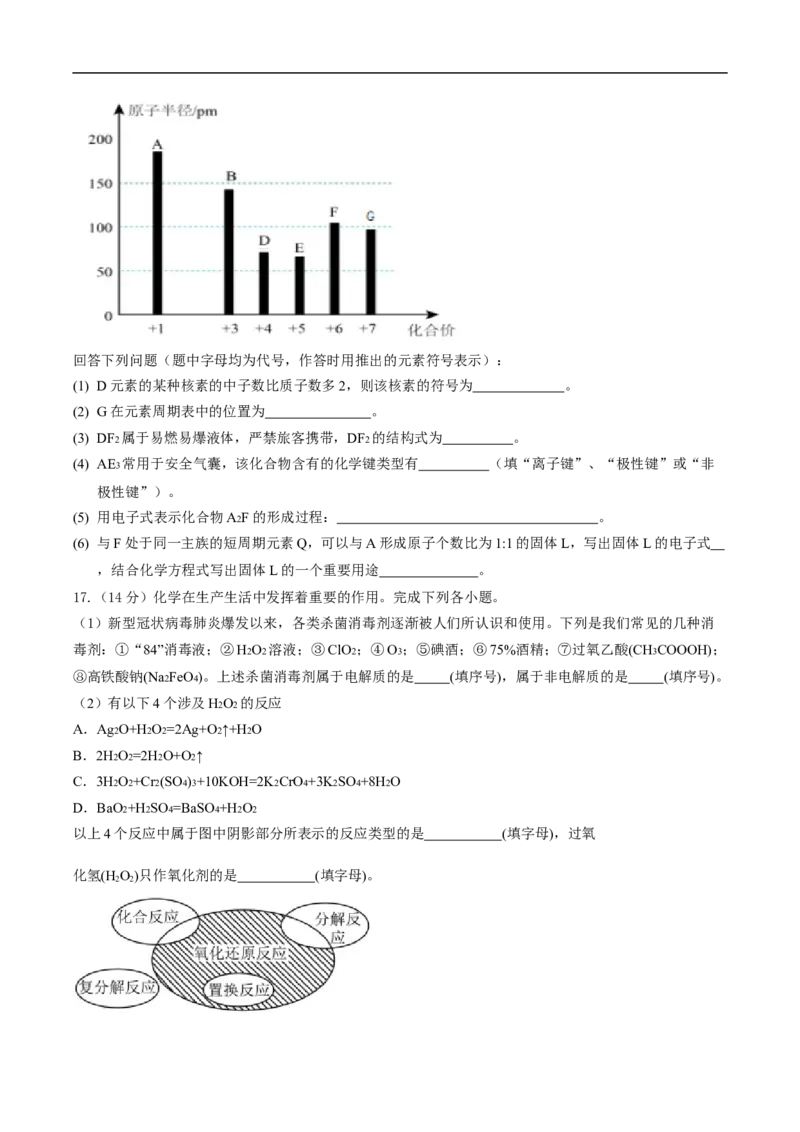
文档内容
2024-2025 学年度(上)沈阳市五校协作体期末考试
高一年级化学试卷
时间:75分钟 分数:100分
试卷说明:试卷共两部分:第一部分:选择题型(1-15题45分)
第二部分:非选择题型(16-19题 55分)
可能用到的相对原子质量:H—1 C—12 N—14 O—16 Na—23 Mg—24 Al—27 S—32
Cl—35.5 Ar—40 Fe—56
第Ⅰ卷(选择题 共 45 分)
每小题只有一个选项符合题目要求,每小题3分。
1.金属及其化合物以及金属材料对于促进生产发展、改善人类生活发挥了巨大作用。下列说法正确的是
A.铝热反应可用于焊接钢轨或冶炼锰、铬等难熔金属,都要用到的反应物是氧化铝
B.铁是人体必需的微量元素,缺铁性贫血患者可通过服用硫酸铁等补血剂,或多食用菠菜和鱼类等食品,
或食用铁强化酱油等方式补充Fe3+
C.储氢合金是一类能够大量吸收H,并与H 结合成金属氢化物的材料,可用于以H 为燃料的汽车
2 2 2
D.被称为“冶金工业的维生素”的稀土元素是镧系元素的15种以及钪和钇共17种元素,它们都位于元
素周期表的IB族
2.对物质进行分类是为了更好地认识物质的共性。下列关于物质分类正确的一组是
选 酸性氧化
电解质 碱 碱性氧化物
项 物
A 盐酸 纯碱 CO2 生石灰
B HI 氨水 SiO2 Al2O3
C 熔融KOH Fe(OH)3 CO MgO
D BaSO4 NaOH SO2 铁红
3.常温下,在给定环境中下列离子能大量共存的是
A.碱性溶液中:CO32- 、Na+ 、Cl- 、[Al(OH)4]-
B.碳酸钠溶液中:OH- 、Ca2+ 、NO3- 、Cl-C.含 的溶液: Na+ 、Fe3+ 、NO3- 、Cl-
D.加入铝粉能产生氢气的溶液:Mg2+ 、NO3- 、Fe2+ 、SO42-
4.下列化学用语表述正确的是
A.NaCl溶液中的水合离子:
B.NaHSO4 在水中的电离:NaHSO4=Na++H++SO42-
C.用电子式表示HCl的形成过程:
D.用双线桥表示电子转移的方向和数目:
5.物质间存在着转化关系。下列选项中的各步转化无法通过一步反应实现的是
A.Na → Na2O2 → Na2CO3 → NaCl → Na
B.Fe → FeCl3 →Fe(OH)3 → Fe2O3 → Fe
C.Al → Al2O3 → Al(OH)3 → AlCl3 → Al
D.Cl2 → NaClO → HClO → HCl → Cl2
6.下列情境下的离子方程式书写正确的是
A.汽车尾气处理:
B.漂白粉溶液中通入少量CO2 气体:ClO—+CO2+H2O=HClO+HCO3—
C.红热的铁与水蒸气反应:2Fe+3H2O(g) Fe2O3+3H2
D.家庭厨卫固体管道疏通剂疏通原理:2Al+2OH—+6H2O=2[Al(OH)4]—+3H2↑
7. 用NA 表示阿伏伽德罗常数的值。下列说法中正确的是
A.将 通入水中,溶液中 、 、HClO的数目之和等于2NA
B.等体积、等物质的量浓度的NaC1和KC1溶液中,阴、阳离子数目之和均为2NA
C.常温常压下92g的NO2 和N2O4 混合气体含有的氧原子数为4NA
D.将0.3mol钠、镁、铝分别投到1L 0.2mol/L的盐酸中,生成标准状况下气体分子
数均为0.1 NA8.W、X、Y、Z为原子序数依次增大的短周期元素。W和X原子序数之和等于Y— 的核外电子数,化合物
W+[ZY6]- 可用作化学电源的电解质。下列叙述正确的是
A.Z的氧化物对应的水化物是强酸
B.简单氢化物的沸点:Y>X>Z
C.简单氢化物的稳定性:Z >Y>X
D.X、Y分别与氢元素形成的二元化合物均为共价化合物
9.下列实验装置能达到实验目的的是
A.验证Na和水的反应是否为放热反应 B.制取Fe(OH)3 胶体
C.观察碳酸钠焰色试验的现象 D.制取纯净的Fe(OH) 沉淀
2
10.侯氏制碱法工艺流程中的主反应为QR+YW3+XZ2+W2Z=QWXZ3+YW4R,其中W、X、Y、Z、Q、R分
别代表相关化学元素。下列说法正确的是
A.热稳定性:QWXZ3>Q2XZ3
B.单质沸点: ZNaNO >I
4 2 2
19.(14分)(1)Al 、 (2) [Al(OH)4]- +CO2=Al(OH)3↓+ HCO3-
(3)
(4)100mL容量瓶 (没有100mL 0分)
(5)FeSO4·H2O 2FeSO4 Fe2O3+SO2↑+SO3↑