文档内容
高二选择性必修二(人教版2019)期末复习能力培优练习
(五)
一、单选题
1.4p轨道填充一半的元素,其原子序数是( )
A.15 B.33 C.35 D.51
2.下列说法不正确的是
A.干冰升华和液氯气化时,都只需克服分子间作用力
B.硫酸氢钠晶体溶于水,需要克服离子键和共价键
C.氯化氢气体溶于水时,只有共价键的断裂,没有化学键的形成
D.石墨转化金刚石,既有化学键的断裂,又有化学键的形成
3.下列说法正确的是
A.元素电负性由大到小的顺序:O>N>C
B.一个乙烯分子含2个π键和4个σ键
C.氯化钠和氯化铯晶体中氯离子的配位数相同
D.第一电离能的大小:Al>Mg>Na
4.下列过程中化学键没有被破坏的是( )
A.水→冰;干冰和I 的升华
2
B.NaOH、HCl、蔗糖溶于水
C.水电解得到氧气与氢气;NH HCO 中闻到了刺激性气味
4 3
D.金刚石加热融化;NaCl颗粒被粉碎
5.科学家最近研制出有望成为高效火箭推进剂的N(NO)(如图所示)。已知该分子中N
2 3
—N—N键角都是108.1°,下列有关N(NO) 的说法不正确的是( )
2 3
A.N(NO) 分子中既含极性键又含非极性键
2 3
B.分子中四个氮原子共平面
C.该物质既有氧化性又有还原性
D.15.2 g该物质含有6.02×1023个原子
6.在半导体生产或灭火剂的使用中,会向空气逸散气体如:NF 、CHClFCF 、C F,
3 3 3 8
它们虽是微量的,有些确是强温室气体,下列推测不正确的是( )
A.由价层电子对互斥理论可确定NF 分子呈三角锥形
3
试卷第1页,总1页B.C F 在CCl 中的溶解度比水中大
3 8 4
C.CHClFCF 存在手性异构
3
D.第一电离能:N<O<F
7.氯化硼的熔点为-107℃,沸点为12.5℃,其分子中键与键之间的夹角为120°,它能
水解,有关叙述不正确的是
A.氯化硼液态时能导电而固态时不导电
B.硼原子以sp2杂化
C.氯化硼分子呈正三角形,属非极性分子
D.氯化硼遇水蒸气会产生白雾
8.下列各离子或原子的电子排布式错误的是( )
A.Ca2+:1s22s22p63s23p6 B.O2-:1s22s22p4
C.K: 1s22s22p63s23p64s1 D.Fe3+:1s22s22p63s23p63d5
9.短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最
外层电子数是最内层电子数的3倍。下列判断正确的是
A.原子半径:r >r >r >r
W Z Y X
B.含Y元素的盐溶液一定显酸性
C.最简单气态氢化物的热稳定性:Z>W
D.X与氢元素组成的化合物XH 与水反应可产生两种气体
5
10.下列说法中正确的是
A.在多电子原子中,p轨道电子能量一定高于s轨道电子能量
B.电子在3P 与3 轨道上的运动状态不相同
X PZ
C.N原子的电子排布 违背了泡利不相容原理
D.B原子由 时,由基态转化为激发态,形成发射光谱
11.下列说法正确的是(N 为阿伏加德罗常数)( )
A
A.12 g石墨中含有C—C键的个数为1.5 N
A
B.12 g金刚石中含有C—C键的个数为4 N
A
C.60 g SiO 中含有Si—O键的个数为2 N
2 A
D.124 g P 中含有P—P键的个数为4 N
4 A
12.下列说法正确的是
试卷第2页,总2页A.凡是中心原子采取sp3杂化的分子,其立体构型都是正四面体形
B.白磷分子和CH 都是正四面体形分子且键角都为109°28'
4
C.若AB 型分子的中心原子A上没有孤电子对,则AB 为非极性分子
n n
D.NH 和PH 分子的VSEPR模型为正四面体形,PH 中P—H键键角大于NH 中N—
3 3 3 3
H键键角
13.下列说法正确的是( )
A. 具有弱酸性,与 分子间存在氢键有关
B.邻硝基苯酚与对硝基苯酚的沸点相同
C. 在水中的溶解度较大,与氢键无关
D. 的沸点低于 的沸点
14.自然界中的分解者可将含硫有机物分解为HS,硫磺细菌和硫化细菌可将HS进
2 2
一步变为硫单质或硫酸盐,下列关于硫化氢说法正确的是
A.HS是一种无色臭鸡蛋气味的有毒气体
2
B.HS分子中所有原子的最外层都达到8电子结构
2
C.将HS通入FeSO 溶液,产生沉淀
2 4
D.HS分子很稳定,受热难分解
2
15.某原子电子排布式为1s22s22p3,下列说法正确的是
A.该元素位于第二周期IIIA族 B.核外有3种能量不同的电子
C.最外层电子占据3个轨道 D.最外层上有3种运动状态不同的电子
二、填空题
16.如图是s能级和p能级的原子轨道图,试回答下列问题:
(1)s电子的原子轨道呈______形,每个s能级有______个原子轨道;p电子的原子轨
道呈________形,每个p能级有________个原子轨道。
(2)元素X的原子最外层电子排布式为nsnnpn+1,原子中能量最高的是________电子,
其电子云在空间有________方向;元素X的名称是_______,它的氢化物的电子式是
____________。若元素X的原子最外层电子排布式为nsn-1npn+1,那么X的元素符号为
________,原子的电子排布图为___________。
试卷第3页,总1页17.化合物YX 、ZX 中,X、Y、Z的核电荷数小于18;X原子最外层的p能级中有
2 2
一个轨道充填了2个电子,Y原子的最外层中p能级的电子数等于前一层电子总数,
且X和Y具有相同的电子层数;Z与X在周期表中位于同一主族。回答下列问题:
(1)Y的价电子轨道表示式为______________________;
(2)YX 的电子式是_______________,分子构型为________,中心原子发生了____
2
杂化。
(3)Y与Z形成的化合物的分子式是_______,该化合物中化学键是________键(填
“极性”或“非极性”),该分子属于__________分子(填“极性”或“非极性”)。
(4)Y的氢化物中分子构型为正四面体的是____________(填名称),键角为
_______,中心原子的杂化形式为_______。
(5)元素X与Y的电负性的大小关系是___________(用元素符号填写,并填﹥、﹤、
﹦)。
X与Z的第一电离能的大小关系是___________。(用元素符号填写,并填﹥、﹤、
﹦)。
三、元素或物质推断题
18.X、Y、Z、W、Q、R六种短周期主族元素,原子序数依次增大。X是周期表中半
径最小的原子,Z基态原子核外有三个未成对电子,Y、Z、W分别与X形成常见化合
物的分子结构依次为正四面体、三角锥形和V形,Q的各级电离能如表,W与R是同
族元素。回答下列有关问题:
Q I I I I I…
1 2 3 4 5
691
电离能(kJ/mol) 496 4562 9543 13353…
2
(1)W原子的电子排布式为_______。
(2)化合物QW 的电子式_______,化合物XYZ的结构式_______。
2 2
(3)Y、Z、W分别与X形成常见化合物的稳定性顺序是_______(用分子式表示)。
(4)RW 分子中的键角_______,RW 分子的立体构型是_______。
3 2
(5)根据等电子原理,指出与Z 互为等电子体的微粒有_______、_______。(要求写一
2
种分子和一种离子)。
四、原理综合题
19.铁、钴、镍位于元素周期表第四周期Ⅷ族,具有相似的性质,它们的单质及化合
物在现代工业生产中有着广泛应用。请回答下列问题:
(1)基态镍原子的核外电子占据的最高能层的符号是_________,占据该能层电子的
试卷第4页,总2页电子云轮廓图形状为_________。
(2)硫化钴可用作有机化合物的氢化催化剂。钴的基态原子中未成对电子个数为
________;电负性:硫元素_________(填“大于”或“小于”)钴元素;基态硫原子的核
外电子排布式为_________。
(3)铁元素能与CO形成Fe(CO) 等金属羰基配合物。与CO互为等电子体的分子和
5
离子分别为_________和_________(各举一种,填化学式);在CO分子中,σ键与π
键数目之比为_________。
(4)下图是金属镍的晶胞结构示意图,其晶胞参数为a nm,则金属镍原子的配位数为
_________;镍原子半径为_________ nm;晶体密度为_________ g·cm-3(阿伏伽德罗
常数的值用N 表示,写出简化后的计算式即可)。
A
20.2019年诺贝尔化学奖授予在研究锂离子电池方面的三位科学家。已知 、
是锂离电池常用的电极材料。回答下列相关问题:
(1)基态Co原子核外有________种不同形状的电子云;基态Fe原子的价电子排布图为
________;科学家通过________法可以得出太阳中存在较多的锂元素。
(2) 中, 、 、O三种元素的电负性大小顺序为________;第二周期元素
中,第一电离能介于 和O之间的元素有________(填写元素符号)。
(3) 结构中, 的空间构型为________,写出一个与之属于等电子体的离
子________。
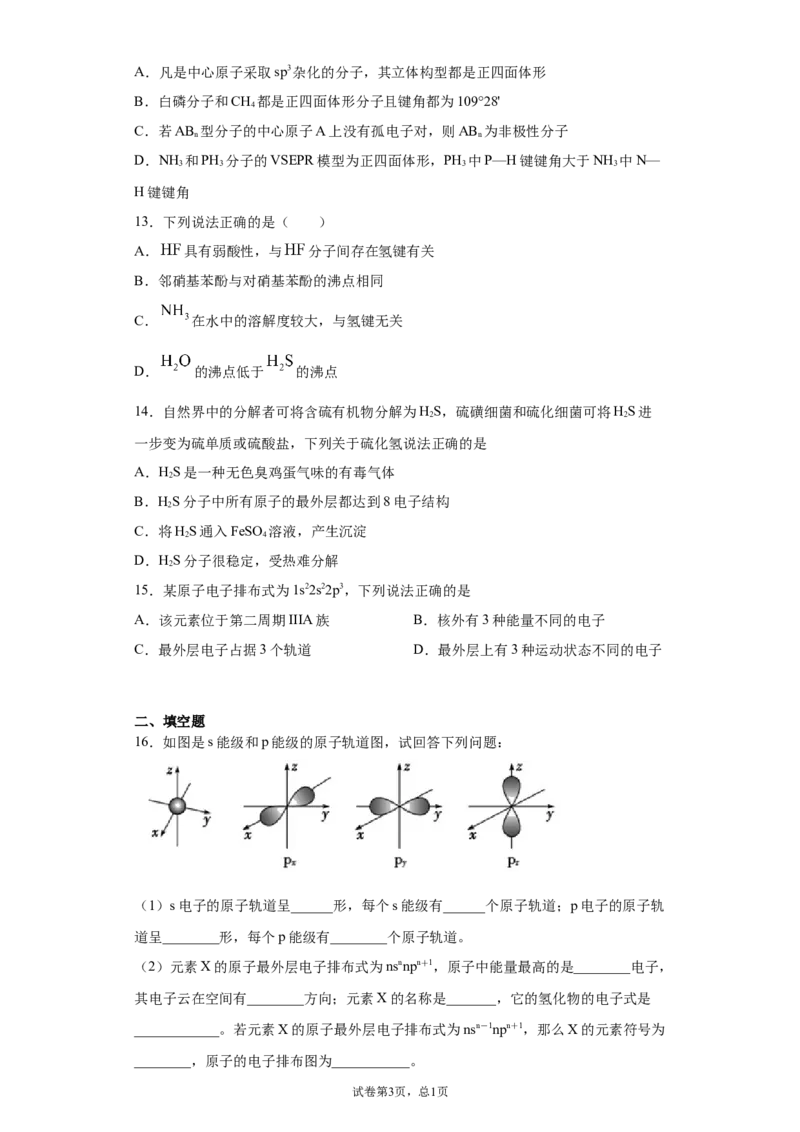
(4) 晶体的结构单元如图所示。
试卷第5页,总1页①若把锂、钴两种原子看作一种金属原子,该晶体属于 型晶型,晶体中O原子
的配位数为_______;晶体中O原子占据金属原子形成的_______(填“四而体空隙”或
“八而体空隙”)。
②若 晶体的结构单元的体积为 ,设 表示阿伏加德罗常数的值,则
的密度为_______ 。
试卷第6页,总2页参考答案
1.B
【详解】
根据能量最低原理可知,4p轨道填充一半的元素,原子核外电子排布应为
1s22s22p63s23p63d104s24p3,原子核外有33个电子,则原子序数为33,故选B。
2.C
【解析】A.干冰和氯气形成的晶体都是分子晶体,所以干冰升华和液氯气化时,都只需
克服分子间作用力,故A正确;B.硫酸氢钠是离子晶体,溶于水需要克服离子键,HSO -
4
在水中电离需要克服共价键,故B正确;C.氯化氢气体溶于水时,H-Cl共价键的断裂,
生成HO+时有共价键的形成,有化学键的形成,故C错误;D.石墨转化金刚石是化学变
3
化,既有化学键的断裂,又有化学键的形成,故D正确;故答案为C。
3.A
【解析】
【详解】
A.元素的非金属性越强,其电负性越大,由于元素的非金属性:O>N>C,所以元素电负性
由大到小的顺序:O>N>C,A正确;
B.一个乙烯分子CH=CH 中含1个π键和5个σ键,B错误;
2 2
C.氯化钠晶体中氯离子的配位数是6,而氯化铯晶体中氯离子的配位数是8,因此配位数不
相同,C错误;
D.一般情况下元素的第一电离能随原子序数的增大而增大,但Mg原子核外电子处于3s轨
道的充满的稳定状态,失去一个电子要比比同一周期的Al第一电离能大,D错误;
故合理选项是A。
4.A
【分析】
一般情况下,非金属元素之间形成的化学键为共价键,由共价键形成的物质在溶于水或发
生化学变化时共价键被破坏,由活泼金属与非金属形成的化合物以及铵盐为离子化合物,
由此分析。
【详解】
A.水、干冰、I 都是由分子构成的,水→冰;干冰和I 的升华破坏的是分子间作用力,化
2 2
学键没有被破坏,故A符合题意;
B.NaOH中存在离子键和共价键,HCl中存在共价键,NaOH溶于水发生电离生成钠离子
答案第1页,总2页和氢氧根离子,破坏了离子键,HCl溶于水形成了盐酸,破坏了共价键,蔗糖溶于水没有
电离,没有破坏化学键,故B不符合题意;
C.水电解得到氧气与氢气,水分子中的共价键发生了断裂;NH HCO 中闻到了刺激性气
4 3
味,是NH HCO 分解生成氨气、水和二氧化碳,NH HCO 是离子晶体,在阴阳离子间存
4 3 4 3
在着离子键,NH HCO 分解铵根离子和碳酸氢根离子间的离子键发生了断裂,生成氨气、
4 3
水和二氧化碳时共价键都发生了断裂,故C不符合题意;
D.金刚石中的碳原子之间以共价键结合,加热融化,破坏共价键;NaCl是离子晶体,在
离子晶体中,阳离子周围有一定数目的阴离子,阴离子周围同样有一定数目的阳离子,在
阴阳离子间存在着离子键,NaCl颗粒被粉碎,断裂的晶面之间原来是靠大量离子键维系着
的,现在破裂了,有键断裂了,破坏了离子键,故D不符合题意;
答案选A。
5.B
【详解】
A. N(NO ) 是一种共价化合物,氮原子之间形成非极性键,N、O间形成的共价键是极性键,
2 3
故A项正确;
B.由题意N—N—N键角都是108.1°,可知分子中四个氮原子不在同一平面上,故B项错误;
C.分子中顶角上的N元素为0价,-NO 原子团中N元素为+4价,故该物质既有氧化性又有
2
还原性,C项正确;
D. 15.2 g该物质为0.1mol, 每个分子含10个原子,共含有6.02×1023个原子,故D项正确。
故答案选B。
6.D
【详解】
A.N原子上有1对孤对电子,有3个N-F键,类似氨气的结构,则NF 分子中N原子是
3
sp3杂化,分子呈三角锥形,故A正确;
B.根据相似相溶原理可知,有机物易溶于有机物,而水为无机物,则C F 在CCl 中的溶
3 8 4
解度比水中大,故B正确;
C.碳原子连有四个不同的基团,则具有手性,则CHClFCF 存在手性异构,故C正确;
3
D.这三种元素的第一电离能顺序为:O<N<F,故D错误;
故选D。
【点晴】
掌握和理解第一电离能、物质的溶解性、手性、杂化类型及空间结构的知识是解答本题的
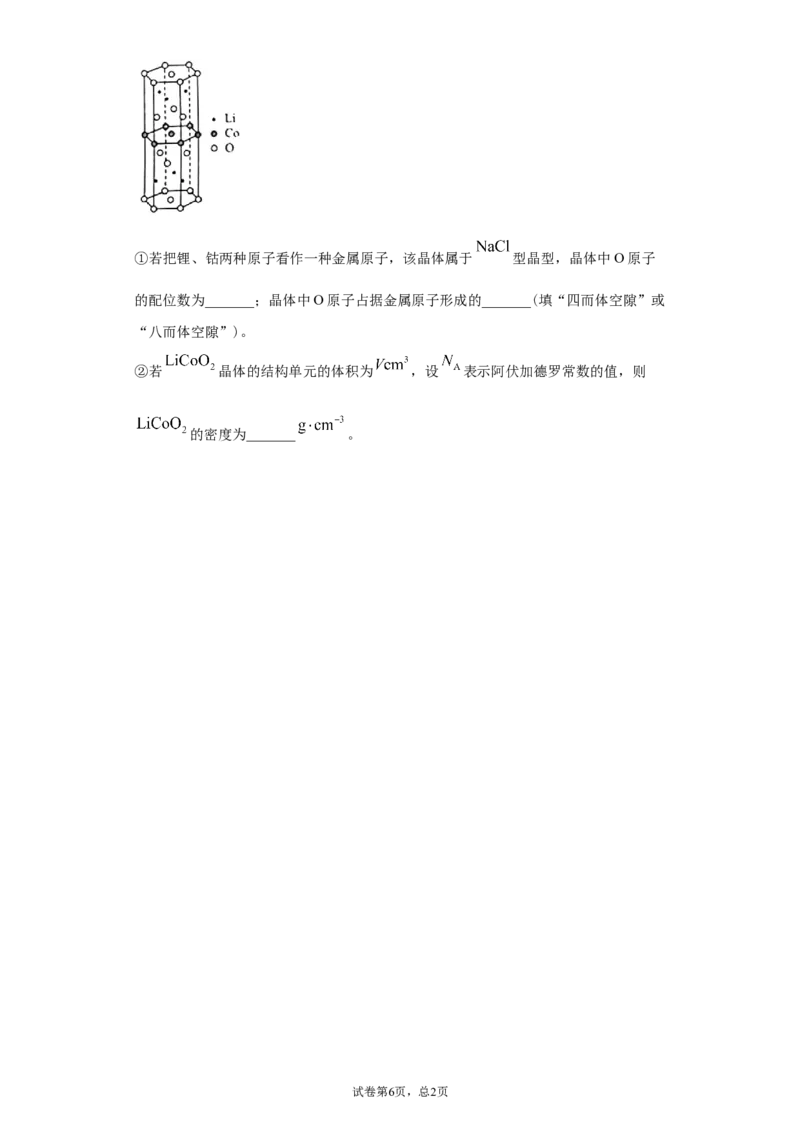
答案第2页,总2页基础。注意第一电离能的异常现象,这是本题的易错点。当外围电子在能量相等的轨道上
形成全空(p0,d0,f0)、半满(p3,d5,f7)或全满(p6,d10,f14)结构时,原子的能量较
低,元素的第一电离能较大(如图 )。
7.A
【分析】
【详解】
A. 根据题意得出氯化硼是分子晶体,液态时不能导电,故A错误;
B. 氯化硼中硼原子价层电子对数为 ,因此为sp2杂化,故B正确;
C. 氯化硼中硼原子价层电子对数为 ,分子空间构型为平面正三
角形,属非极性分子,故C正确;
D. 氯化硼能水解,遇水蒸气反应生成HCl和HBO,氯化氢遇水蒸气会产生白雾,故D正
3 3
确。
综上所述,答案为A。
【点睛】
根据价层电子对数分析杂化方式和空间构型。
8.B
【详解】
A.Ca2+核外电子数为18,其电子排布式为1s22s22p63s23p6,A正确;
答案第3页,总2页B.O2-核外电子数为10,电子排布式为1s22s22p6,B错误;
C.K原子核外电子数为19,电子排布式为1s22s22p63s23p64s1,C正确;
D.Fe3+核外电子数为23,电子排布式为1s22s22p63s23p63d5,D正确;
故选B。
9.D
【分析】
W原子的最外层电子数是最内层电子数的3倍可知W为S,根据四种元素在周期表中的相
对位置,可知X为N、Z为Si、Y为Al。
【详解】
A项,原子半径:Y>Z>W>X,错误;
B项,AlCl 溶液呈酸性,NaAlO 溶液呈碱性,错误;
3 2
C项,气态氢化物的稳定性W>Z,错误;
D项,NH 为NH H,与水反应:NH H+HO= NH↑+HO+H↑,正确。
5 4 4 2 3 2 2
故选D。
10.B
【详解】
A.同一层即同一能级中的p轨道电子的能量一定比s轨道电子能量高,但不同能层时,外
层s轨道电子能量则比内层p轨道电子能量高,故A错误;
B.3P 与3P 为同一能层上的轨道,其能量相同,但在同一原子里,没有运动状态完全相同
X Z
的电子存在,则电子在3P 与3 轨道上的运动状态不相同,故B正确;
X PZ
C.N原子核外电子数为7,处于2p能级上的3个电子应尽可能分占3个不同2p原子轨道,
且自旋状态相同, 违背了洪特规则,故C错误;
D.B原子的基态原子电子排布式为 ,由基态转化为激发态 时,电子
的能力增大,需吸收能量,形成吸收光谱,故D错误;
答案选B。
11.A
【详解】
答案第4页,总2页A.12g石墨中含有碳原子个数= N mol-1=N ,石墨中每个碳原子含有 个C-C
A A
键,所以12g石墨中含有C-C键个数是1.5N ,故A正确;
A
B.12g金刚石中含有碳原子个数= N mol-1=N ,金刚石中每个碳原子含有2个
A A
C-C键,所以12g金刚石中含有C-C键个数是2N ,故B错误;
A
C.60g二氧化硅中含有的硅原子个数═ N mol-1=N ,每个硅原子含有4个Si-O
A A
键,所以60g二氧化硅中含有的Si-O键的个数为4N ,故C错误;
A
D.124g白磷中含有的磷分子个数= N mol-1=N ,一个白磷分子中含有6个P-P
A A
键,所以124g P 含有的P-P键的个数为6N ,故D错误;
4 A
故选A。
【点睛】
本题考查阿伏伽德罗常数的有关计算,明确物质结构是解本题关键,注意石墨和金刚石结
构的区别,为易错点,石墨为平面六边形结构,金刚石为空间正四面体结构。
12.C
【详解】
A.通过sp3杂化形成的中性分子,分子中价层电子对数是4,若不含孤电子对,如CH 或
4
CF,分子为正四面体结构;分子中价层电子对数是4,若含有一个孤电子对,如NH 或
4 3
NF ,分子为三角锥形结构;分子中价层电子对数是4,若含有两个孤电子对,如HO,分
3 2
子为V形结构,A错误;
B.P 的空间结构为正四面体,体中心无原子,键角是60°,B错误;
4
C.若AB 型分子的中心原子A上没有孤对电子,则AB 为非极性分子,这是判断极性分
n n
子和非极性分子的重要经验规律,C正确;
D.由于电负性N强于P,中心原子的电负性越大,成键电子对离中心原子越近,成键电
子对之间的距离越小,成键电子对之间的排斥力越大,因此键角变大,即PH 中P—H键键
3
角小于NH 中N—H键键角,D错误;
3
故选C。
答案第5页,总2页13.A
【详解】
A. 由于氟原子电负性高,半径很小,HF分子间存在氢键,在水中与水分子也能形成氢键,
使其更难电离出H+,从而酸性减弱, 具有弱酸性,与 分子间存在氢键有关,A正
确;
B. 邻硝基苯酚主要形成分子内氢键,对硝基苯酚主要形成分子间氢键,分子间氢键使物质
的熔沸点更高,所以对硝基苯酚沸点高于邻硝基苯酚,B错误;
C. 氨气与水分子之间能形成氢键,所以氨气极易溶于水,与氢键有关,C错误;
D. 分子间存在氢键, 沸点高于 的沸点,D错误;故答案为:A。
14.A
【详解】
A.通常情况下,硫化氢气体是一种无色有臭鸡蛋气味的有毒气体,密度比空气大,能溶
于水,A正确;
B.HS分子中H原子最外层只有2个电子,B错误;
2
C.FeS沉淀溶于酸,将HS通入FeSO 溶液,没有沉淀生成,C错误;
2 4
D.硫化氢分子不稳定,受热能分解生成S和氢气,D错误;
故选A。
15.B
【分析】
由原子电子排布式为1s22s22p3,可知原子结构中有2个电子层,最外层电子数为5,共7个
电子,有7个不同运动状态的电子,但同一能级上电子的能量相同,以此来解答。
【详解】
A.有2个电子层,最外层电子数为5,则该元素位于第二周期VA族,故A错误;
B.核外有3种能量不同的电子,分别为1s、2s、3p上电子,故B正确;
C.最外层电子数为5,占据1个2s、3个2p轨道,共4个轨道,故C错误;
D.最外层电子数为5,则最外层上有5种运动状态不同的电子,故D错误;
故答案为B。
16.球 1 哑铃 3 2p 三个互相垂直的伸展 氮 S
答案第6页,总2页【详解】
(1)s电子的原子轨道都是球形的,每个s能级有1个原子轨道;p电子的原子轨道都是哑
铃形的,每个p能级有3个原子轨道,它们相互垂直,分别以p、p、p 表示。
x y z
(2)因为元素X的原子最外层电子排布式为nsnnn+1,np轨道已排上电子,说明ns轨道已
排满电子,即n=2,则元素X的原子核外电子排布式为1s22s22p3,是氮元素,其中原子中
能量最高的是2p电子,其电子云在空间有三个互相垂直的伸展方向;氮元素的氢化物是氨
气,含有极性键,其电子式是 ;当元素X的原子最外层电子排布式为nsn-1npn+1时,
根据上述分析,有n-1=2,则n=3,所以X元素的原子核外电子排布式为
1s22s22p63s23p4,是硫元素;硫元素的元素符号为S,其原子的电子排布图为
。
17. 直线型 sp CS 极性 非
2
极性 甲烷 109.5° sp3 O﹥C O﹥S
【分析】
X原子最外层的p能级中有一个轨道充填了2个电子,X可能为氧,也可能为硫。 Y原子
的最外层中p能级的电子数等于前一层电子总数,Y只能为碳,且X和Y具有相同的电子
层数,所以X为氧。Z与X在周期表中位于同一主族,Z为硫。
【详解】
(1)Y为碳,价电子排布式为2s22p2,其轨道表示式为 ;
(2)CO 的电子式为 ,是直线型分子,中心原子碳原子发生了sp杂化。
2
故答案为 ,直线型,sp;
(3)碳和硫形成的化合物为CS,该分子和CO 为等电子体,化学键为极性键,分子构型
2 2
为直线型,是非极性分子。故答案为CS,极性,非极性;
2
答案第7页,总2页(4)碳的氢化物中分子构型为正四面体的是甲烷,键角为109.5°,中心原子碳原子的杂
化方式为sp3。故答案为甲烷,109.5°,sp3;
(5)氧原子对电子的吸引能力大于碳,所以氧的电负性大于碳。氧和硫是同族元素,氧在
第二周期,硫在第三周期,氧对电子的束缚能力强于硫,所以氧的第一电离能大于硫。故
答案为O﹥C,O﹥S。
18.1s22s22p4 H-C≡N HO>NH >CH 120˚ V形
2 3 4
CO CN-
【分析】
X、Y、Z、W、Q、R六种短周期主族元素,X是周期表中半径最小的原子,X为H;由Q
的各级电离能可知Q原子中核外电子数超过5,其中I I,说明Q原子的最外层只有1个
1 2
电子,则Q为Na;X、Y、Z、W、Q、R的原子序数依≪次增大,Z基态原子核外有三个未
成对电子,Y、Z、W分别与X形成常见化合物的分子结构依次为正四面体、三角锥形和V
形,则Y、Z、W依次为C、N、O;W与R是同族元素,R为S;据此分析作答。
【详解】
根据分析,X、Y、Z、W、Q、R依次为H、C、N、O、Na、S;
(1)W为O,O原子核外有8个电子,其电子排布式为1s22s22p4;故答案为:1s22s22p4。
(2)Q W 为NaO,NaO 中存在离子键和非极性键,电子式为 ;XYZ
2 2 2 2 2 2
为HCN,其结构式为H-C≡N;故答案为: ;H-C≡N。
(3)Y、Z、W分别与X形成的常见化合物为CH、NH 、HO,C、N、O都属于第二周期,
4 3 2
同周期从左到右元素的非金属性逐渐增强,气体氢化物的稳定性逐渐增强,因为非金属性:
O>N>C,则稳定性顺序为HO>NH >CH;故答案为:HO>NH >CH。
2 3 4 2 3 4
(4)RW 为SO ,其中S原子上的孤电子对数为 ,σ键电子对数为3,价层电
3 3
子对数为3,S采取sp2杂化,立体构型为平面正三角形,键角为120°;RW 为SO ,S原子
2 2
上的孤电子对数为 ,σ键电子对数为2,价层电子对数为3,VSEPR模型为
平面三角形,立体构型为V形;故答案为:120°;V形。
答案第8页,总2页(5)Z 为N,用替代法,与其互为等电子体的分子有CO,离子有CN-、 等;故答案为:
2 2
CO、CN-。
19.N 球形 3 大于 1s22s22p63s23p4 N CN- 1:2 12
2
【详解】
(1)镍是28号元素,核外电子排布式为:[Ar]3d84s2,基态镍原子的核外电子占据的最高
能层的符号是N,占据该能层电子位于4s能级,电子云轮廓图形状为球形;
故答案为:N;球形;
(2)硫化钴可用作有机化合物的氢化催化剂,钴是27号元素,核外电子排布式为:
[Ar]3d74s2,基态原子中未成对电子个数为3;非金属性越强,电负性越强,则电负性:硫
大于钴;基态硫原子的核外电子排布式为1s22s22p63s23p4;
故答案为:3;大于;1s22s22p63s23p4;
(3)铁元素能与CO形成Fe(CO) 等金属羰基配合物,与CO互为等电子体的分子和离子
5
具有2个原子,10个价电子,分别为N 和CN-;在CO分子中,形成碳氧三键,σ键与π
2
键数目之比为1:2;
故答案为:N;CN-;1:2;
2
(4)根据金属镍的晶胞结构示意图可知,该晶胞是面心立方最密堆积,其晶胞参数为a
nm,金属镍原子的配位数为12;对角线的 为镍原子半径 nm;晶体密度为
。
20.3 光谱分析(或原子光谱) Be、B、
答案第9页,总2页C 正四面体形 (其他合理答案也可) 6 八面体空隙
【详解】
(1)基态 、 原子的电子排布式分别为 , ,可以得出基态
原子有3种能级,电子云形状有3种;基态 原子价电子排布图为 ;光谱
分析法是确定元素常用的方法,科学家通过原子光谱法得出太阳中含有哪些具体元素,故
答案为:3; ;光谱分析(或原子光谱);
(2)非金属性越强,电负性数值越大, 、 、O三种元素的电负性大小顺序为
;同一周期,从左到右,元素的第一电离能逐渐增大,但第ⅡA族、第VA
族元素的第一电离能大于相邻元素,第一电离能介于 与O之间的有 、B、C三种,
故答案为: ; 、B、C;
(3) 中P原子的价层电子对数=4+ =4,P原子采用 杂化,空间构型为正
四面体形,与 互为等电子体的离子有 、 等,故答案为:正四面体形;
(或 );
(4)①若把锂、钴原子看作一种金属原子,属于 型,根据氯化钠晶胞的结构单元
答案第10页,总2页,显然O原子配位数为6,晶体中O原子占据金属原子形成的八面体中心
( ),故答案为:6;八面体空隙;
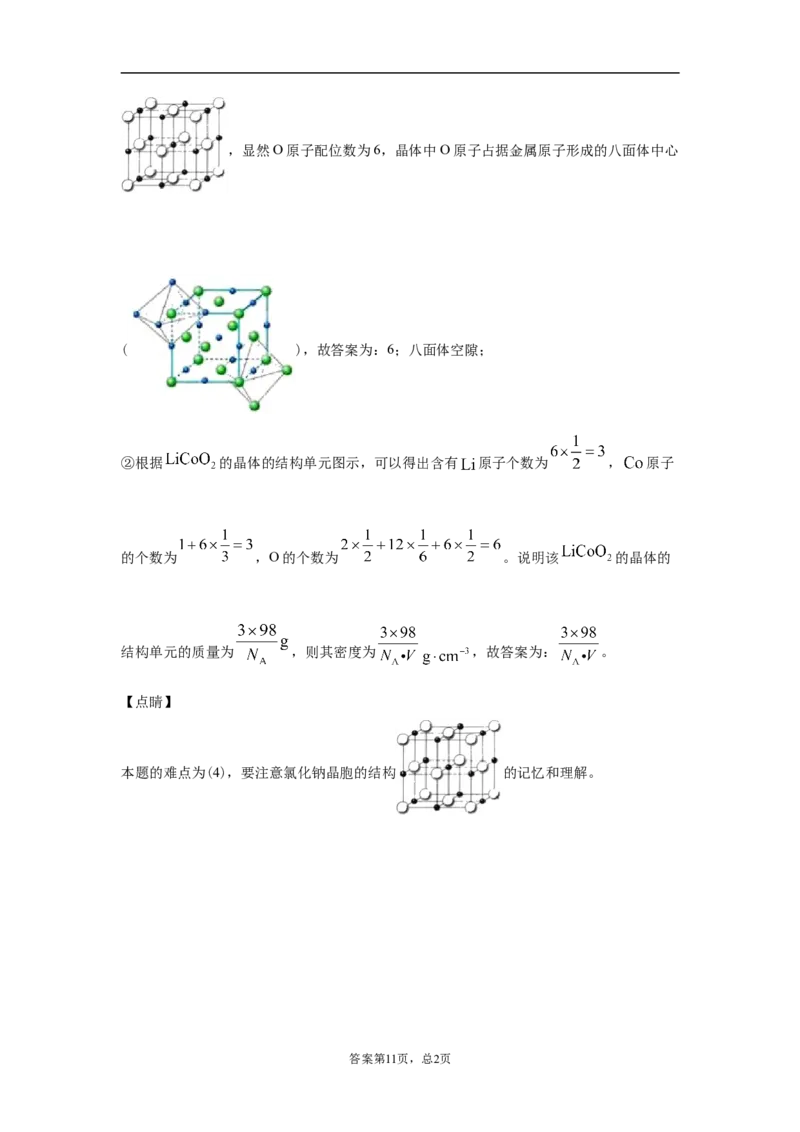
②根据 的晶体的结构单元图示,可以得出含有 原子个数为 , 原子
的个数为 ,O的个数为 。说明该 的晶体的
结构单元的质量为 ,则其密度为 ,故答案为: 。
【点睛】
本题的难点为(4),要注意氯化钠晶胞的结构 的记忆和理解。
答案第11页,总2页