文档内容
第一单元 物质及其变化
第三节 氧化还原反应(一)
一、基础巩固
1 . Cu Hgl 是 一 种 红 色 固 体 , 常 用 作 示 温 涂 料 。 制 备 反 应 为 :
2 4
2CuSO +K Hgl +SO +2H O═Cu Hgl ↓+K SO +2H SO .下列说法正确的是( )
4 2 4 2 2 2 4 2 4 2 4
A.上述反应的产物Cu HgI 中,Hg的化合价为+1
2 4
B.上述反应中Hg元素与Cu元素均被还原
C.上述反应中生成1mol Cu HgI 时,转移的电子数为4N
2 4 A
D.由以上信息可推知:可发生反应2CuSO +2NaCl+SO +2H O═2CuCl↓+Na SO +2H SO
4 2 2 2 4 2 4
【答案】D
【解析】A.Cu HgI 中,I元素化合价为﹣1价,Cu元素化合价为+1价,所以Hg的化合价为+2,故A
2 4
错误;
B.从反应2CuSO +K Hgl +SO +2H O═Cu Hgl ↓+K SO +2H SO 分析,Hg的化合价不变,Cu从+2价
4 2 4 2 2 2 4 2 4 2 4
变成+1被还原,故B错误;
C.从反应2CuSO +K Hgl +SO +2H O═Cu Hgl ↓+K SO +2H SO 分析,Cu从+2价变成+1被还原,则
4 2 4 2 2 2 4 2 4 2 4
每生成1mol Cu HgI 时,转移的电子数为:1mol×2×(2﹣1)=2mol即2N ,故C错误;
2 4 A
D.由反应2CuSO +K Hgl +SO +2H O═Cu Hgl ↓+K SO +2H SO 可知,SO ,可将二价铜离子还原成
4 2 4 2 2 2 4 2 4 2 4 2
+1价的铜的化合物,所以可发生反应2CuSO +2NaCl+SO +2H O═2CuCl↓+Na SO +2H SO ,故D正确;
4 2 2 2 4 2 4
2.加入氧化剂才能实现的过程是( )
A.Cl →ClO﹣ B.SO →SO 2﹣ C.N →NH D.Al3+→AlO ﹣
2 2 4 2 3 2
【答案】B
【解析】A.Cl →ClO﹣,Cl 与NaOH溶液反应即可实现,氯气是氧化剂也是还原剂,不需要加氧化剂,
2 2
故A错误;
B.SO →SO 2﹣中S元素化合价升高,被氧化,应加入氧化剂,故B正确;
2 4
C.N →NH 中N元素化合价降低,被还原,应加入还原剂,故C错误;
2 3
D.Al3+→AlO ﹣中无元素的化合价变化,不需加入氧化剂和还原剂,故D错误。
2故选:B。
3.下列属于氧化还原反应的是( )
A.CO +NaOH═NaHCO
2 3
B.2NO +2NaOH═NaNO +NaNO +H O
2 2 3 2
C.ICl+2NaOH═NaCl+NaIO+H O
2
D.NaOH+HCl═NaCl+H O
2
【答案】B
【解析】A.该反应中没有元素化合价变化,所以不属于氧化还原反应,属于化合反应,故A错误;
B.该反应中N元素化合价由+4价变为+3价、+5价,所以属于氧化还原反应,故B正确;
C.该反应中没有元素化合价变化,不属于氧化还原反应,故C错误;
D.该反应中没有元素化合价变化,不属于氧化还原反应,属于复分解反应,故D错误;
故选:B。
4.下列反应中,属于氧化还原反应且H O既不做氧化剂又不做还原剂的是( )
2
A.Cl +H O HCl+HClO B.2Na+2H O═2NaOH+H ↑
2 2 2 2
C.2F
2
+2H
2
O⇌═4HF+O
2
D.SO
2
+H
2
O═H
2
SO
3
【答案】A
【解析】A.该反应中Cl 中Cl元素化合价由0价变为﹣1价、+1价,所以属于氧化还原反应,水中各
2
元素化合价不变,则水既不是氧化剂也不是还原剂,故A正确;
B.该反应中Na元素化合价由0价变为+1价、H元素化合价由+1价变为0价,则水是氧化剂,故B错
误;
C.该反应中F元素化合价由0价变为﹣1价、O元素化合价由﹣2价变为0价,则水是还原剂,故C错
误;
D.该反应中各元素化合价不变,不属于氧化还原反应,故D错误;
故选:A。
5.物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度有关。下列各组物
质:①Fe与HNO 溶液 ②Al与H SO 溶液 ③Zn与HNO 溶液 ④Cu与HNO 溶液⑤Fe与H SO
3 2 4 3 3 2 4
溶液,其中由于浓度不同而能发生不同氧化还原反应的是( )
A.①②③④ B.②③ C.①②③ D.①②③④⑤
【答案】D
【解析】①Fe与HNO 溶液反应,浓硝酸加热反应生成二氧化氮,稀硝酸反应生成一氧化氮,过量的
3
铁和硝酸得到硝酸亚铁,少量的铁则得到硝酸铁,与浓度有关,故①符合题意;②Al与H SO 溶液中,若为稀硫酸,发生 2Al+3H SO ═2Al (SO ) +3H ↑,若为浓硫酸,则发生
2 4 2 4 2 4 3 2
2Al+6H SO (浓) Al (SO ) +3SO ↑+6H O,故②符合题意;
2 4 2 4 3 2 2
③Zn与HNO 溶液,浓硝酸与金属反应生成二氧化氮,Zu+4HNO ═Zu(NO ) +2NO ↑+2H O,稀硝
3 3 3 2 2 2
酸与金属反应生成一氧化氮,3Zu+8HNO ═3Zu(NO ) +2NO↑+4H O,故③符合题意;
3 3 2 2
④Cu与HNO 溶液中,若为浓硝酸,发生Cu+4HNO ═Cu(NO ) +2NO ↑+2H O,若为稀硝酸,则发
3 3 3 2 2 2
生3Cu+8HNO ═3Cu(NO ) +2NO↑+4H O,故④符合题意;
3 3 2 2
⑤Fe与H SO 溶液,与稀硫酸反应生成氢气,与浓硫酸加热反应生成二氧化硫,2Fe+6H SO
2 4 2 4
Fe (SO ) +6H O+3SO ↑,故⑤符合题意;
2 4 3 2 2
故选:D。
6.已知黑火药爆炸的反应:S+2KNO +3C→K S+3CO +N ↑,下列说法正确的是( )
3 2 2 2
A.该反应中氧化剂只有硝酸钾
B.该反应中还原剂只有碳
C.每生成0.1mol N 转移电子1mol
2
D.产物中有两种共价化合物
【答案】B
【解析】A.反应中N和S元素化合价降低,被还原,C元素化合价升高,所以还原剂是C、氧化剂是
S和KNO ,故A错误;
3
B.反应中只有C元素化合价升高,还原剂只有C,故B正确;
C.由S+2KNO +3C═K S+N ↑+3CO ↑~12e﹣可知,生成1molN 时转移12mol电子,故每生成0.1mol
3 2 2 2 2
N 转移电子1.2mol,故C错误;
2
D.产物中只有CO 为共价化合物,故产物中有一种共价化合物,故D错误。
2
故选:B。
7.氯气可以用于制备“战略金属”钛,其中有关反应如下,用双线桥(或单线桥)标出反应中电子转移
的方向和数目。TiO +2C+2Cl TiCl +2CO
2 2 4
反应中氧化剂是 ,被氧化的物质是 。
【答案】 或 ;氯气;碳。【解析】TiO +2C+2Cl TiCl +2CO中,C元素的化合价升高,Cl元素的化合价降低,该反应转
2 2 4
移4e﹣,氧化剂是氯气,被氧化的物质是碳,电子转移的方向和数目是
或 ,
故答案为: 或 ;氯气;碳。
二、拓展提升
8.已知下列反应:
①SO +H O═H SO ②C+H O═H +CO
2 2 2 3 2 2
③2A1+6H+═2A13++3H ↑ ④2Mg+CO 2Mg+C
2 2
⑤2Na O +2H O═4NaOH+O ↑ ⑥Ca C +2H O═Ca(OH) +C H ↑
2 2 2 2 2 2 2 2 2 2
(1)上述反应中不属于氧化还原反应的有 ①⑥ (填各反应的序号,下同);反应物中H O被还原
2
的是 ② :还原产物为单质的是 ②③④ 。
(2)①②④反应中涉及的所有物质中属于电解质的有 H O 、 MgO 、 H SO (填物质化学式)。
2 2 3
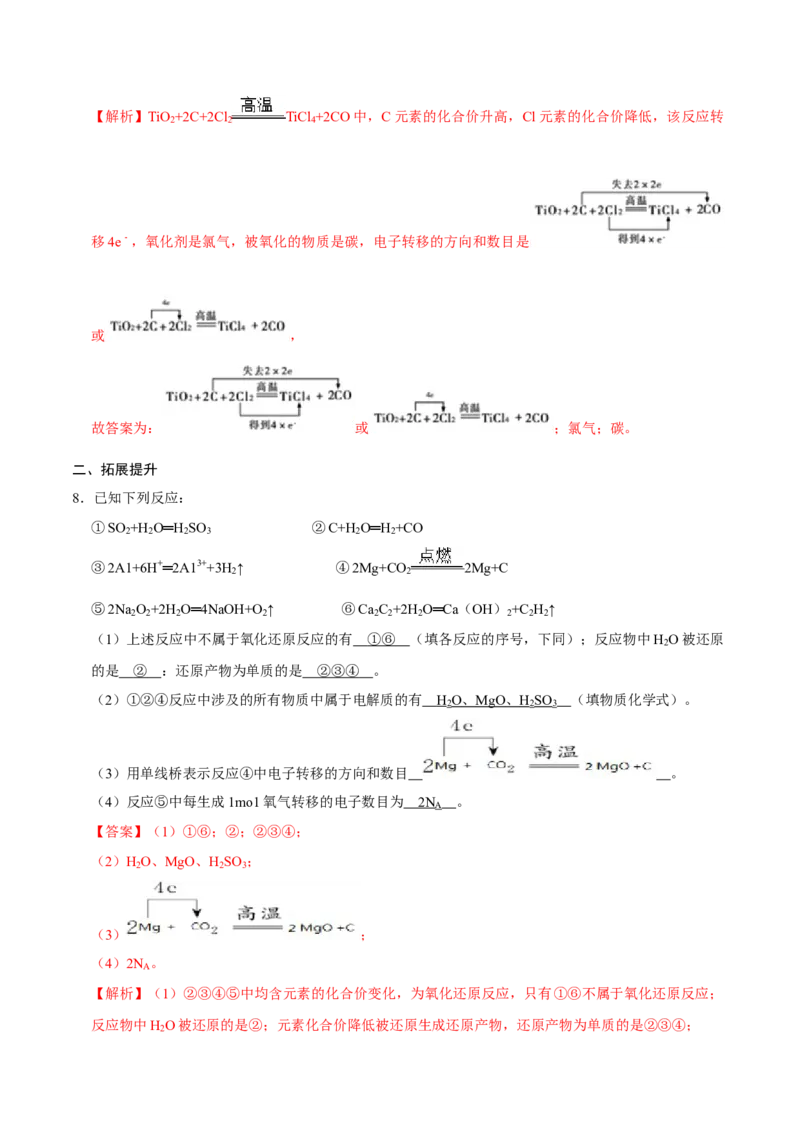
(3)用单线桥表示反应④中电子转移的方向和数目 。
(4)反应⑤中每生成1mo1氧气转移的电子数目为 2N 。
A
【答案】(1)①⑥;②;②③④;
(2)H O、MgO、H SO ;
2 2 3
(3) ;
(4)2N 。
A
【解析】(1)②③④⑤中均含元素的化合价变化,为氧化还原反应,只有①⑥不属于氧化还原反应;
反应物中H O被还原的是②;元素化合价降低被还原生成还原产物,还原产物为单质的是②③④;
2故答案为:①⑥;②;②③④;
(2)酸碱盐、金属氧化物、水均为电解质,上述各反应所涉及到的物质中,属于电解质的是H O、
2
MgO、H SO ,
2 3
故答案为:H O、MgO、H SO ;
2 2 3
(3)2Mg+CO ═2MgO+C中Mg失去电子,C得到电子,转移4e﹣,单线桥表示反应电子转移的方向
2
和数目为 ,
故答案为: ;
(4)2Na O +2H O═4NaOH+O ↑反应中部分O元素的化合价从﹣1价升高到0价,部分O 元素的化合
2 2 2 2
价从﹣1价降低到﹣2价,则每生成1mo1氧气转移的电子数目为2N ;
A
故答案为:2N 。
A
9.配平下列方程式
(1) Mg N + H O﹣ Mg(OH) + NH
3 2 2 2 3
(2) Ag+ HNO (稀)﹣ AgNO + NO+ H O
3 3 2
(3) Cl + KOH﹣ KC1+ KC1O + H O
2 3 2
(4) NO ﹣+ Zn+ OH﹣+ H O﹣ NH + Zn(OH) 2﹣
3 2 3 4
【答案】(1)1,6,3,2;
(2)3,4,3,1,2;
(3)3,6,5,1,3;
(4)1,4,7,6,1,4。
【解析】(1)反应中元素化合价不变,是非氧化还原反应,依据得失电子守恒可知设氮化镁系数为
1,则氢氧化镁系数为3,氨气系数为2,水系数为6,反应的方程式:Mg N +6H O=3Mg(OH)
3 2 2
+2NH ↑;
2 3
故答案为:1,6,3,2;
(2)银元素从0价升高为+1价,氮元素从+5价降为+2价,化合价升降最小公倍数为:3,则银系数为
3,一氧化氮系数为 1,硝酸银系数为 3,依据原子个数守恒,反应方程式:3Ag+4HNO (稀)=
3
3AgNO +NO↑+2H O;
3 2
故答案为:3,4,3,1,2;(3)反应中氯元素化合价部分从0升高为+5价,部分从0降为﹣1价,为歧化反应,化合价升降最小
公倍数为5,则氯化钾系数为5,氯酸钾系数为1,依据原子个数守恒,反应方程式:
6KOH+3Cl ═5KCl+KClO +3H O;
2 3 2
故答案为:3,6,5,1,3;
(4)反应中氮元素化合价从+5价降为﹣3价,锌元素从0价升高为+2价,化合价升降最小公倍数为:
8,则锌的系数为4,硝酸根离子系数为1,氨气系数为1,四羟基合锌酸根子系数为,4依据原子个数
守恒、电荷守恒反应的离子方程式:1NO ﹣+4Zn+7OH﹣+6H O=1NH +4Zn(OH) 2﹣;
3 2 3 4
故答案为:1,4,7,6,1,4。
10.实验探究是体验知识的产生或形成过程的基本途径。下面是某同学探究实验报告的一部分,请填空:
实验药品:NaCl溶液、KBr溶液、KI溶液、氯水、溴水、四氯化碳
实验步骤 实验结论
①NaCl溶液+氯水+1mL CCl ,振荡、静置、观察CCl 溶液 氧化性从强到弱的
4 4
顺序:氯、溴、碘
②NaBr溶液+氯水+1mLCCl ,振荡、静置、观察CCl 溶液
4 4
③KI溶液+氯水+1mL CCl ,振荡、静置、观察CCl 溶液
4 4
(1)由题中信息(如题干、药品、步骤或结论)可分析得出该实验的目的是 。
(2)完成该实验需用到的仪器是胶头滴管和 。
(3)由实验①和②可以比较出 Cl 和 Br 的氧化性强弱。写出②中反应的化学方程式
2 2
。
(4 )该同 学的实验缺 陷是 ,改进的办法是 。
【答案】(1)利用Cl 、Br 、I 间的置换反应来比较其单质的氧化性强弱。
2 2 2
(2)试管;
(3)Cl +2NaBr=Br +2NaCl;
2 2
(4)没有比较Br 和I 的氧化性强弱;把第③步改为:将溴水滴在KI淀粉试纸上,观察试纸是否变蓝
2 2
色(或KI溶液+溴水+1 mL CCl ,振荡,静置,观察四氯化碳层颜色)。
4
【解析】(1)由题中信息可知,该实验的目的是利用Cl 、Br 、I 间的置换反应来比较其单质的氧化
2 2 2
性强弱,
故答案为:利用Cl 、Br 、I 间的置换反应来比较其单质的氧化性强弱。
2 2 2
(2)该实验可以在试管中进行反应,要用胶头滴管滴加液体,则需用到的仪器是胶头滴管和试管,故
答案为:试管;
(3)②中Cl 与NaBr发生氧化还原反应,NaBr被氧化为为Br ,Cl 被还原为NaCl,反应化学方程式
2 2 2
为:Cl +2NaBr=Br +2NaCl,
2 2故答案为:Cl +2NaBr=Br +2NaCl;
2 2
(4)设计的实验中不能证明溴的氧化性强于碘,把第③步改为:将溴水滴在KI淀粉试纸上,观察试
纸是否变蓝色(或KI溶液+溴水+1 mL CCl ,振荡,静置,观察四氯化碳层颜色),
4
故答案为:没有比较Br 和I 的氧化性强弱;把第③步改为:将溴水滴在KI淀粉试纸上,观察试纸是
2 2
否变蓝色(或KI溶液+溴水+1 mL CCl ,振荡,静置,观察四氯化碳层颜色)。
4