文档内容
第三章 第四节 第2课时 沉淀溶解平衡的应用 测试题
榆次一中 李金虎
一、选择题(本题共有15小题,每小题4分,共60分,每小题只有一个正确选项)
1. 下列化学原理的应用,主要用沉淀溶解平衡原理来解释的是( )
①热纯碱溶液去油污能力强
②误将钡盐[BaCl 、Ba(NO )]当作食盐混用后,常用0.5%的NaSO 溶液解毒
2 3 2 2 4
③溶洞、珊瑚的形成
④碳酸钡不能作“钡餐”而硫酸钡则能
⑤泡沫灭火器灭火的原理
A.②③④ B.①②③
C.③④⑤ D.①②③④⑤
2. 一定温度下,Mg(OH) 固体在水溶液中达到下列平衡时:Mg(OH) (s) Mg2+(aq)+2OH-
2 2
(aq),使Mg(OH) 固体减少而c(Mg2+)不变,可采取的措施是
2
A.加MgSO 固体 B.加HCl溶液
4
C.加NaOH固体 D.加少量水
3. 非结合胆红素(VCB)分子中有羟基(—OH),被氧化后生成羧基(—COOH)与钙离子结合形成胆
红素钙,胆结石的形成与此反应有关。从动态平衡的角度分析能预防胆结石的方法是( )
A.大量食用纯碱可和钙离子沉淀完全,防止胆结石的生成
B.不食用含钙的食品
C.适量服用低维生素E、低维生素C等抗氧化自由基可以防止胆结石
D.手术切除胆囊是最好的方法
4. 可溶性钡盐有毒,医院中常用无毒硫酸钡作为内服“钡餐”造影剂。医院抢救钡离子中毒者时,
除催吐外,还需要向中毒者胃中灌入硫酸钠溶液。已知:某温度下,K (BaCO)=5.1×10-9,
sp 3
K (BaSO)=1.1×10-10。下列推断正确的是 ( )
sp 4
A.不用碳酸钡作为内服造影剂,是因为碳酸钡比硫酸钡更难溶
B.可以用0.36 mol·L-1的NaSO 溶液给钡离子中毒者洗胃
2 4
C.抢救钡离子中毒者时,若没有硫酸钠也可以用碳酸钠溶液代替
D.误饮c(Ba2+)=1.0×10-5 mol·L-1的溶液时,会引起钡离子中毒
5. 工业上用化学法除锅炉的水垢时,先向锅炉中注入饱和 NaCO 溶液浸泡,将水垢中的CaSO
2 3 4
转化为CaCO ,再用盐酸除去[已知:K (CaCO)=1×10-10,K (CaSO)=9×10-6]。下列说法错
3 sp 3 sp 4
误的是( )
A.温度升高,NaCO 溶液的K 和c(OH-)均会增大
2 3 W
B.沉淀转化的离子方程式为CO(aq)+CaSO(s) CaCO (s)+SO(aq)
4 3
C.该条件下,CaCO 的溶解度约为1×10-3 g
3
D.CaCO 和CaSO 共存的悬浊液中,=9×104
3 4
1
学科网(北京)股份有限公司6. HgS常作着色剂、防腐剂。不同温度下,HgS在水中的沉淀溶解平衡曲线如图所示。pHg=-
lg c(Hg2+),pS=-lg c(S2-)。下列说法正确的是( )
A.若HgS(s) Hg2+(aq)+S2-(aq) ΔH>0,则图像中T<20 ℃
B.图中各点对应的HgS K 大小关系:K (f)>K (c)=K (e)
sp sp sp sp
C.升高温度,f点的饱和溶液的组成由f点沿fd线向d方向移动
D.向d点溶液中加入少量KS固体,溶液组成由d点沿cde线向e方向移动
2
7. 化工生产中含Cu2+的废水常用MnS(s)作沉淀剂,其反应原理为Cu2+(aq)+MnS(s) CuS(s)
+Mn2+(aq)。下列有关该反应的推理不正确的是( )
A.该反应达到平衡时,c(Cu2+)=c(Mn2+)
B.CuS的溶解度比MnS的溶解度小
C.往平衡体系中加入少量Cu(NO )(s)后,c(Mn2+)变大
3 2
D.该反应平衡常数K=
8. 以MnO 为原料制得的MnCl 溶液中常含有Cu2+、Pb2+、Cd2+等金属离子,通过添加过量难溶
2 2
电解质MnS,可使这些金属离子形成硫化物沉淀,经过滤除去包括MnS在内的沉淀,再经蒸
发、结晶,可得纯净的MnCl 。根据上述实验事实,可推知MnS具有的相关性质是( )
2
A.具有吸附性
B.溶解度与CuS、PbS、CdS等相同
C.溶解度大于CuS、PbS、CdS的溶解度
D.溶解度小于CuS、PbS、CdS的溶解度
9. 已知25 ℃时,FeS、CuS的K 分别为6.3×10-18、1.3×10-36,HS的电离平衡常数K =9.1×10-8、
sp 2 a1
K =1.1×10-12,下列有关说法正确的是( )
a2
A.除去工业废水中的Cu2+可以选用FeS作沉淀剂
B.将足量CuSO 固体溶解在0.1 mol/L H S溶液中,Cu2+的最大浓度为1.3×10-35 mol/L
4 2
C.因为HSO 是强酸,所以反应CuSO +H S=== CuS↓+HSO 不能发生
2 4 4 2 2 4
D.向HS的饱和溶液中通入少量SO 气体,溶液的酸性增强
2 2
10.往锅炉中注入NaCO 溶液浸泡,将水垢中的CaSO 转化为CaCO ,再用盐酸去除,下列叙述
2 3 4 3
中正确的是( )
A.温度升高,Na CO 溶液的K 增大,c(OH-)减小
2 3 W
B.CaSO 能转化为CaCO ,说明K (CaCO)>K (CaSO)
4 3 sp 3 sp 4
C.CaCO 溶解于盐酸而CaSO 不溶,是因为硫酸酸性强于盐酸
3 4
D.沉淀转化的离子方程式为CO2- (aq)+CaSO (s) CaCO (s)+SO2- (aq)
3 4 3 4
11.二氧化碳的过量排放可对海洋生物的生存环境造成很大影响,其原理如下图所示。下列叙述错
误的是( )
2
学科网(北京)股份有限公司A.海水酸化能引起HCO-浓度增大、CO2-浓度减小
3 3
B.海水酸化能促进CaCO 的溶解,导致珊瑚礁减少
3
C.CO 能引起海水酸化,其原理为HCO- H++CO2-
2 3 3
D.使用太阳能、氢能等新能源可改善珊瑚的生存环境
12.工业上常先以MnO 为原料制得粗MnCl 溶液,通过添加过量难溶电解质MnS,使溶液中含有
2 2
的Cu2+、Pb2+、Cd2+等金属离子形成硫化物沉淀,经过滤除去包括MnS在内的沉淀,再经蒸发、
结晶,可得纯净的MnCl 。根据上述实验事实,下列分析正确的是( )
2
A.MnS的K 小于CuS、PbS、CdS等硫化物的K
sp sp
B.除杂试剂MnS也可用FeS代替
C.MnS与Cu2+反应的离子方程式是Cu2+(aq)+MnS(s) CuS(s)+Mn2+(aq)
D.整个过程中涉及的反应类型只有复分解反应
13.已知在pH为4~5的环境中,Cu2+、Fe2+几乎不水解,而Fe3+几乎完全水解。工业上制CuCl 溶
2
液是将浓盐酸加热到80 ℃左右,再慢慢加入粗氧化铜(含少量杂质FeO),充分搅拌使之溶解。
欲除去溶液中的杂质离子,下述方法中可行的是 ( )
A.向溶液中通入Cl,再加入纯净的CuO粉末调节pH为4~5
2
B.向溶液中通入HS使Fe2+沉淀
2
C.向溶液中通入Cl,再通入NH ,调节pH为4~5
2 3
D.加入纯Cu将Fe2+还原为Fe
14.粗制的CuSO ·5H O晶体中含有Fe2+。提纯时,为了除去Fe2+,常加入少量HO ,然后加入少
4 2 2 2
量碱至溶液pH=4,可以达到除去铁离子而不损失硫酸铜的目的。下列说法不正确的是( )
A.溶解CuSO ·5H O晶体时要加入少量稀HSO
4 2 2 4
B.加入HO,将Fe2+氧化,2Fe2++H O+2H+===2Fe3++2H O
2 2 2 2 2
C.由于CuSO 的催化作用,会使部分HO 分解而损失
4 2 2
D.调溶液pH=4的依据是Cu(OH) 比Fe(OH) 更难溶
2 3
15.绚丽多彩的无机颜料的应用曾创造了古代绘画和彩陶的辉煌。硫化镉(CdS)是一种难溶于水的
黄色颜料,其在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是( )
3
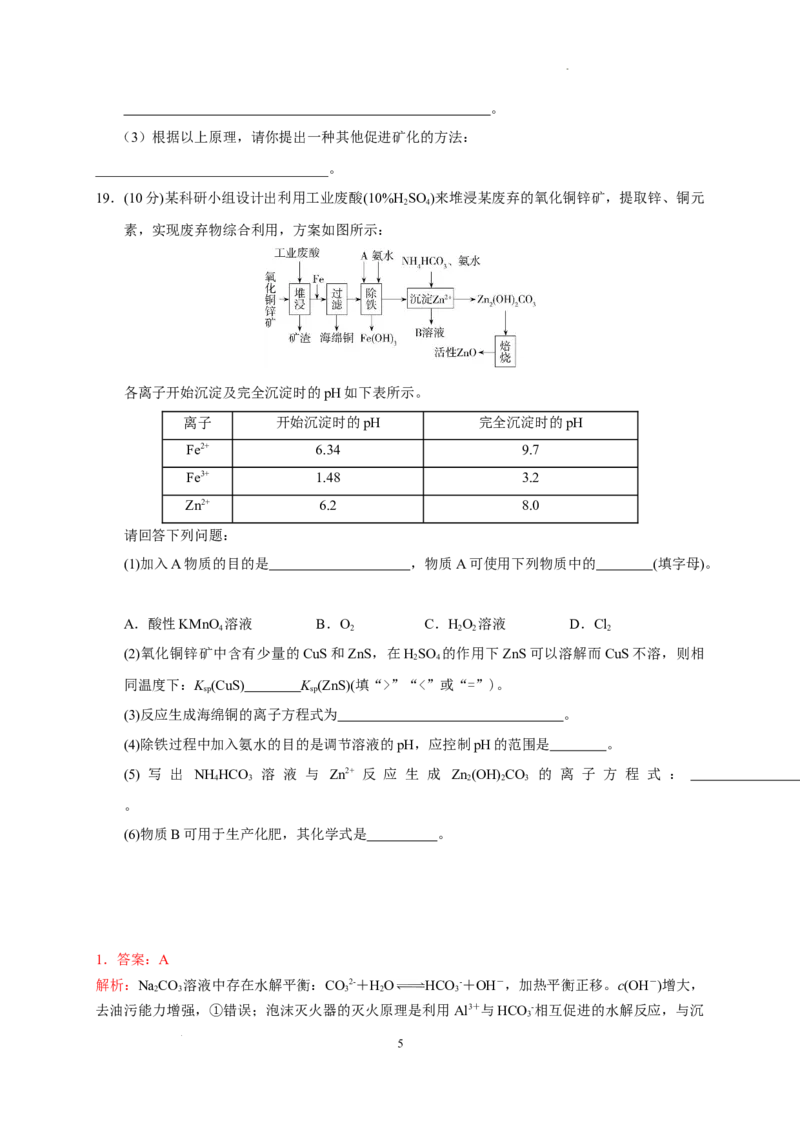
学科网(北京)股份有限公司A.图中a和b分别为T、T 温度下CdS在水中的溶解度
1 2
B.图中各点对应的K 的关系为:K (m)=K (n)”“<”或“=”)。
sp sp
(3)反应生成海绵铜的离子方程式为 。
(4)除铁过程中加入氨水的目的是调节溶液的pH,应控制pH的范围是 。
(5) 写 出 NH HCO 溶 液 与 Zn2+ 反 应 生 成 Zn(OH) CO 的 离 子 方 程 式 :
4 3 2 2 3
。
(6)物质B可用于生产化肥,其化学式是 。
1.答案:A
解析:NaCO 溶液中存在水解平衡:CO2-+HO HCO -+OH-,加热平衡正移。c(OH-)增大,
2 3 3 2 3
去油污能力增强,①错误;泡沫灭火器的灭火原理是利用Al3+与HCO -相互促进的水解反应,与沉
3
5
学科网(北京)股份有限公司淀溶解平衡原理无关,⑤错误;②、③、④均与沉淀溶解平衡有关。
2.答案:D
解析:Mg(OH) (s) Mg2+(aq)+2OH—(aq),加MgSO 固体使该溶解平衡左移,Mg(OH) 固体增
2 4 2
多,c(Mg2+)变大;加HCl溶液使该溶解平衡右移,Mg(OH) 固体减少,c(Mg2+)变大;加NaOH固
2
体使该溶解平衡左移,Mg(OH) 固体增多,c(Mg2+)变小。
2
3.答案:C
解析:预防胆结石的生成,就是防止羟基(一OH)被氧化后生成羧基与钙离子结合形成沉淀。所以
适量服用抗氧化自由基的药物可以预防胆结石的生成。答案:C
4.答案:B
解析:碳酸钡能与胃酸反应生成可溶性钡盐,钡离子有毒,所以不能用碳酸钡作为内服造影剂,A
1.1×10-10
错误;用 0.36 mol·L-1 的 NaSO 溶液给钡离子中毒者洗胃,反应后 c(Ba2+)=
2 4 0.36
mol·L-1≈3.1×10-10 mol·L-1< mol·L-1,B正确;碳酸钡与胃酸反应转化为可溶性钡盐,
❑√1.1×10-10
起不到解毒的作用,C 错误;饱和 BaSO 溶液中 c(Ba2+)= =
4 ❑√K (BaSO ) ❑√1.1×10-10
sp 4
mol·L-1>1.0×10-5 mol·L-1,所以误饮c(Ba2+)=1.0×10-5 mol·L-1的溶液时,不会引起钡离子中毒,D错
误。
5.答案:C
解析:K (CaCO)=1×10-10,c(CaCO)=1×10-5 mol·L-1,S=×100 g=1.0×10-4 g,C项错误。
sp 3 3
6.答案:B
解析:因HgS的溶解过程是吸热过程,分析题图可知,温度为T时HgS的K 较大,故温度T高于
sp
20 ℃,A项错误;溶度积只与温度有关,c、e点对应温度相同,故两点处HgS的K 相等,f点
sp
HgS的K 较c、e点大,B项正确;降低温度,f点的饱和溶液的组成由f点沿fd线向d方向移动,
sp
C项错误;向d点溶液中加入少量KS固体,溶液组成由d点沿edc线向c方向移动,D项错误。
2
7.答案:A
解析:依据沉淀的转化条件溶解度大的向溶解度小的转移,B选项正确;C选项,加入Cu(NO )(s)
3 2
后平衡右移,正确;反应平衡常数K==,可知D选项正确。答案:A
8.答案:C
解析:添加过量的MnS是为了除去MnCl 溶液中的Cu2+、Pb2+、Cd2+,为了不引入MnS杂质,
2
MnS应该具有难溶的性质,但又能提供 S2-,以便与Cu2+、Pb2+、Cd2+结合,所以MnS的溶解度
应大于CuS、PbS、CdS。答案:C
9.答案:A
解析:CuS比FeS难溶,除去工业废水中的Cu2+可以选用FeS作沉淀剂,A正确;HS是弱酸,0.1
2
6
学科网(北京)股份有限公司mol/L的HS溶液中硫离子的最大浓度为0.1 mol/L,CuS的K 为1.3×10-36,所以溶液中Cu2+的最小
2 sp
浓度为1.3×10-35 mol/L,B错误;CuSO +H S===CuS↓+H SO 能够发生,C错误;HS与SO 反应生
4 2 2 4 2 2
成单质硫和水,氢离子浓度减小,溶液的酸性减弱,D错误。
10.答案:D
解析:温度升高,促进水的电离,K 增大;温度升高,促进NaCO 的水解,溶液中c(OH-)增大,
W 2 3
A项错误。K (CaCO)Cu知,D错误。
4
14.答案:D
解析:为防止 Cu2+水解生成 Cu(OH) 使溶液变浑浊,溶解 CuSO ·5H O 晶体时要加入少量稀
2 4 2
HSO ,A项正确;HO 具有强氧化性,能与Fe2+发生氧化还原反应,即2Fe2++H O+2H+===2Fe3+
2 4 2 2 2 2
+2H O,B项正确;HO 在CuSO 催化下可发生分解反应,C项正确;溶液pH=4时,Fe3+可水解生
2 2 2 4
成Fe(OH) 而除去,即Fe(OH) 比Cu(OH) 更难溶,D项错误。
3 3 2
15.答案:B
解析:CdS在水中达到溶解平衡时Cd2+、S2-浓度相等,可求出一定温度下CdS在水中的溶解度,A
项正确;m、p、n为同一温度下的CdS的溶解平衡状态,三点的K 相等,B项错误;向m点溶液
sp
7
学科网(北京)股份有限公司中加入NaS,S2-浓度增大,但K 不变,则溶液组成由m沿T 时的平衡曲线向p方向移动,C项正
2 sp 1
确;温度降低,K 减小,q沿qp线向p方向移动,D项正确。
sp
16.答案:(1)K =c2(Ag+)·c(S2-) (2)④
sp
(3)加足量MgCl 溶液,充分搅拌,过滤,洗涤即得纯Mg(OH)
2 2
解析:(2)①Cl-抑制AgCl溶解,正确;②物质的溶解大多是吸热的,正确;③正确;④除去溶液
中的Mg2+,用OH-沉淀比用CO好,是因为Mg(OH) 的K 更小,剩余的Mg2+更少,错误;⑤正
2 sp
确。
17.答案: (1)5 (2)2.2×10-8 0.20
解析:(1)K =c(Cr3+)·c3(OH-)=10-32,则c(OH-)== mol·L-1=10-9 mol·L-1,
sp
c(H+)==mol·L-1=10-5 mol·L-1,pH=–lg c(H+)=–lg 10-5=5。 (2)pH=8时c(OH–)=10-6
mol·L-1,由氢氧化铜的溶度积常数可知:K =2.2×10-20=10-12 ×c(Cu2+),得 c(Cu2+)=2.2×10-8
sp
mol·L-1;使Cu2+完全沉淀为CuS,已知c(Cu2+)=0.10 mol·L-1,根据反应关系式:Cu2+~2H+得
c(H+)=0.20 mol·L-1。
18.答案:(1)有机羧酸电离出H+与Ca (PO )OH电离出的OH−发生反应:H++OH−===HO,使
5 4 3 2
Ca (PO )OH的溶解平衡向右移动 (2)F−与Ca (PO )OH溶解产生的Ca2+、 发生反应生成更
5 4 3 5 4 3
难溶的Ca (PO )F:5Ca2++3 +F−===Ca (PO )F↓(3)在牙膏中加Ca2+,使题中溶解平衡向左移
5 4 3 5 4 3
动
19.答案:(1)将Fe2+氧化成Fe3+,方便后续生成沉淀除去 BC (2)<
(3)Fe+Cu2+===Fe2++Cu (4)3.2≤pH<6.2
(5)2Zn2++4HC ===Zn(OH) CO↓+H O+3CO↑ (6)(NH )SO
O- 2 2 3 2 2 4 2 4
3
解析:(1)根据表中数据可知Fe3+易被除去,将Fe2+氧化成Fe3+,以便除去;除铁过程中加入A和氨
水,使Fe2+变成Fe(OH) 沉淀,故A应为氧化剂,为不引入新的杂质,应选BC。(2)相同条件下,溶
3
解度大的物质先溶解,结合在 HSO 作用下 ZnS 可溶解而 CuS 不溶,则相同温度下:
2 4
8
学科网(北京)股份有限公司K (CuS)