文档内容
第二单元 海水中的重要元素——钠和氯
第三节 物质的量(一)
一、基础巩固
1.已知N 是阿伏加德罗常数的值,下列说法正确的是( )
A
A.22.4L甲烷分子所含质子数为10N
A
B.标准状况下,22.4L二氯甲烷的分子数约为N 个
A
C.1mol苯分子中含有的碳碳单键数为6N
A
D.常温常压下,28.0g乙烯和丁烯的混合气体中含有的碳原子数目为2N
A
2.N 表示阿伏加德罗常数的值。下列叙述正确的是( )
A
A.22.4L H 与2mol I 反应生成HI的分子数为2N
2 2 A
B.5.6g铁与足量稀硝酸反应转移的电子数为0.2N
A
C.32g氧气与32g硫所含的质子数相等
D.1L 0.1mol•L﹣1NH H PO 溶液中阴阳离子数相等
4 2 4
3.N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.50mL 18.4mol•L﹣1浓硫酸与足量铜微热反应,生成SO 分子的数目为0.46N
2 A
B.含N 个Na+的Na O溶解于1L水中,所得溶液中Na+的物质的量浓度为1mol•L﹣1
A 2
C.在H O +Cl ═2HCl+O 反应中,每生成32g氧气,则转移2N 个电子
2 2 2 2 A
D.常温下,1L 0.50mol•L﹣1NH Cl溶液与2L 0.25mol•L﹣1NH Cl溶液所含NH +物质的量相同
4 4 4
4.设N 为阿伏加德罗常数的值,下列说法不正确的是( )
A
A.一定条件下,合成氨反应中有0.5mol N 发生反应,则反应中转移电子数为3N
2 A
B.10克环己烷与2﹣丙醇的混合液中,碳元素的质量分数为72%,则其中所含的氧原子数目为 N
A
C.过量铜与含0.4mol HNO 的浓硝酸反应,则反应中电子转移数为0.2N
3 A
D.常温常压下有28g单晶硅晶体,则其中所含的Si﹣Si键数目为2N
A
5.设N 表示阿伏加德罗常数的值,下列说法正确的是( )
A
A.1L0.1mol•L﹣1氨水中含有0.1N NH 分子
A 3B.46g NO 和N O 混合气体中含有的原子数为3N
2 2 4 A
C.1mol Na O 中含有的阴离子数为2N
2 2 A
D.常温常压下,12g14C所含中子数为6N
A
6.摩尔是( )
A.物质中所含的微粒数
B.表示物质质量的单位
C.表示物质的量的单位
D.既是物质的数量单位又是物质质量的单位
7.(1)同温同压下,同体积的N 和SO 分子数之比为 ,物质的量之比为 ,原子总数之比
2 2
为 ,摩尔质量之比为 ,质量之比为 ,密度之比为 。
(2)现有质量比为11:14的CO 和CO的混合气体,则该混合气体中的CO 和CO物质的量之比为
2 2
,碳原子和氧原子的个数比为 ,该混合气体的摩尔质量为 。
(3)12.4gNa X中含Na+0.4mol,则Na X的摩尔质量是 ,X的相对原子质量是 。
2 2
(4)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,
11.2L“人造空气”的质量是4.8g,其中氧气和氦气的分子数之比是 ,氧气的质量是 。
(5)某元素的一个原子的质量为ag,一个12C原子的质量为bg,阿伏加德罗常数为N ,则该原子的
A
相对原子质量数值可表示为 或 。
二、拓展提升
8.(1)在25℃、101 kPa的条件下,相同质量的CH 和A气体的体积之比是15:8,则A的摩尔质量为
4
。
(2)两个相同容积的密闭容器X、Y,在25℃下,X中充入a g A气体,Y中充入a g CH 气体,X与
4
Y内的压强之比是4:11,则A的摩尔质量为 。
9.根据所学知识,回答下列问题:
(1)在配制 500mL 0.1mol•L﹣1硫酸亚铁溶液时,需要称量绿矾晶体(FeSO •7H O) 的质量为
4 2
。
(2)标准状况下,672mLSO 的物质的量是 mol,质量是 g;标准状况下,9.03×1023个H 分
2 2
子的物质的量是 mol,体积约为 L。
(3)胶体和溶液的本质区别是 。
A.能否发生电泳
B.分散质粒子直径大小不同
C.能否发生丁达尔效应10. 化学实验是科学探究过程中的一种重要方法,掌握化学实验的基本操作和物质的制备、转化及性质的
探究尤为重要,请结合所学化学实验知识回答以下问题。
Ⅰ.实验室配制220mL 1 mol•L﹣1的稀H SO 溶液:
2 4
(1)用量筒量取浓H SO (密度为1.84g•mL﹣1,质量分数为98%)的体积为 mL。
2 4
(2)误差分析:下列情况使配制结果偏大的是 。
①溶解后未冷却即转移、定容
②定容时仰视容量瓶刻度线
③用量筒量取一定体积的浓硫酸时俯视
④将量筒、烧杯、玻璃棒洗涤2~3次,转移至容量瓶
Ⅱ. 某研究性学习小组在查阅资料时发现:化工厂常用氨气来检验氯气是否泄漏。于是他们设计实验
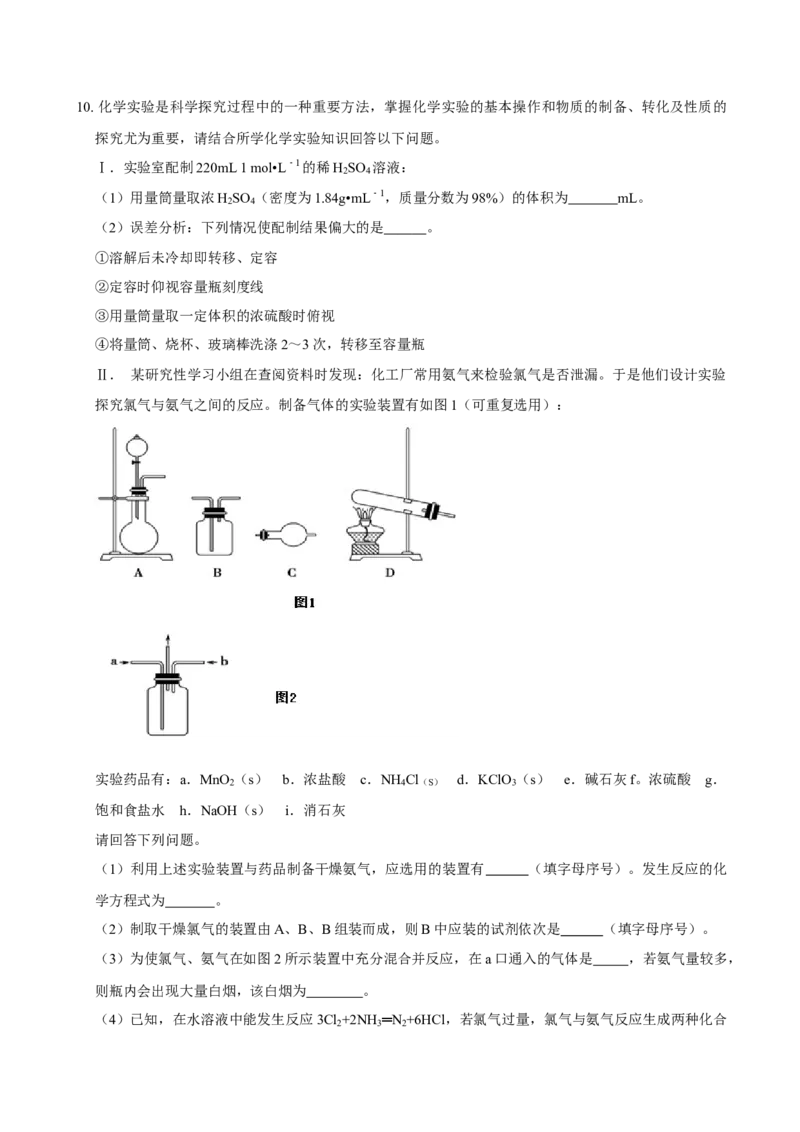
探究氯气与氨气之间的反应。制备气体的实验装置有如图1(可重复选用):
实验药品有:a.MnO
2
(s) b.浓盐酸 c.NH
4
Cl(S) d.KClO
3
(s) e.碱石灰f。浓硫酸 g.
饱和食盐水 h.NaOH(s) i.消石灰
请回答下列问题。
(1)利用上述实验装置与药品制备干燥氨气,应选用的装置有 (填字母序号)。发生反应的化
学方程式为 。
(2)制取干燥氯气的装置由A、B、B组装而成,则B中应装的试剂依次是 (填字母序号)。
(3)为使氯气、氨气在如图2所示装置中充分混合并反应,在a口通入的气体是 ,若氨气量较多,
则瓶内会出现大量白烟,该白烟为 。
(4)已知,在水溶液中能发生反应3Cl +2NH ═N +6HCl,若氯气过量,氯气与氨气反应生成两种化合
2 3 2物,其中一种化合物分子的空间构型与NH 相似,则该反应的化学方程式为 。
3