文档内容
《化学反应限度》小测验
限时:45分钟 总分:100分
一、选择题(每小题4分,共48分,每小题有1个正确选项)
1.下列对可逆反应的认识正确的是( )
A.SO+Br+2HO===HSO+2HBr与2HBr+HSO(浓)===Br+SO↑+2HO互为可逆反应
2 2 2 2 4 2 4 2 2 2
B.既能向正反应方向进行,又能向逆反应方向进行的反应叫可逆反应
C.在同一条件下,同时向正、逆两个方向进行的反应叫可逆反应
D.电解水生成氢气和氧气与氢气和氧气点燃生成水的反应是可逆反应
2.下列说法正确的是( )
A.密闭容器中充入1 mol N 和3 mol H 可生成2 mol NH
2 2 3
B.一定条件下,可逆反应达到平衡状态,该反应就达到了这一条件下的最大限度
C.对于任何反应增大压强,化学反应速率均增大
D.化学平衡是一种动态平衡,条件改变,原平衡状态不会被破坏
3.在一定温度时,将1 mol A和2 mol B放入容积为5 L的某密闭容器中发生如下反应:
A(s)+2B(g) C(g)+2D(g),经5 min后,测得容器内B的浓度减少了0.2 mol·L-1。则下列
叙述不正确的是( )
A.在5 min内该反应用C的浓度变化表示的反应速率为0.02 mol·(L·min)-1
B.在5 min时,容器内D的浓度为0.2 mol·L-1
C.该可逆反应随反应的进行,容器内压强逐渐增大
D.5 min时容器内气体总的物质的量为3 mol
4.一定条件下,可逆反应2A(g)B(g)+3C(g),下列四项中处于平衡状态的是( )
正反应速率 逆反应速率
A v(A)=2 mol/(L·min) v(B)=2 mol/(L·min)
B v(A)=2 mol/(L·min) v(C)=2 mol/(L·min)
C v(A)=1 mol/(L·min) v(B)=2 mol/(L·min)
D v(A)=1 mol/(L·min) v(C)=1.5 mol/(L·min)
5.可逆反应2NO(g) 2NO(g)+O(g)在体积固定的密闭容器中,达到平衡状态的标志是( )
2 2
①单位时间内生成n mol O 的同时生成2n mol NO
2 2
②单位时间内生成n mol O 的同时生成2n mol NO
2
③用NO、NO、O 表示的反应速率的比为2∶2∶1的状态
2 2
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的平均相对分子质量不再改变的状态
A.①④⑥⑦ B.②③⑤⑦ C.①③④⑤ D.全部
6.下列关于物质“反应程度”的说法正确的是( )
A.一定条件下,2 mol SO 与足量O 反应可得到2 mol SO
2 2 3
B.含4 mol HCl的浓盐酸与足量的MnO 加热反应可制备1 mol Cl
2 2
1
学科网(北京)股份有限公司C.10 mL 18.0 mol/L HSO 与足量铜加热反应可制备0.09 mol SO
2 4 2
D.一定条件下,1 mol N 与3 mol H 反应可制备1.0 mol NH
2 2 3
7.2SO(g)+O(g)2SO(g)是制备硫酸的重要反应。下列叙述正确的是( )
2 2 3
A.催化剂VO 不改变该反应的逆反应速率
2 5
B.升高反应体系的温度,反应速率一定增大
C.因该反应是放热反应,所以降低温度将缩短反应达到平衡的时间
D.在t、t时刻,O(g)的浓度分别是c、c,则时间间隔t~t内,SO(g)生成的平均速率为v=
1 2 2 1 2 1 2 3
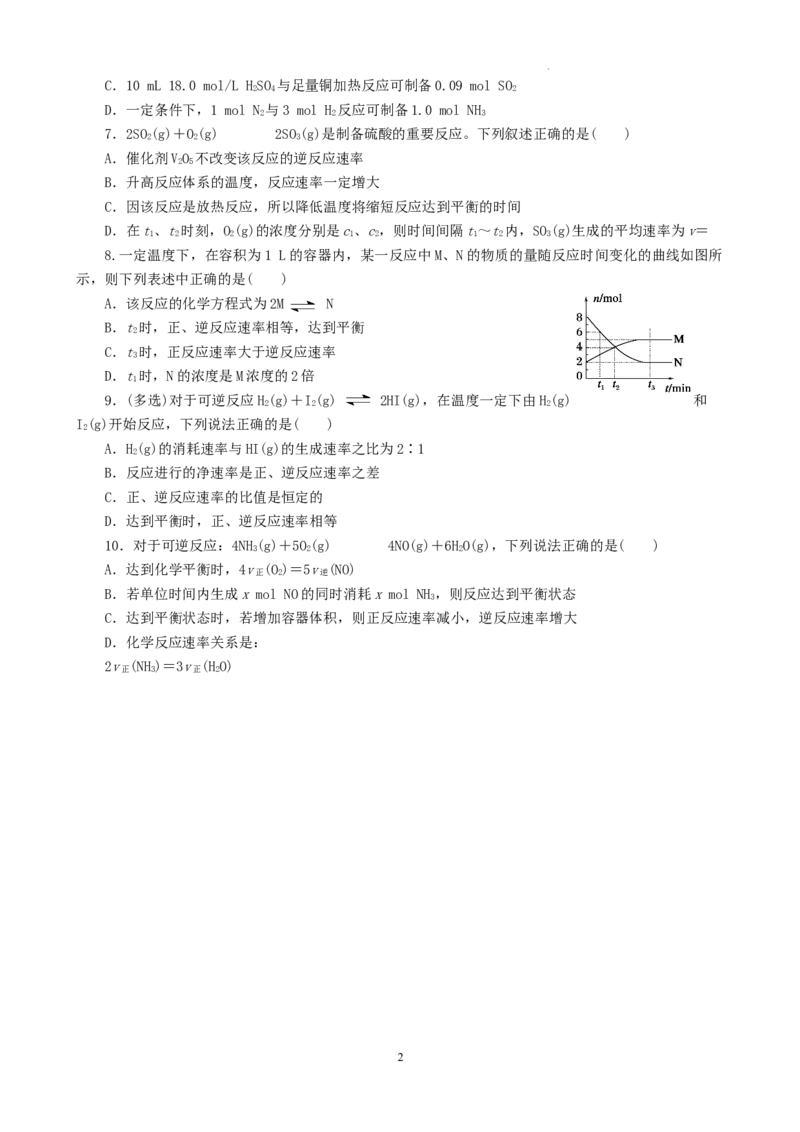
8.一定温度下,在容积为1 L的容器内,某一反应中M、N的物质的量随反应时间变化的曲线如图所
示,则下列表述中正确的是( )
A.该反应的化学方程式为2M N
B.t时,正、逆反应速率相等,达到平衡
2
C.t时,正反应速率大于逆反应速率
3
D.t时,N的浓度是M浓度的2倍
1
9.(多选)对于可逆反应H(g)+I(g) 2HI(g),在温度一定下由H(g) 和
2 2 2
I(g)开始反应,下列说法正确的是( )
2
A.H(g)的消耗速率与HI(g)的生成速率之比为2∶1
2
B.反应进行的净速率是正、逆反应速率之差
C.正、逆反应速率的比值是恒定的
D.达到平衡时,正、逆反应速率相等
10.对于可逆反应:4NH(g)+5O(g)4NO(g)+6HO(g),下列说法正确的是( )
3 2 2
A.达到化学平衡时,4v (O)=5v (NO)
正 2 逆
B.若单位时间内生成x mol NO的同时消耗x mol NH,则反应达到平衡状态
3
C.达到平衡状态时,若增加容器体积,则正反应速率减小,逆反应速率增大
D.化学反应速率关系是:
2v (NH)=3v (HO)
正 3 正 2
2
学科网(北京)股份有限公司11.在372K时,把0.5molNO 通入体积为5L的真空密闭容器中,立即出现红棕色。反应进行到 2s
2 4
时,NO 的浓度为 0.02mol·L-1。在60s时,体系已达平衡,此时容器内压强为开始时的 1.6倍。下列说
2
法正确的是( )
A. 前2s以NO 的浓度变化表示的平均反应速率为0.01mol·L-1·s-1
2 4
B. 在2s时体系内压强为开始时的1.1倍
C. 在平衡时体系内含有NO0.25mol
2 4
D. 平衡时,NO 的转化率为40%
2 4
12.在一个6L的密闭容器中放入3mol X和2molY,在一定条件下发生反应4X(g)+3Y(g) 2Q(g)
+nR(g),达到平衡后,容器内的压强比原来增加5%,X浓度减小,则该反应方程式中的n值是( )
A.3 B.4 C.5 D.6
二、填空题(共52分)
13.(12分)t℃时,将2 mol SO 和1 mol O 通入体积为2 L的恒温恒容密闭容器中,发生如下反应:
2 2
2SO(g)+O(g) 2SO(g),2 min时反应达到平衡,此时测得反应物O 还剩余0.8 mol,请填写下列空
2 2 3 2
白:
(1)从反应开始到化学平衡,生成SO 的平均反应速率为________;平衡时SO 转化率为________。
3 2
(2)下列叙述能说明该反应已达到化学平衡状态的是________。
A.容器内压强不再发生变化
B.SO 的体积分数不再发生变化
2
C.容器内气体原子总数不再发生变化
D.相同时间内消耗2n mol SO 的同时消耗n mol O
2 2
E.相同时间内消耗2n mol SO 的同时生成n mol O
2 2
(3)t℃时,若将物质的量之比为1∶1的SO 和O 混合气体通入一个恒温恒压的密闭容器中,反应达
2 2
到平衡时,混合气体体积减少了20%。SO 的转化率为________。
2
14.(12分)在某一容积为5 L的密闭容器内,加入0.2 mol 的CO和0.2 mol的HO(g),在催化剂存
2
在的条件下高温加热,发生如下反应:CO(g)+HO(g)CO(g)+H(g),反应放出热量。反应中CO
2 2 2 2
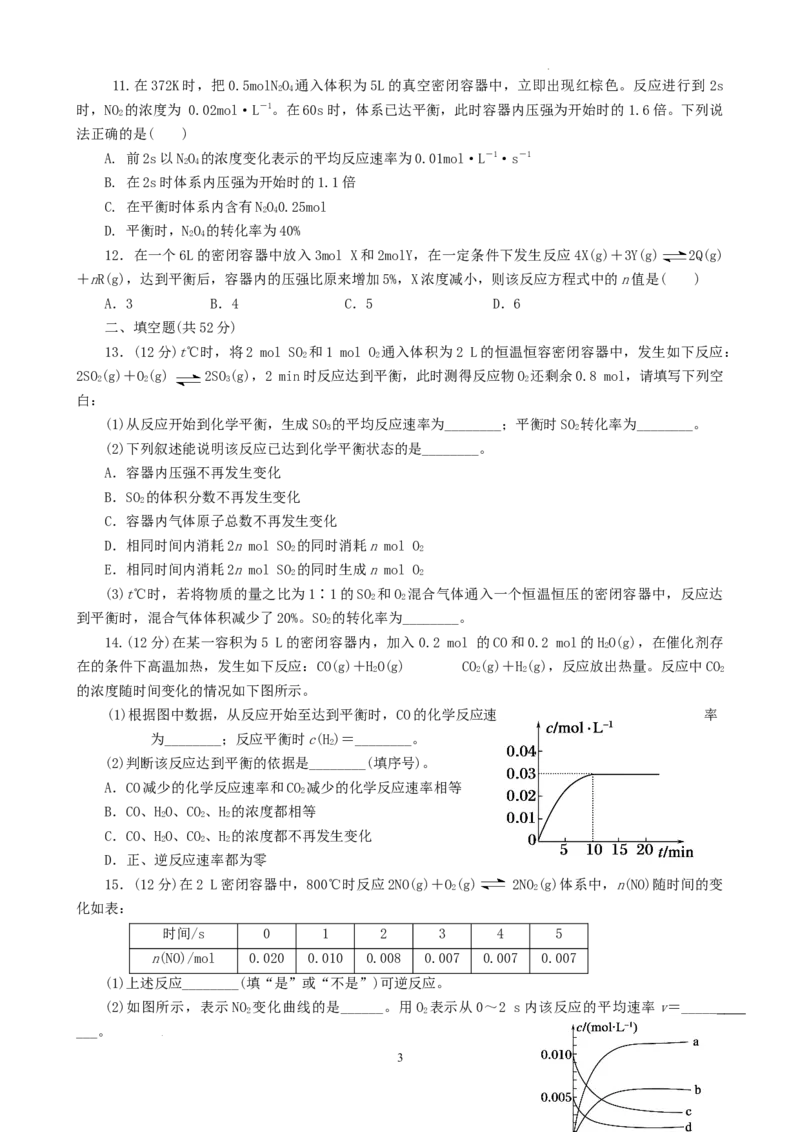
的浓度随时间变化的情况如下图所示。
(1)根据图中数据,从反应开始至达到平衡时,CO的化学反应速 率
为________;反应平衡时c(H)=________。
2
(2)判断该反应达到平衡的依据是________(填序号)。
A.CO减少的化学反应速率和CO 减少的化学反应速率相等
2
B.CO、HO、CO、H 的浓度都相等
2 2 2
C.CO、HO、CO、H 的浓度都不再发生变化
2 2 2
D.正、逆反应速率都为零
15.(12分)在2 L密闭容器中,800℃时反应2NO(g)+O(g) 2NO(g)体系中,n(NO)随时间的变
2 2
化如表:
时间/s 0 1 2 3 4 5
n(NO)/mol 0.020 0.010 0.008 0.007 0.007 0.007
(1)上述反应________(填“是”或“不是”)可逆反应。
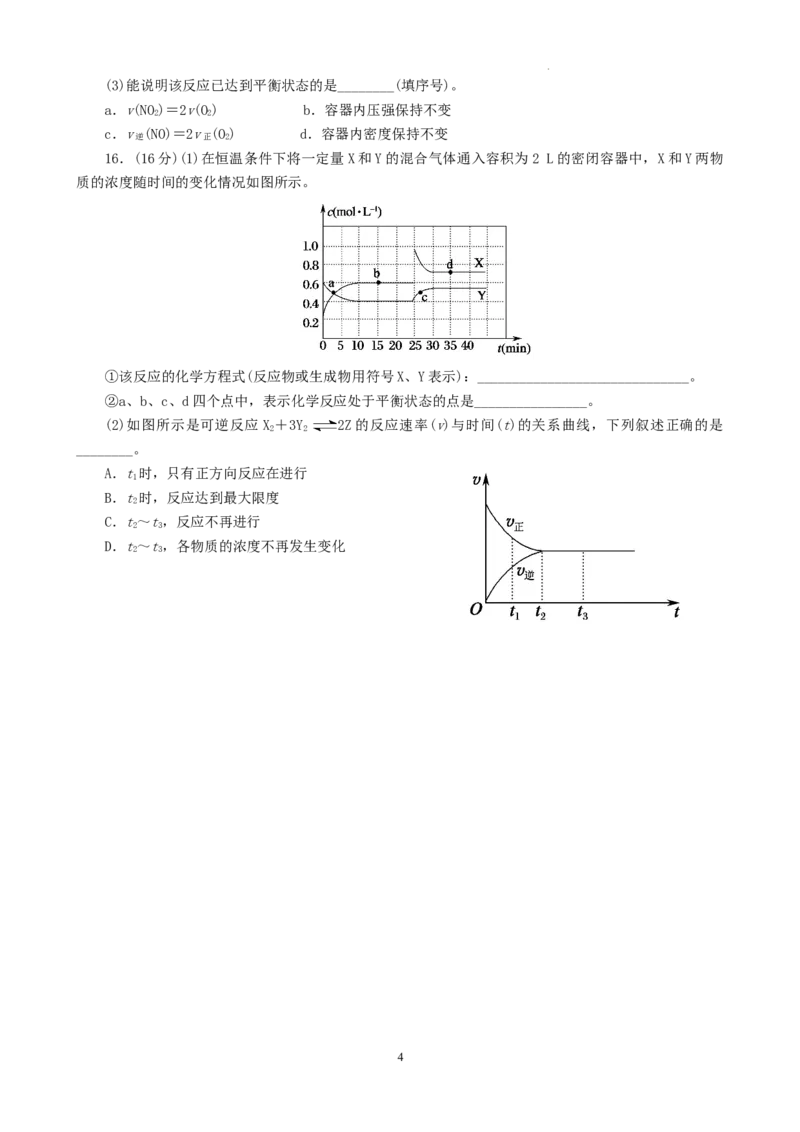
(2)如图所示,表示NO 变化曲线的是______。用O 表示从0~2 s内该反应的平均速率v=_____
2 2
___。
3
学科网(北京)股份有限公司(3)能说明该反应已达到平衡状态的是________(填序号)。
a.v(NO)=2v(O) b.容器内压强保持不变
2 2
c.v (NO)=2v (O) d.容器内密度保持不变
逆 正 2
16.(16分)(1)在恒温条件下将一定量X和Y的混合气体通入容积为2 L的密闭容器中,X和Y两物
质的浓度随时间的变化情况如图所示。
①该反应的化学方程式(反应物或生成物用符号X、Y表示):______________________________。
②a、b、c、d四个点中,表示化学反应处于平衡状态的点是________________。
(2)如图所示是可逆反应X +3Y 2Z的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是
2 2
________。
A.t时,只有正方向反应在进行
1
B.t时,反应达到最大限度
2
C.t~t,反应不再进行
2 3
D.t~t,各物质的浓度不再发生变化
2 3
4
学科网(北京)股份有限公司答案
1.C 理解好可逆反应定义中的“同一条件下”“同时”“正、逆两个方向”等关键字眼。
2.B N 和H 生成NH 的反应为可逆反应,1 mol N 和3 mol H 不能完全反应生成2 mol NH ,A项错;
2 2 3 2 2 3
压强是影响化学反应速率的一个因素,但并不适合于所有的反应,必须有气体参与的反应才适合,C不正
确;化学平衡是一种动态平衡,该平衡是建立在一定条件下的平衡,如果条件改变,平衡将发生移动,D
项不正确。
3.D 根据题意,可以计算v(B)=0.04 mol·(L·min)-1,则v(C)=0.02 mol·(L·min)-1,A正确。
5 min时,c(C)=0.1 mol·L-1,则c(D)=0.2 mol·L-1,B正确。该反应为气体物质的量增加的反应,
随反应的进行,容器内压强增大,C正确。5 min时,Δn(B)=0.2 mol·L-1×5 L=1 mol,Δn(C)=0.5
mol,Δn(D)=1 mol。因此气体的物质的量为2 mol-1 mol+0.5 mol+1 mol=2.5 mol,D说法错误。
4.D 可逆反应达到平衡状态时,正逆反应的反应速率相等,即用不同物质表示的化学反应速率之
比应等于化学方程式中的化学计量数之比,只有D正确。
5.A ②中均表示的是正反应速率,不能说明v(正)、v(逆)是否相等;③中反应的任意时刻用NO 、
2
NO、O 表示的反应速率之比均为2∶2∶1;⑤中根据质量守恒定律和ρ= 可知反应过程中混合气体的密
2
度一直不变化。
6.D 因为SO 与O 的反应、N 与H 的反应都是可逆反应,反应物不可能完全转化为生成物,故A不
2 2 2 2
正确,D正确;MnO 只能与浓盐酸反应制取Cl ,含4 mol HCl的浓盐酸与足量MnO 反应产生的Cl 将少于
2 2 2 2
1 mol,B也不正确。
7.B 加入催化剂同时改变正、逆反应速率,A不正确;升高温度,化学反应速率一定加快,B正确;
降低温度,使反应速率降低,将增大反应达到平衡的时间,C不正确;t~t时间段内,SO(g)的生成速
1 2 3
率为v=,D不正确。
8.D 反应达到平衡时M增加了3 mol,N减小了6 mol,所以该反应的化学方程式为2NM,A
项错误;t时M、N的浓度相等,但是正、逆反应速率不相等,故未达到平衡,B项错误;t时,M、N的
2 3
浓度不再变化,正反应速率等于逆反应速率,达到平衡状态,C项错误;t时,N的浓度为6 mol·L-1,M
1
的浓度为3 mol·L-1,D项正确。
9.BD 速率之比等于各物质的化学计量数之比,H(g)的消耗速率与HI(g)的生成速率比为1∶2,A
2
项错误。刚开始时,正反应速率最大,逆反应速率为 0,随着反应的进行,正反应速率逐渐减小,逆反应
速率逐渐增大,二者的比值是变化的,C项错误。净速率是正、逆反应速率之差,B项正确。正、逆反应
速率相等是化学反应达到平衡的标志,D项正确。
10.A 根据反应速率之比等于化学方程式的计量数之比有:
4v (O)=5v (NO),所以4v (O)=5v (NO)时表示化学反应达到平衡,故A项正确;生成NO、消
正 2 正 正 2 逆
耗NH 均为正反应的变化,未表示逆反应的变化情况,故 B项错误;由于反应物、生成物均为气体,所以
3
增加容器体积,正反应速率和逆反应速率都会减小,故C项错误;因为v (NH)∶v (HO)=2∶3,即3v
正 3 正 2
(NH)=2v (HO),故D项错误。
正 3 正 2
11. B NO 和NO 存在如下转化关系
2 4 2
NO2NO,前2s时
2 4 2
NO 2NO
2 4 2
起始(mol) 0.5 0
5
学科网(北京)股份有限公司反应(mol) 0.05 0.02×5
2s时(mol) 0.5-0.05 0.02×5
v(NO)==0.005mol·L-1·s-1
2 4
气体总的物质的量为0.5mol-0.05mol+0.02mol·L-1×5L=0.55mol。
2s时与开始的压强之比为p(2s)∶p(始)=0.55∶0.5=1.1∶1。
60 s达到平衡时,设参加反应的NO 的物质的量为x。则有
2 4
NO2NO
2 4 2
起始(mol) 0.5 0
反应(mol) x 2x
平衡(mol) 0.5-x 2x
平衡时,气体总的物质的量为0.5 mol-x+2x=0.5 mol+x,所以有=1.6,解得x=0.3 mol。平
衡体系中含0.2 mol NO,NO 的转化率为×100%=60%。
2 4 2 4
12. D 解法一:平衡体系存在于一个恒容的容器中,据阿伏加德罗定律气体的物质的量之比等于压
强之比。压强比原来增加5%,说明物质的量比原来增加5%,设初态有3molX和2molY,X浓度减小1/3,
说明反应中消耗X的物质的量为1 mol,据方程式由差量法可知当消耗4mol X,气体物质的量增加(2+n)
-(4+3)=n-5,所以(n-5)/4=(2+3)×5%,解得n=6。
解法二:仔细审题可知反应是一个物质的量增加的反应则有4+3<2+n,分析选项知只有选D符合题
意。所以在做选择题时对于有数据似乎需要计算的题目,不要忙于按常规计算,应分析选项直接求解。
13.(1)0.1 mol·L-1·min-1 20% (2)ABE (3)80%
解析:(1) 2SO(g)+O(g)2SO(g)
2 2 3
起始浓度(mol·L-1) 1 0.5 0
转化浓度(mol·L-1) 0.2 0.1 0.2
平衡浓度(mol·L-1) 0.8 0.4 0.2
v(SO)==0.1 mol·L-1·min-1 α(SO)=×100%=20%
3 2
(3)设SO 、O 的物质的量均为1 mol,反应过程中减小了0.4 mol,即反应了0.8 mol SO ,SO 的转
2 2 2 2
化率为80%。
14.(1)0.003 mol·(L·min)-1
0.03 mol·L-1 (2)AC
解析:(1)由图可知第10 min时反应达到平衡,所以v(CO)=v(CO)===0.003 mol·(L·min)-1,
2
反应时转化的浓度之比=化学方程式的化学计量数之比,所以Δc(H)=Δc(CO)=0.03 mol·L-1。
2
(2)达到平衡的标志是各物质的百分含量保持一定,浓度不变,正、逆反应速率相等且不为0。
15.(1)是
(2)b 1.5×10-3 mol·(L·s)-1 (3)bc
解析:(1)该反应是可逆反应。
(2)由平衡体系2NO(g)+O(g)2NO(g)知,NO 为生成物,n(NO)=Δn(NO)=0.020 mol-
2 2 2 2
0.007 mol=0.013 mol
c(NO)==0.006 5 mol·L-1
2
故表示NO 变化曲线的为b。
2
v(NO)====0.003 mol·(L·s)-1,
则v(O)=v(NO)=0.001 5 mol·(L·s)-1。
2
6
学科网(北京)股份有限公司(3)a项中未指明正、逆反应速率,故无法说明该反应是否达到平衡状态;由于该反应是反应前后气
体体积不相等的反应,当容器内压强保持不变时,说明该反应已达到平衡状态,故b项正确;c项中已说
明正、逆反应速率相等,故说明该反应已达到平衡状态;由于气体总质量不变,气体总体积也不变,因
此,无论该反应是否达到平衡,容器内密度保持不变,故d项无法说明该反应是否达到平衡状态。
16.(1)①Y2X ②bd (2)BD
解析:(1)从浓度变化趋势来看,X为生成物,Y为反应物。15 min时X增加了0.4 mol·L-1,Y减小
了0.2 mol·L-1,故X、Y的化学计量数之比为2∶1,10~25 min内,X、Y的浓度不发生变化,达到化学
平衡状态,则该反应为可逆反应,反应方程式为Y2X。b、d两点处于化学平衡状态。(2)对于可逆反
应,反应开始后的任何时刻,正、逆反应均在进行。根据图象可知 0~t反应处于非平衡状态,t后,正、
2 2
逆反应速率相等,但不等于0;处于平衡状态时,各物质的浓度不再发生变化,故B、D正确。
7
学科网(北京)股份有限公司8
学科网(北京)股份有限公司