文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
2024年九年级中考化学专题复习:溶液的形成
一、选择题
1.下列叙述中,正确的是
A.复分解反应前后物质种类都是化合物
B.含有氧元素的化合物一定是氧化物
C.溶液一定是均一、稳定、无色的混合物
D.催化剂一定能加快化学反应速率
2.如图所示,室温下,盛有水的烧杯内放置了两支试管甲和乙,试管甲和乙分别盛放
的是KNO 饱和溶液和一定溶质质量分数的石灰水。向烧杯内的水中加入NaOH固体
3
后,乙中观察到变浑浊的现象。(不考虑溶剂蒸发)下列说法正确的是:
A.加入NaOH固体前,石灰水一定是饱和溶液
B.加入NaOH固体后,甲中溶质质量分数会变小
C.若加入的固体是NH NO ,甲中一定有固体析出
4 3
D.实验后,将甲乙试管中溶液倒一起,硝酸钾溶液仍为饱和溶液
3.在一定温度下,将ag食盐溶于bg水中,待完全溶解后,再加入cg硝酸钾,固体全
部溶解,此时溶液的质量是
A.(a+b)g B.(a+c)g C.(b+c)g D.(a+b+c)g
4.如图为KCl和NaCO 的溶解度曲线,下列说法正确的是
2 3
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.t℃时,NaCO 饱和溶液的溶质质量分数为49.0%
1 2 3
B.t℃时,等质量的KCl和NaCO 溶液中溶质质量相等
2 2 3
C.t℃时,分别将等质量的KCl和NaCO 溶于水配成饱和溶液,所得溶液的质量
3 2 3
前者大于后者
D.若KCl溶液中含有少量NaCO,可采取蒸发浓缩、控制温度t℃以上降温结晶、
2 3 1
过滤等操作提纯
5.某化学兴趣小组的同学进行的硝酸钾固体溶解实验,过程如图所示(不考虑水分蒸
发),下列判断错误的是
A.②③中溶液的溶质质量不相等 B.②③中溶液的质量不相等
C.③中溶液一定是该温度下硝酸钾不饱和溶液 D.②中溶液一定是该温度下
硝酸钾饱和溶液
6.某固体M中加入一定量水后,红墨水向左移动,则固体M可能是下列哪种物质
A.氢氧化钠 B.蔗糖 C.氯化钠 D.硝酸铵
7.下列有关物质的性质与用途具有对应关系的是
A.金刚石硬度大,可做装饰品—钻石 B.铁具有良好的导电性,可用于制造炊
具
C.氩气的化学性质稳定,可用作电光源 D.洗洁精具有乳化作用,可用于去除油
污
8.甲、乙两种固体(不含结晶水)的溶解度曲线如图所示。下列说法正确的是
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.t℃时,甲、乙溶液溶质的质量分数相等
1
B.甲中含有少量乙时,可用降温结晶法提纯甲
C.t℃时,将10g甲加入10g水中,可得到20g溶液
2
D.t℃时的甲、乙饱和溶液分别降温到t℃时,析出晶体的质量甲大于乙
2 1
9.下列实验方案不能达到实验目的的是
A.鉴别硝酸铵和氢氧化钠:比较溶于水时溶液的温度变化
B.除去铜粉中混有的氧化铜:加入过量炭粉,隔绝空气加强热
C.验证氯化氢分子在不断运动:按如图所示装置进行实验
D.鉴别H 和CO:分别点燃,用冷而干燥的烧杯罩在火焰上方
2
10.如图是甲、乙、丙三种固体物质(不含结晶水)的溶解度曲线,下列叙述错误的
是
A.t℃时,60g丙完全溶解可配制出160g丙的饱和溶液
B.甲中含有少量乙,可用冷却热的饱和溶液的方法提纯甲
C.20℃甲、乙的饱和溶液(溶液中无晶体)升温到40℃,溶质质量分数相等
D.40℃时,甲、丙两物质的饱和溶液降温到t℃时,析出晶体的质量一定不相等
11.用如图所示的密闭实验装置,能使液面a比液面b高,过一段时间又回到持平的
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
一组固体和液体可以是
A.食盐和水 B.蔗糖和水 C.硝酸铵和水 D.固体氢氧化钠
和水
12.溶液用途广泛,与人们的生活息息相关。下列说法正确的是
A.碘酒中的溶剂是碘
B.溶液不一定是无色透明的液体
C.均一、稳定的液体一定是溶液
D.饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液
二、实验题
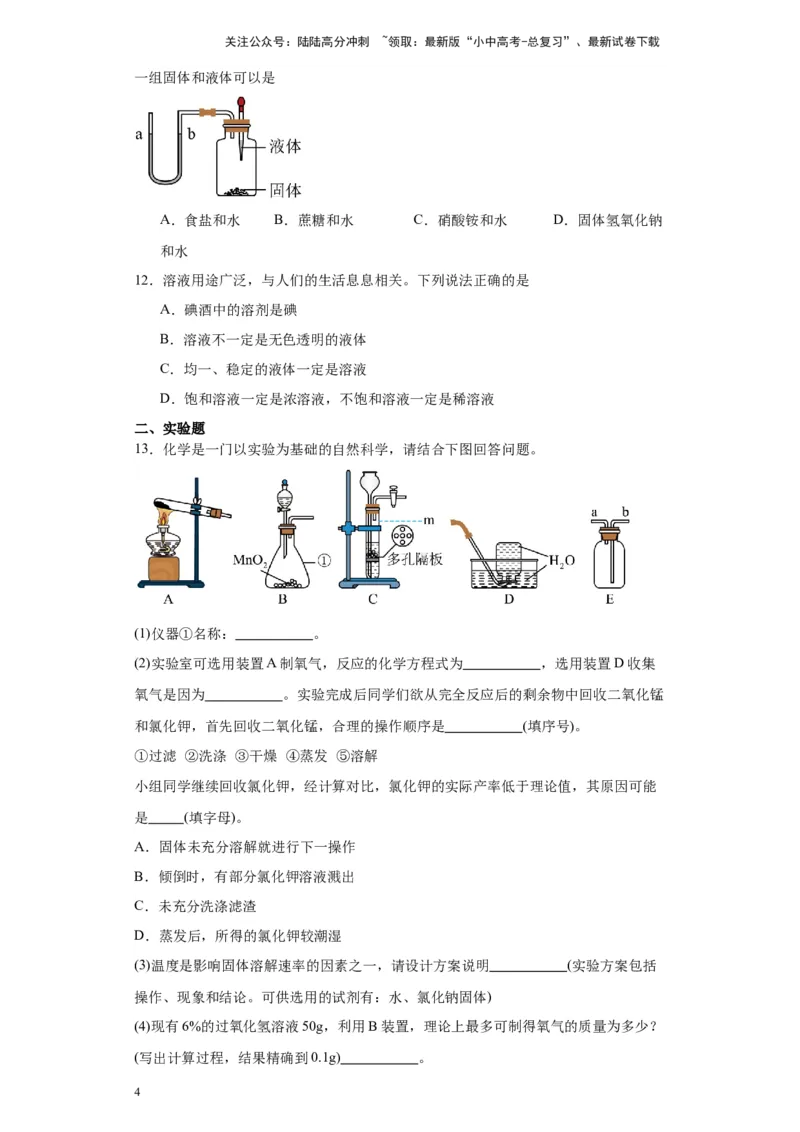
13.化学是一门以实验为基础的自然科学,请结合下图回答问题。
(1)仪器①名称: 。
(2)实验室可选用装置A制氧气,反应的化学方程式为 ,选用装置D收集
氧气是因为 。实验完成后同学们欲从完全反应后的剩余物中回收二氧化锰
和氯化钾,首先回收二氧化锰,合理的操作顺序是 (填序号)。
①过滤 ②洗涤 ③干燥 ④蒸发 ⑤溶解
小组同学继续回收氯化钾,经计算对比,氯化钾的实际产率低于理论值,其原因可能
是 (填字母)。
A.固体未充分溶解就进行下一操作
B.倾倒时,有部分氯化钾溶液溅出
C.未充分洗涤滤渣
D.蒸发后,所得的氯化钾较潮湿
(3)温度是影响固体溶解速率的因素之一,请设计方案说明 (实验方案包括
操作、现象和结论。可供选用的试剂有:水、氯化钠固体)
(4)现有6%的过氧化氢溶液50g,利用B装置,理论上最多可制得氧气的质量为多少?
(写出计算过程,结果精确到0.1g) 。
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(5)实验室选用装置C制取CO,加入稀盐酸的量不宜太多,若实验时,试管中液面处
2
于m处(此时稀盐酸有剩余),则关闭活塞可能导致的后果是 。用装置E收
集二氧化碳,则验满的操作是 。
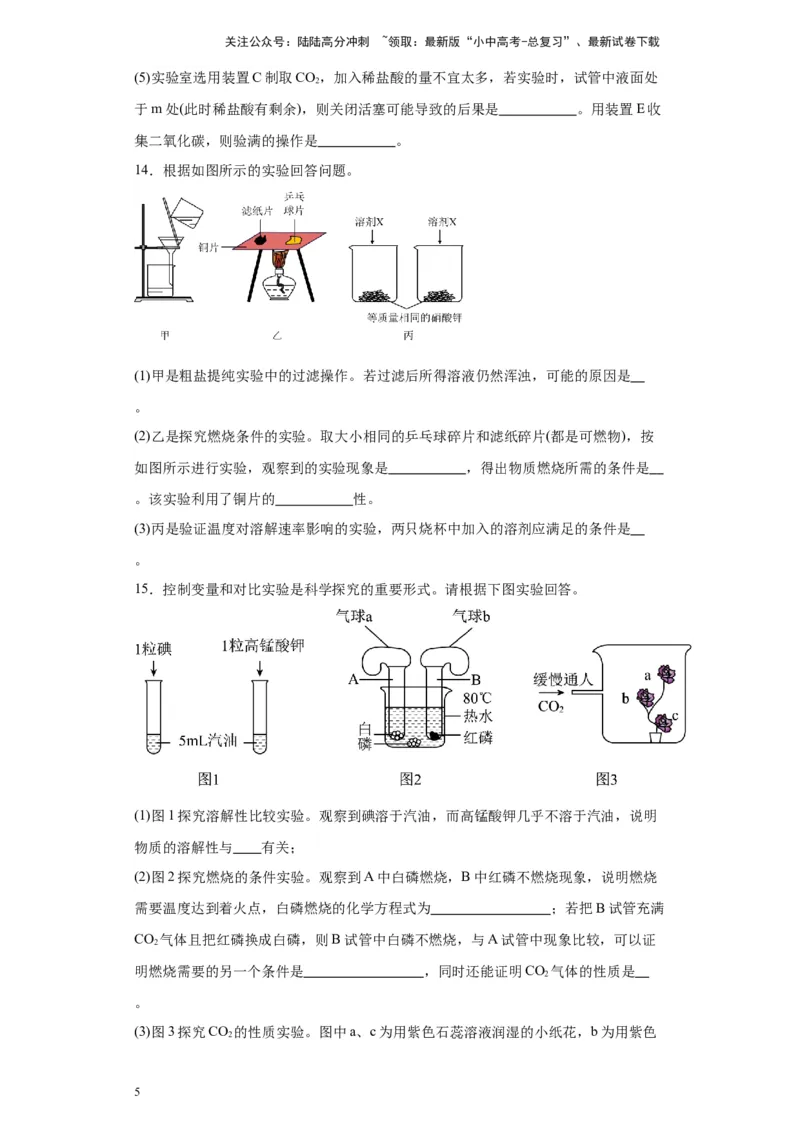
14.根据如图所示的实验回答问题。
(1)甲是粗盐提纯实验中的过滤操作。若过滤后所得溶液仍然浑浊,可能的原因是
。
(2)乙是探究燃烧条件的实验。取大小相同的乒乓球碎片和滤纸碎片(都是可燃物),按
如图所示进行实验,观察到的实验现象是 ,得出物质燃烧所需的条件是
。该实验利用了铜片的 性。
(3)丙是验证温度对溶解速率影响的实验,两只烧杯中加入的溶剂应满足的条件是
。
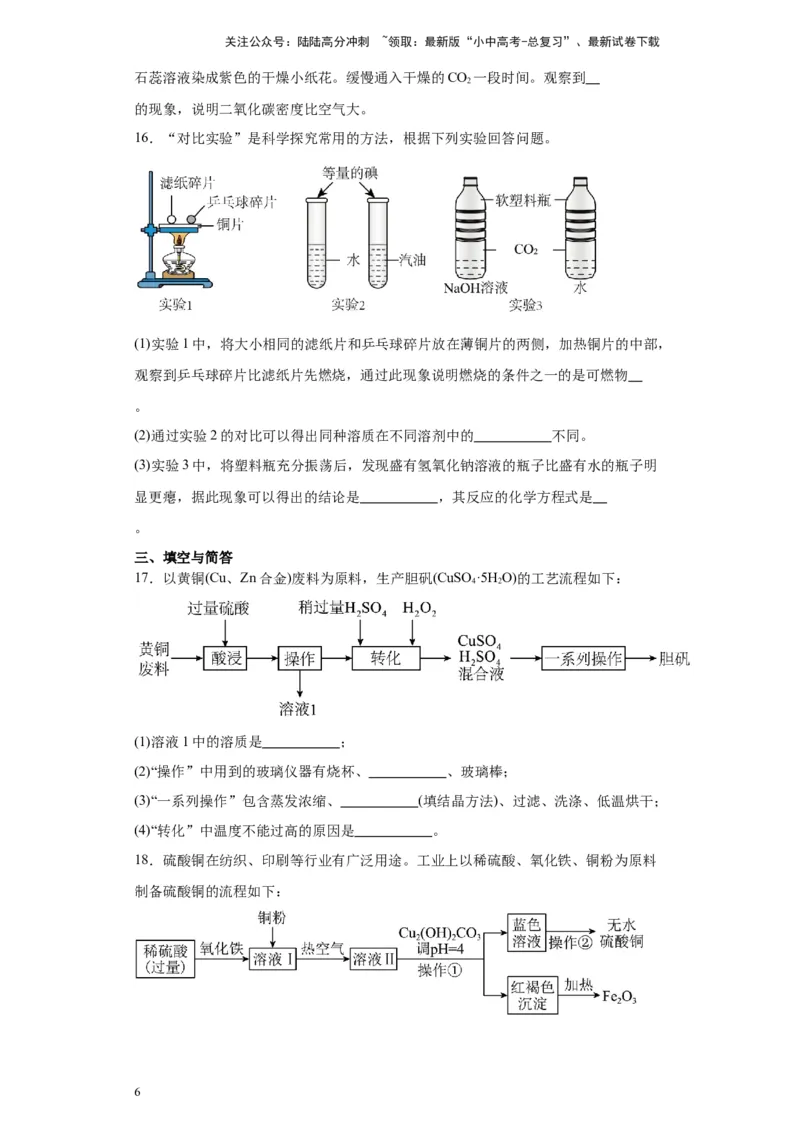
15.控制变量和对比实验是科学探究的重要形式。请根据下图实验回答。
(1)图1探究溶解性比较实验。观察到碘溶于汽油,而高锰酸钾几乎不溶于汽油,说明
物质的溶解性与 有关;
(2)图2探究燃烧的条件实验。观察到A中白磷燃烧,B中红磷不燃烧现象,说明燃烧
需要温度达到着火点,白磷燃烧的化学方程式为 ;若把B试管充满
CO 气体且把红磷换成白磷,则B试管中白磷不燃烧,与A试管中现象比较,可以证
2
明燃烧需要的另一个条件是 ,同时还能证明CO 气体的性质是
2
。
(3)图3探究CO 的性质实验。图中a、c为用紫色石蕊溶液润湿的小纸花,b为用紫色
2
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
石蕊溶液染成紫色的干燥小纸花。缓慢通入干燥的CO 一段时间。观察到
2
的现象,说明二氧化碳密度比空气大。
16.“对比实验”是科学探究常用的方法,根据下列实验回答问题。
(1)实验1中,将大小相同的滤纸片和乒乓球碎片放在薄铜片的两侧,加热铜片的中部,
观察到乒乓球碎片比滤纸片先燃烧,通过此现象说明燃烧的条件之一的是可燃物
。
(2)通过实验2的对比可以得出同种溶质在不同溶剂中的 不同。
(3)实验3中,将塑料瓶充分振荡后,发现盛有氢氧化钠溶液的瓶子比盛有水的瓶子明
显更瘪,据此现象可以得出的结论是 ,其反应的化学方程式是
。
三、填空与简答
17.以黄铜(Cu、Zn合金)废料为原料,生产胆矾(CuSO ·5H O)的工艺流程如下:
4 2
(1)溶液1中的溶质是 ;
(2)“操作”中用到的玻璃仪器有烧杯、 、玻璃棒;
(3)“一系列操作”包含蒸发浓缩、 (填结晶方法)、过滤、洗涤、低温烘干;
(4)“转化”中温度不能过高的原因是 。
18.硫酸铜在纺织、印刷等行业有广泛用途。工业上以稀硫酸、氧化铁、铜粉为原料
制备硫酸铜的流程如下:
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
已知:① ②Fe2+易被氧化成Fe3+
(1)写出该流程中一种氧化物 。
(2)写出氧化铁和稀硫酸反应的化学方程式 。
(3)操作①的名称是 ,操作②经蒸发浓缩、 、过滤、洗涤、干燥
而获得无水硫酸铜。
(4)调pH时需不断测量溶液的pH,用pH试纸测量溶液pH的方法是 。
19.某工厂的工业废水中含有大量的FeSO 和CuSO ,为减少污染并变废为宝,工厂
4 4
计划从该废水中回收FeSO 和金属铜,流程如图所示。请回答下列问题:
4
(1)在①中加入足量试剂⑦的目的是 ,写出发生反应的化学方程式 。
(2)在工业废水中加入足量试剂⑤发生反应的化学方程式为 。
(3)⑥与⑧的操作方法是 。
(4)滤液②、④合并后经蒸发浓缩、 、过滤、洗涤、干燥即获得FeSO ∙7H O晶
4 2
体。
20.某工厂的工业废水中含有大量的FeSO 和CuSO ,为减少污染并变废为宝,工厂
4 4
计划从该废水中回收FeSO 和金属铜,流程如图所示。请回答下列问题:
4
(1)在①中加入足量试剂⑦的目的是 。
(2)在工业废水中加入足量试剂⑤发生反应的化学方程式为 。
(3)⑥与⑧的操作方法是 ;此操作用到的玻璃仪器是 (写一种)。
(4)滤液②、④合并后经蒸发浓缩、 、过滤、洗涤、干燥即获得FeSO ∙7H O晶体。
4 2
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
参考答案:
1.A
2.C
3.D
4.D
5.C
6.D
7.D
8.B
9.B
10.A
11.D
12.B
13.(1)锥形瓶
(2) 不易溶于水 ⑤①②③ ABC
(3)取等质量的(颗粒大小相同的)氯化钠固体分别倒入两个烧杯中,将等体积(足量)温度相同
的水倒入两个烧杯中,用酒精灯给一只烧杯加热,另一只烧杯常温静置,被加热的烧杯中
固体消失得快,则温度越高,固体溶解速率越快/取等质量的氯化钠放入两个烧杯中,分别
倒入等体积20℃的水(足量)和60℃的水,恒温静置,60℃的水中氯化钠固体消失得快,则
温度越高,固体溶解速率越快(合理即可)
(4)设理论上最多可制得氧气的质量是x,
x=1.4g
答:理论上最多可制得1.4g氧气。
(5) 液体从长颈漏斗口溢出 将燃着的木条放在a导管口,若熄灭,则已满
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
14.(1)滤纸破损(答案合理即可)
(2) 乒乓球碎片比滤纸碎片先燃烧 温度达到可燃物的着火点 导热
(3)不同温度、相同质量的同种溶剂
15.(1)溶质种类
(2) 燃烧需要有空气 二氧化碳不燃烧也不支持燃烧
(3)c纸花先变红,a纸花后变红
16.(1)温度要达到着火点
(2)溶解性/溶解能力
(3) CO 能和氢氧化钠反应
2
17.(1)H SO ZnSO
2 4 4
(2)漏斗
(3)降温结晶
(4)防止过氧化氢受热分解
18.(1)氧化铁/Fe O
2 3
(2)
(3) 过滤 降温结晶(或冷却热饱和溶液)
(4)取一小段pH试纸置于表面皿中,用玻璃棒蘸取试液滴在pH试纸上,再与标准比色卡对
照读出pH值
19.(1) 除去过量的铁粉
(2)
(3)过滤
(4)冷却结晶 (或降温结晶)
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
20.(1)除去过量的铁粉
(2)
(3) 过滤 烧杯/漏斗/玻璃棒
(4)降温结晶
3