文档内容
D.常温常压下,22.4L乙烯中C﹣H键数为4N
2010年江苏省高考化学试卷 A
6.(2分)常温下,下列各组离子在指定溶液中能大量共存的是( )
一、选择题:本题包括7小题,每小题2分,共计14分.每小题只有一个选项符合题意. A.pH=1的溶液中:Fe2+、NO ﹣、SO 2﹣、Na+
3 4
1.(2分)化学与能源开发、环境保护、资源利用等密切相关.下列说法正确的是( )
B.由水电离的c(H+)=1×10﹣14mol•L﹣1的溶液中:Ca2+、K+、Cl﹣、HCO ﹣
3
A.为提高农作物的产量和质量,应大量使用化肥和农药
C.c(H+)/c(OH﹣)=1012的溶液中:NH +、Al3+、NO ﹣、Cl﹣
4 3
B.绿色化学的核心是应用化学原理对环境污染进行治理
D.c(Fe3+)=0.1mol•L﹣1的溶液中:K+、ClO﹣、SO 2﹣、SCN﹣
4
C.实现化石燃料清洁利用,就无需开发新能源
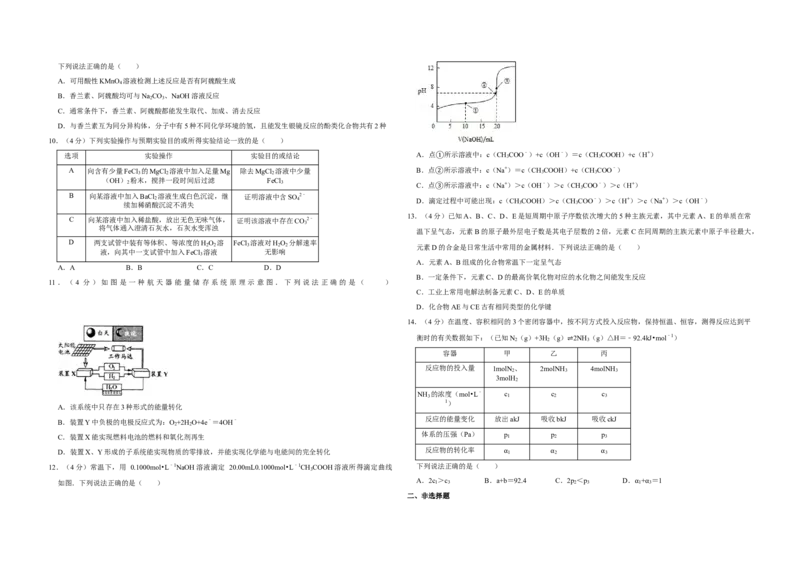
7.(2分)下列有关实验原理或操作正确的是( )
D.垃圾是放错地方的资源,应分类回收利用
2.(2分)水是最宝贵的资源之一.下列表述正确的是( )
A.H O的电子式为
2
B.4℃时,纯水的pH=7
C.D 16O中,质量数之和是质子数之和的两倍
2
D.273K、101kPa,水分子间的平均距离d:d(气态)>d(液态)>d(固态)
A.选择合适的试剂,用图1所示装置可分别制取并收集少量CO
2
、NO和O
2
3.(2分)下列离子方程式表达正确的是( )
B.制备乙酸乙酯时,向乙醇中缓慢加入浓硫酸和冰醋酸
C.洗涤沉淀时(见图2),向漏斗中加适量水,搅拌并滤干
A.用惰性电极电解熔融氯化钠:2Cl﹣+2H 2 O Cl 2 ↑+H 2 ↑+2OH﹣ D.用广泛pH试纸测得0.10mol•L﹣1NH Cl溶液的pH=5.2
4
二、不定项选择题:本题包括7小题,每小题4分,共计28分.每小题有一个或两个选项符合题意.若正确答
B.用氢氧化钠溶液除去铝表面的氧化膜:Al O +2OH﹣═2AlO ﹣+H O
2 3 2 2
案只包括一个选项,多选时,该题得0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都
C.用稀氢氧化钠溶液吸收二氧化氮:2OH﹣+2NO ═NO ﹣+NO↑+H O
2 3 2
正确的得满分,但只要选错一个,该小题就得0分.
D.用食醋除去水瓶中的水垢:CO 2﹣+2CH COOH═2CH COO﹣+CO ↑+H O
3 3 3 2 2
8.(4分)下列说法不正确的是( )
4.(2分)下列有关物质的性质或应用的说法不正确的是( )
A.铅蓄电池在放电过程中,负极质量减小,正极质量增加
A.二氧化硅是生产光纤制品的基本原料
B.常温下,反应C(s)+CO (g)=2CO(g)不能自发进行,则该反应的△H>0
2
B.水玻璃可用于生产黏合剂和防火剂
C.一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率
C.盐析可提纯蛋白质并保持其生理活性
D.相同条件下,溶液中Fe3+、Cu2+、Zn2+的氧化性依次减弱
D.石油分馏可获得乙烯、丙烯和丁二烯
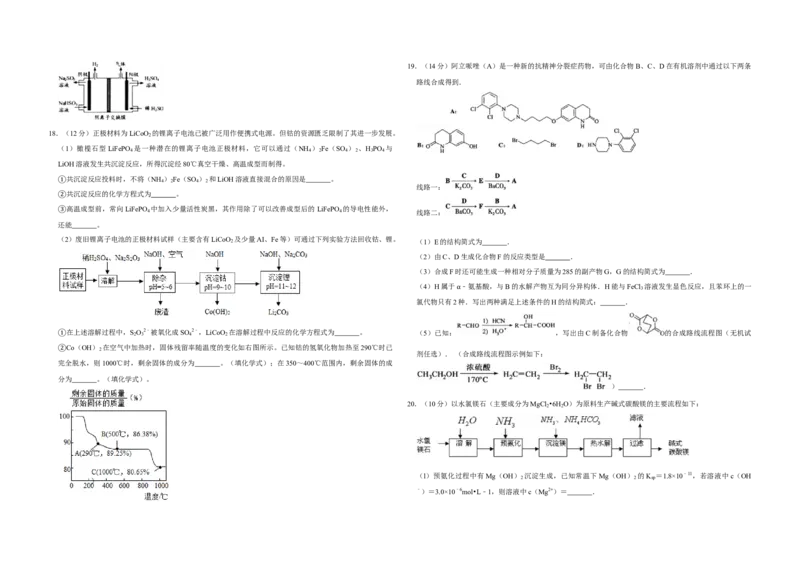
9.(4分)阿魏酸在食品、医药等方面有着广泛用途.一种合成阿魏酸的反应可表示为
5.(2分)设N 为阿伏加德罗常数的值,下列叙述正确的是( )
A
A.常温下,1L0.1mol•L﹣1的NH NO 溶液中氮原子数为0.2N
4 3 A
B.1mol羟基中电子数为10N
A
C.在反应KIO +6HI=KI+3I +3H O中,每生成3molI 转移的电子数为6N
3 2 2 2 A下列说法正确的是( )
A.可用酸性KMnO 溶液检测上述反应是否有阿魏酸生成
4
B.香兰素、阿魏酸均可与Na CO 、NaOH溶液反应
2 3
C.通常条件下,香兰素、阿魏酸都能发生取代、加成、消去反应
D.与香兰素互为同分异构体,分子中有5种不同化学环境的氢,且能发生银镜反应的酚类化合物共有2种
10.(4分)下列实验操作与预期实验目的或所得实验结论一致的是( )
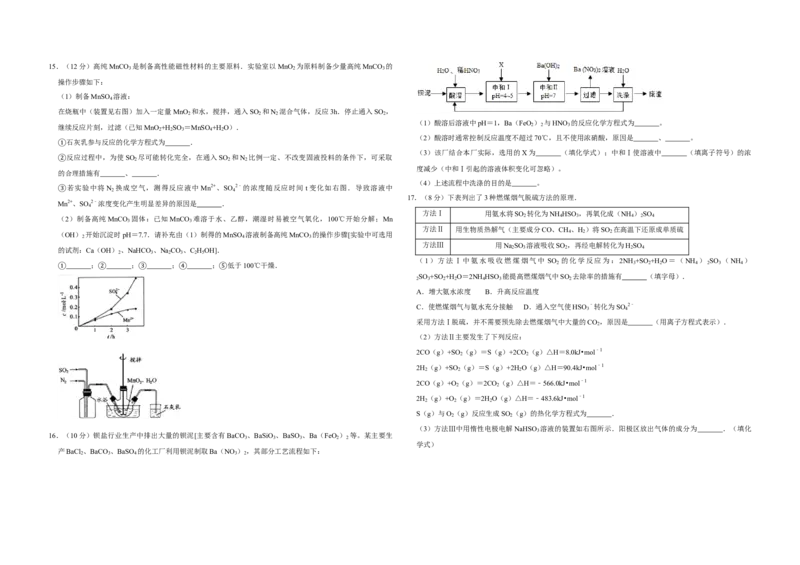
选项 实验操作 实验目的或结论 A.点 所示溶液中:c(CH 3 COO﹣)+c(OH﹣)=c(CH 3 COOH)+c(H+)
A 向含有少量FeCl 3 的MgCl 2 溶液中加入足量Mg 除去MgCl 2 溶液中少量 B.点①所示溶液中:c(Na+)=c(CH 3 COOH)+c(CH 3 COO﹣)
(OH) 粉末,搅拌一段时间后过滤 FeCl
2 3 C.点②所示溶液中:c(Na+)>c(OH﹣)>c(CH COO﹣)>c(H+)
3
B 向某溶液中加入BaCl 溶液生成白色沉淀,继 证明溶液中含SO 2﹣
2 4 D.滴③定过程中可能出现:c(CH COOH)>c(CH COO﹣)>c(H+)>c(Na+)>c(OH﹣)
续加稀硝酸沉淀不消失 3 3
13.(4分)已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常
C 向某溶液中加入稀盐酸,放出无色无味气体, 证明该溶液中存在CO 2﹣
3
将气体通入澄清石灰水,石灰水变浑浊
温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,
D 两支试管中装有等体积、等浓度的H O 溶 FeCl 溶液对H O 分解速率
2 2 3 2 2 元素D的合金是日常生活中常用的金属材料.下列说法正确的是( )
液,向其中一支试管中加入FeCl 溶液 无影响
3
A.元素A、B组成的化合物常温下一定呈气态
A.A B.B C.C D.D
B.一定条件下,元素C、D的最高价氧化物对应的水化物之间能发生反应
11 . ( 4 分 ) 如 图 是 一 种 航 天 器 能 量 储 存 系 统 原 理 示 意 图 . 下 列 说 法 正 确 的 是 ( )
C.工业上常用电解法制备元素C、D、E的单质
D.化合物AE与CE古有相同类型的化学键
14.(4分)在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平
衡时的有关数据如下:(已知N (g)+3H (g) 2NH (g)△H=﹣92.4kJ•mol﹣1)
2 2 3
容器 甲 乙 ⇌ 丙
反应物的投入量 1molN 、 2molNH 4molNH
2 3 3
3molH
2
NH 的浓度(mol•L﹣ c c c
3 1 2 3
1)
A.该系统中只存在3种形式的能量转化
B.装置Y中负极的电极反应式为:O +2H O+4e﹣=4OH﹣ 反应的能量变化 放出akJ 吸收bkJ 吸收ckJ
2 2
体系的压强(Pa) p p p
C.装置X能实现燃料电池的燃料和氧化剂再生 1 2 3
反应物的转化率
D.装置X、Y形成的子系统能实现物质的零排放,并能实现化学能与电能间的完全转化 1 2 3
12.(4分)常温下,用 0.1000mol•L﹣1NaOH溶液滴定 20.00mL0.1000mol•L﹣1CH COOH溶液所得滴定曲线 下列说法正确的是( ) α α α
3
如图.下列说法正确的是( ) A.2c 1 >c 3 B.a+b=92.4 C.2p 2 <p 3 D. 1 + 3 =1
二、非选择题 α α15.(12分)高纯MnCO 是制备高性能磁性材料的主要原料.实验室以MnO 为原料制备少量高纯MnCO 的
3 2 3
操作步骤如下:
(1)制备MnSO 溶液:
4
在烧瓶中(装置见右图)加入一定量MnO 和水,搅拌,通入SO 和N 混合气体,反应3h.停止通入SO ,
2 2 2 2
(1)酸溶后溶液中pH=1,Ba(FeO ) 与HNO 的反应化学方程式为 。
继续反应片刻,过滤(已知MnO +H SO =MnSO +H O). 2 2 3
2 2 3 4 2
(2)酸溶时通常控制反应温度不超过70℃,且不使用浓硝酸,原因是 、 。
石灰乳参与反应的化学方程式为 .
(3)该厂结合本厂实际,选用的X为 (填化学式);中和Ⅰ使溶液中 (填离子符号)的浓
①反应过程中,为使SO
2
尽可能转化完全,在通入SO
2
和N
2
比例一定、不改变固液投料的条件下,可采取
度减少(中和Ⅰ引起的溶液体积变化可忽略)。
②的合理措施有 、 .
(4)上述流程中洗涤的目的是 。
若实验中将N 换成空气,测得反应液中 Mn2+、SO 2﹣的浓度随反应时间 t变化如右图.导致溶液中
2 4
17.(8分)下表列出了3种燃煤烟气脱硫方法的原理.
③Mn2+、SO 2﹣浓度变化产生明显差异的原因是 .
4
方法Ⅰ 用氨水将SO 转化为NH HSO ,再氧化成(NH ) SO
2 4 3 4 2 4
(2)制备高纯MnCO 固体:已知MnCO 难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;Mn
3 3
方法Ⅱ 用生物质热解气(主要成分CO、CH 、H )将SO 在高温下还原成单质硫
4 2 2
(OH) 开始沉淀时pH=7.7.请补充由(1)制得的MnSO 溶液制备高纯MnCO 的操作步骤[实验中可选用
2 4 3
方法Ⅲ 用Na SO 溶液吸收SO ,再经电解转化为H SO
的试剂:Ca(OH) 、NaHCO 、Na CO 、C H OH]. 2 3 2 2 4
2 3 2 3 2 5
(1)方法Ⅰ中氨水吸收燃煤烟气中 SO 的化学反应为:2NH +SO +H O=(NH ) SO (NH )
; ; ; ; 低于100℃干燥. 2 3 2 2 4 2 3 4
SO +SO +H O=2NH HSO 能提高燃煤烟气中SO 去除率的措施有 (填字母).
2 3 2 2 4 3 2
① ② ③ ④ ⑤
A.增大氨水浓度 B.升高反应温度
C.使燃煤烟气与氨水充分接触 D.通入空气使HSO ﹣转化为SO 2﹣
3 4
采用方法Ⅰ脱硫,并不需要预先除去燃煤烟气中大量的CO ,原因是 (用离子方程式表示).
2
(2)方法Ⅱ主要发生了下列反应:
2CO(g)+SO (g)=S(g)+2CO (g)△H=8.0kJ•mol﹣1
2 2
2H (g)+SO (g)=S(g)+2H O(g)△H=90.4kJ•mol﹣1
2 2 2
2CO(g)+O (g)=2CO (g)△H=﹣566.0kJ•mol﹣1
2 2
2H (g)+O (g)=2H O(g)△H=﹣483.6kJ•mol﹣1
2 2 2
S(g)与O (g)反应生成SO (g)的热化学方程式为 .
2 2
(3)方法Ⅲ中用惰性电极电解NaHSO 溶液的装置如右图所示.阳极区放出气体的成分为 .(填化
3
16.(10分)钡盐行业生产中排出大量的钡泥[主要含有BaCO 、BaSiO 、BaSO 、Ba(FeO ) 等。某主要生
3 3 3 2 2
学式)
产BaCl 、BaCO 、BaSO 的化工厂利用钡泥制取Ba(NO ) ,其部分工艺流程如下:
2 3 4 3 219.(14分)阿立哌唑(A)是一种新的抗精神分裂症药物,可由化合物B、C、D在有机溶剂中通过以下两条
路线合成得到.
18.(12分)正极材料为LiCoO 的锂离子电池已被广泛用作便携式电源。但钴的资源匮乏限制了其进一步发展。
2
(1)橄榄石型LiFePO 是一种潜在的锂离子电池正极材料,它可以通过(NH ) Fe(SO ) 、H PO 与
4 4 2 4 2 3 4
LiOH溶液发生共沉淀反应,所得沉淀经80℃真空干燥、高温成型而制得。
共沉淀反应投料时,不将(NH ) Fe(SO ) 和LiOH溶液直接混合的原因是 。
4 2 4 2
线路一:
①共沉淀反应的化学方程式为 。
②高温成型前,常向LiFePO
4
中加入少量活性炭黑,其作用除了可以改善成型后的 LiFePO
4
的导电性能外,
线路二:
③还能 。
(2)废旧锂离子电池的正极材料试样(主要含有LiCoO 及少量AI、Fe等)可通过下列实验方法回收钴、锂。
2 (1)E的结构简式为 .
(2)由C、D生成化合物F的反应类型是 .
(3)合成F时还可能生成一种相对分子质量为285的副产物G,G的结构简式为 .
(4)H属于 ﹣氨基酸,与B的水解产物互为同分异构体.H能与FeCl 溶液发生显色反应,且苯环上的一
3
氯代物只有2α种.写出两种满足上述条件的H的结构简式: .
在上述溶解过程中,S
2
O
3
2﹣被氧化成SO
4
2﹣,LiCoO
2
在溶解过程中反应的化学方程式为 。 (5)已知: ,写出由C制备化合物 的合成路线流程图(无机试
①Co(OH)
2
在空气中加热时,固体残留率随温度的变化如右图所示。已知钴的氢氧化物加热至290℃时已
剂任选). (合成路线流程图示例如下:
②完全脱水,则1000℃时,剩余固体的成分为 。(填化学式);在350~400℃范围内,剩余固体的成
分为 。(填化学式)。
) .
20.(10分)以水氯镁石(主要成分为MgCl •6H O)为原料生产碱式碳酸镁的主要流程如下:
2 2
(l)预氨化过程中有Mg(OH) 沉淀生成,已知常温下Mg(OH) 的K =1.8×10﹣11,若溶液中c(OH
2 2 sp
﹣)=3.0×10﹣6mol•L﹣1,则溶液中c(Mg2+)= .(2)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为 . (l)上述实验中过滤的目的是 .
(3)高温煅烧碱式碳酸镁得到MgO.取碱式碳酸镁4.66g,高温煅烧至恒重,得到固体2.00g和标准状况下 (2)滤液在分液漏斗中洗涤静置后,有机层处于 层(填“上”或'下”);放液时,若发现液体流不
CO 0.896L,通过计算确定碱式碳酸镁的化学式. 下来,其可能原因除分液漏斗活塞堵塞外,还有 .
2
(4)若热水解不完全,所得碱式碳酸镁中将混有MgCO ,则产品中镁的质量分数 (填“升高”、 (3)下列给出了催化剂种类及用量对甲苯硝化反应影响的实验结果.
3
“降低”或“不变”). 催化剂 n(催化剂) 硝化产物中各种异构体质量分数(%) 总产率(%)
三、本题包括第21、22两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容.请选定 n(甲苯) 对硝基甲苯 邻硝基甲苯 间硝
基甲
其中一题,并在相应的答题区域内作答.若两题都做,则按第21题评分. 苯
21.(12分)乙炔是有机合成工业的一种原料.工业上曾用CaC 与水反应生成乙炔. 浓H SO 1.0 35.6 60.2 4.2 98.0
2 2 4
(1)CaC 中C 2﹣与O 2+互为等电子体,O 2+的电子式可表示为 ;1mol O 2+中含有的 键数目为 1.2 36.5 59.5 4.0 99.8
2 2 2 2 2
. π NaHSO 4 0.15 44.6 55.1 0.3 98.9
(2)将乙炔通入[Cu(NH ) ]Cl溶液生成Cu C 红棕色沉淀.Cu+基态核外电子排布式为 . 0.25 46.3 52.8 0.9 99.9
3 2 2 2
(3)乙炔与氢氰酸反应可得丙烯腈(H C=CH﹣C≡N).丙烯腈分子中碳原子轨道杂化类型是 ; 0.32 47.9 51.8 0.3 99.9
2
0.36 45.2 54.2 0.6 99.9
分子中处于同一直线上的原子数目最多为 .
(4)CaC 晶体的晶胞结构与NaCl晶体的相似(如右图所示),但CaC 晶体中含有的中哑铃形C 2﹣的存在, NaHSO 4 催化制备对硝基甲苯时,催化剂与甲苯的最佳物质的量之比为 .
2 2 2
使晶胞沿一个方向拉长.CaC 晶体中1个Ca2+周围距离最近的C 2﹣数目为 .
①由甲苯硝化得到的各种产物的含量可知,甲苯硝化反应的特点是 .
2 2
②与浓硫酸催化甲苯硝化相比,NaHSO
4
催化甲苯硝化的优点有 、 .
③
22.对硝基甲苯是医药、染料等工业的一种重要有机中间体,它常以浓硝酸为硝化剂,浓硫酸为催化剂,通过
甲苯的硝化反应制备.
一种新的制备对硝基甲苯的实验方法是:以发烟硝酸为硝化剂,固体 NaHSO 为催化剂(可循环使用),在
4
CCl 溶液中,加入乙酸酐(有脱水作用),45℃反应1h.反应结束后,过滤,滤液分别用5% NaHCO ,溶
4 3
液、水洗至中性,再经分离提纯得到对硝基甲苯.