文档内容
2010年高考理综化学试题(浙江卷)
1、下列说法中正确的是
A. 光导纤维、棉花、油脂、ABS树脂都是由高分子化合物组成的物质
B. 开发核能、太阳能等新能源,推广基础甲醇汽油,使用无磷洗涤剂都可直接降低碳
排放
C. 红外光谱仪、核磁共振仪、质谱仪都可用于有机化合物结构的分析
D. 阴极射线、 -粒子散射现象及布朗运动的发现都对原子结构模型的建立作出了贡
献
2、有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族;
X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是
一种重要的半导体材料。下列说法中,正确的是
A. X、M两种元素只能形成XM型化合物
2
B. 由于W、Z、M元素的氢气化物相对分子质量依次减小,所以其沸点依次降低
C. 元素Y、Z、W的单质晶体属于同种类型的晶体
D. 元素W和M的某些单质可作为水处理中的消毒剂
3、Li-Al/FeS电池是一种正在开发的车载电池,该电池中正极的电极反应式为:
2Li+FeS+2e-=LiS+Fe有关该电池的下列中,正确的是
2
A. Li-Al在电池中作为负极材料,该材料中Li的化合价为+1价
B. 该电池的电池反应式为:2Li+FeS=LiS+Fe
2
C. 负极的电极反应式为Al-3 e-=Al3+
D. 充电时,阴极发生的电极反应式为:LiS+Fe-2e-=2Li++FeS
2
4、核黄素又称为维生素B2,可促进发育和细胞再生,有利于增进视力,减轻眼睛疲劳。
核黄素分子的结构为:
已知:
+HO +
2有关核黄素的下列说法中,不正确的是:
A.该化合物的分子式为C H NO
17 22 4 6
B.酸性条件下加热水解,有CO 生成
2
C.酸性条件下加热水解,所得溶液加碱后有NH 生成
3
D.能发生酯化反应
5、下列关于实验原理或操作的叙述中,不正确的是:
A、 从碘水中提取单质碘时,不能用无水乙醇代替CCl
4
B、 可用新制的Cu(OH) 悬浊液检验牙膏中存在的甘油
2
C、 纸层析实验中,须将滤纸上的试样点浸入展开剂中
D、 实验室中提纯混有少量乙酸的乙醇,可采用先加生石灰,过滤后再蒸馏的方法
6、下列热化学方程式或离子方程式中,正确的是:
A、甲烷的标准燃烧热为-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:
CH(g)+2O(g)=CO(g)+2HO(g) △H=-890.3kJ·mol-1
4 2 2 2
B.500℃、30MPa下,将0.5molN 和1.5mol H 置于密闭容器中充分反应生成NH (g),放
2 2 3
热19.3kJ,其热化学方程式为:
N(g)+3H(g) 2NH (g) △H=-38.6kJ·mol-1
2 2 3
C.氯化镁溶液与氨水反应:Mg2++2OH-=Mg(OH) ↓
2
D.氧化铝溶于NaOH溶液:Al O+2OH-+3H O=2Al(OH) -
2 3 2 4
7、某钠盐溶液中可能含有NO -、SO 2-、SO 2-、CO2-、Cl-、I-等阴离子。某同学取5
2 4 3 3
份此溶液样品,分别进行了如下实验:
①用pH计测得溶液pH大于7
②加入盐酸,产生有色刺激性气体
③加入硝酸酸化的AgNO 溶液产生白色沉淀,且放出有色刺激性气体
3
④加足量BaCl 溶液,产生白色沉淀,该沉淀溶于稀硝酸且放出气体,将气体通入品红溶
2
液,溶液不褪色
⑤加足量BaCl 溶液,产生白色沉淀,在滤液中加入酸化的(NH ) Fe(SO ) 溶液,再
2 4 2 4 2
滴加KSCN溶液,显红色该同学最终确定在上述六种离子中仅含NO -、CO2-、Cl-三种阴离子。
2 3
请分析,该同学只需要完成上述哪几个实验,即可得出此结论。
A. ①②④⑤ B. ③④ C. ③④⑤ D. ②③⑤
8、洗车安全气囊是行车安全的重要保障。当车辆发生碰撞的瞬间,安全装置通电点火使其
中的粉末分解释放出大量的氮气形成气囊,从而保护司机及乘客免受伤害。为研究安全气
囊工作的化学原理,取安全装置中的固体粉末进行实验。经组成分析,确定该粉末仅Na、
Fe、N、O四种元素。水溶性试验表明,固体粉末部分溶解。经检测,可溶物为化合物甲;
不溶物为红棕色固体,可溶于盐酸。
取13.0g化合物甲,加热使其完全分解,生成氮气和单质乙,生成的氮气折合成标准状
况下的体积为6.72L。单质乙就在高温隔绝空气的条件下与不溶物红棕色粉末反应生成化
合物丙和另和一种单质。化合物丙与空气接触可转化为可溶性盐。
请回答下列问题:
(1)甲的化学方程式为 ,丙的电子式
为 。
(2)若丙在空气中转化为碳酸氢盐,则反应的化学方程式为 。
(3)单质乙与红棕色粉末发生反应的化学方程式为 ,安全气囊中红棕色粉末
的作用是 。
(4)以下物质中,有可能作为安全气囊中红棕色粉末替代品的是
。
A. KCl B. KNO C. Na S D. CuO
3 2
(5)设计一个实验方案,探究化合物丙与空气接触后生成可溶性盐的成分(不考虑结晶水
合物) 。
9、已知:
①25℃时弱电解质高电离平衡常数:K(CHCOOH)=1.8×10-5,K(HSCN)=0.13;难
a 3 a
溶电解质的溶度积学数:K (CaF )=1.5×10-10
sp 2
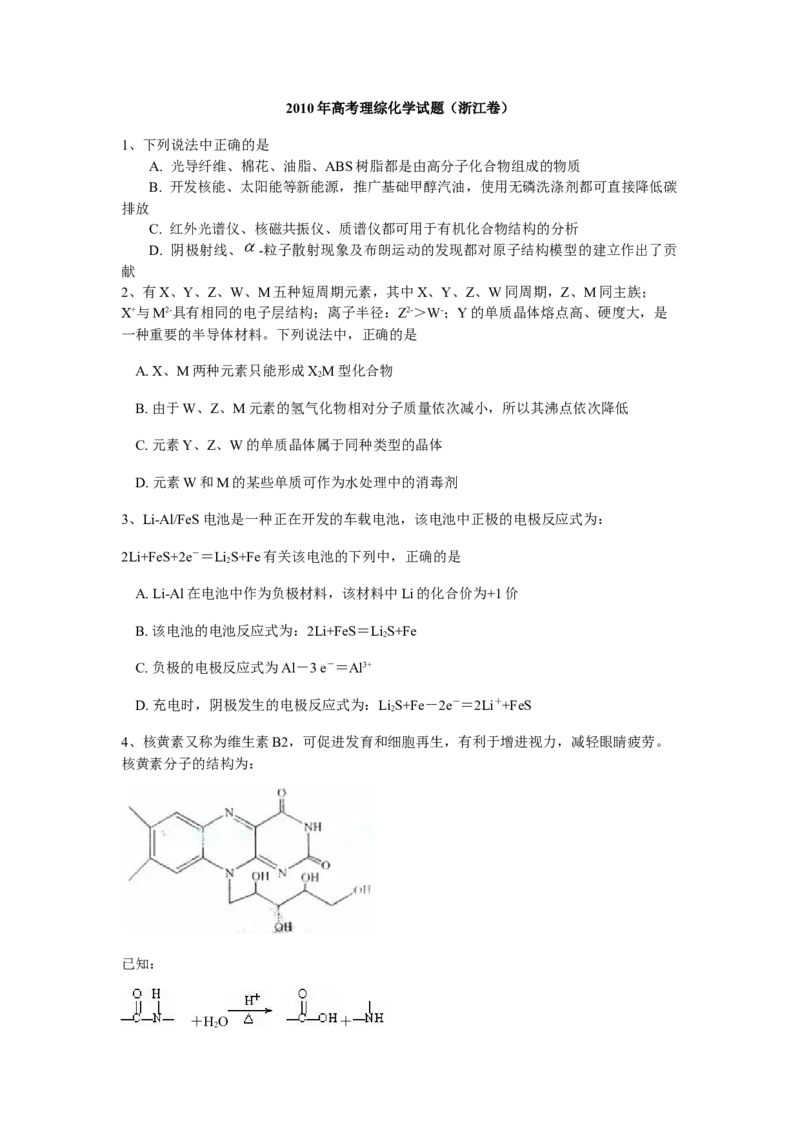
②25℃时,2.0×10-3mol·L-1氢氟酸水溶液中,调节溶液pH(忽略体积变化),得到c
(HF)、c(F-)与溶液pH的变化关系,如下图所示:请根据以下信息回答下旬问题:
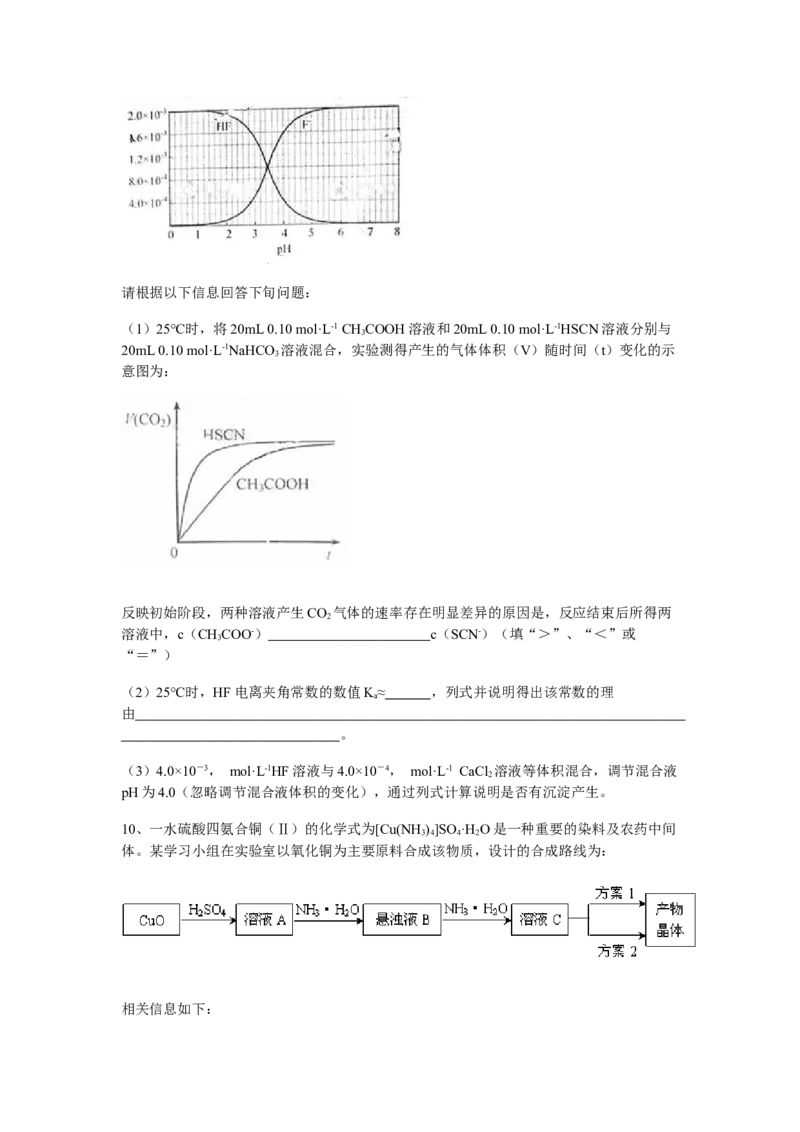
(1)25℃时,将20mL 0.10 mol·L-1 CHCOOH溶液和20mL 0.10 mol·L-1HSCN溶液分别与
3
20mL 0.10 mol·L-1NaHCO 溶液混合,实验测得产生的气体体积(V)随时间(t)变化的示
3
意图为:
反映初始阶段,两种溶液产生CO 气体的速率存在明显差异的原因是,反应结束后所得两
2
溶液中,c(CHCOO-) c(SCN-)(填“>”、“<”或
3
“=”)
(2)25℃时,HF电离夹角常数的数值K≈ ,列式并说明得出该常数的理
a
由
。
(3)4.0×10-3, mol·L-1HF溶液与4.0×10-4, mol·L-1 CaCl 溶液等体积混合,调节混合液
2
pH为4.0(忽略调节混合液体积的变化),通过列式计算说明是否有沉淀产生。
10、一水硫酸四氨合铜(Ⅱ)的化学式为[Cu(NH )]SO ·H O是一种重要的染料及农药中间
3 4 4 2
体。某学习小组在实验室以氧化铜为主要原料合成该物质,设计的合成路线为:
相关信息如下:①[Cu(NH )]SO ·H O在溶液中存在以下电离(解离)过程:
3 4 4 2
[Cu(NH )]SO ·H O=[Cu(NH )]2++SO2-+H O
3 4 4 2 3 4 4 2
[Cu(NH )]2+ Cu2++4NH
3 4 3
②(NH )SO 在水中可溶,在乙醇中难溶。
4 2 4
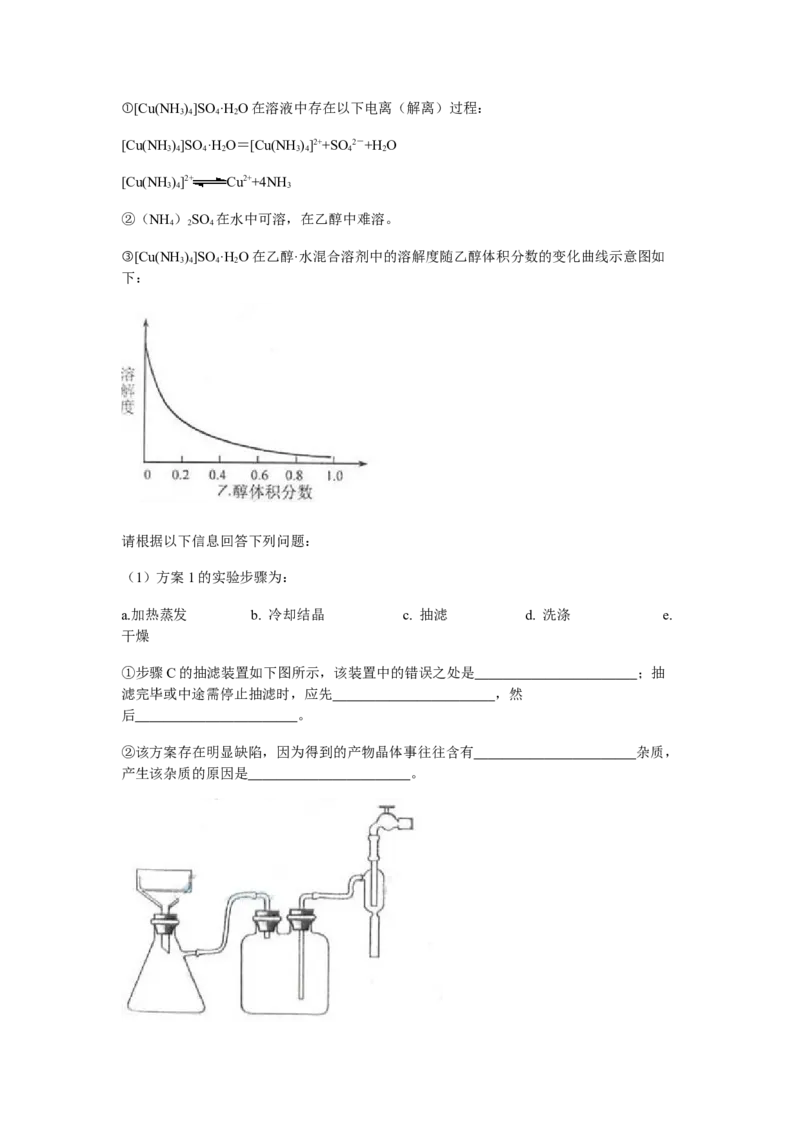
③[Cu(NH )]SO ·H O在乙醇·水混合溶剂中的溶解度随乙醇体积分数的变化曲线示意图如
3 4 4 2
下:
请根据以下信息回答下列问题:
(1)方案1的实验步骤为:
a.加热蒸发 b. 冷却结晶 c. 抽滤 d. 洗涤 e.
干燥
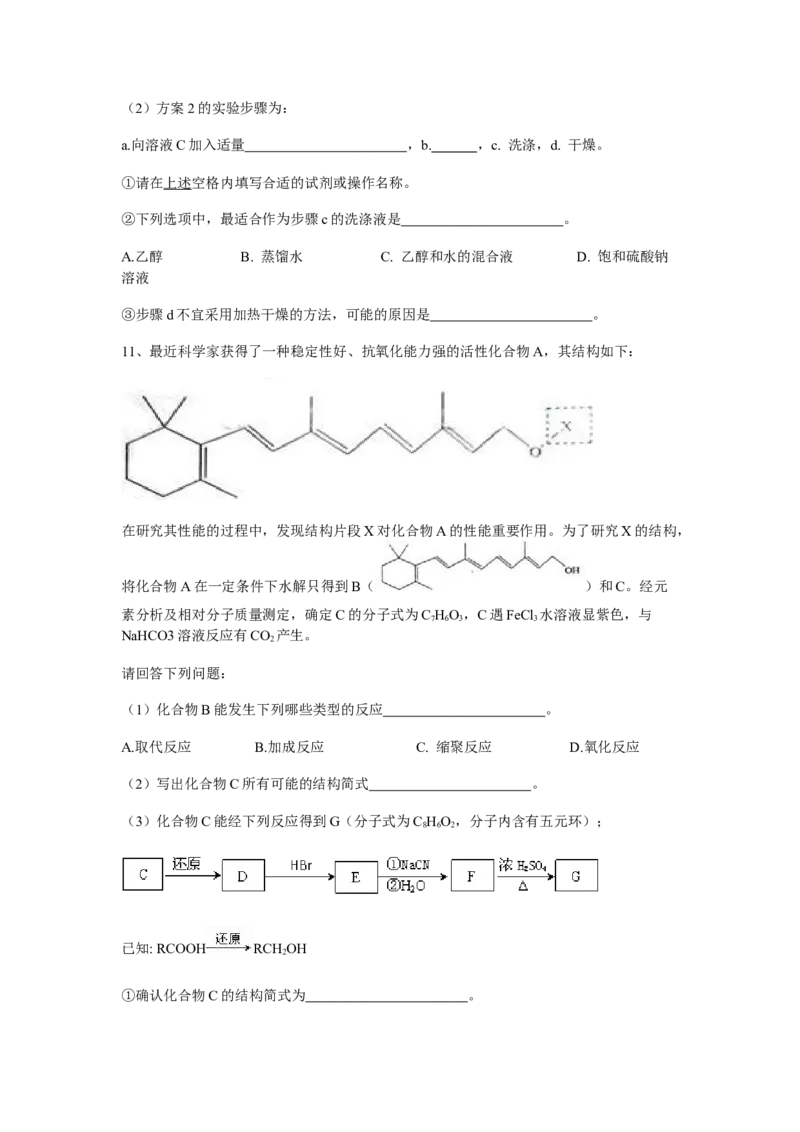
①步骤C的抽滤装置如下图所示,该装置中的错误之处是 ;抽
滤完毕或中途需停止抽滤时,应先 ,然
后 。
②该方案存在明显缺陷,因为得到的产物晶体事往往含有 杂质,
产生该杂质的原因是 。(2)方案2的实验步骤为:
a.向溶液C加入适量 ,b. ,c. 洗涤,d. 干燥。
①请在上述空格内填写合适的试剂或操作名称。
②下列选项中,最适合作为步骤c的洗涤液是 。
A.乙醇 B. 蒸馏水 C. 乙醇和水的混合液 D. 饱和硫酸钠
溶液
③步骤d不宜采用加热干燥的方法,可能的原因是 。
11、最近科学家获得了一种稳定性好、抗氧化能力强的活性化合物A,其结构如下:
在研究其性能的过程中,发现结构片段X对化合物A的性能重要作用。为了研究X的结构,
将化合物A在一定条件下水解只得到B( )和C。经元
素分析及相对分子质量测定,确定C的分子式为C HO,C遇FeCl 水溶液显紫色,与
7 6 3 3
NaHCO3溶液反应有CO 产生。
2
请回答下列问题:
(1)化合物B能发生下列哪些类型的反应 。
A.取代反应 B.加成反应 C. 缩聚反应 D.氧化反应
(2)写出化合物C所有可能的结构简式 。
(3)化合物C能经下列反应得到G(分子式为C HO,分子内含有五元环);
8 6 2
已知: RCOOH RCHOH
2
①确认化合物C的结构简式为 。②F→C反应的化学方程式为 。
③化合物E有多种同分异构体,1H核磁共振谱图表明,其中某些同分异构体含有苯环,且
苯环下有两种不同化学环境的氢,写出这些同分异构体中任意三种的结构简式
。