文档内容
2011 年广东化学试题
一、单选题
7. 下列说法正确的是
A.纤维素和淀粉遇碘水均显蓝色
B.蛋白质、乙酸和葡萄糖均属电解质
C.溴乙烷与NaOH乙醇溶液共热生成乙烯
D.乙酸乙酯和食用植物油均可水解生成乙醇
8. 能在水溶液中大量共存的一组离子是
A. H+、I―、NO―、SiO2- B. Ag+、Fe3+、Cl―、SO2―
3 3 4
C.K+、SO2-、Cu2+、NO― D.NH+、OH-、Cl-、HCO-
4 3 4 3
9.设n 为阿伏伽德罗常数的数值,下列说法正确的是
A
A、常温下,23g NO 含有n 个氧原子
2 A
B、1L0.1mol•L-1的氨水含有0.1n 个OH―
A
C、常温常压下,22.4LCCl 含有个nCCl 分子
4 A 4
D、1molFe2+与足量的HO 溶液反应,转移2n 个电子
2 2 A
10、某同学通过系列实验探究Mg及其化合物的性质,操作正确且能达到目的的是
A、将水加入浓硫酸中得到稀硫酸,置镁条于其中探究Mg的活泼性
B、将NaOH溶液缓慢滴入MgSO 溶液中,观察Mg(OH) 沉淀的生成
4 2
C、将Mg(OH) 浊液直接倒入已装好滤纸的漏斗中过滤,洗涤并收集沉淀
2
D、将Mg(OH) 沉淀转入蒸发皿中,加足量稀盐酸,加热蒸干得无水MgCl 固体
2 2
11、对于0.1mol•L-1 NaSO 溶液,正确的是
2 3
A、升高温度,溶液的pH降低
B、c(Na+)=2c(SO2―)+ c(HSO―)+ c(HSO)
3 3 2 3
C、c(Na+)+c(H+)=2 c(SO2―)+ 2c(HSO―)+ c(OH―)
3 3
D、加入少量NaOH固体,c(SO2―)与c(Na+)均增大
3
12、某小组为研究电化学原理,设计如图2装置。下列叙述不正确的是
A、a和b不连接时,铁片上会有金属铜析出
B、a和b用导线连接时,铜片上发生的反应为:Cu2++2e-= Cu
C、无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色
D、a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动
22、短周期元素甲、乙、丙、丁的原子序数依次增大,甲和乙形成的气态氢化物的水溶液呈碱性,乙位
于第VA族,甲和丙同主族,丁的最外层电子数和电子层数相等,则A、原子半径:丙>丁>乙
B、单质的还原性:丁>丙>甲
C、甲、乙、丙的氧化物均为共价化合物
D、乙、丙、丁的最高价氧化物对应的水化物能相互反应
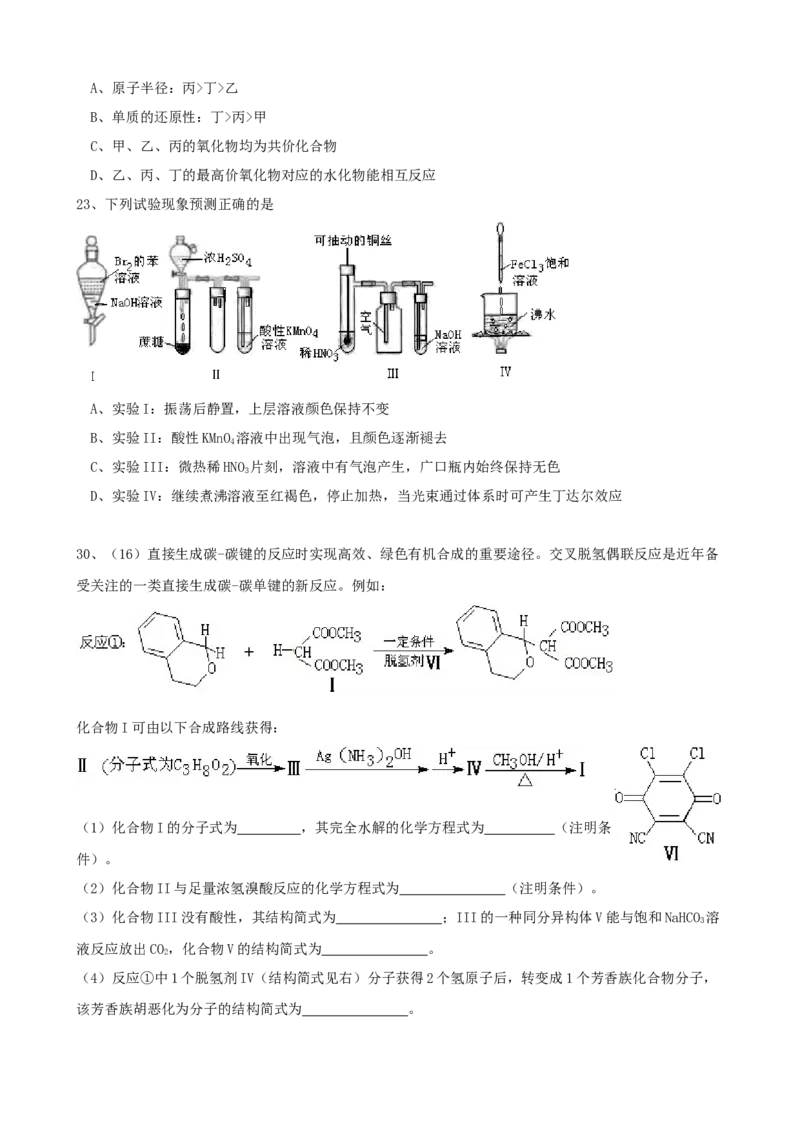
23、下列试验现象预测正确的是
A、实验I:振荡后静置,上层溶液颜色保持不变
B、实验II:酸性KMnO 溶液中出现气泡,且颜色逐渐褪去
4
C、实验III:微热稀HNO 片刻,溶液中有气泡产生,广口瓶内始终保持无色
3
D、实验IV:继续煮沸溶液至红褐色,停止加热,当光束通过体系时可产生丁达尔效应
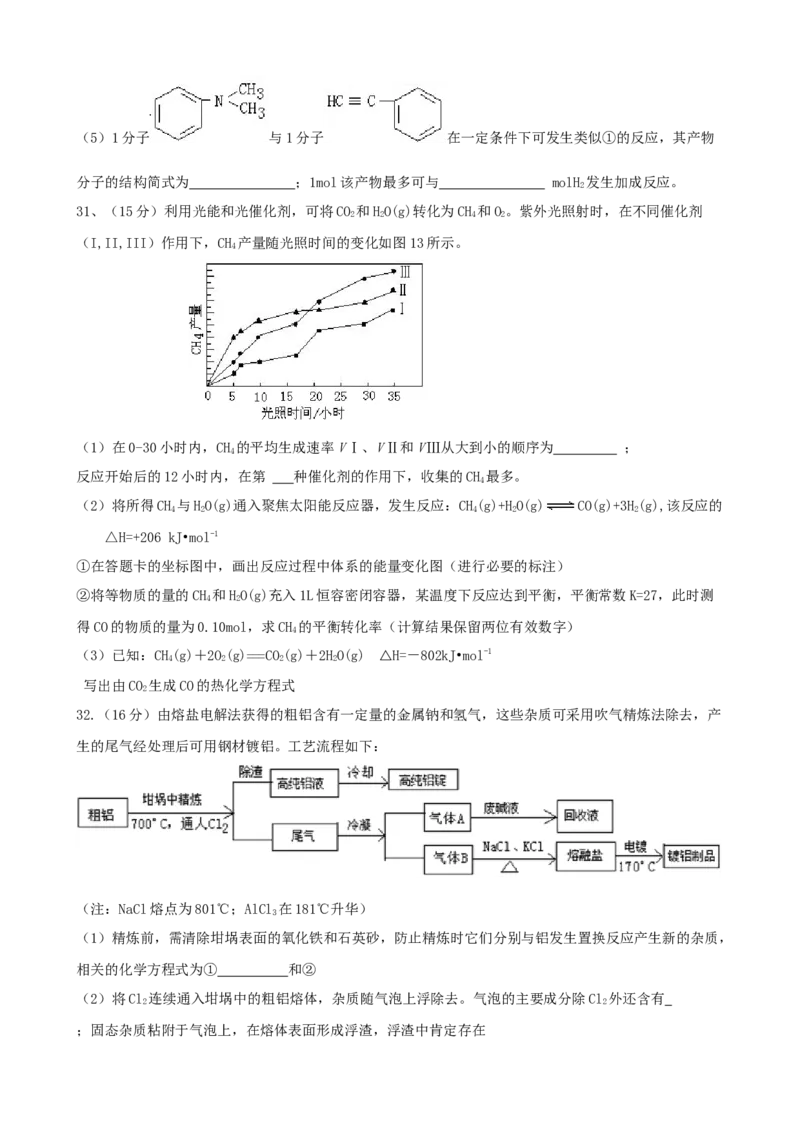
30、(16)直接生成碳-碳键的反应时实现高效、绿色有机合成的重要途径。交叉脱氢偶联反应是近年备
受关注的一类直接生成碳-碳单键的新反应。例如:
化合物I可由以下合成路线获得:
(1)化合物I的分子式为 ,其完全水解的化学方程式为 (注明条
件)。
(2)化合物II与足量浓氢溴酸反应的化学方程式为 (注明条件)。
(3)化合物III没有酸性,其结构简式为 ;III的一种同分异构体V能与饱和NaHCO 溶
3
液反应放出CO,化合物V的结构简式为 。
2
(4)反应①中1个脱氢剂IV(结构简式见右)分子获得2个氢原子后,转变成1个芳香族化合物分子,
该芳香族胡恶化为分子的结构简式为 。(5)1分子 与1分子 在一定条件下可发生类似①的反应,其产物
分子的结构简式为 ;1mol该产物最多可与 molH 发生加成反应。
2
31、(15分)利用光能和光催化剂,可将CO 和HO(g)转化为CH 和O。紫外光照射时,在不同催化剂
2 2 4 2
(I,II,III)作用下,CH 产量随光照时间的变化如图13所示。
4
(1)在0-30小时内,CH 的平均生成速率VⅠ、VⅡ和VⅢ从大到小的顺序为 ;
4
反应开始后的12小时内,在第 种催化剂的作用下,收集的CH 最多。
4
(2)将所得CH 与HO(g)通入聚焦太阳能反应器,发生反应:CH(g)+HO(g) CO(g)+3H(g),该反应的
4 2 4 2 2
△H=+206 kJ•mol-1
①在答题卡的坐标图中,画出反应过程中体系的能量变化图(进行必要的标注)
②将等物质的量的CH 和HO(g)充入1L恒容密闭容器,某温度下反应达到平衡,平衡常数K=27,此时测
4 2
得CO的物质的量为0.10mol,求CH 的平衡转化率(计算结果保留两位有效数字)
4
(3)已知:CH
4
(g)+2O
2
(g)===CO
2
(g)+2H
2
O(g) △H=-802kJ•mol-1
写出由CO 生成CO的热化学方程式
2
32.(16分)由熔盐电解法获得的粗铝含有一定量的金属钠和氢气,这些杂质可采用吹气精炼法除去,产
生的尾气经处理后可用钢材镀铝。工艺流程如下:
(注:NaCl熔点为801℃;AlCl 在181℃升华)
3
(1)精炼前,需清除坩埚表面的氧化铁和石英砂,防止精炼时它们分别与铝发生置换反应产生新的杂质,
相关的化学方程式为① 和②
(2)将Cl 连续通入坩埚中的粗铝熔体,杂质随气泡上浮除去。气泡的主要成分除Cl 外还含有
2 2
;固态杂质粘附于气泡上,在熔体表面形成浮渣,浮渣中肯定存在(3)在用废碱液处理A的过程中,所发生反应的离子方程式为
(4)镀铝电解池中,金属铝为 极,熔融盐电镀中铝元素和氯元素主要以AlCl― 和AlCl―形式
4 2 7
存在,铝电极的主要电极反应式为
(5)钢材镀铝后,表面形成的致密氧化铝膜能防止钢材腐蚀,其原因是
33、(17分)某同学进行试验探究时,欲配制1.0mol•L-1Ba(OH) 溶液,但只找到在空气中暴露已久的
2
Ba(OH)·8HO试剂(化学式量:315)。在室温下配制溶液时发现所取试剂在水中仅部分溶解,烧杯中存
2 2
在大量未溶物。为探究原因,该同学查得Ba(OH)·8HO在283K、293K和303K时的溶解度(g/100g
2 2
HO)分别为2.5、3.9和5.6。
2
(1)烧杯中未溶物仅为BaCO,理由是
3
(2)假设试剂由大量Ba(OH)·8HO和少量BaCO 组成,设计试验方案,进行成分检验,在答题卡上写出
2 2 3
实验步骤、预期现象和结论。(不考虑结晶水的检验;室温时BaCO3饱和溶液的pH=9.6)
限选试剂及仪器:稀盐酸、稀硫酸、NaOH溶液、澄清石灰水、pH计、烧杯、试管、带塞导气管、滴管
实验步骤 预期现象和结论
步骤1:取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静
置,过滤,得滤液和沉淀。
步骤2:取适量滤液于试管中,滴加稀硫酸。
步骤3:取适量步骤1中的沉淀于是试管中,
步骤4:
(3)将试剂初步提纯后,准确测定其中Ba(OH)·8HO的含量。实验如下:
2 2
①配制250ml 约0.1mol•L-1Ba(OH)·8HO溶液:准确称取w克试样,置于烧杯中,加适量蒸馏水,
2 2
,将溶液转入 ,洗涤,定容,摇匀。
②滴定:准确量取25.00ml所配制Ba(OH) 溶液于锥形瓶中,滴加指示剂,将
2
(填“0.020”、“0.05”、“0.1980”或“1.5”)mol•L-1盐酸装入50ml酸式滴定管,
滴定至终点,记录数据。重复滴定2次。平均消耗盐酸Vml。
③ 计算Ba(OH)·8HO的质量分数= (只列出算式,不做运算)
2 2
(4)室温下, (填“能”或“不能”) 配制1.0 mol•L-1Ba(OH) 溶液
2
2011年高考答案:
7. 解析:A.纤维素不能B.蛋白质,葡萄糖不是D, 食用植水解有甘油生成
8.解析:A. H+、I―、NO―、三者发生氧化还原反应;H+,SiO2- 生成沉淀 。
3 3
B. Ag+与Cl―、SO2―形成沉淀。D.NH+与OH-和OH-与HCO-均反应
4 4 39.解析:B、弱电解质部分电离,小于0.1n 个。C、条件和状态不对。D、1molFe2+作还原剂,转移n 个电
A A
子
10.解析:A、稀释方法不对。C、不能直接倒入,应采用玻璃棒引流。D、加热蒸干得MgO固体
11.解析:A、水解为吸热,升高温度,溶液的pH升高。B、物料守恒:应为c(Na+)=2c(SO2―)+2 c
3
(HSO―)+2 c(HSO)。C、电荷守恒应为:c(Na+)+c(H+)=2 c(SO2―)+ c(HSO―)+ c(OH―)
3 2 3 3 3
12.解析:A、发生置换反应,正确。B、形成原电池,铜片作正极,溶液中Cu2+先放电,正确;铁片作负
极失去电子形成Fe2+,溶液从蓝色逐渐变成浅绿色,所以C、正确。D、a和b分别连接直流电源正、负极,
a作阳极,铜片失去电子形成为Cu2+。Cu2+向铁电极移动。错误
22.解析:甲为H ,乙为N ,丙为Na ,丁为Al 。所以AD正确。C、丙的氧化物为离子化合物
23.解析:A、Br 与NaOH溶液反应,上层溶液颜色变为无色。B、产生的SO 与酸性KMnO 溶液发生氧化还
2 2 4
原反应,正确。C、NO与空气反应生成红棕色NO。D、制取氢氧化铁胶体要注意:在沸水中加入饱和的氯
2
化铁溶液,继续煮沸溶液至红褐色,停止加热,即可。
30.解析:(1)化合物Ⅰ的分子式为CHO,
5 8 4
(2)
(3) ;
(4) (5) ;8
31.解析:(1)VⅢ>VⅡ> VⅠ;Ⅱ。(2)①略②根据平衡的三步计算可求CH 的平衡转化率为:
4
0.1/0.11=0.91 (3) CO(g) +3HO(g) ===2O(g) +CO(g)+3H(g) △H=+1008 kJ•mol-1
2 2 2 2
32.解析:(1)①2Al +Fe O =Al O+2Fe ②4Al+3SiO===3Si+ 2Al O(2)H、AlCl;NaCl。
2 3 2 3 2 2 3 2 3
(3)Cl+2OH—=Cl—+ClO—+HO(4)阳极;阳极:Al-3e-=Al3+、(阴极:4AlCl― +3e- = 7AlCl―+Al )(5)铝
2 2 2 7 4
在空气中易形成一层极薄的致密而坚固的氧化膜,它能阻止氧化深入内部,起到防腐保护作用
33.解析:(1)Ba(OH)·8HO与CO2作用转化为BaCO(2)步骤2:预期现象和结论:有白色沉淀生成,
2 2 3
说明有Ba2+。步骤3:取适量步骤1中的沉淀于是试管中,滴加稀盐酸,用带塞导气管塞紧试管,把导气
管插入装有澄清石灰水的烧杯中。预期现象和结论:试管中有气泡生成,烧杯中的澄清石灰水变浑浊,
结合步骤2说明沉淀是BaCO 。步骤4:取适量滤液于烧杯中,用pH计测其pH值。预期现象和结论:
3
pH>9.6,说明有大量的OH—,综合上面步骤可知试剂由大量Ba(OH)·8HO和少量BaCO 组成,假设成立。
2 2 3
(3)①溶解、过滤;250ml的容量瓶中。②0.1980 思路:0.025x0.1x2=C’x0.05------(盐酸体积最多不能多于50ml) 得C’=0.1 mol•L-1 所以应该是选大于0.1 mol•L-1而且接近的③25xCx2=0.1980xV
得C=(0.1980/50)V , Ba(OH)·8HO的质量分数=250x10—3x0.1980Vx315x100%/50w。(4)不能
2 2