文档内容
2012 年北京市高考化学试卷
一、选择题(共 7小题,每小题 3分,满分 21分)
1.(3分)下列用品的有效成分及用途对应错误的是( )
A B C D
用品 食盐 小苏打 明矾 漂白粉
有效成分 NaCl Na CO KAl(SO ) •12H O Ca(ClO)
2 3 4 2 2 2
用途 做调味品 做发酵粉 净水剂 做消毒剂
A.A B.B C.C D.D
2.(3分)下列解释实验现象的反应方程式正确的是( )
A.切开的金属Na暴露在空气中,光亮表面逐渐变暗:
2Na+O ═Na O
2 2 2
B.向 AgCl 悬浊液中滴加Na S 溶液,白色沉淀变成黑色:
2
2AgCl+S2﹣═Ag S+2Cl﹣
2
C.Na O 在潮湿的空气中放置一段时间,变成白色黏稠物:
2 2
2Na O +2CO ═2Na CO +O
2 2 2 2 3 2
D.向NaHCO 溶液中加入过量的澄清石灰水,出现白色沉淀:
3
2HCO ﹣+Ca2++2OH﹣═CaCO ↓+CO 2﹣+2H O
3 3 3 2
3.(3分)如图试验中,所选装置不合理的是( )
A.分离Na CO 溶液和CH COOC H ,选④
2 3 3 2 5
B.用 CCl 提取碘水中的碘,选③
4
C.用 FeCl 溶液吸收Cl 选⑤
2 2
D.粗盐提纯,选①和②
第1页(共7页)4.(3分)已知 As、 Br位于同一周期.下列关系正确的是( )
33 35
A.原子半径:As>Cl>P B.热稳定性:HCl>AsH >HBr
3
C.还原性:As3﹣>S2﹣>Cl﹣ D.酸性:H AsO >H SO >H PO
3 4 2 4 3 4
5.(3 分)用如图所示装置进行下列实验,实验结果与预测的现象不一致的是
( )
① ② ③
A 淀粉 KI溶液 浓硝酸 无明显变化
B 酚酞溶液 浓盐酸 无明显变化
C AlCl 溶液 浓氨水 有白色沉淀
3
D 湿润红纸条 饱和氯水 红纸条褪色
A.A B.B C.C D.D
6.(3分)下列说法正确的是( )
A.天然植物油常温下一般呈液态,难溶于水,有恒定的熔点、沸点
B.麦芽糖与蔗糖的水解产物均含葡萄糖,故二者均为还原型二糖
C.若两种二肽互为同分异构体,则二者的水解产物不一致
D.乙醛、氯乙烯和乙二醇均可作为合成聚合物的单体
7.(3分)人工光合作用能够借助太阳能,用 CO 和 H O 制备化学原料.下
2 2
图是通过人工光合作用制备 HCOOH 的原理示意图,下列说法不正确的是
( )
A.该过程是将太阳能转化为化学能的过程
第2页(共7页)B.催化剂 a表面发生氧化反应,有O 产生
2
C.催化剂 a附近酸性减弱,催化剂b附近酸性增强
D.催化剂b表面的反应是CO +2H++2e一═HCOOH
2
二、解答题(共 4小题,满分 57分)
8.(13分)直接排放含 SO 的烟气会形成酸雨,危害环境.利用钠碱循环法
2
可脱除烟气中的SO .
2
(1)用化学方程式表示SO 形成硫酸型酸雨的反应: .
2
(2)在钠碱循环法中,Na SO 溶液作为吸收液,可由 NaOH 溶液吸收 SO 制
2 3 2
得,该反应的离子方程式是 .
(3)吸收液吸收 SO 的过程中,pH 随 n(SO 2﹣):n(HSO ﹣)变化关系如下
2 3 3
表:
n(SO 2﹣):n(HSO ﹣) 91:9 1:1 9:91
3 3
pH 8.2 7.2 6.2
①上表判断NaHSO 溶液显 性,用化学平衡原理解释: .
3
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母): .
a.c(Na+)=2c(SO 2﹣)+c(HSO ﹣)
3 3
b.c(Na+)>c(HSO ﹣)>c(SO 2﹣)>c(H+)=c(OH﹣)
3 3
c.c(Na+)+c(H+)=c(SO 2﹣)+c(HSO ﹣)+c(OH﹣)
3 3
(4)当吸收液的pH 降至约为6时,需送至电解槽再生.再生示意图如下:
①HSO ﹣在阳极放电的电极反应式是 .
3
②当阴极室中溶液 PH 升至 8以上时,吸收液再生并循环利用.简述再生原
理: .
第3页(共7页)9.(12分)用 Cl 生产某些含氯有机物时会产生副产物 HCl.利用反应 A,可
2
实现氯的循环利用.反应 A:4HCl+O 2Cl +2H O
2 2 2
(1)已知:i.反应A 中,4mol HCl被氧化,放出115.6kJ 的热量.
(2)ii.
①H O 的电子式是 .
2
②反应A 的热化学方程式是 .
③断开 1mol H﹣O 键与断开 1mol H﹣Cl 键所需能量相差约为 kJ,H O
2
中H﹣O 键比HCl中H﹣Cl键(填“强”或“弱”) .
(2)对于反应 A,如图是 4种投料比[n(HCl):n(O ),分别为 1:1、2:
2
1、4:1、6:1]下,反应温度对 HCl平衡转化率影响的曲线.
①曲线b对应的投料比是 .
②当曲线 b、c、d对应的投料比达到相同的 HCl平衡转化率时,对应的反应温
度与投料比的关系是 .
③投料比为 2:1、温度为 400℃时,平衡混合气中 Cl 的物质的量分数
2
是 .
10.(15分)有文献记载:在强碱性条件下,加热银氨溶液可能析出银镜.某
同学进行如下验证和对比实验.
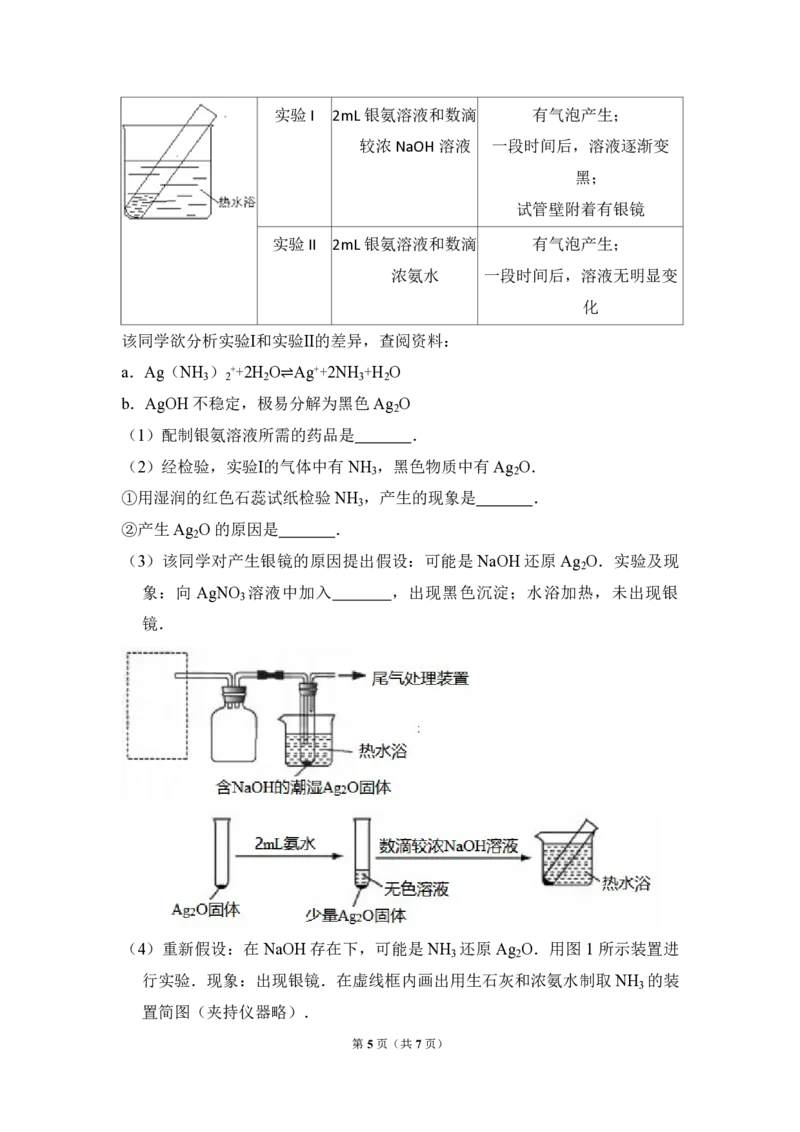
装置 实验序号 试管中的药品 现象
第4页(共7页)实验 I 2mL 银氨溶液和数滴 有气泡产生;
较浓 NaOH溶液 一段时间后,溶液逐渐变
黑;
试管壁附着有银镜
实验II 2mL 银氨溶液和数滴 有气泡产生;
浓氨水 一段时间后,溶液无明显变
化
该同学欲分析实验Ⅰ和实验Ⅱ的差异,查阅资料:
a.Ag(NH ) ++2H O⇌Ag++2NH +H O
3 2 2 3 2
b.AgOH 不稳定,极易分解为黑色Ag O
2
(1)配制银氨溶液所需的药品是 .
(2)经检验,实验Ⅰ的气体中有NH ,黑色物质中有Ag O.
3 2
①用湿润的红色石蕊试纸检验NH ,产生的现象是 .
3
②产生Ag O 的原因是 .
2
(3)该同学对产生银镜的原因提出假设:可能是 NaOH 还原 Ag O.实验及现
2
象:向 AgNO 溶液中加入 ,出现黑色沉淀;水浴加热,未出现银
3
镜.
(4)重新假设:在 NaOH 存在下,可能是 NH 还原 Ag O.用图 1所示装置进
3 2
行实验.现象:出现银镜.在虚线框内画出用生石灰和浓氨水制取 NH 的装
3
置简图(夹持仪器略).
第5页(共7页)(5)该同学认为在(4)的实验中会有 Ag(NH ) OH 生成.由此又提出假
3 2
设:在 NaOH 存在下,可能是 Ag(NH ) OH 也参与了 NH 还原 Ag O 的
3 2 3 2
反应.进行如图2实验:
①有部分Ag O 溶解在氨水中,该反应的化学方程式是 .
2
②实验结果证实假设成立,依据的现象是 .
(6)用HNO 清洗试管壁上的Ag,该反应的化学方程式是 .
3
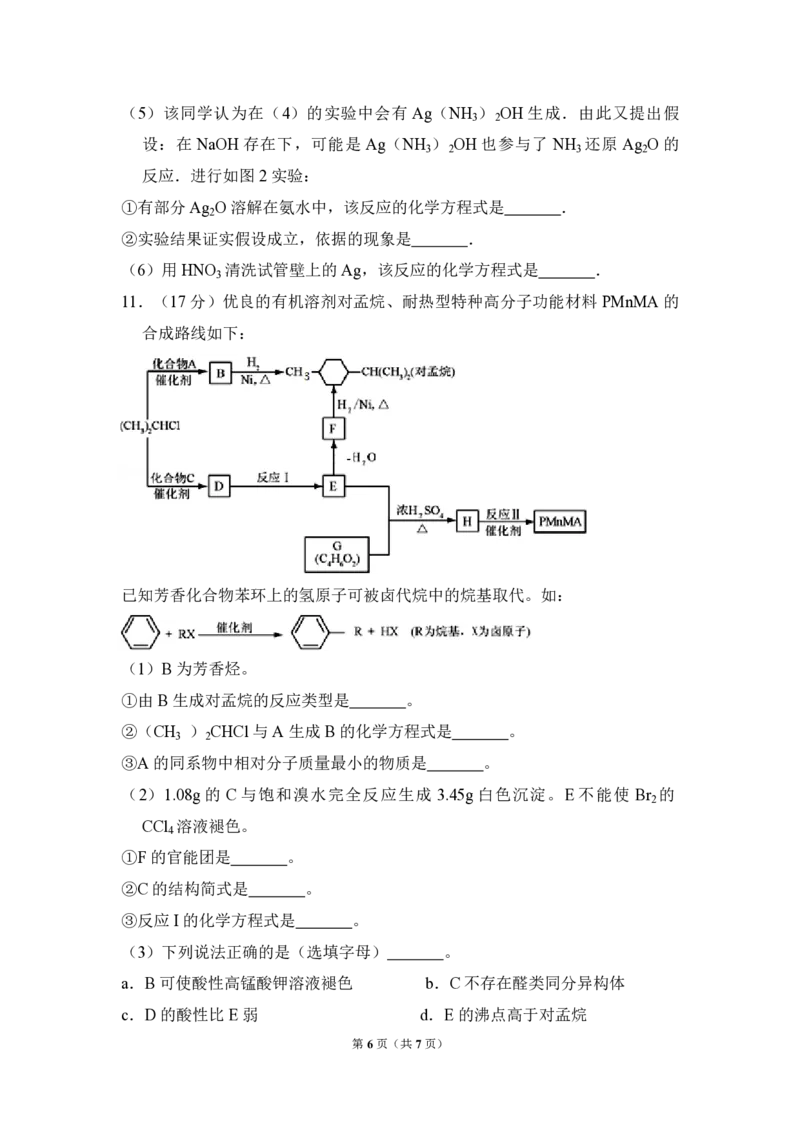
11.(17分)优良的有机溶剂对孟烷、耐热型特种高分子功能材料 PMnMA 的
合成路线如下:
已知芳香化合物苯环上的氢原子可被卤代烷中的烷基取代。如:
(1)B 为芳香烃。
①由B 生成对孟烷的反应类型是 。
②(CH ) CHCl 与A 生成B 的化学方程式是 。
3 2
③A 的同系物中相对分子质量最小的物质是 。
(2)1.08g的 C与饱和溴水完全反应生成 3.45g 白色沉淀。E不能使 Br 的
2
CCl 溶液褪色。
4
①F 的官能团是 。
②C的结构简式是 。
③反应I的化学方程式是 。
(3)下列说法正确的是(选填字母) 。
a.B可使酸性高锰酸钾溶液褪色 b.C不存在醛类同分异构体
c.D 的酸性比E弱 d.E的沸点高于对孟烷
第6页(共7页)(4)G 的核磁共振氢谱有 3种峰,其峰面积之比为 3:2:1.G 与 NaHCO 反
3
应放出CO .反应II 的化学方程式是 。
2
第7页(共7页)