文档内容
2013年全国统一高考化学试卷(大纲版)
一、选择题
1.下面有关发泡塑料饭盒的叙述,不正确的是( )
A.主要材质是高分子材料 B.价廉、质轻、保温性能好
C.适用于微波炉加热食品 D.不适于盛放含油较多的食品
2.反应X(g)+Y(g) 2Z(g);△H<0,达到平衡时,下列说法正确的是
( )
⇌
A.减小容器体积,平衡向右移动 B.加入催化剂,Z的产率增大
C.增大c(X),X的转化率增大 D.降低温度,Y的转化率增
大
3.下列关于同温同压下的两种气体12C18O和14N 的判断正确的是( )
2
A.体积相等时密度相等 B.原子数相等时具有的中子数相等
C.体积相等时具有的电子数相等 D.质量相等时具有的质子数相等
4.电解法处理酸性含铬废水(主要含有 Cr O 2﹣)时,以铁板作阴、阳极,处
2 7
理过程中存在反应 Cr O 2﹣+6Fe2++14H+═2Cr3++6Fe3++7H O,最后 Cr3+以 Cr
2 7 2
(OH) 形式除去,下列说法不正确的是( )
3
A.阳极反应为Fe﹣2e﹣═Fe2+
B.电解过程中溶液pH不会变化
C.过程中有Fe(OH) 沉淀生成
3
D.电路中每转移12mol电子,最多有1mol Cr O 2﹣被还原
2 7
5.下列操作不能达到目的是( )
选项 目的 操作
A. 配制100 mL 1.0 mol/L CuSO 溶液 将25 g CuSO •5H 0溶于100 mL蒸馏水中
4 4 2
B. 除去KNO 中少量NaCl 将混合物制成热的饱和溶液,冷却结
3
晶,过滤
C. 在溶液中将MnO ﹣完全转化为 向酸性KMnO 溶液中滴加H O 溶液至紫
4 4 2 2
Mn2+ 色消失
D. 确定NaCl溶液中是否混有Na CO 取少量溶液滴加CaCl 溶液,观察是否出
2 3 2
现白色浑浊
A.A B.B C.C D.D
6.能正确表示下列反应的离子方程式是( )A.用过量氨水吸收工业尾气中的SO :2NH •H 0+SO ═2NH ++SO 2﹣+H O
2 3 2 2 4 3 2
B.氯化钠固体与浓硫酸混合加热:H SO +2Cl﹣ SO ↑+Cl ↑+H O
2 4 2 2 2
C.磁性氧化铁溶于稀硝酸:3Fe2++4H++NO ﹣═3Fe3++NO↑+3H O
3 2
D.明矾溶液中滴入Ba(OH) 溶液使SO 2﹣恰好完全沉淀:2Ba2++3OH﹣
2 4
+Al3++2SO 2﹣═2BaSO ↓+Al(OH) ↓
4 4 3
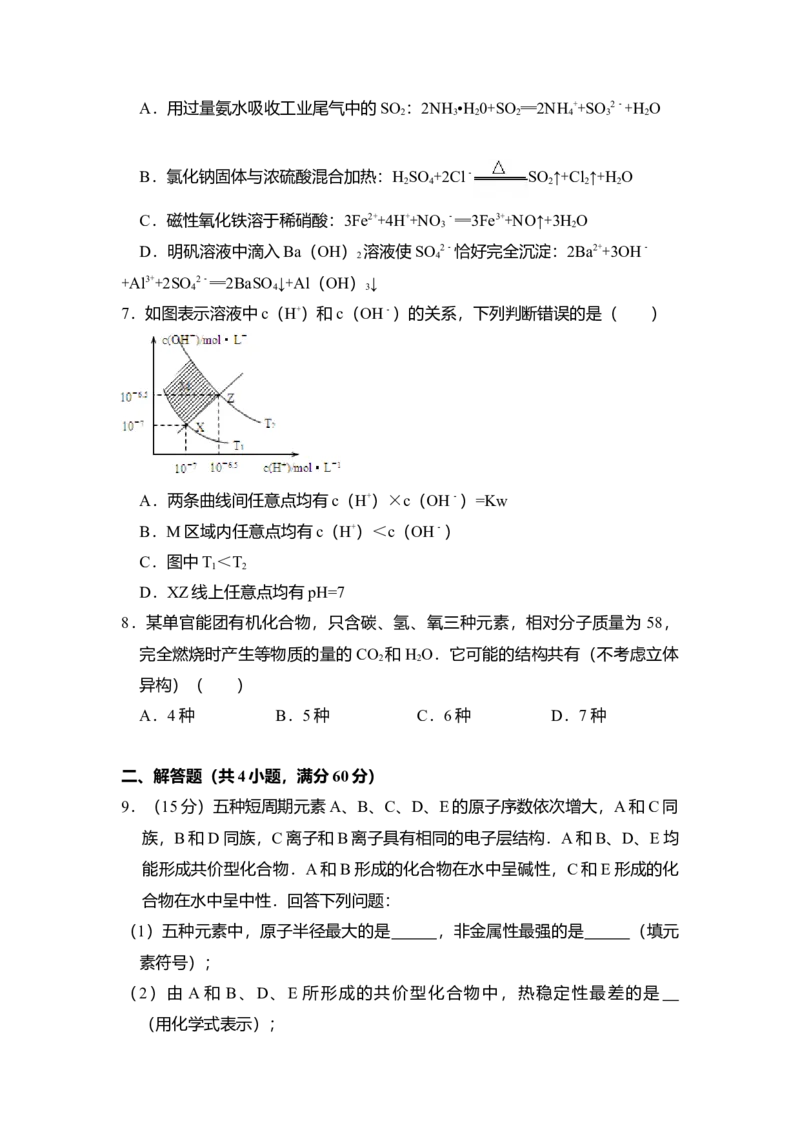
7.如图表示溶液中c(H+)和c(OH﹣)的关系,下列判断错误的是( )
A.两条曲线间任意点均有c(H+)×c(OH﹣)=Kw
B.M区域内任意点均有c(H+)<c(OH﹣)
C.图中T <T
1 2
D.XZ线上任意点均有pH=7
8.某单官能团有机化合物,只含碳、氢、氧三种元素,相对分子质量为 58,
完全燃烧时产生等物质的量的CO 和H O.它可能的结构共有(不考虑立体
2 2
异构)( )
A.4种 B.5种 C.6种 D.7种
二、解答题(共4小题,满分60分)
9.(15分)五种短周期元素A、B、C、D、E的原子序数依次增大,A和C同
族,B和D 同族,C离子和B离子具有相同的电子层结构.A和B、D、E均
能形成共价型化合物.A和B形成的化合物在水中呈碱性,C和E形成的化
合物在水中呈中性.回答下列问题:
(1)五种元素中,原子半径最大的是 ,非金属性最强的是 (填元
素符号);
(2)由 A 和 B、D、E 所形成的共价型化合物中,热稳定性最差的是
(用化学式表示);(3)A和E形成的化合物与A和B形成的化合物反应,产物的化学式为 ,
其中存在的化学键类型为 ;
(4)D最高价氧化物的水化物的化学式为 ;
(5)单质D在充足的单质E中燃烧,反应的化学方程式为 ;D在不充足
的E中燃烧,生成的主要产物的化学式为 ;
(6)单质E与水反应的离子方程式为 .
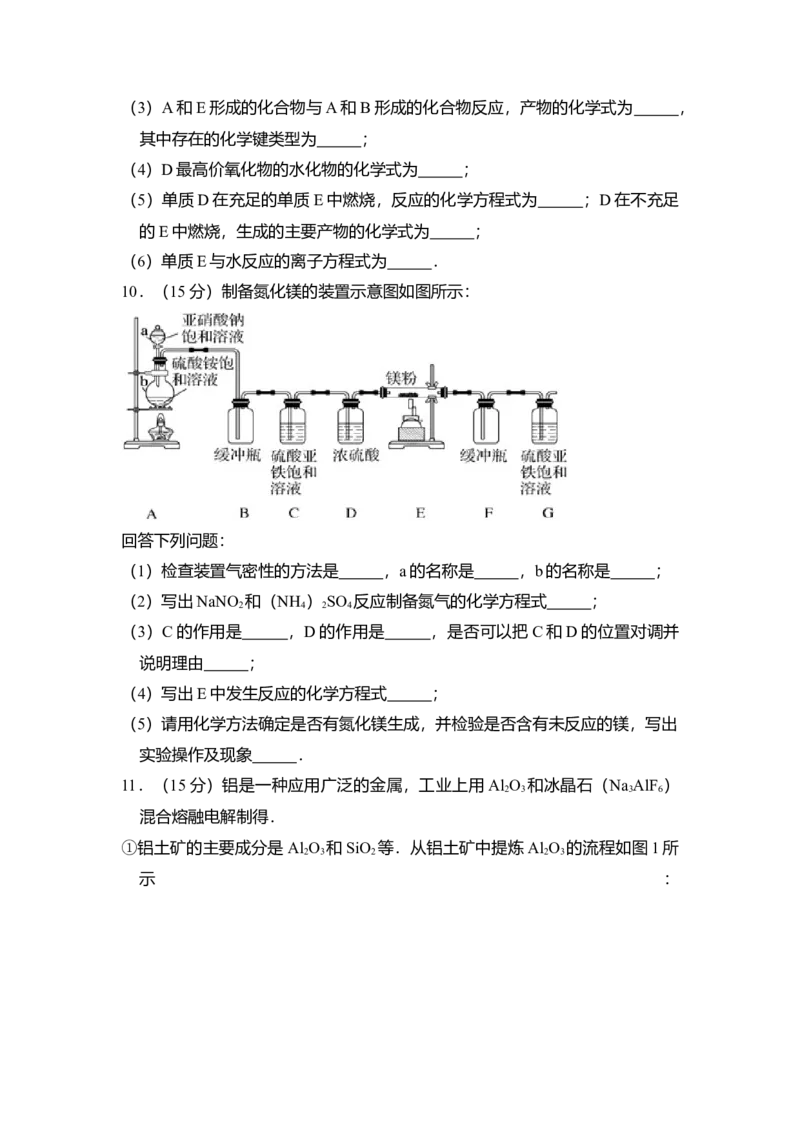
10.(15分)制备氮化镁的装置示意图如图所示:
回答下列问题:
(1)检查装置气密性的方法是 ,a的名称是 ,b的名称是 ;
(2)写出NaNO 和(NH ) SO 反应制备氮气的化学方程式 ;
2 4 2 4
(3)C的作用是 ,D的作用是 ,是否可以把C和D的位置对调并
说明理由 ;
(4)写出E中发生反应的化学方程式 ;
(5)请用化学方法确定是否有氮化镁生成,并检验是否含有未反应的镁,写出
实验操作及现象 .
11.(15分)铝是一种应用广泛的金属,工业上用 Al O 和冰晶石(Na AlF )
2 3 3 6
混合熔融电解制得.
①铝土矿的主要成分是Al O 和SiO 等.从铝土矿中提炼Al O 的流程如图1所
2 3 2 2 3
示 :图1
图2
②以萤石(CaF )和纯碱为原料制备冰晶石的流程如图2所示:
2
回答下列问题:
(1)写出反应1的化学方程式 ;
(2)滤液Ⅰ中加入CaO生成的沉淀是 ,反应2的离子方程式为 ;
(3)E可作为建筑材料,化合物C是 ,写出由D制备冰晶石的化学方程
式 ;
(4)电解制铝的化学方程式是 ,以石墨为电极,阳极产生的混合气体的
成分是 .
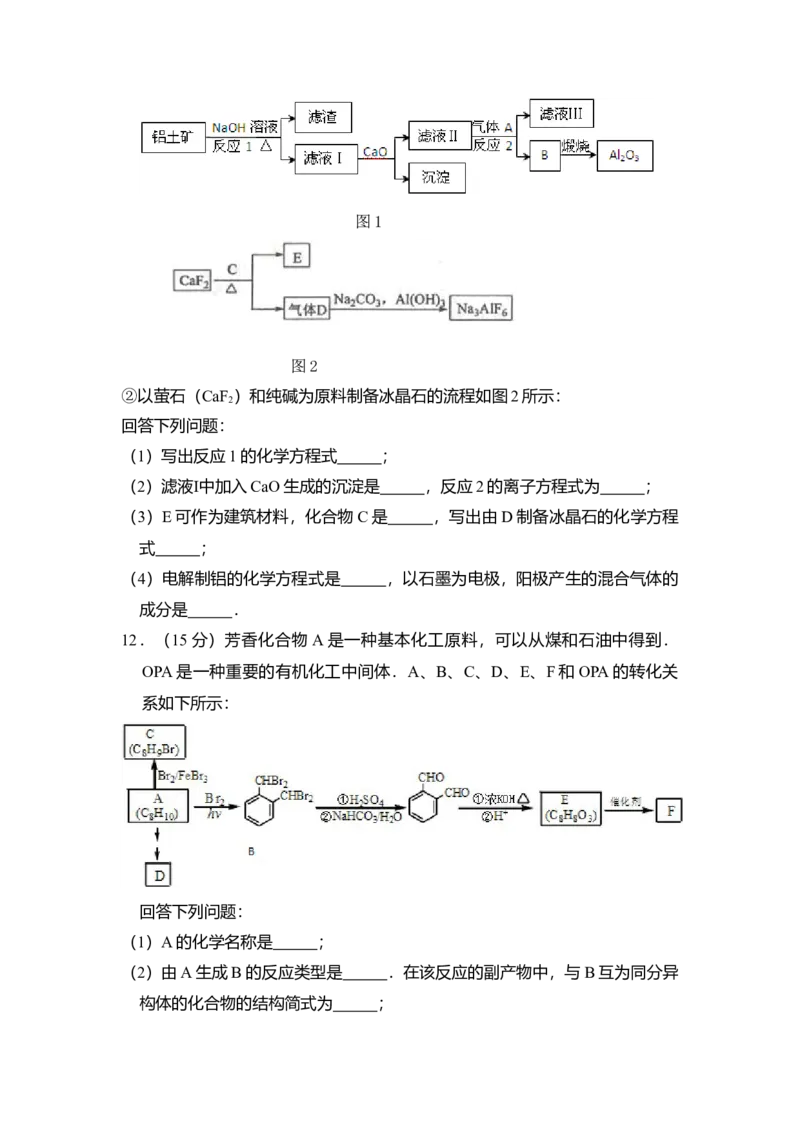
12.(15分)芳香化合物 A是一种基本化工原料,可以从煤和石油中得到.
OPA是一种重要的有机化工中间体.A、B、C、D、E、F和OPA的转化关
系如下所示:
回答下列问题:
(1)A的化学名称是 ;
(2)由A生成B 的反应类型是 .在该反应的副产物中,与B互为同分异
构体的化合物的结构简式为 ;(3)写出C所有可能的结构简式 ;
(4)D(邻苯二甲酸二乙酯)是一种增塑剂.请用A、不超过两个碳的有机物
及合适的无机试剂为原料,经两步反应合成D.用化学方程式表示合成路线
;
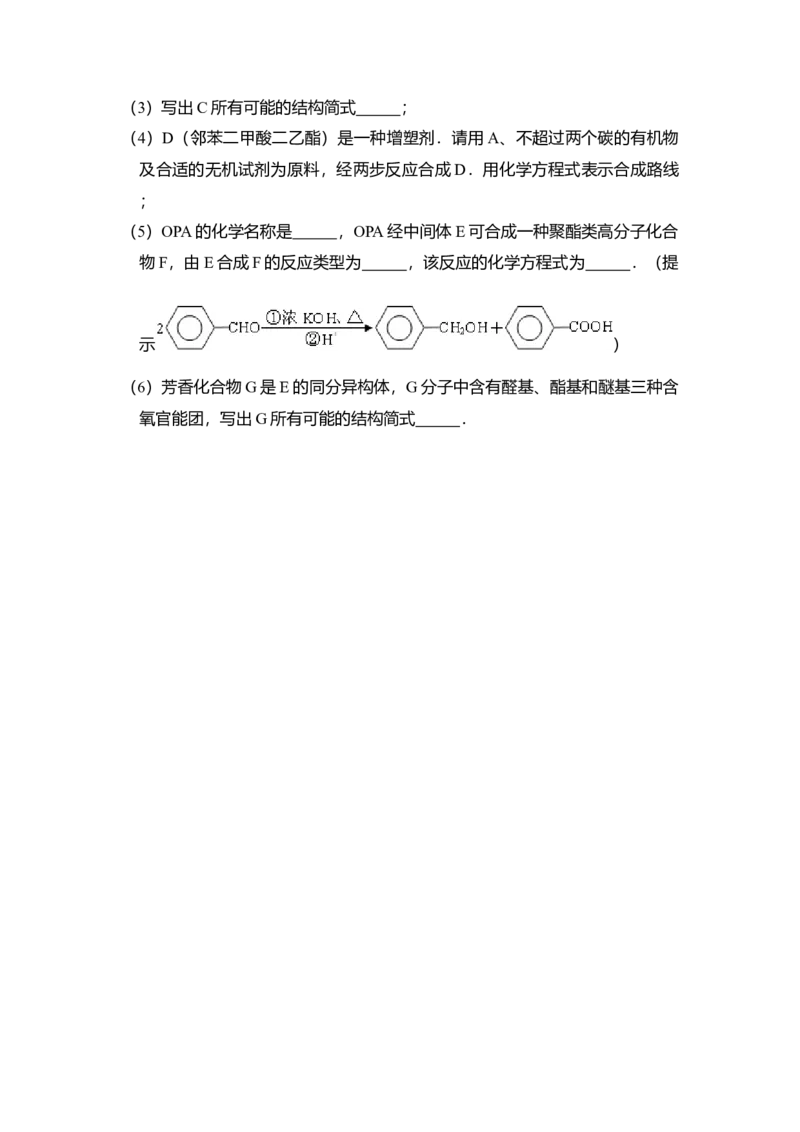
(5)OPA的化学名称是 ,OPA经中间体E可合成一种聚酯类高分子化合
物F,由E合成F的反应类型为 ,该反应的化学方程式为 .(提
示 )
(6)芳香化合物G是E的同分异构体,G分子中含有醛基、酯基和醚基三种含
氧官能团,写出G所有可能的结构简式 .