文档内容
2013 年福建省高考化学试卷
一、选择题(共7小题,每小题6分,共42分)
6.化学与社会、生产、生活紧切相关.下列说法正确的是( )
A.石英只能用于生产光导纤维
B.从海水中提取物质都必须通过化学反应才能实现
C.为了增加食物的营养成分,可以大量使用食品添加剂
D.“地沟油”禁止食用,但可以用来制肥皂
7.下列关于有机化合物的说法正确的是( )
A.乙酸和乙酸乙酯可用Na CO 溶液加以区别
2 3
B.戊烷(C H )有两种同分异构体
5 12
C.乙烯、聚氯乙烯和苯分子中均含有碳碳双键
D.糖类、油脂和蛋白质均可发生水解反应
8.室温下,对于0.10mol•L-1的氨水,下列判断正确的是( )
A.与AlCl 溶液发生反应的离子方程式为Al3++3OH-═Al(OH) ↓
3 3
B.加水稀释后,溶液中c(NH +)•c(OH-)变大
4
C.用HNO 溶液完全中和后,溶液不显中性
3
D.其溶液的pH=13
9.四种短周期元素在周期表中的位置如右图,其中只
有M为金属元素.下列说法不正确的是( )
A.原子半径Z<M
B.Y的最高价氧化物对应水化物的酸性比X的弱
C.X的最简单气态氢化物的热稳定性比Z的小
D.Z位于元素周期表中第2周期、第ⅥA族
10.下列有关实验的做法不正确的是( )
A.分液时,分液漏斗中的上层液体应由上口倒出
B.用加热分解的方法区分碳酸钠和碳酸氢钠两种固体C.配置0.1000 mol•L-1氯化钠溶液时,将液体转移到容量瓶中需用玻璃棒引
流
D.检验NH +时,往试样中加入NaOH溶液,微热,用湿润的蓝色石蕊试纸
4
检验逸出的气体
11.某科学家利用二氧化铈(CeO )在太阳能作用下将H O、CO 转变为
2 2 2
H 、CO.其过程如下:
2
下列说法不正确的是( )
A.该过程中CeO 没有消耗
2
B.该过程实现了太阳能向化学能的转化
C.右图中△H = H + H
1 2 3
D.以CO和O 构△成的△碱性燃料电池的负极反应式CO+4OH--2e-═CO 2-
2 3
+2H O
2
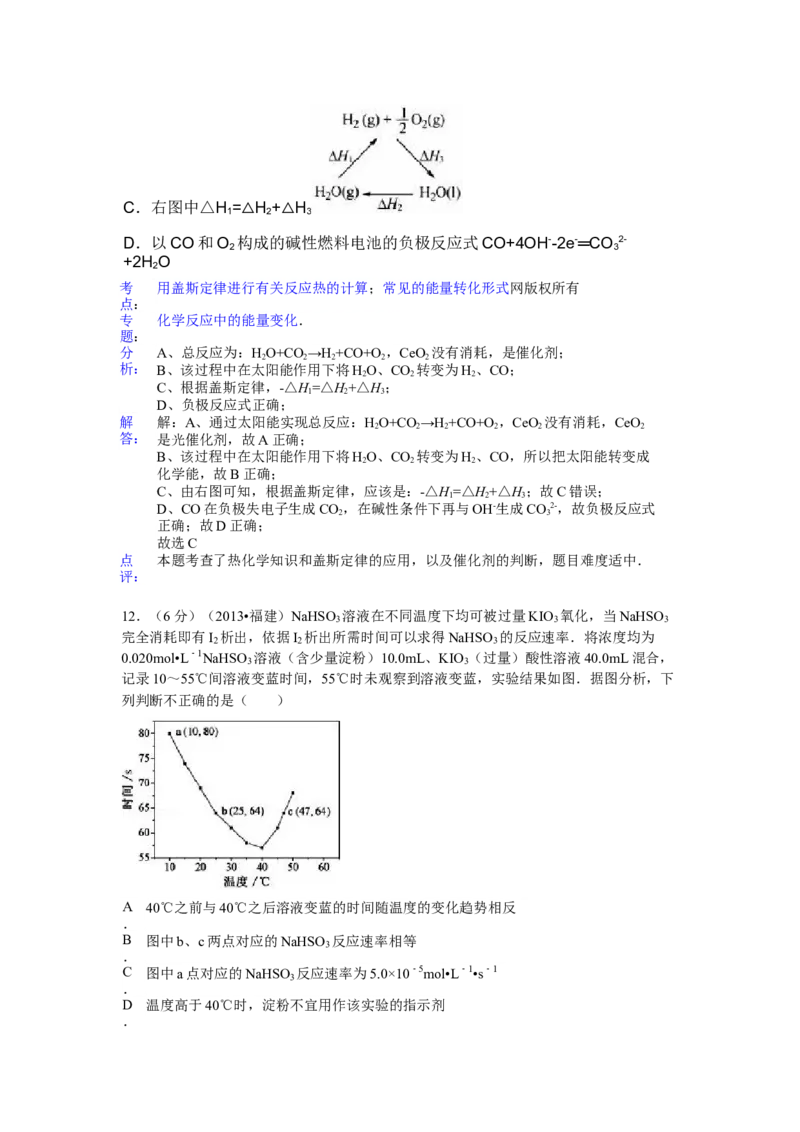
12..NaHSO 溶液在不同温度下均可被过量KIO 氧化,当NaHSO 完全消耗
3 3 3
即有I 析出,依据I 析出所需时间可以求得NaHSO 的反应速率.将浓度均为
2 2 3
0.020mol•L-1NaHSO 溶液(含少量淀粉)10.0mL、KIO (过量)酸性溶液
3 3
40.0mL混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结
果如图.据图分析,下列判断不正确的是( )
A.40℃之前与40℃之后溶液变蓝的时间随温度的变化趋势相反B.图中b、c两点对应的NaHSO 反应速率相等
3
C.图中a点对应的NaHSO 反应速率为5.0×10-5mol•L-1•s-1
3
D.温度高于40℃时,淀粉不宜用作该实验的指示剂
二、解答题(共5小题)
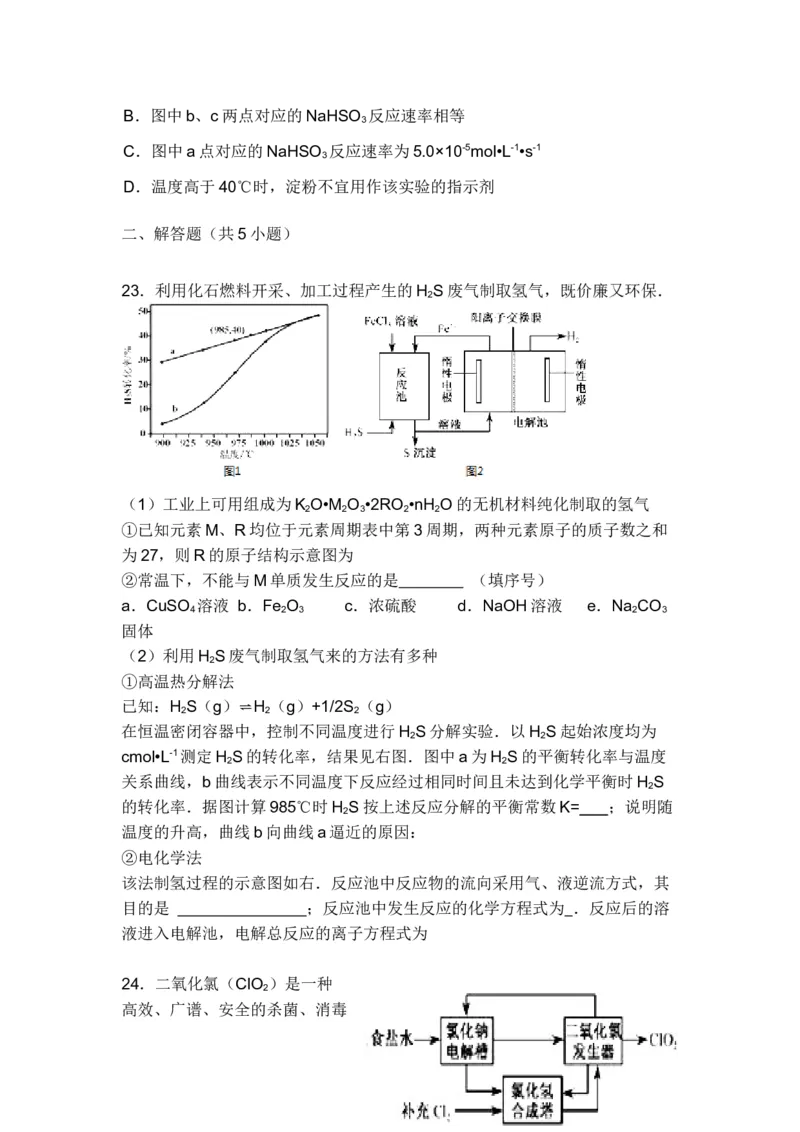
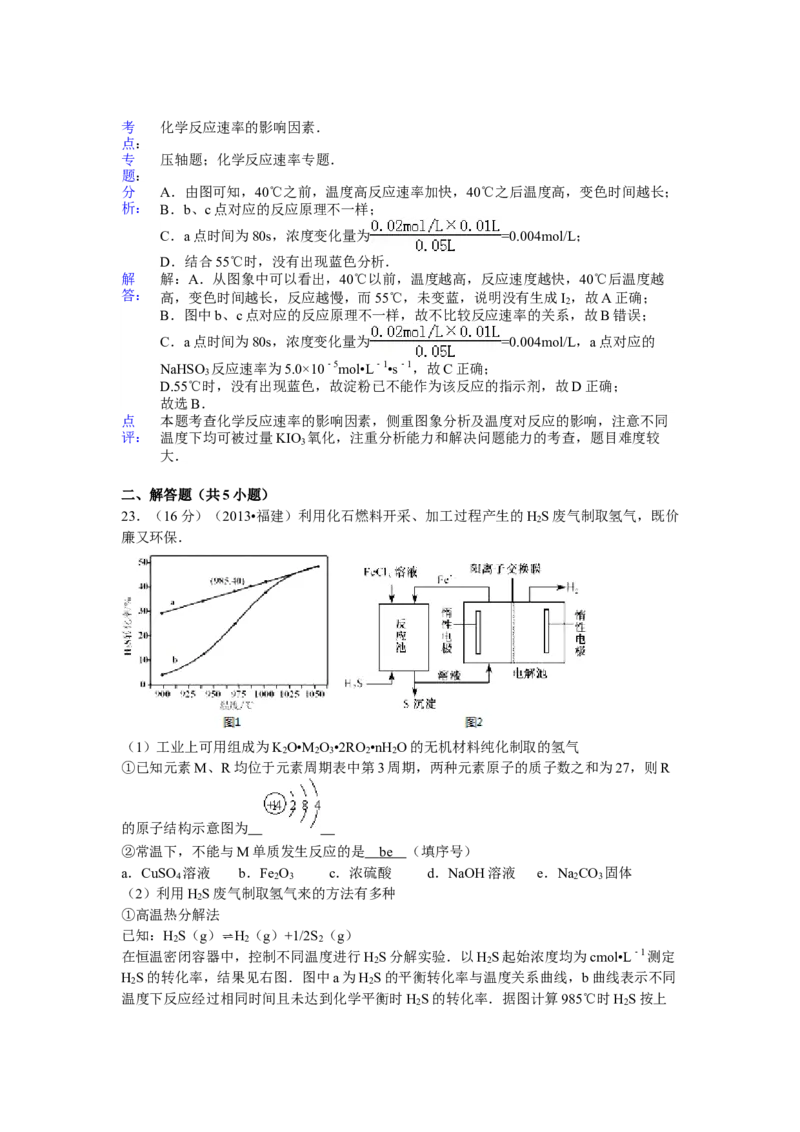
23.利用化石燃料开采、加工过程产生的H S废气制取氢气,既价廉又环保.
2
(1)工业上可用组成为K O•M O •2RO •nH O的无机材料纯化制取的氢气
2 2 3 2 2
①已知元素M、R均位于元素周期表中第3周期,两种元素原子的质子数之和
为27,则R的原子结构示意图为
②常温下,不能与M单质发生反应的是 (填序号)
a.CuSO 溶液 b.Fe O c.浓硫酸 d.NaOH溶液 e.Na CO
4 2 3 2 3
固体
(2)利用H S废气制取氢气来的方法有多种
2
①高温热分解法
已知:H
2
S(g) ⇌H
2
(g)+1/2S
2
(g)
在恒温密闭容器中,控制不同温度进行H S分解实验.以H S起始浓度均为
2 2
cmol•L-1测定H S的转化率,结果见右图.图中a为H S的平衡转化率与温度
2 2
关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H S
2
的转化率.据图计算985℃时H S按上述反应分解的平衡常数K= ;说明随
2
温度的升高,曲线b向曲线a逼近的原因:
②电化学法
该法制氢过程的示意图如右.反应池中反应物的流向采用气、液逆流方式,其
目的是 ;反应池中发生反应的化学方程式为 .反应后的溶
液进入电解池,电解总反应的离子方程式为
24.二氧化氯(ClO )是一种
2
高效、广谱、安全的杀菌、消毒剂.
(1)氯化钠电解法是一种可靠的工业生产ClO 方法.
2
①用于电解的食盐水需先除去其中的Ca2+、Mg2+、SO 2-等杂质.其次除杂操作
4
时,往粗盐水中先加入过量的 (填化学式),至沉淀不再产生后,再加入过
量的Na CO 和NaOH,充分反应后将沉淀一并滤去.经检测发现滤液中仍含
2 3
有一定量的SO 2-,其原因是
4
【已知:Ksp(BaSO )=1.1×10-10、Ksp(BaCO )=5.1×10-9】
4 3
②该法工艺原理如图.其过程是将食盐水在特定条件下电解得到的氯酸钠
(NaClO )与盐酸反应生成ClO .工艺中可以利用的单质有 (填
3 2
化学式),发生器中生成ClO 的化学方程式为 .
2
(2)纤维素还原法制ClO 是一种新方法,其原理是:纤维素水解得到的最终
2
产物D与NaClO 反应生成ClO .完成反应的化学方程式:
3 2
(3)ClO 和Cl 均能将电镀废水中的CN-氧化为无毒的物质,自身被还原为
2 2
Cl-.处理含CN-相同时的电镀废水,所需Cl 的物质的量是ClO 的 倍.
2 2
25.固体硝酸盐加热易分解且产物较复杂.某学习小组以Mg(NO ) 为研究
3 2
对象,拟通过实验探究其热分解的产物,提出如下4种猜想:
甲:Mg(NO ) 、NO 、O 乙:MgO、NO 、O 丙:Mg N 、O 丁:
3 2 2 2 2 2 3 2 2
MgO、NO 、N
2 2
(1)实验前,小组成员经讨论认定猜想丁不成立,理由是
.
查阅资料得知:2NO +2NaOH═NaNO +NaNO +H O
2 3 2 2
针对甲、乙、丙猜想,设计如下图所示的实验装置(图中加热、夹持仪器等均
省略):
(2)实验过程
①仪器连接后,放入固体试剂之前,关闭k,微热硬质玻璃管(A),观察到E
中有气泡连续放出,表明
②称取Mg(NO ) 固体3.7g置于A中,加热前通入N 以驱尽装置内的空气,
3 2 2
其目的是;关闭K,用酒精灯加热时,正确操作是先 然后固
定在管中固体部位下加热.
③观察到A中有红棕色气体出现,C、D中未见明显变化.
④待样品完全分解,A装置冷却至室温、称量,测得剩余固体的质量为1.0g.
⑤取少量剩余固体于试管中,加入适量水,未见明显现象.
(3)实验结果分析讨论
①根据实验现象和剩余固体的质量经分析可初步确认猜想 是正确的.
②根据D中无明显现象,一位同学认为不能确认分解产物中有O ,因为若有
2
O ,D中将发生氧化还原反应: (填写化学方
2
程式),溶液颜色会退去;小组讨论认定分解产物中有O 存在,未检侧到的原
2
因是 .
③小组讨论后达成的共识是上述实验设计仍不完善,需改进装置进一步研究.
31.(1)依据第2周期元素第一电离能的变化规律,
参照右图B、F元素的位置,用小黑点标出C、N、O三
种元素的相对位置.
(2)NF 可由NH 和F 在Cu催化剂存在下反应直接得
3 3 2
到:
2NH +3F ==Cu===NF +3NH F
3 2 3 4
①上述化学方程式中的5种物质所属的晶体类型有
(填序号).
a.离子晶体b.分子晶体c.原子晶体d.金属晶体
②基态铜原子的核外电子排布式为
(3)BF 与一定量水形成(H O) •BF 晶体Q,Q在一定条件下可转化为R:
3 2 2 3
①晶体Q中各种微粒间的作用力不涉及 (填序号).
a.离子键 b.共价键 c.配位键 d.金属键 e.氢键 f.范德华力
②R中阳离子的空间构型为 ,阴离子的中心原子轨道采用
杂化.
(4)已知苯酚( )具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离
形成的离子 能形成分子内氢键.据此判断,相同温度下电离平衡常
数K (水杨酸) K (苯酚)(填“>”或“<”),其原因是
a2 a
.
32.已知:
为合成某种液晶材料的中间体M,有人提出如下不同的合成途径(1)常温下,下列物质能与A发生反应的有 (填序号)
a.苯 b.Br /CCl c.乙酸乙酯 d.KMnO /H+溶液
2 4 4
(2)M中官能团的名称是 ,由C→B反应类型为
(3)由A催化加氢生成M的过程中,可能有中间生成物
和 (写结构简式)生成
(4)检验B中是否含有C可选用的试剂是 (任写一种名称).
(5)物质B也可由C H Cl与NaOH水溶液共热生成,C H Cl的结构简式
10 13 10 13
为 .
(6)C的一种同分异构体E具有如下特点:
a.分子中含-OCH CH b.苯环上只有两种化学环境不同的氢原子
2 3
写出E在一定条件下发生加聚反应的化学方程式
2013 年福建省高考化学试卷
参考答案与试题解析
一、选择题(共7小题,每小题6分,共42分)
6.(6分)(2013•福建)化学与社会、生产、生活紧切相关.下列说法正确的是( )
A 石英只能用于生产光导纤维
.
B 从海水中提取物质都必须通过化学反应才能实现.
C 为了增加食物的营养成分,可以大量使用食品添加剂
.
D “地沟油”禁止食用,但可以用来制肥皂
.
考 硅和二氧化硅;海水资源及其综合利用;常见的食品添加剂的组成、性质和作用.
菁优网版权所有
点:
专 化学应用.
题:
分 A.石英的主要成分是二氧化硅;
析: B.从海水中可以提取氯化钠;
C.食品添加剂应适量添加;
D.“地沟油”主要成分是油脂.
解 解:A.石英的主要成分是二氧化硅,纯净的二氧化硅用于生产光导纤维,结晶的二
答: 氧化硅(如水晶、玛瑙等)用作饰物,故A错误;
B.从海水中提取蒸馏水和盐时,通过蒸馏、蒸发等物理变化就能实现,提取溴、
碘、镁等物质时,必须通过化学反应才能实现,故B错误;
C.食品添加剂应适量添加,过量会对人体产生危害,故C错误;
D.“地沟油”禁止食用,但其主要成分是油脂,在碱性溶液中发生水解反应,又称
皂化反应,可用于制取肥皂,故D正确.
故选D.
点 本题考查二氧化硅的用途、物质的分离、食品添加剂、油脂等,难度不大,注意
评: “地沟油”禁止食用,但其主要成分是油脂,在碱性溶液中发生水解反应,又称皂
化反应,可用于制取肥皂.
7.(6分)(2013•福建)下列关于有机化合物的说法正确的是( )
A 乙酸和乙酸乙酯可用Na CO 溶液加以区别
2 3
.
B 戊烷(C H )有两种同分异构体
5 12
.
C 乙烯、聚氯乙烯和苯分子中均含有碳碳双键
.
D 糖类、油脂和蛋白质均可发生水解反应
.
考 有机物的鉴别;同分异构现象和同分异构体;油脂的性质、组成与结构;氨基酸、
点: 蛋白质的结构和性质特点.
菁优网版权所有
专 有机物的化学性质及推断;有机物分子组成通式的应用规律.
题:
分 A.乙酸可与碳酸钠反应,乙酸乙酯不溶于饱和碳酸钠溶液;
析: B.戊烷有3种同分异构体;
C.聚乙烯和苯分子中不含碳碳双键;
D.单糖不能发生水解.
解 解:A.酸可与碳酸钠反应,乙酸乙酯不溶于饱和碳酸钠溶液,二者现象不同,可鉴
答: 别,故A正确;
B.戊烷有正戊烷、异戊烷、新戊烷3种同分异构体,故B错误;
C.聚乙烯和苯分子中不含碳碳双键,故C错误;
D.糖中的单糖不能发生水解,故D错误.
故选A.
点 本题考查较为综合,涉及有机物的鉴别、同分异构体、有机物结构和性质等知识,
评: 题目难度不大,注意相关基础知识的积累.
8.(6分)(2013•福建)室温下,对于0.10mol•L﹣1的氨水,下列判断正确的是( )A 与AlCl 溶液发生反应的离子方程式为Al3++3OH﹣═Al(OH) ↓
3 3
.
B 加水稀释后,溶液中c(NH +)•c(OH﹣)变大
4
.
C 用HNO 溶液完全中和后,溶液不显中性
3
.
D 其溶液的pH=13
.
考 弱电解质在水溶液中的电离平衡.
菁优网版权所有
点:
专 电离平衡与溶液的pH专题.
题:
分 A.弱电解质要写化学式,且氢氧化铝不溶于弱碱;
析: B.加水稀释促进一水合氨电离,但铵根离子、氢氧根离子浓度都减小;
C.硝酸铵是强酸弱碱盐,其溶液呈酸性;
D.一水合氨是弱电解质,在氨水中部分电离.
解 解:A.一水合氨是弱电解质,离子方程式中要写化学式,该反应的离子方程式为:
答: Al3++3NH .H O═Al(OH) ↓+3NH +,故A错误;
3 2 3 4
B.加水稀释促进一水合氨电离,但铵根离子、氢氧根离子浓度都减小,所以c
(NH +)•c(OH﹣)减小,故B错误;
4
C.含有弱根离子的盐,谁强谁显性,硝酸铵是强酸弱碱盐,所以其溶液呈酸性,故
C正确;
D.一水合氨是弱电解质,在氨水中部分电离,所以0.10mol•L﹣1氨水的pH小于
13,故D错误;
故选C.
点 本题考查弱电解质的电离、离子方程式的书写、盐类的水解等知识点,根据盐类水
评: 解特点、弱电解质的电离特点、离子方程式的书写规则来分析解答即可,难度中
等.
9.(6分)(2013•福建)四种短周期元素在周期表中的位置如右图,其中只有M为金属
元素.下列说法不正确的是( )
A 原子半径Z<M
.
B Y的最高价氧化物对应水化物的酸性比X的弱
.
C X的最简单气态氢化物的热稳定性比Z的小
.
D Z位于元素周期表中第2周期、第ⅥA族
.
考 位置结构性质的相互关系应用.
菁优网版权所有
点:
专 元素周期律与元素周期表专题.
题:
分 根据元素在周期表中的位置可知,这Y、Z处于第二周期,M、X处于第三周期,只
析: 有M为金属元素,掌握M为Al元素,则X为Si元素、Y为氮元素、Z为氧元素,
据此结合元素周期律解答.
解 解:根据元素在周期表中的位置可知,这Y、Z处于第二周期,M、X处于第三周
答: 期,只有M为金属元素,掌握M为Al元素,则X为Si元素、Y为氮元素、Z为氧
元素,A.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径O<
Al,故A正确;
B.非金属性N>Si,故酸性HNO >H SiO ,故B错误;
3 2 3
C.非金属性Si<O,故氢化物稳定性SiH <H O,故C正确;
4 2
D.Z为氧元素,位于元素周期表中第2周期第ⅥA族,故D正确;
故选B.
点 本题考查结构性质位置关系、元素周期律等,难度不大,推断元素是解题关键,注
评: 意对元素周期表的整体把握,注意对元素周期律的理解掌握.
10.(6分)(2013•福建)下列有关实验的做法不正确的是( )
A 分液时,分液漏斗中的上层液体应由上口倒出
.
B 用加热分解的方法区分碳酸钠和碳酸氢钠两种固体
.
C 配置0.1000 mol•L﹣1氯化钠溶液时,将液体转移到容量瓶中需用玻璃棒引流
.
D 检验NH +时,往试样中加入NaOH溶液,微热,用湿润的蓝色石蕊试纸检验逸出的气
4
. 体
考 分液和萃取;铵离子检验;配制一定物质的量浓度的溶液;探究碳酸钠与碳酸氢钠
点: 的性质.
菁优网版权所有
专 实验评价题.
题:
分 A.本题根据分液操作时下层液体从下口放出,上层液体从上口倒出;
析: B.碳酸氢钠受热分解生成二氧化碳和水;
C.转移溶液时可使用玻璃棒引流;
D.氨气遇红色石蕊试纸变蓝色.
解 解:A.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出,一避
答: 免两种液体相互污染,故A正确;
B.碳酸钠受热不分解;碳酸氢钠受热分解生成二氧化碳和水,故B正确;
C.将液体转移到容量瓶中需用玻璃棒引流,故C正确;
D.检验氨气时应该是用湿润的红色石蕊试纸检验,故D错误.
故选D.
点 本题考查分液、物质的检验、实验基本操作等,难度不大,注意检验氨气时应该是
评: 用湿润的红色石蕊试纸检验.
11.(6分)(2013•福建)某科学家利用二氧化铈(CeO )在太阳能作用下将H O、CO
2 2 2
转变为H 、CO.其过程如下:
2
下列说法不正确的是( )
A.该过程中CeO 没有消耗
2
B.该过程实现了太阳能向化学能的转化C.右图中△H = H + H
1 2 3
D.以CO和O 构△成的△碱性燃料电池的负极反应式CO+4OH--2e-═CO 2-
2 3
+2H O
2
考 用盖斯定律进行有关反应热的计算;常见的能量转化形式网版权所有
点:
专 化学反应中的能量变化.
题:
分 A、总反应为:HO+CO→H+CO+O ,CeO 没有消耗,是催化剂;
2 2 2 2 2
析: B、该过程中在太阳能作用下将HO、CO 转变为H、CO;
2 2 2
C、根据盖斯定律,-△H=△H+△H;
1 2 3
D、负极反应式正确;
解 解:A、通过太阳能实现总反应:HO+CO→H+CO+O ,CeO 没有消耗,CeO
2 2 2 2 2 2
答: 是光催化剂,故A正确;
B、该过程中在太阳能作用下将HO、CO 转变为H、CO,所以把太阳能转变成
2 2 2
化学能,故B正确;
C、由右图可知,根据盖斯定律,应该是:-△H=△H+△H;故C错误;
1 2 3
D、CO在负极失电子生成CO,在碱性条件下再与OH-生成CO2-,故负极反应式
2 3
正确;故D正确;
故选C
点 本题考查了热化学知识和盖斯定律的应用,以及催化剂的判断,题目难度适中.
评:
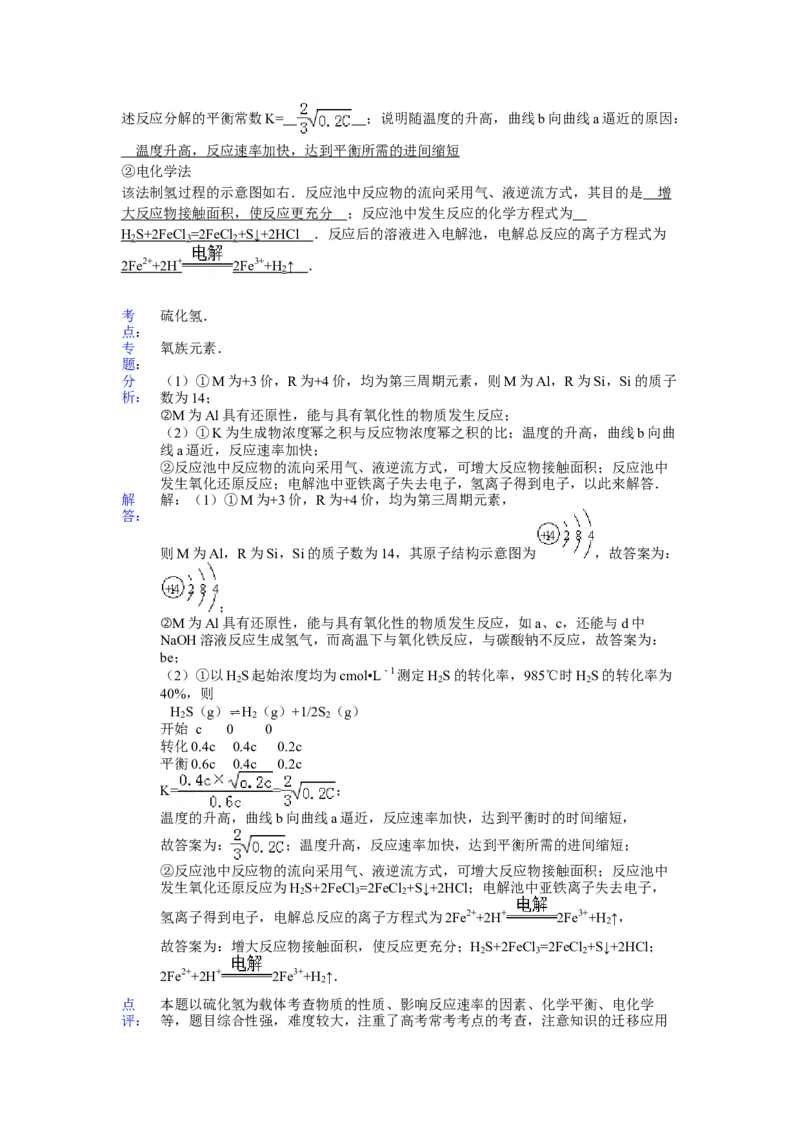
12.(6分)(2013•福建)NaHSO 溶液在不同温度下均可被过量KIO 氧化,当NaHSO
3 3 3
完全消耗即有I 析出,依据I 析出所需时间可以求得NaHSO 的反应速率.将浓度均为
2 2 3
0.020mol•L﹣1NaHSO 溶液(含少量淀粉)10.0mL、KIO (过量)酸性溶液40.0mL混合,
3 3
记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图.据图分析,下
列判断不正确的是( )
A 40℃之前与40℃之后溶液变蓝的时间随温度的变化趋势相反
.
B 图中b、c两点对应的NaHSO 反应速率相等
3
.
C 图中a点对应的NaHSO 反应速率为5.0×10﹣5mol•L﹣1•s﹣1
3
.
D 温度高于40℃时,淀粉不宜用作该实验的指示剂
.考 化学反应速率的影响因素.
菁优网版权所有
点:
专 压轴题;化学反应速率专题.
题:
分 A.由图可知,40℃之前,温度高反应速率加快,40℃之后温度高,变色时间越长;
析: B.b、c点对应的反应原理不一样;
C.a点时间为80s,浓度变化量为 =0.004mol/L;
D.结合55℃时,没有出现蓝色分析.
解 解:A.从图象中可以看出,40℃以前,温度越高,反应速度越快,40℃后温度越
答: 高,变色时间越长,反应越慢,而55℃,未变蓝,说明没有生成I ,故A正确;
2
B.图中b、c点对应的反应原理不一样,故不比较反应速率的关系,故B错误;
C.a点时间为80s,浓度变化量为 =0.004mol/L,a点对应的
NaHSO 反应速率为5.0×10﹣5mol•L﹣1•s﹣1,故C正确;
3
D.55℃时,没有出现蓝色,故淀粉已不能作为该反应的指示剂,故D正确;
故选B.
点 本题考查化学反应速率的影响因素,侧重图象分析及温度对反应的影响,注意不同
评: 温度下均可被过量KIO 氧化,注重分析能力和解决问题能力的考查,题目难度较
3
大.
二、解答题(共5小题)
23.(16分)(2013•福建)利用化石燃料开采、加工过程产生的H S废气制取氢气,既价
2
廉又环保.
(1)工业上可用组成为K O•M O •2RO •nH O的无机材料纯化制取的氢气
2 2 3 2 2
①已知元素M、R均位于元素周期表中第3周期,两种元素原子的质子数之和为27,则R
的原子结构示意图为
②常温下,不能与M单质发生反应的是 b e (填序号)
a.CuSO 溶液 b.Fe O c.浓硫酸 d.NaOH溶液 e.Na CO 固体
4 2 3 2 3
(2)利用H S废气制取氢气来的方法有多种
2
①高温热分解法
已知:H
2
S(g) ⇌H
2
(g)+1/2S
2
(g)
在恒温密闭容器中,控制不同温度进行H S分解实验.以H S起始浓度均为cmol•L﹣1测定
2 2
H S的转化率,结果见右图.图中a为H S的平衡转化率与温度关系曲线,b曲线表示不同
2 2
温度下反应经过相同时间且未达到化学平衡时H S的转化率.据图计算985℃时H S按上
2 2述反应分解的平衡常数K= ;说明随温度的升高,曲线b向曲线a逼近的原因:
温度升高,反应速率加快,达到平衡所需的进间缩短
②电化学法
该法制氢过程的示意图如右.反应池中反应物的流向采用气、液逆流方式,其目的是 增
大反应物接触面积,使反应更充分 ;反应池中发生反应的化学方程式为
H S+2FeCl =2FeCl +S↓+2HCl .反应后的溶液进入电解池,电解总反应的离子方程式为
2 3 2
2Fe 2+ +2H + 2Fe 3+ +H ↑ .
2
考 硫化氢.
菁优网版权所有
点:
专 氧族元素.
题:
分 (1)①M为+3价,R为+4价,均为第三周期元素,则M为Al,R为Si,Si的质子
析: 数为14;
②M为Al具有还原性,能与具有氧化性的物质发生反应;
(2)①K为生成物浓度幂之积与反应物浓度幂之积的比;温度的升高,曲线b向曲
线a逼近,反应速率加快;
②反应池中反应物的流向采用气、液逆流方式,可增大反应物接触面积;反应池中
发生氧化还原反应;电解池中亚铁离子失去电子,氢离子得到电子,以此来解答.
解 解:(1)①M为+3价,R为+4价,均为第三周期元素,
答:
则M为Al,R为Si,Si的质子数为14,其原子结构示意图为 ,故答案为:
;
②M为Al具有还原性,能与具有氧化性的物质发生反应,如a、c,还能与d中
NaOH溶液反应生成氢气,而高温下与氧化铁反应,与碳酸钠不反应,故答案为:
be;
(2)①以H S起始浓度均为cmol•L﹣1测定H S的转化率,985℃时H S的转化率为
2 2 2
40%,则
H
2
S(g) ⇌H
2
(g)+1/2S
2
(g)
开始 c 0 0
转化0.4c 0.4c 0.2c
平衡0.6c 0.4c 0.2c
K= = ;
温度的升高,曲线b向曲线a逼近,反应速率加快,达到平衡时的时间缩短,
故答案为: ;温度升高,反应速率加快,达到平衡所需的进间缩短;
②反应池中反应物的流向采用气、液逆流方式,可增大反应物接触面积;反应池中
发生氧化还原反应为H S+2FeCl =2FeCl +S↓+2HCl;电解池中亚铁离子失去电子,
2 3 2
氢离子得到电子,电解总反应的离子方程式为2Fe2++2H+ 2Fe3++H ↑,
2
故答案为:增大反应物接触面积,使反应更充分;H S+2FeCl =2FeCl +S↓+2HCl;
2 3 2
2Fe2++2H+ 2Fe3++H ↑.
2
点 本题以硫化氢为载体考查物质的性质、影响反应速率的因素、化学平衡、电化学
评: 等,题目综合性强,难度较大,注重了高考常考考点的考查,注意知识的迁移应用和信息的处理.
24.(14分)(2013•福建)二氧化氯(ClO )是一种高效、广谱、安全的杀菌、消毒剂.
2
(1)氯化钠电解法是一种可靠的工业生产ClO 方法.
2
①用于电解的食盐水需先除去其中的Ca2+、Mg2+、SO 2﹣等杂质.其次除杂操作时,往粗
4
盐水中先加入过量的 BaC l (填化学式),至沉淀不再产生后,再加入过量的Na CO
2 2 3
和NaOH,充分反应后将沉淀一并滤去.经检测发现滤液中仍含有一定量的SO 2﹣,其原
4
因是 BaSO 和 BaCO 的 K 相差不大,当溶液中存在大量 CO 2﹣ 时, BaSO ( s )会部分
4 3 sp 3 4
转化为 BaCO ( s ) 【已知:Ksp(BaSO )=1.1×10﹣10、Ksp(BaCO )=5.1×10﹣9】
3 4 3
②该法工艺原理如图.其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO )与盐
3
酸反应生成ClO .工艺中可以利用的单质有 H 、 C l (填化学式),发生器中生成
2 2 2
ClO 的化学方程式为 2NaClO +4HCl=2ClO ↑+Cl ↑+2NaCl+2H O .
2 3 2 2 2
(2)纤维素还原法制ClO 是一种新方法,其原理是:纤维素水解得到的最终产物D与
2
NaClO 反应生成ClO .完成反应的化学方程式: 1 C H O +24NaClO +12H SO =
3 2 6 12 6 3 2 4
24 ClO ↑+ 6 CO ↑+18H O+ 1 2 N a SO
2 2 2 2 4
(3)ClO 和Cl 均能将电镀废水中的CN﹣氧化为无毒的物质,自身被还原为Cl﹣.处理含
2 2
CN﹣相同时的电镀废水,所需Cl 的物质的量是ClO 的 2. 5 倍.
2 2
考 难溶电解质的溶解平衡及沉淀转化的本质;氧化还原反应方程式的配平;粗盐提
点: 纯.
菁优网版权所有
专 氧化还原反应专题;电离平衡与溶液的pH专题.
题:
分 (1)①在除杂的过程中每步加入的试剂必须是过量的,使离子除尽;过量的离子在
析: 下一步中必须出去,故先加入BaCl ,除去硫酸根,过量的钡离子,加入Na CO 除
2 2 3
去.根据提供的Ksp数据,在后面加入碳酸钠时,发生BaSO (s)+CO 2﹣ (aq)
4 3
=BaCO (s)+SO 2﹣ (aq);
3 4
②电解饱和食盐水生成H 、Cl 和NaOH;故可以利用的单质为H 、Cl ,合成
2 2 2 2
HCl,根据流程图可知加入物质为NaClO 和HCl,生成ClO ;可以写出方程式,并
3 2
用化合价升降法配平得到;
(2)纤维素为多糖,水解最终产物为葡萄糖(C H O ),具有还原性,可将
6 12 6
NaClO 还原得到ClO .Cl从+5到+4价,降低1价,葡萄糖(C H O )C均价为
3 2 6 12 6
0,到+4价,升高4价,然后配平得到;
(3)每摩尔Cl 得到2mol电子,而每摩尔ClO 得到5mol电子,故为2.5倍.
2 2
解 解:(1)①加入过量的Na CO 和NaOH,可分别除去Ca2+、Mg2+,在除杂的过程
2 3
答: 中每步加入的试剂必须是过量的,使离子除尽;过量的离子在下一步中必须出去,
故先加入BaCl ,除去硫酸根,过量的钡离子,加入Na CO 除去.BaSO 和BaCO
2 2 3 4 3
的K 相差不大,当溶液中存在大量CO 2﹣时,发生BaSO (s)+CO 2﹣ (aq)
sp 3 4 3
=BaCO (s)+SO 2﹣ (aq),BaSO (s)会部分转化为BaCO (s),
3 4 4 3
故答案为:BaCl ;BaSO 和BaCO 的K 相差不大,当溶液中存在大量CO 2﹣时,
2 4 3 sp 3
BaSO (s)会部分转化为BaCO (s);
4 3
②电解饱和食盐水生成H 、Cl 和NaOH;故可以利用的单质为H 、Cl ,合成
2 2 2 2
HCl,根据流程图可知加入物质为NaClO 和HCl,生成ClO ;发生氧化还原反应,
3 2
NaClO 被还原生成ClO ,HCl被氧化生成Cl ,同时生成水,反应的化学方程式为
3 2 2
2NaClO +4HCl=2ClO ↑+Cl ↑+2NaCl+2H O,
3 2 2 2故答案为:H 、Cl ;2NaClO +4HCl=2ClO ↑+Cl ↑+2NaCl+2H O;
2 2 3 2 2 2
(2)纤维素为多糖,水解最终产物为葡萄糖(C H O ),具有还原性,可将
6 12 6
NaClO 还原得到ClO .Cl从+5到+4价,降低1价,葡萄糖(C H O )C均价为
3 2 6 12 6
0,到+4价,升高4价,则配平后的化学方程式为1 C H O +24
6 12 6
NaClO +12H SO =24 ClO ↑+6 CO ↑+18H O+12 Na SO ,
3 2 4 2 2 2 2 4
故答案为:1;C H O ;24;6;12;Na SO ;
6 12 6 2 4
(3)每摩尔Cl 得到2mol电子,而每摩尔ClO 得到5mol电子,则所需Cl 的物质
2 2 2
的量是ClO 的2.5倍,故答案为:2.5.
2
点 本题考查化学工艺流程,涉及氧化还原反应相关概念、配平及计算,化学实验基本
评: 方法(除杂)等相关知识,题目难度中等,注意把握物质的分离、提纯操作方法.
25.(15分)(2013•福建)固体硝酸盐加热易分解且产物较复杂.某学习小组以Mg
(NO ) 为研究对象,拟通过实验探究其热分解的产物,提出如下4种猜想:
3 2
甲:Mg(NO ) 、NO 、O 乙:MgO、NO 、O 丙:Mg N 、O 丁:
3 2 2 2 2 2 3 2 2
MgO、NO 、N
2 2
(1)实验前,小组成员经讨论认定猜想丁不成立,理由是 不符合氧化还原反应原理(或
其它合理答案) .
查阅资料得知:2NO +2NaOH═NaNO +NaNO +H O
2 3 2 2
针对甲、乙、丙猜想,设计如下图所示的实验装置(图中加热、夹持仪器等均省略):
(2)实验过程
①仪器连接后,放入固体试剂之前,关闭k,微热硬质玻璃管(A),观察到E中有气泡连
续放出,表明 装置气密性良好
②称取Mg(NO ) 固体3.7g置于A中,加热前通入N 以驱尽装置内的空气,其目的是
3 2 2
避免对产物 O 检验产生干扰(或其它合理答案) ;关闭K,用酒精灯加热时,正确操作
2
是先 移动酒精灯预热硬质玻璃管 然后固定在管中固体部位下加热.
③观察到A中有红棕色气体出现,C、D中未见明显变化.
④待样品完全分解,A装置冷却至室温、称量,测得剩余固体的质量为1.0g.
⑤取少量剩余固体于试管中,加入适量水,未见明显现象.
(3)实验结果分析讨论
①根据实验现象和剩余固体的质量经分析可初步确认猜想 乙 是正确的.
②根据D中无明显现象,一位同学认为不能确认分解产物中有O ,因为若有O ,D中将发
2 2
生氧化还原反应: 2N a SO +O =2Na SO (填写化学方程式),溶液颜色会退去;小组
2 3 2 2 4
讨论认定分解产物中有O 存在,未检侧到的原因是 O 在通过装置 B 时已参与反应(或
2 2
其它合理答案) .
③小组讨论后达成的共识是上述实验设计仍不完善,需改进装置进一步研究.
考 探究物质的组成或测量物质的含量.
菁优网版权所有
点:专 实验探究和数据处理题.
题:
分 (1)根据氧化还原反应化合价升降相等判断;
析: (2)①反应前检验装置的气密性;
②甲、乙、丙中都有氧气,避免空气中氧气干扰;根据加热试管的操作要求完成;
(3)①根据硝酸镁的反应现象进行判断;
②D中亚硫酸钠具有还原性,能够和氧气反应生成硫酸钠,溶液褪色;二氧化氮和
氢氧化钠溶液反应生成一氧化氮,一氧化氮会消耗氧气.
解 解:(1)由于产物中化合价只有升高情况,没有降低产物,
答: 故答案为:不符合氧化还原反应原理(或其它合理答案);
(2)①实验前需要检验装置的气密性,方法是关闭k,微热硬质玻璃管(A),观
察到E中有气泡连续放出,证明装置气密性良好,
故答案为:装置气密性良好;
②由于甲乙丙猜想中产物都有氧气,没有氮气,用氮气排出装置中空气避免对产物
氧气检验的干扰,
集中加热前先预热硬质试管,然后固定在管中固体部位下加热,
故答案为:避免对产物O 检验产生干扰(或其它合理答案);移动酒精灯预热硬质
2
玻璃管;
(3)①硝酸镁分解,红棕色气体是二氧化氮,镁元素不会还是硝酸镁形式,所以乙
正确;
故答案为:乙;
②亚硫酸钠和氧气的反应,反应方程式是:2Na SO +O =2Na SO ,
2 3 2 2 4
在B装置中,二氧化氮和氢氧化钠溶液反应生成一氧化氮,生成的一氧化氮消耗了
氧气,
故答案为:2Na SO +O =2Na SO ;O 在通过装置B时已参与反应(或其它合理答
2 3 2 2 4 2
案).
点 本题探究硝酸镁分解产物,提出假想,通过实验验证,涉及了化学方程式的书写、
评: 加热操作的考查,本题难度中等.
31.(13分)(2013•福建)(1)依据第2周期元素第一电离能的变化规律,参照右图
B、F元素的位置,用小黑点标出C、N、O三种元素的相对位置.
(2)NF 可由NH 和F 在Cu催化剂存在下反应直接得到:
3 3 2
2NH +3F NF +3NH F
3 2 3 4
①上述化学方程式中的5种物质所属的晶体类型有 ab d (填序号).
a.离子晶体b.分子晶体c.原子晶体d.金属晶体
②基态铜原子的核外电子排布式为 1 s 2 2 s 2 2 p 6 3 s 2 3 p 6 3 d 1 0 4 s 1 .
(3)BF 与一定量水形成(H O) •BF 晶体Q,Q在一定条件下可转化为R:
3 2 2 3
①晶体Q中各种微粒间的作用力不涉及 a d (填序号).
a.离子键 b.共价键 c.配位键 d.金属键 e.氢键
f.范德华力
②R中阳离子的空间构型为 三角锥型 ,阴离子的中心原子轨道采用 s p 3 杂化.
(4)已知苯酚( )具有弱酸性,其Ka=1.1×10﹣10;水杨酸第一级电离形成的离子
能形成分子内氢键.据此判断,相同温度下电离平衡常数K (水杨酸)
a2< K (苯酚)(填“>”或“<”),其原因是 中形成分子内氢键,使
a
其更难电离出 H + .
考 位置结构性质的相互关系应用;判断简单分子或离子的构型;原子轨道杂化方式及
点: 杂化类型判断;不同晶体的结构微粒及微粒间作用力的区别.
菁优网版权所有
专 元素周期律与元素周期表专题;化学键与晶体结构.
题:
分 (1)同周期自左而右元素的第一电离能呈增大趋势,但氮元素的2p能级容纳3个
析: 电子,处于半满稳定状态,能力降低,氮元素的第一电离能高于同周期相邻元素;
(2)①Cu是金属,属于金属晶体,NH F是盐,属于离子晶体,NH 、F 、NF 都
4 3 2 3
属于分子晶体;
②Cu原子核外有29个电子,根据核外电子排布规律书写;
(3)①由Q的结构可知,Q分子中处于在氢键、共价键、配位键(O与B之间)、
分子间作用力;
②R中阳离子为H
3
+O,中心原子氧原子价层电子对数=3+ =4,孤电子对
= =1,据此判断;
(4) 中形成分子内氢键,使其更难电离出H+.
解 解:(1)同周期自左而右元素的第一电离能呈增大趋势,但氮元素的2p能级容纳3
答: 个电子,处于半满稳定状态,能力降低,氮元素的第一电离能高于同周期相邻元
素,故C、N、O三种元素的相对位置为: ,故答案为:
;(2)①Cu是金属,属于金属晶体,NH F是盐,属于离子晶体,NH 、F 、NF 都
4 3 2 3
属于分子晶体,
故答案为:abd;
②Cu原子核外有29个电子,基态铜原子的核外电子排布式为:
1s22s22p63s23p63d104s1,
故答案为:1s22s22p63s23p63d104s1;
(3)①由Q的结构可知,Q分子中处于在氢键、共价键、配位键(O与B之间)、
分子间作用力,
故答案为:ad;
②R中阳离子为H
3
+O,中心原子氧原子价层电子对数=3+ =4,孤电子对
= =1,为三角锥型,氧原子采取sp3杂化,
故答案为:三角锥型;sp3;
(4) 中形成分子内氢键,使其更难电离出H+,故相同温度下电离平
衡常数K (水杨酸)<K (苯酚),
a2 a
故答案为:<; 中形成分子内氢键,使其更难电离出H+.
点 本题考查电离能、晶体类型、化学键及氢键对物质性质的影响、分子结构与杂化理
评: 论等,难度中等,需要学生全面掌握基础知识,并能运用分析解决问题.
32.(13分)(2013•福建)已知:
为合成某种液晶材料的中间体M,有人提出如下不同的合成途径
(1)常温下,下列物质能与A发生反应的有 b 、 d (填序号)
a.苯 b.Br /CCl c.乙酸乙酯 d.KMnO /H+溶液
2 4 4
(2)M中官能团的名称是 羟基 ,由C→B反应类型为 加成反应(或还原反应) .
(3)由A催化加氢生成M的过程中,可能有中间生成物 和
(写结构简式)生成
(4)检验B中是否含有C可选用的试剂是 银氨溶液(或新制氢氧化铜悬浊液) (任
写一种名称).
(5)物质B也可由C H Cl与NaOH水溶液共热生成,C H Cl的结构简式为
10 13 10 13
.
(6)C的一种同分异构体E具有如下特点:
a.分子中含﹣OCH CH b.苯环上只有两种化学环境不同的氢原子
2 3写出E在一定条件下发生加聚反应的化学方程式
.
考 有机物的合成.
菁优网版权所有
点:
专 有机物的化学性质及推断.
题:
分 由合成流程可知,A→M发生﹣CHO和C=C的加成反应,B→M为苯环的加成反
析: 应,结合信息可知,D→C发生取代反应,C为CH CH CH C H CHO,名称为对丙
3 2 2 6 4
基苯甲醛,C→B为﹣CHO的加成反应,然后结合有机物的结构与性质来解答.
解 解:由合成流程可知,A→M发生﹣CHO和C=C的加成反应,B→M为苯环的加成
答: 反应,结合信息可知,D→C发生取代反应,C为CH CH CH C H CHO,名称为对
3 2 2 6 4
丙基苯甲醛,C→B为﹣CHO的加成反应,
(1)含C=C,能与溴水发生加成反应,C=C、﹣CHO均能被高锰酸钾氧化,故答
案为:b、d;
(2)由结构简式可知,M中含﹣OH,名称为羟基,C→B为﹣CHO的加成反应
(或还原反应),
故答案为:羟基;加成反应(或还原反应);
(3)由A催化加氢生成M的过程中,C=C、﹣CHO均能与氢气发生加成反应,则
生成中间体为 或 ,
故答案为: ;
(4)B中是否含有C,利用醛基的性质可知,选银氨溶液(或新制氢氧化铜悬浊
液)产生银镜(或砖红色沉淀)即可证明,故答案为:银氨溶液(或新制氢氧化铜
悬浊液);
(5)B也可由C H Cl与NaOH水溶液共热生成,碳链骨架不变,则C H Cl的结
10 13 10 13
构简式为 ,故答案为: ;
(6)C为CH CH CH C H CHO,其同分异构体E具有如下特点:
3 2 2 6 4
a.分子中含﹣OCH CH 、b.苯环上只有两种化学环境不同的氢原子,则另一取代
2 3
基为乙烯基,二者为对位的位置,苯环上只有两种H,
则E在一定条件下发生加聚反应的化学方程式为
,故答案为:
.
点 本题考查有机物的合成,题目难度中等,注意信息分析C物质,体会官能团与性质
评: 的关系,把握反应条件、反应类型及官能团变化即可解答,有机合成题是高考热点
题型.分
一级考点 二级考点 三级考点 比例
值
16.81
物质结构与性质 物质结构 8J:位置结构性质的相互关系应用 19
%
化学反应原理 化学反应与能量 BF:用盖斯定律进行有关反应热的计算 6 5.31%
化学反应速率和化学
CA:化学反应速率的影响因素 6 5.31%
平衡
电解质溶液 D5:弱电解质在水溶液中的电离平衡 6 5.31%
DH:难溶电解质的溶解平衡及沉淀转化 12.39
14
的本质 %
常见无机物及其 14.16
氧族与碳族及其应用 FB:硫化氢 16
应用 %
FH:硅和二氧化硅 6 5.31%
常见有机物及其 有机化合物的组成与
HA:有机物的鉴别 6 5.31%
应用 结构
11.50
HC:有机物的合成 13
%
物质的分离、提纯和
化学实验 P4:分液和萃取 6 5.31%
检验
13.27
定量实验与探究实验 RD:探究物质的组成或测量物质的含量 15
%