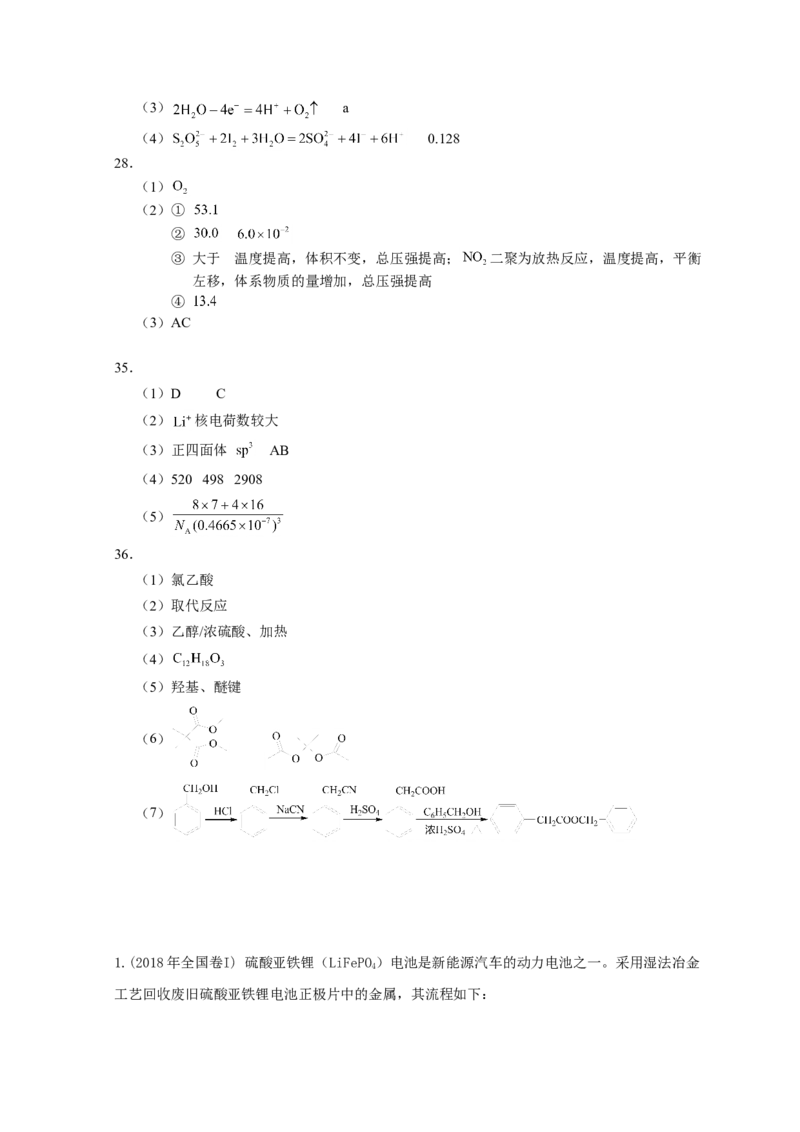文档内容
绝密★启用前
2018 年普通高等学校招生全国统一考试
理科综合能力测试
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需
改动,用橡皮擦干净后,再选涂其它答案标号。回答非选择题时,将答案写在答题卡上。写在
本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 S 32 Cl 35.5
Ar 40 Fe 56 I 127
一、选择题:本题共13小题,每小题6分,共78分。在每小题给出的四个选项中,只有一项是
符合题目要求的。
7.磷酸亚铁锂(LiFePO )电池是新能源汽车的动力电池之一。采用湿法冶金工艺回收废旧磷
4
酸亚铁锂电池正极片中的金属,其流程如下:
下列叙述错误的是
A.合理处理废旧电池有利于保护环境和资源再利用
B.从“正极片”中可回收的金属元素有Al、Fe、Li
C.“沉淀”反应的金属离子为
D.上述流程中可用硫酸钠代替碳酸钠
8.下列说法错误的是
A.蔗糖、果糖和麦芽糖均为双糖
B.酶是一类具有高选择催化性能的蛋白质
C.植物油含不饱和脂肪酸酯,能使 褪色
D.淀粉和纤维素水解的最终产物均为葡萄糖
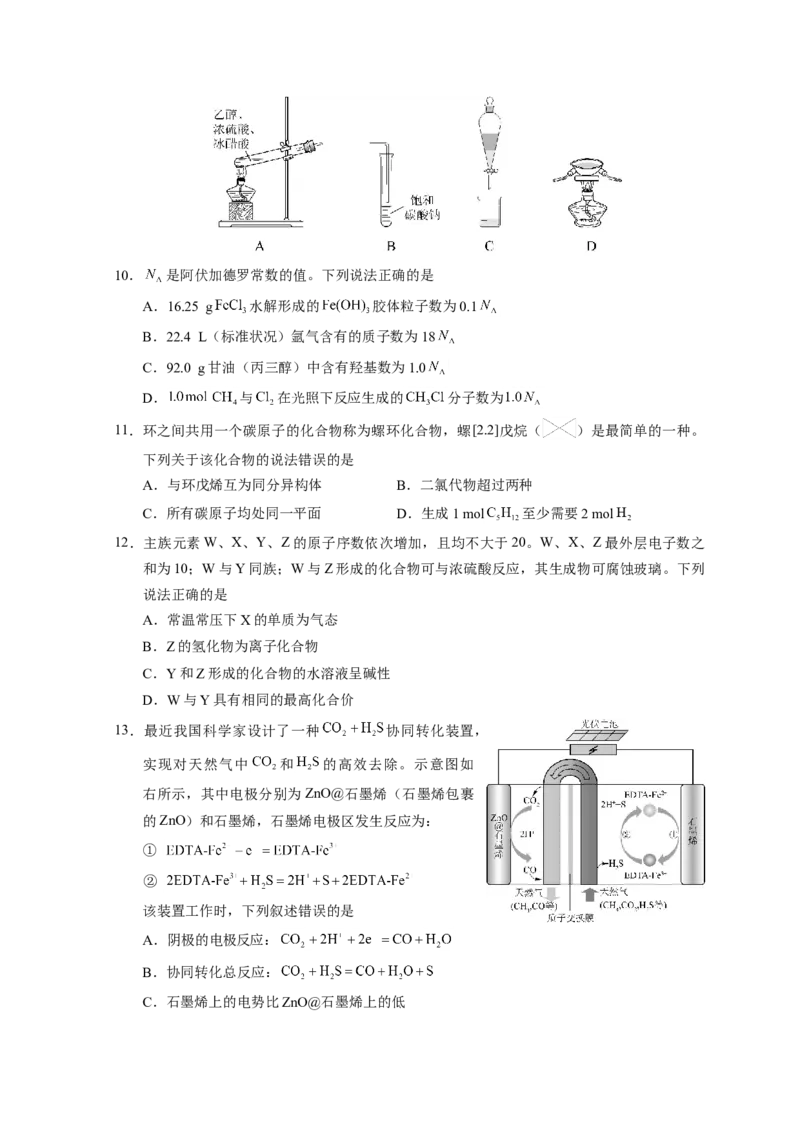
9.在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是10. 是阿伏加德罗常数的值。下列说法正确的是
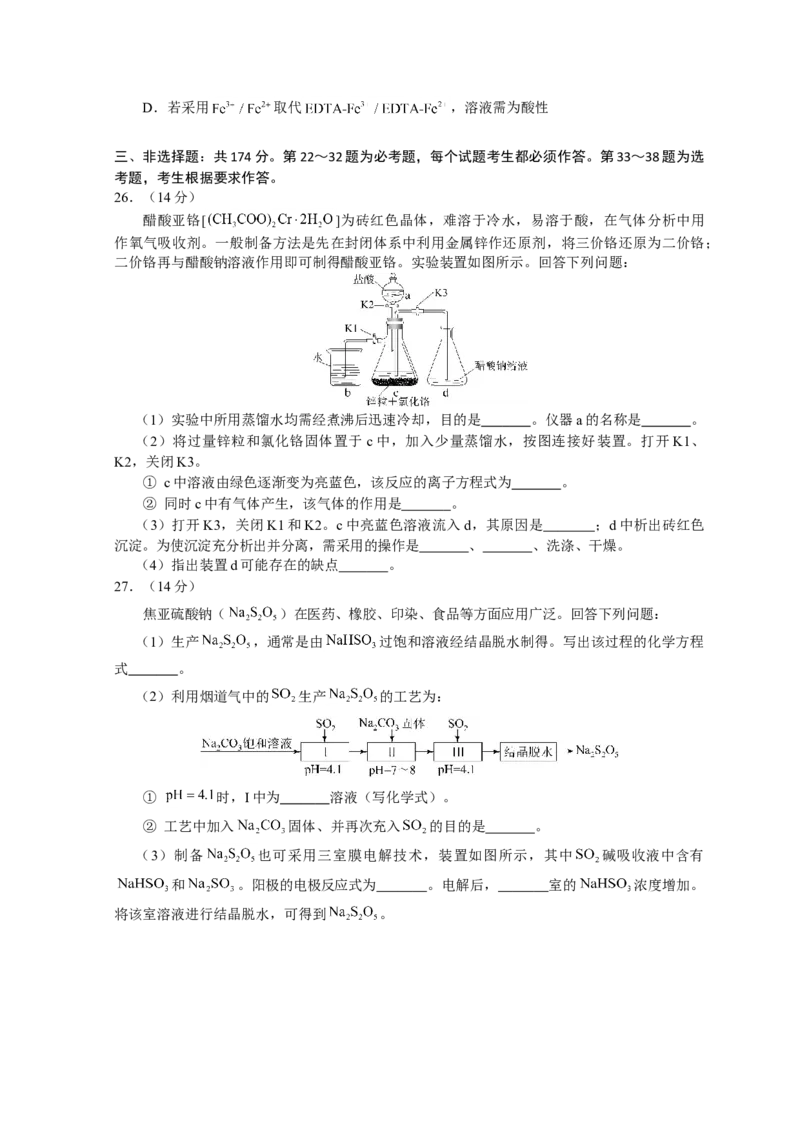
A.16.25 g 水解形成的 胶体粒子数为0.1
B.22.4 L(标准状况)氩气含有的质子数为18
C.92.0 g甘油(丙三醇)中含有羟基数为1.0
D. 与 在光照下反应生成的 分子数为
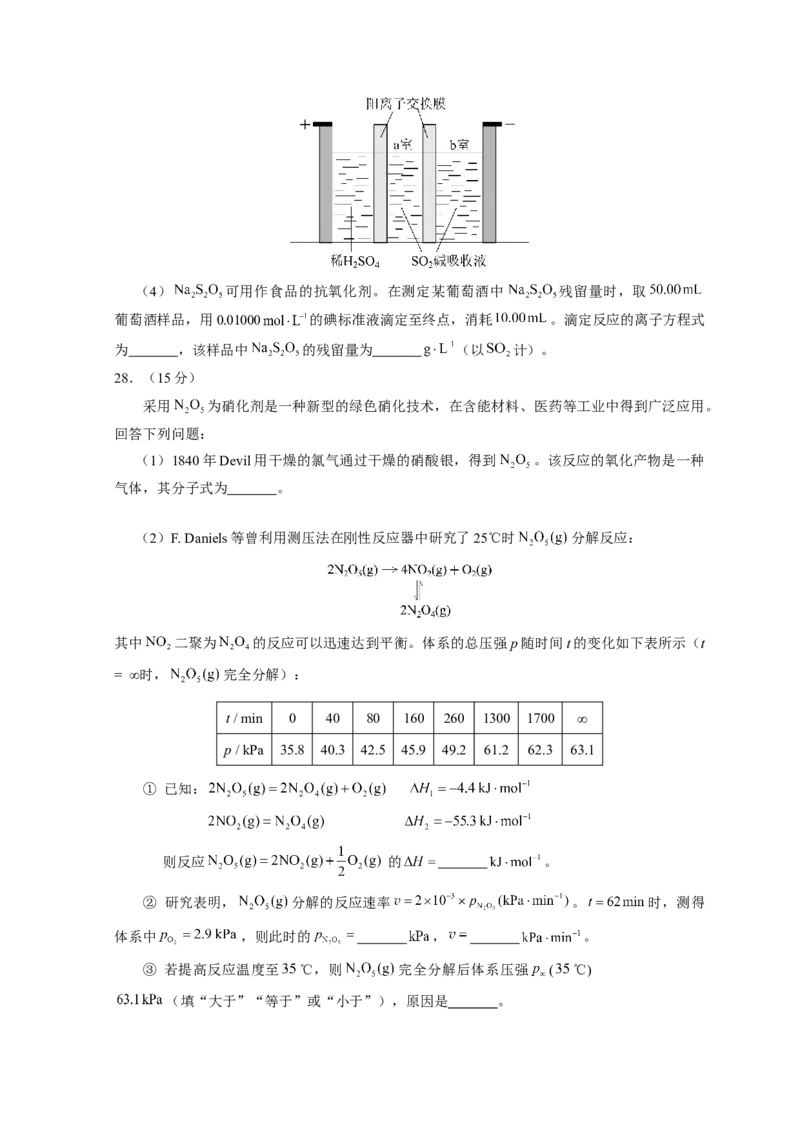
11.环之间共用一个碳原子的化合物称为螺环化合物,螺[2.2]戊烷( )是最简单的一种。
下列关于该化合物的说法错误的是
A.与环戊烯互为同分异构体 B.二氯代物超过两种
C.所有碳原子均处同一平面 D.生成1 mol 至少需要2 mol
12.主族元素W、X、Y、Z的原子序数依次增加,且均不大于20。W、X、Z最外层电子数之
和为10;W与Y同族;W与Z形成的化合物可与浓硫酸反应,其生成物可腐蚀玻璃。下列
说法正确的是
A.常温常压下X的单质为气态
B.Z的氢化物为离子化合物
C.Y和Z形成的化合物的水溶液呈碱性
D.W与Y具有相同的最高化合价
13.最近我国科学家设计了一种 协同转化装置,
实现对天然气中 和 的高效去除。示意图如
右所示,其中电极分别为ZnO@石墨烯(石墨烯包裹
的ZnO)和石墨烯,石墨烯电极区发生反应为:
①
②
该装置工作时,下列叙述错误的是
A.阴极的电极反应:
B.协同转化总反应:
C.石墨烯上的电势比ZnO@石墨烯上的低D.若采用 取代 ,溶液需为酸性
三、非选择题:共174分。第22~32题为必考题,每个试题考生都必须作答。第33~38题为选
考题,考生根据要求作答。
26.(14分)
醋酸亚铬[ ]为砖红色晶体,难溶于冷水,易溶于酸,在气体分析中用
作氧气吸收剂。一般制备方法是先在封闭体系中利用金属锌作还原剂,将三价铬还原为二价铬;
二价铬再与醋酸钠溶液作用即可制得醋酸亚铬。实验装置如图所示。回答下列问题:
(1)实验中所用蒸馏水均需经煮沸后迅速冷却,目的是 。仪器a的名称是 。
(2)将过量锌粒和氯化铬固体置于 c中,加入少量蒸馏水,按图连接好装置。打开K1、
K2,关闭K3。
① c中溶液由绿色逐渐变为亮蓝色,该反应的离子方程式为 。
② 同时c中有气体产生,该气体的作用是 。
(3)打开K3,关闭K1和K2。c中亮蓝色溶液流入d,其原因是 ;d中析出砖红色
沉淀。为使沉淀充分析出并分离,需采用的操作是 、 、洗涤、干燥。
(4)指出装置d可能存在的缺点 。
27.(14分)
焦亚硫酸钠( )在医药、橡胶、印染、食品等方面应用广泛。回答下列问题:
(1)生产 ,通常是由 过饱和溶液经结晶脱水制得。写出该过程的化学方程
式 。
(2)利用烟道气中的 生产 的工艺为:
① 时,I中为 溶液(写化学式)。
② 工艺中加入 固体、并再次充入 的目的是 。
(3)制备 也可采用三室膜电解技术,装置如图所示,其中 碱吸收液中含有
和 。阳极的电极反应式为 。电解后, 室的 浓度增加。
将该室溶液进行结晶脱水,可得到 。(4) 可用作食品的抗氧化剂。在测定某葡萄酒中 残留量时,取
葡萄酒样品,用0.01000 的碘标准液滴定至终点,消耗 。滴定反应的离子方程式
为 ,该样品中 的残留量为 (以 计)。
28.(15分)
采用 为硝化剂是一种新型的绿色硝化技术,在含能材料、医药等工业中得到广泛应用。
回答下列问题:
(1)1840年Devil用干燥的氯气通过干燥的硝酸银,得到 。该反应的氧化产物是一种
气体,其分子式为 。
(2)F. Daniels等曾利用测压法在刚性反应器中研究了25℃时 分解反应:
其中 二聚为 的反应可以迅速达到平衡。体系的总压强p随时间t的变化如下表所示(t
= 时, 完全分解):
t / min 0 40 80 160 260 1300 1700
p / kPa 35.8 40.3 42.5 45.9 49.2 61.2 62.3 63.1
① 已知:
则反应 的 。
② 研究表明, 分解的反应速率 。 时,测得
体系中 ,则此时的 , 。
③ 若提高反应温度至 ℃,则 完全分解后体系压强 ( ℃)
(填“大于”“等于”或“小于”),原因是 。④ 25℃时 反应的平衡常数 ( 为以分压表示的平
衡常数,计算结果保留1位小数)。
(3)对于反应 ,R. A. Ogg提出如下反应历程:
其中可近似认为第二步反应不影响第一步的平衡。下列表述正确的是 (填标号)。
A. (第一步的逆反应)> (第二步反应) B.反应的中间产物只有
C.第二步中 与 的碰撞仅部分有效 D.第三步反应活化能较高
35.[化学——选修3:物质结构与性质](15分)
Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密度大等优良性能,
得到广泛应用。回答下列问题:
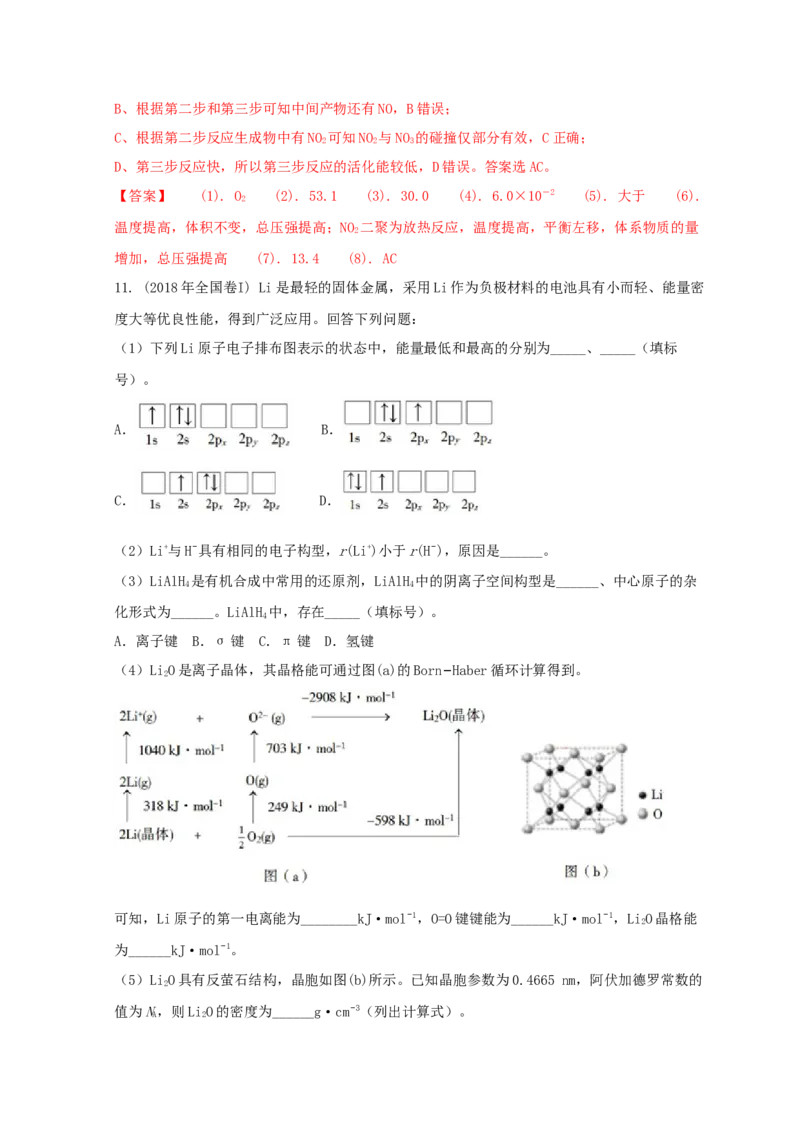
(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为 、
(填标号)。
A. B.
C. D.
(2) 与 具有相同的电子构型, 小于 ,原因是 。
(3) 是有机合成中常用的还原剂, 中的阴离子空间构型是 、中心原
子的杂化形式为 。 中,存在 (填标号)。
A.离子键 B.键 C.键 D.氢键
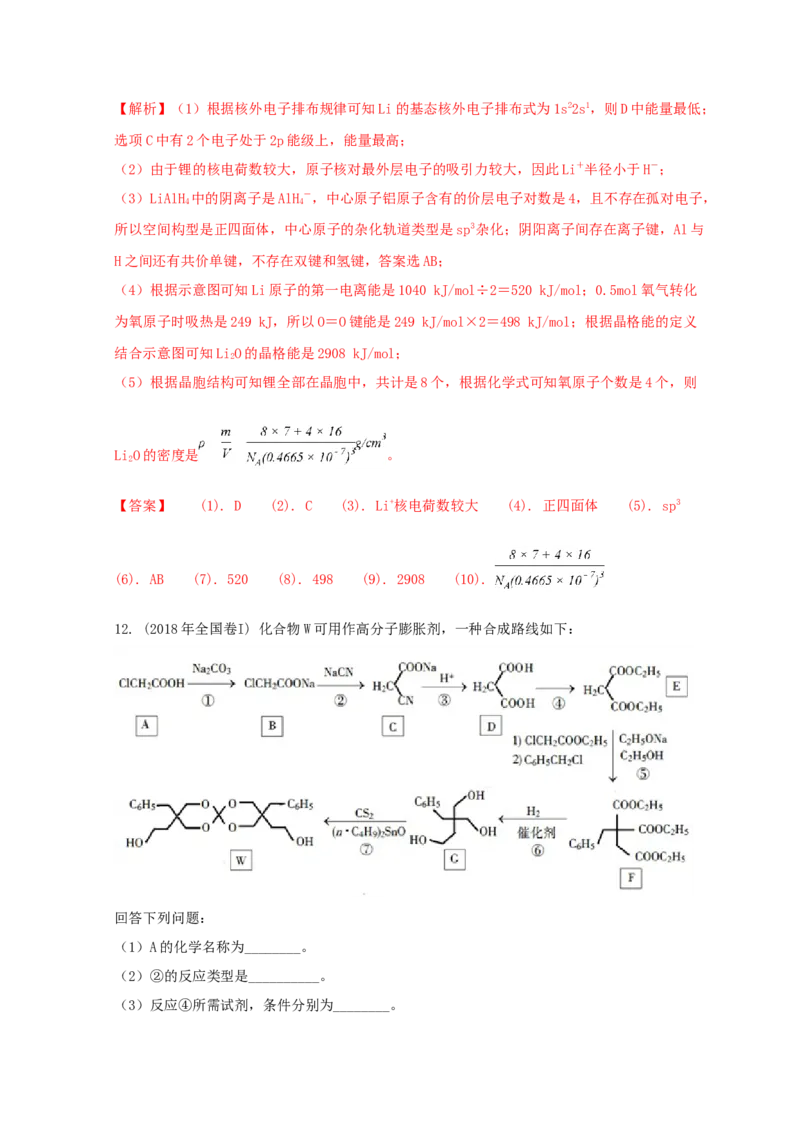
(4) 是离子晶体,其晶格能可通过图(a)的Born-Haber循环计算得到。
图(a) 图(b)
可知,Li原子的第一电离能为 ,O=O键键能为 , 晶格
能为 。
(5) 具有反萤石结构,晶胞如图(b)所示。已知晶胞参数为 ,阿伏加德罗
常数的值为N ,则 的密度为 (列出计算式)。
A36.[化学——选修5:有机化学基础](15分)
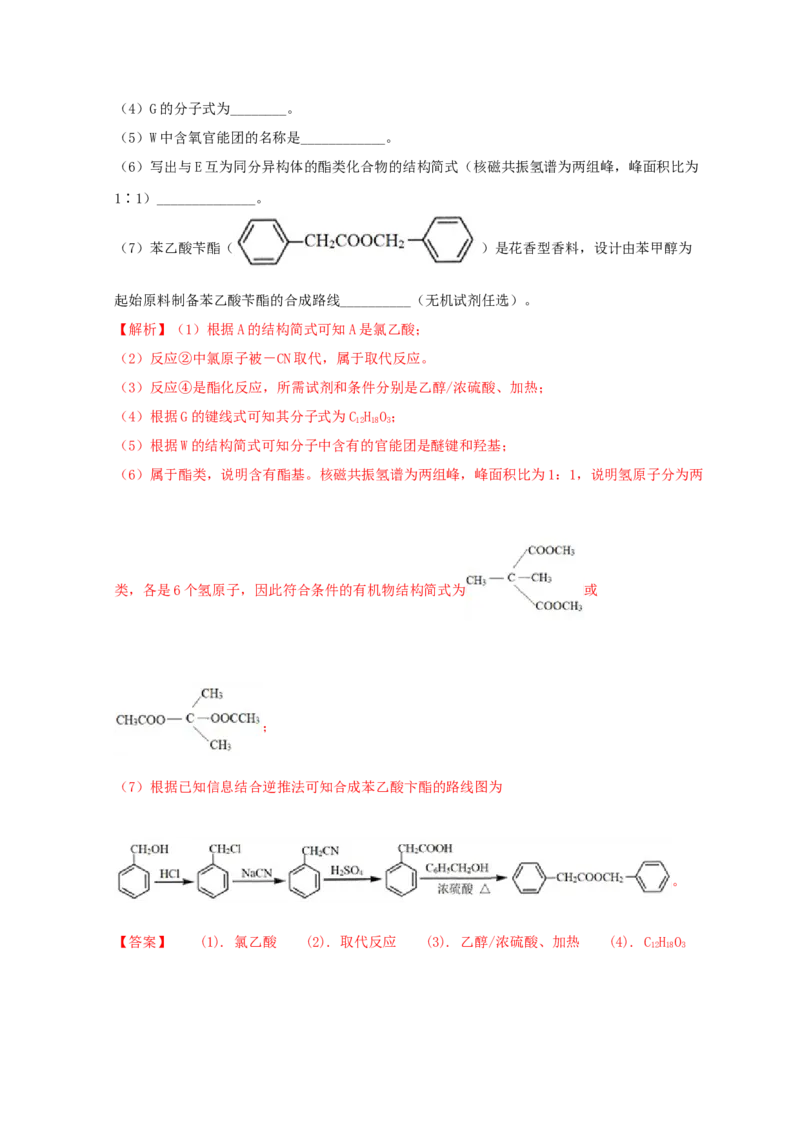
化合物W可用作高分子膨胀剂,一种合成路线如下:
回答下列
问题:
(1)A的化学名称为 。
(2)②的反应类型是 。
(3)反应④所需试剂、条件分别为 。
(4)G的分子式为 。
(5)W中含氧官能团的名称是 。
(6)写出与E互为同分异构体的酯类化合物的结构简式(核磁共振氢谱为两组峰,峰面积
比为 ) 。
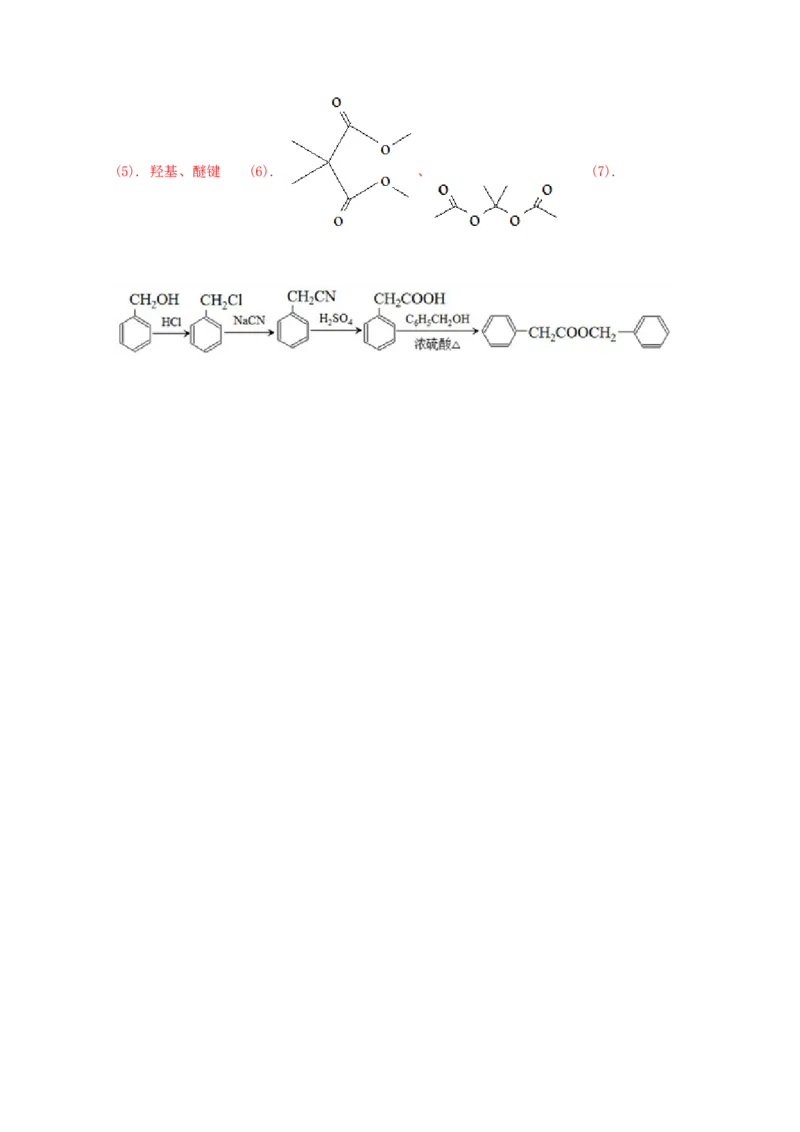
(7)苯乙酸苄酯( )是花香型香料,设计由苯甲醇为起始原
料制备苯乙酸苄酯的合成路线 (无机试剂任选)。
2018年普通高等学校招生全国统一考试
理科综合能力测试试题参考答案
7.D 8.A 9.D 10.B 11.C 12.B 13.C
26.
(1)去除水中溶解氧 分液(或滴液)漏斗
(2)①
② 排除c中空气
(3)c中产生 使压强大于大气压 (冰浴)冷却 过滤
(4)敞开体系,可能使醋酸亚铬与空气接触
27.
(1)
(2)①
② 得到 过饱和溶液(3) a
(4) 0.128
28.
(1)
(2)①
②
③ 大于 温度提高,体积不变,总压强提高; 二聚为放热反应,温度提高,平衡
左移,体系物质的量增加,总压强提高
④
(3)AC
35.
(1)D C
(2) 核电荷数较大
(3)正四面体 AB
(4)520 498 2908
(5)
36.
(1)氯乙酸
(2)取代反应
(3)乙醇/浓硫酸、加热
(4)
(5)羟基、醚键
(6)
(7)
1.(2018年全国卷I) 硫酸亚铁锂(LiFePO)电池是新能源汽车的动力电池之一。采用湿法冶金
4
工艺回收废旧硫酸亚铁锂电池正极片中的金属,其流程如下:下列叙述错误的是( )
A. 合理处理废旧电池有利于保护环境和资源再利用
B. 从“正极片”中可回收的金属元素有Al、Fe、Li
C. “沉淀”反应的金属离子为Fe3+
D. 上述流程中可用硫酸钠代替碳酸钠
【解析】A、废旧电池中含有重金属,随意排放容易污染环境,因此合理处理废旧电池有利于保
护环境和资源再利用,A正确;B、根据流程的转化可知从正极片中可回收的金属元素有Al、
Fe、Li,B正确;C、得到含Li、P、Fe的滤液,加入碱液生成氢氧化铁沉淀,因此“沉淀”反
应的金属离子是Fe3+,C正确;D、硫酸锂能溶于水,因此上述流程中不能用硫酸钠代替碳酸钠,
D错误。
【答案】D
2. (2018年全国卷I)下列说法错误的是( )
A. 蔗糖、果糖和麦芽糖均为双糖
B. 酶是一类具有高选择催化性能的蛋白质
C. 植物油含不饱和脂肪酸酯,能使Br₂/CCl 褪色
4
D. 淀粉和纤维素水解的最终产物均为葡萄糖
【解析】A、果糖不能再发生水解,属于单糖,A错误;B、酶是由活细胞产生的具有催化活性和
高度选择性的蛋白质,B正确;C、植物油属于油脂,其中含有碳碳不饱和键,因此能使Br/
2
CCl 溶液褪色,C正确;D、淀粉和纤维素均是多糖,其水解的最终产物均为葡萄糖,D正确。答
4
案选A。
【答案】A
3. (2018年全国卷I) 在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是( )A. A B. B C. C D. D
【解析】A、反应物均是液体,且需要加热,因此试管口要高于试管底,A正确;
【答案】D
4. (2018年全国卷I)N是阿伏加德罗常数的值,下列说法正确的是( )
A
A. 16.25 g FeCl 水解形成的Fe(OH) 胶体粒子数为0.1 N
3 3 A
B. 22.4 L(标准状况)氨气含有的质子数为18N
A
C. 92.0 g甘油(丙三醇)中含有羟基数为1.0N
A
D. 1.0 mol CH 与Cl 在光照下反应生成的CHCl分子数为1.0N
4 2 3 A
【解析】A、16.25g氯化铁的物质的量是16.25g÷162.5g/mol=0.1mol,由于氢氧化铁胶体是
分子的集合体,因此水解生成的Fe(OH) 胶体粒子数小于0.1 N,A错误;B、标准状况下22.4L
3 A
氩气的物质的量是1mol,氩气是一个Ar原子组成的单质,其中含有的质子数是18 N,B正确;
A
C、1分子丙三醇含有3个羟基,92.0g丙三醇的物质的量是1mol,其中含有羟基数是3 N,C错
A
误;D、甲烷与氯气在光照条件下发生取代反应生成的卤代烃不止一种,因此生成的CHCl分子
3
数小于1.0 N,D错误。
A
【答案】B
5. (2018年全国卷I)环之间共用一个碳原子的化合物称为螺环化合物,螺2,2]戊烷(
)是最简单的一种。下列关于该化合物的说法错误的是( )A. 与环戊烯互为同分异构体
B. 二氯代物超过两种
C. 所有碳原子均处同一平面
D. 生成1 molCH 至少需要2 molH
5 12 2
【解析】A、螺2,2]戊烷的分子式为CH,环戊烯的分子式也是CH,结构不同,互为同分异构
5 8 5 8
体,A正确;B、分子中的8个氢原子完全相同,二氯代物中可以取代同一个碳原子上的氢原子,
也可以是相邻碳原子上或者不相邻的碳原子上,因此其二氯代物超过两种,B正确;C、由于分
子中4个碳原子均是饱和碳原子,而与饱和碳原子相连的4个原子一定构成四面体,所以分子中
所有碳原子不可能均处在同一平面上,C错误;D、戊烷比螺2,2]戊烷多4个氢原子,所以生成
1 molCH 至少需要2 molH,D正确。
5 12 2
【答案】C
6. (2018年全国卷I) 主族元素W、X、Y、Z的原子序数依次增加,且均不大于20。W、X、Z最
外层电子数之和为10;W与Y同族;W与Z形成的化合物可与浓硫酸反应,其生成物可腐蚀玻璃。
下列说法正确的是( )
A. 常温常压下X的单质为气态
B. Z的氢化物为离子化合物
C. Y和Z形成的化合物的水溶液呈碱性
D. W与Y具有相同的最高化合价
【解析】根据以上分析可知W、X、Y、Z分别是F、Na、Cl、Ca。则A、金属钠常温常压下是固态,
A错误;B、CaH 中含有离子键,属于离子化合物,B正确;C、Y与Z形成的化合物是氯化钠,
2
其水溶液显中性,C错误;D、F是最活泼的非金属,没有正价,Cl元素的最高价是+7价,D错
误。答案选B。
【答案】B
7. (2018年全国卷I) 最近我国科学家设计了一种CO+HS协同转化装置,实现对天然气中CO 和
2 2 2
HS的高效去除。示意图如图所示,其中电极分别为ZnO@石墨烯(石墨烯包裹的ZnO)和石墨烯,
2
石墨烯电极区发生反应为:①EDTA-Fe2+-e-=EDTA-Fe3+
②2EDTA-Fe3++HS=2H++S+2EDTA-Fe2+
2
该装置工作时,下列叙述错误的是( )
A. 阴极的电极反应:CO+2H++2e-=CO+HO
2 2
B. 协同转化总反应:CO+HS=CO+HO+S
2 2 2
C. 石墨烯上的电势比ZnO@石墨烯上的低
D. 若采用Fe3+/Fe2+取代EDTA-Fe3+/EDTA-Fe2+,溶液需为酸性
B、根据石墨烯电极上发生的电极反应可知①+②即得到HS-2e-=2H++S,因此总反应式为
2
CO+HS=CO+HO+S,B正确;
2 2 2
C、石墨烯电极为阳极,与电源的正极相连,因此石墨烯上的电势比ZnO@石墨烯电极上的高,C
错误;
D、由于铁离子、亚铁离子均易水解,所以如果采用Fe3+/Fe2+取代EDTA-Fe3+/EDTA-Fe2+,溶液
需要酸性,D正确。
【答案】C
8. (2018年全国卷I)醋酸亚铬(CHCOO)Cr·HO]为砖红色晶体,难溶于冷水,易溶于酸,在气
3 2 2
体分析中用作氧气吸收剂。一般制备方法是先在封闭体系中利用金属锌作还原剂,将三价铬还
原为二价铬;二价铬再与醋酸钠溶液作用即可制得醋酸亚铬。实验装置如图所示,回答下列问题:
(1)实验中所用蒸馏水均需经煮沸后迅速冷却,目的是_________,仪器a的名称是_______。
(2)将过量锌粒和氯化铬固体置于c中,加入少量蒸馏水,按图连接好装置,打开K1、K2,关
闭K3。
①c中溶液由绿色逐渐变为亮蓝色,该反应的离子方程式为_________。
②同时c中有气体产生,该气体的作用是_____________。
(3)打开K3,关闭K1和K2。c中亮蓝色溶液流入d,其原因是________;d中析出砖红色沉淀,
为使沉淀充分析出并分离,需采用的操作是___________、_________、洗涤、干燥。
(4)指出装置d可能存在的缺点______________。
【解析】(1)由于醋酸亚铬易被氧化,所以需要尽可能避免与氧气接触,因此实验中所用蒸馏
水均需煮沸后迅速冷却,目的是去除水中溶解氧;根据仪器构造可知仪器a是分液(或滴液)
漏斗;%网
(2)①c中溶液由绿色逐渐变为亮蓝色,说明Cr3+被锌还原为Cr2+,反应的离子方程式为
Zn+2Cr3+=Zn2++2Cr2+;
②锌还能与盐酸反应生成氢气,由于装置中含有空气,能氧化Cr2+,所以氢气的作用是排除c
中空气;
(3)打开K,关闭K 和K,由于锌继续与盐酸反应生成氢气,导致c中压强增大,所以c中亮
3 1 2
蓝色溶液能流入d装置,与醋酸钠反应;根据题干信息可知醋酸亚铬难溶于水冷水,所以为使
沉淀充分析出并分离,需要采取的操作是(冰浴)冷却、过滤、洗涤、干燥。
(4)由于d装置是敞开体系,因此装置的缺点是可能使醋酸亚铬与空气接触被氧化而使产品不
纯。
【答案】 (1). 去除水中溶解氧 (2). 分液(或滴液)漏斗 (3). Zn+2Cr3+=Zn2+
+2Cr2+ (4). 排除c中空气 (5). c中产生H 使压强大于大气压 (6). (冰浴)冷却
2
(7). 过滤 (8). 敞开体系,可能使醋酸亚铬与空气接触9. (2018年全国卷I)焦亚硫酸钠(NaSO)在医药、橡胶、印染、食品等方面应用广泛。回答
2 2 5
下列问题:
(1)生产NaSO,通常是由NaHSO 过饱和溶液经结晶脱水制得。写出该过程的化学方程式
2 2 5 3
__________。
(2)利用烟道气中的SO 生产NaSO 的工艺为:
2 2 2 5
①pH=4.1时,Ⅰ中为__________溶液(写化学式)。
②工艺中加入NaCO 固体、并再次充入SO 的目的是__________。
2 3 2
(3)制备NaSO 也可采用三室膜电解技术,装置如图所示,其中SO 碱吸收液中含有NaHSO 和
2 2 5 2 3
NaSO。阳极的电极反应式为_____________。电解后,__________室的NaHSO 浓度增加。将该
2 3 3
室溶液进行结晶脱水,可得到NaSO。
2 2 5
(4)NaSO 可用作食品的抗氧化剂。在测定某葡萄酒中NaSO 残留量时,取50.00 mL葡萄酒
2 2 5 2 2 5
样品,用0.01000 mol·L−1的碘标准液滴定至终点,消耗10.00 mL。滴定反应的离子方程式为
_____________,该样品中NaSO 的残留量为____________g·L−1(以SO 计)。
2 2 5 2
【解析】(1)亚硫酸氢钠过饱和溶液脱水生成焦亚硫酸钠,根据原子守恒可知反应的方程式为
2NaHSO=NaSO+HO;
3 2 2 5 2
(2)①碳酸钠饱和溶液吸收SO 后的溶液显酸性,说明生成物是酸式盐,即Ⅰ中为NaHSO;
2 3
②要制备焦亚硫酸钠,需要制备亚硫酸氢钠过饱和溶液,因此工艺中加入碳酸钠固体、并再次
充入二氧化硫的目的是得到NaHSO 过饱和溶液;
3
(3)阳极发生失去电子的氧化反应,阳极区是稀硫酸,氢氧根放电,则电极反应式为2HO-4e
2
-=4H++O↑。阳极区氢离子增大,通过阳离子交换膜进入a室与亚硫酸钠结合生成亚硫酸钠。
2
阴极是氢离子放电,氢氧根浓度增大,与亚硫酸氢钠反应生成亚硫酸钠,所以电解后a室中亚硫酸氢钠的浓度增大。
(4)单质碘具有氧化性,能把焦亚硫酸钠氧化为硫酸钠,反应的方程式为SO2-+2I+3HO=
2 5 2 2
2SO2-+4I-+6H+;消耗碘的物质的量是0.0001mol,所以焦亚硫酸钠的残留量(以SO 计)是
4 2
。
【答案】 (1). 2NaHSO=NaSO+HO (2). NaHSO (3). 得到NaHSO 过饱和溶液
3 2 2 5 2 3 3
(4). 2HO-4e-=4H++O↑ (5). a (6). SO2-+2I+3HO=2SO2-+4I-+6H+ (7).
2 2 2 5 2 2 4
0.128
10. (2018年全国卷I) 采用NO 为硝化剂是一种新型的绿色硝化技术,在含能材料、医药等工
2 5
业中得到广泛应用。回答下列问题
(1)1840年 Devil用干燥的氯气通过干燥的硝酸银,得到NO。该反应的氧化产物是一种气体,
2 5
其分子式为___________。
(2)F. Daniels等曾利用测压法在刚性反应器中研究了25℃时NO(g)分解反应:
2 5
其中NO 二聚为NO 的反应可以迅速达到平衡。体系的总压强p随时间t的变化如下表所示
2 2 4
(t=∞时,NO(g)完全分解):
2 4
t/min 0 40 80 160 260 1300 1700 ∞
p/kPa 35.8 40.3 42.5. 45.9 49.2 61.2 62.3 63.1
①已知:2NO(g)=2NO(g)+O(g) ΔH=−4.4 kJ·mol−1
2 5 2 5 2 1
2NO(g)=NO(g) ΔH=−55.3 kJ·mol−1
2 2 4 2
则反应NO(g)=2NO(g)+ O(g)的ΔH=_______ kJ·mol−1。
2 5 2 2
②研究表明,NO(g)分解的反应速率 。t=62 min时,测得体系中
2 5
p =2.9 kPa,则此时的 =________kPa,v=_______kPa·min−1。
O2
③若提高反应温度至35℃,则NO(g)完全分解后体系压强p(35℃)____63.1 kPa(填“大于”
2 5 ∞
“等于”或“小于”),原因是________。
④25℃时NO(g) 2NO(g)反应的平衡常数K=_______kPa(K为以分压表示的平衡常数,计
2 4 2 p p算结果保留1位小数)。
(3)对于反应2NO(g)→4NO(g)+O(g),R.A.Ogg提出如下反应历程:
2 5 2 2
第一步 NO NO+NO 快速平衡
2 5 2 3
第二步 NO+NO→NO+NO+O 慢反应
2 3 2 2
第三步 NO+NO→2NO 快反应
3 2
其中可近似认为第二步反应不影响第一步的平衡。下列表述正确的是_______(填标号)。
A.v(第一步的逆反应)>v(第二步反应)
B.反应的中间产物只有NO
3
C.第二步中NO 与NO 的碰撞仅部分有效
2 3
D.第三步反应活化能较高
【解析】(1)氯气在反应中得到电子作氧化剂,硝酸银中只有氧元素化合价会升高,所以氧化
产物是氧气,分子式为O;
2
(2)①已知:
ⅰ、2NO(g)=2NO(g)+O(g) △H=-4.4kJ/mol
2 5 2 4 2 1
ⅱ、2NO(g)=NO(g) △H=-55.3kJ/mol
2 2 4 2
根据盖斯定律可知ⅰ÷2-ⅱ即得到NO(g)=2NO(g)+1/2O(g) △H=+53.1kJ/mol;
2 5 2 2 1
②根据方程式可知氧气与消耗五氧化二氮的物质的量之比是1:2,又因为压强之比是物质的量之
比,所以消耗五氧化二氮减少的压强是2.9kPa×2=5.8kPa,则此时五氧化二氮的压强是
35.8kPa-5.8kPa=30.0kPa,因此此时反应速率v=2.0×10-3×30=6.0×10-2(kPa·min-
1);
③由于温度升高,容器容积不变,总压强提高,且二氧化氮二聚为放热反应,温度提高,平衡
左移,体系物质的量增加,总压强提高,所以若提高反应温度至35℃,则NO(g)完全分解后体
2 5
系压强p(35℃)大于63.1 kPa。
∞
④根据表中数据可知五氧化二氮完全分解时的压强是63.1kPa,根据方程式可知完全分解时最初
生成的二氧化氮的压强是35.8kPa×2=71.6 kPa,氧气是35.8kPa÷2=17.9 kPa,总压强应该
是71.6 kPa+17.9 kPa=89.5 kPa,平衡后压强减少了89.5 kPa-63.1kPa=26.4kPa,所以根
据方程式2NO(g) NO(g)可知平衡时四氧化二氮对应的压强是26.4kPa,二氧化氮对应的压
2 2 4
强是71.6 kPa-26.4kPa×2=18.8kPa,则反应的平衡常数 。
(3)A、第一步反应快,所以第一步的逆反应速率大于第二步的逆反应速率,A正确;B、根据第二步和第三步可知中间产物还有NO,B错误;
C、根据第二步反应生成物中有NO 可知NO 与NO 的碰撞仅部分有效,C正确;
2 2 3
D、第三步反应快,所以第三步反应的活化能较低,D错误。答案选AC。
【答案】 (1). O (2). 53.1 (3). 30.0 (4). 6.0×10-2 (5). 大于 (6).
2
温度提高,体积不变,总压强提高;NO 二聚为放热反应,温度提高,平衡左移,体系物质的量
2
增加,总压强提高 (7). 13.4 (8). AC
11. (2018年全国卷I) Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密
度大等优良性能,得到广泛应用。回答下列问题:
(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为_____、_____(填标
号)。
A. B.
C. D.
(2)Li+与H−具有相同的电子构型,r(Li+)小于r(H−),原因是______。
(3)LiAlH 是有机合成中常用的还原剂,LiAlH 中的阴离子空间构型是______、中心原子的杂
4 4
化形式为______。LiAlH 中,存在_____(填标号)。
4
A.离子键 B.σ键 C.π键 D.氢键
(4)LiO是离子晶体,其晶格能可通过图(a)的Born−Haber循环计算得到。
2
可知,Li原子的第一电离能为________kJ·mol−1,O=O键键能为______kJ·mol−1,LiO晶格能
2
为______kJ·mol−1。
(5)LiO具有反萤石结构,晶胞如图(b)所示。已知晶胞参数为0.4665 nm,阿伏加德罗常数的
2
值为N,则LiO的密度为______g·cm−3(列出计算式)。
A 2【解析】(1)根据核外电子排布规律可知Li的基态核外电子排布式为1s22s1,则D中能量最低;
选项C中有2个电子处于2p能级上,能量最高;
(2)由于锂的核电荷数较大,原子核对最外层电子的吸引力较大,因此Li+半径小于H-;
(3)LiAlH 中的阴离子是AlH-,中心原子铝原子含有的价层电子对数是4,且不存在孤对电子,
4 4
所以空间构型是正四面体,中心原子的杂化轨道类型是sp3杂化;阴阳离子间存在离子键,Al与
H之间还有共价单键,不存在双键和氢键,答案选AB;
(4)根据示意图可知Li原子的第一电离能是1040 kJ/mol÷2=520 kJ/mol;0.5mol氧气转化
为氧原子时吸热是249 kJ,所以O=O键能是249 kJ/mol×2=498 kJ/mol;根据晶格能的定义
结合示意图可知LiO的晶格能是2908 kJ/mol;
2
(5)根据晶胞结构可知锂全部在晶胞中,共计是8个,根据化学式可知氧原子个数是4个,则
LiO的密度是 。
2
【答案】 (1). D (2). C (3). Li+核电荷数较大 (4). 正四面体 (5). sp3
(6). AB (7). 520 (8). 498 (9). 2908 (10).
12. (2018年全国卷I) 化合物W可用作高分子膨胀剂,一种合成路线如下:
回答下列问题:
(1)A的化学名称为________。
(2)②的反应类型是__________。
(3)反应④所需试剂,条件分别为________。(4)G的分子式为________。
(5)W中含氧官能团的名称是____________。
(6)写出与E互为同分异构体的酯类化合物的结构简式(核磁共振氢谱为两组峰,峰面积比为
1∶1)______________。
(7)苯乙酸苄酯( )是花香型香料,设计由苯甲醇为
起始原料制备苯乙酸苄酯的合成路线__________(无机试剂任选)。
【解析】(1)根据A的结构简式可知A是氯乙酸;
(2)反应②中氯原子被-CN取代,属于取代反应。
(3)反应④是酯化反应,所需试剂和条件分别是乙醇/浓硫酸、加热;
(4)根据G的键线式可知其分子式为C H O;
12 18 3
(5)根据W的结构简式可知分子中含有的官能团是醚键和羟基;
(6)属于酯类,说明含有酯基。核磁共振氢谱为两组峰,峰面积比为1:1,说明氢原子分为两
类,各是6个氢原子,因此符合条件的有机物结构简式为 或
;
(7)根据已知信息结合逆推法可知合成苯乙酸卞酯的路线图为
。
【答案】 (1). 氯乙酸 (2). 取代反应 (3). 乙醇/浓硫酸、加热 (4). C H O
12 18 3(5). 羟基、醚键 (6). 、 (7).