文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
专题 10 溶液
知识点一、溶液
1.定义:一种或几种物质分散到另一种物质里,形 一、 的 。
2.溶液的组成及其特征:溶液由 和 ,最常用的溶剂是 ;另外常用的溶剂还有 、汽
油。溶液的基本特征是 、 、 。
3.溶解过程:物质在溶解过程中发生了两种变化,一种是 过程,此过程 热量,另一种是
过程,此过程 热量,氢氧化钠、 、生石灰等物质溶于水放热, 等物质溶于水吸热,
、蔗糖等物质溶于水温度不变。
4.乳化现象:洗洁精、洗发液等因为具有 作用,所以可去油污,它们使油类物质以细小的液滴
的形态分散在水中,形成不易分层、比较稳定的混合物这种现象叫做 现象。(用汽油洗掉油污
是 作用,形成 ;用洗涤剂洗油污是 作用,形成 。)
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
5.饱和溶液和不饱和溶液
(1)定义:在一定温度下,在一定量的溶剂里,不能再溶解某种溶质的溶液,叫这种溶质的
; 还能继续溶解某种溶质的溶液的溶液,叫这种溶质的的 。
(2)饱和溶液与不饱和溶液之间的转化方法:(对大多数固体物质)
a 针对大多数溶解度随温度升高而增大的物质:
b 对于Ca(OH) 等溶解度随温度升高而减小的物质:
2
知识点二、溶液组成的定量表示
1.溶质质量分数定义:定量表示溶液组成的方法很多,化学上常用 来表示溶液的组
成。它是溶质与 溶液的质量之比。
2.其定义公式为:溶质的质量分数= ×100%。
3.变形公式:溶质质量= × ;溶剂质量= 的质量— 的质量
4.溶液的稀释问题
(1)通过向一定溶质质量分数的溶液中加入水或蒸发水,改变其溶质质量分数,在此过程中,浓
稀溶液中 的质量不变。
(2)稀释前浓溶液质量×浓溶液 =稀释后稀溶液质量× 稀溶液
知识点三、配制溶液
1.步骤
(1) ;需要食盐 克;需要水 克;即42毫升。
(2) ;用托盘天平称取食盐8g,用 量取42毫升水。
(3) ;先将食盐放入烧杯中,然后将量取的水加入,并用 不断搅拌。
(4) ;将配好的溶液放入试剂瓶中,注意标签(注明药品的名称和 )向外。
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
2.误差分析:
(1)如果配制的溶液的溶质质量分数低于16%,可能的原因是什么?
取水;砝码缺损;食盐 ;左物右码放反了,并且 等。
(2)如果配制的溶液的溶质质量分数大于16%呢?
取水;砝码 等。
(3)对溶质质量分数没影响?
装瓶存放时撒了一些溶液;左物右码放反了,但 等。
知识点四、溶解度及曲线
(一)固体的溶解度
1.概念:固体物质溶解度指的是在 ,某固态物质在 里达到
时所溶解的 。
2.理解溶解度概念的四要素:①、条件: ②、标准: ③、状
态: ④、单位 3.影响固体物质的溶解度因素:内因 、
;外因是 。
4.固体物质溶解度的变化规律:
(1)大多数固体物质的溶解度 ;如KNO;
3
(2)少数固体物质的溶解度 ;如 ;
(3)极少数固体物质的溶解度 。如 。
5、物质的溶解性
溶解性 易溶物质 可溶物质 微溶物质 难溶物质
20℃溶解度(g)
(二)气体的溶解度
1.定义:气体的溶解度是指气体物质在 、 一体积水最多溶解气体的
来表示。
2.影响气体的溶解度因素:内因 、 ;外因是 。
3.在一定压强下,温度越高气体的溶解度越 ,温度越低气体的溶解度越 ;在一定温度下,压强
越大气体的溶解度越 ,压强越小气体的溶解度越 。
(三)混合物的分离
(1)过滤法:分离 物 + 物(分离氯酸钾和二氧化锰加热后的剩余物)
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(2)结晶法:分离几种可溶性物质
,如NaCl(海水晒盐)适用于溶解度 的物质。
结晶的两种方法 析出晶体后溶液的溶质质量分数不变
( 溶液,如KNO )适用于溶解度 的物质。
3
析出晶体后溶液的溶质质量分数减小。
(四)溶解度曲线
1.溶解度曲线:用纵坐标表示 ,横坐标表示 ,根据物质在不同温度下的溶解度绘制成不
同物质随 变化的曲线。
2.线的含义:三线:①“陡升型” :大多数固体物的溶解度随温度升高而 。如KNO;
3
② “缓升型”:少数固体物质的溶解度受温度的影响很小。如 ;
③“下降型”:极少数物质溶解度随温度升高而降低。如 。
3.点的含义:四点:
① 曲线上的点:所示某温度下某物质的溶解度是多少(该温度下 状态)。
② 两曲线的交点:表示在该点所示的温度下,两种物质的 相等。
③ 线上方的点表示:在该温度下,该溶液是 且有部分 ;
④ 线下方的点表示:该温度下,该溶液是 。
考点一.溶液的概念、组成及其特点
1.(2023•自贡)溶液用途广泛,与人们的生活息息相关。下列说法正确的是( )
A.溶液是由溶质和溶剂组成的
B.溶液都是无色透明的液体
C.溶液是具有均一性、稳定性的纯净物
D.饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液
考点二.影响溶解快慢的因素
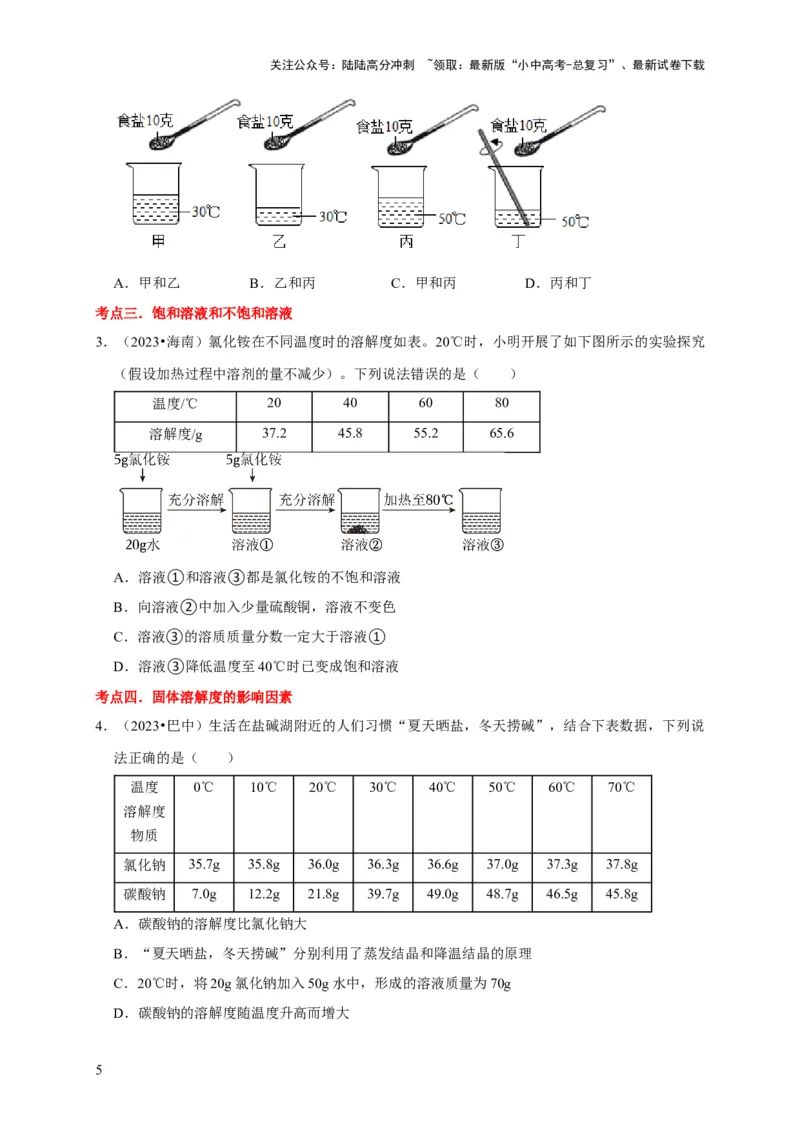
2.(2023•平遥县二模)若研究温度对食盐溶解快慢的影响,在图中应选用哪两个装置进行对照实
验( )
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.甲和乙 B.乙和丙 C.甲和丙 D.丙和丁
考点三.饱和溶液和不饱和溶液
3.(2023•海南)氯化铵在不同温度时的溶解度如表。20℃时,小明开展了如下图所示的实验探究
(假设加热过程中溶剂的量不减少)。下列说法错误的是( )
温度/℃ 20 40 60 80
溶解度/g 37.2 45.8 55.2 65.6
A.溶液①和溶液③都是氯化铵的不饱和溶液
B.向溶液②中加入少量硫酸铜,溶液不变色
C.溶液③的溶质质量分数一定大于溶液①
D.溶液③降低温度至40℃时已变成饱和溶液
考点四.固体溶解度的影响因素
4.(2023•巴中)生活在盐碱湖附近的人们习惯“夏天晒盐,冬天捞碱”,结合下表数据,下列说
法正确的是( )
温度 0℃ 10℃ 20℃ 30℃ 40℃ 50℃ 60℃ 70℃
溶解度
物质
氯化钠 35.7g 35.8g 36.0g 36.3g 36.6g 37.0g 37.3g 37.8g
碳酸钠 7.0g 12.2g 21.8g 39.7g 49.0g 48.7g 46.5g 45.8g
A.碳酸钠的溶解度比氯化钠大
B.“夏天晒盐,冬天捞碱”分别利用了蒸发结晶和降温结晶的原理
C.20℃时,将20g氯化钠加入50g水中,形成的溶液质量为70g
D.碳酸钠的溶解度随温度升高而增大
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
考点五.固体溶解度曲线及其作用
5.(2023•广西)甲、乙、丙三种固体物质的溶解度曲线如图所示。下列说法一定正确的是
( )
A.t ℃时,等质量的甲、乙、丙的溶液降温到t ℃时,析出晶体最多的是甲的溶液
3 1
B.t ℃时,将25g乙加入到50g水中,再降温到t ℃,所得溶液的溶质质量分数约为33.3%
2 1
C.t ℃时,将等质量的甲、乙、丙分别溶于水,配成饱和溶液,所需水的质量大小关系为乙<
1
甲=丙
D.t ℃时,甲、乙、丙的饱和溶液中,所含溶质的质量大小关系为乙>甲=丙
1
6.(2023•宜宾)晾晒海水制盐在我国有着悠久的历史,利用该工艺可得到氯化钠和氯化镁等物质。
氯化钠和氯化镁的溶解度曲线如图,下列说法正确的是( )
A.海水晒盐利用了蒸发结晶的方法获得晶体
B.氯化钠的溶解度受温度影响较大
C.t℃时,氯化镁饱和溶液中溶质质量分数为70%
D.采用降温结晶的方法可除去氯化钠饱和溶液中少量的氯化镁杂质
7.(2023•大庆)已知硝酸钾的溶解度(S)、饱和NaCl溶液中溶质的质量分数(w%)与温度的
关系如图所示。下列说法正确的是( )
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.M点表示硝酸钾和氯化钠的溶解度相同
B.20℃时,饱和KNO 溶液中溶质的质量分数为31.6%
3
C.20℃时,100g15.8%的KNO 溶液蒸发掉30g水变为饱和溶液
3
D.将N点的NaCl溶液降温至40℃,N点转化为P点
8.(2023•扬州)KNO 和NaCl的溶解度曲线如图所示。下列说法正确的是( )
3
A.KNO 的溶解度比NaCl大
3
B.将室温下KNO 的饱和溶液升高温度,溶液仍饱和
3
C.KNO 和NaCl均属于难溶物质
3
D.除去KNO 中少量NaCl可用冷却热饱和溶液结晶的方法
3
9.(2023•淄博)如图为硝酸钾的溶解度曲线,下列说法错误的是( )
A.20℃时,硝酸钾的溶解度为31.6g
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
B.硝酸钾的溶解度随温度的升高而增大
C.将80℃的硝酸钾饱和溶液269g冷却到20℃时,析出137.4g硝酸钾
D.80℃时,向50g水中加入90g硝酸钾,充分溶解,得到140g饱和溶液
10.(2023•济宁)t ℃时,将等质量的硝酸钾和氯化钾分别加入到盛有 100g水的两个烧杯中,充
1
分搅拌后现象如图 1所示,硝酸钾和氯化钾的溶解度曲线如图 2所示,下列说法错误的是
( )
A.烧杯①中溶解的溶质是氯化钾
B.烧杯②中的上层清液属于饱和溶液
C.将t ℃时50g硝酸钾的饱和溶液稀释成5%的溶液,需加水150g
1
D.t ℃时,将两个烧杯中的溶液混合,充分搅拌后,烧杯中一定还有剩余固体
1
11.(2023•南通)常温下,工业可利用Na SO +KCl→NaCl+K SO (未配平)原理制备K SO 。
2 4 2 4 2 4
Na SO 、KCl、NaCl和K SO 的溶解度曲线如图所示。下列说法正确的是( )
2 4 2 4
A.KCl的溶解度一定大于NaCl的溶解度
B.Na SO 的溶解度随温度的升高一直增大
2 4
C.60℃时,Na SO 、KCl溶液中溶质的质量分数一定相等
2 4
D.该制备反应利用了常温下K SO 溶解度相对较小的性质
2 4
12.(2023•南山区校级三模)t ℃时,将a、b两种固体物质各25g,分别加入盛有100g水的烧杯
1
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
中,充分搅拌后现象如图甲所示;升温到 t ℃时(忽略水分蒸发),现象如图乙所示;图丙是
2
a、b两种固体物质在水中的溶解度曲线。下列说法正确的是( )
A.图丙中曲线N表示b物质的溶解度曲线
B.图甲中两烧杯内a、b溶液的溶质质量分数相等
C.图乙中烧杯内b溶液的溶质质量分数为25%
D.可用降温结晶的方法从饱和a溶液中得到固体a
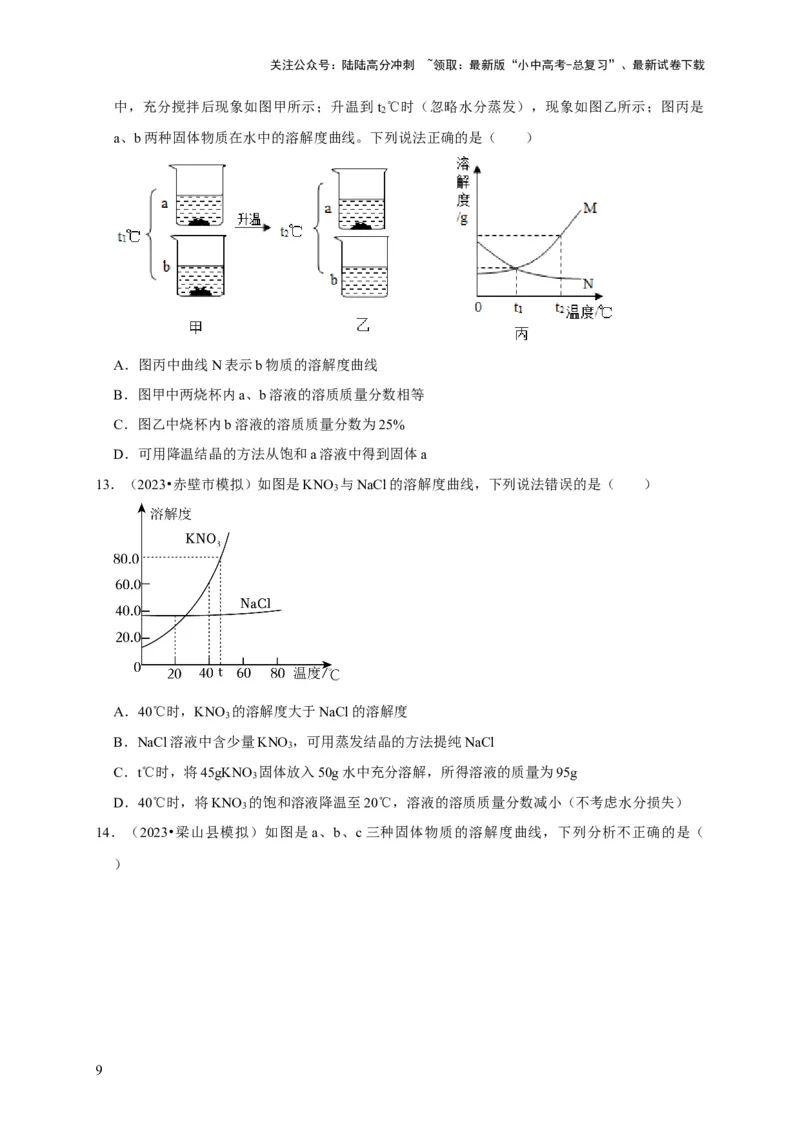
13.(2023•赤壁市模拟)如图是KNO 与NaCl的溶解度曲线,下列说法错误的是( )
3
A.40℃时,KNO 的溶解度大于NaCl的溶解度
3
B.NaCl溶液中含少量KNO ,可用蒸发结晶的方法提纯NaCl
3
C.t℃时,将45gKNO 固体放入50g水中充分溶解,所得溶液的质量为95g
3
D.40℃时,将KNO 的饱和溶液降温至20℃,溶液的溶质质量分数减小(不考虑水分损失)
3
14.(2023•梁山县模拟)如图是a、b、c三种固体物质的溶解度曲线,下列分析不正确的是(
)
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.t ℃时,125gb的饱和溶液中含有b物质25g
2
B.t ℃时,分别将等质量的a、b饱和溶液降温至t ℃,析出的固体质量关系是:a>b
3 2
C.分别将t ℃时a、c的饱和溶液升温到t ℃,均变为不饱和溶液
1 2
D.a中含有少量b时,可采用冷却a的热饱和溶液的方法提纯a
15.(2023•龙江县四模)如图为A、B、C三种固体物质的溶解度曲线图。
(1)t ℃时,溶解度最大的物质是 。
1
(2)若将M点处C的不饱和溶液变成饱和溶液,可以选择的方法是 (填序号)。
①降低温度
②增加溶质
③蒸发溶剂
(3)t ℃时,将等质量的A、B、C的饱和溶液都升温到t ℃,溶液中溶剂质量的大小关系是
2 3
(忽略水的挥发) 。
16.(2023•贺兰县校级模拟)甲、乙、丙三种物质的溶解度曲线如图所示,请回答下列问题。
(1) ℃时,甲和乙的溶解度相等。
(2)溶解度随温度的升高而减小的物质是 ;若甲中混有少量乙,可用 方
法提纯甲。
(3)将甲物质的不饱和溶液变成饱和溶液,可采取的方法是 (填序号)。
A.增加甲物质
B.升高温度
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C.蒸发溶剂
(4)下列说法正确的是 (填序号)。
A.t ℃时,甲、乙两种溶液溶质质量分数一定相等
2
B.t ℃时,配制300g甲的饱和溶液,需要固体甲的质量为100g
3
C.t ℃时,甲、乙两种物质的饱和溶液降温到t ℃,甲析出的晶体一定比乙多
3 1
D.t ℃时,将等质量的甲、乙、丙三种物质配成该温度下的饱和溶液,所需溶剂的质量甲=丙>
1
乙
考点六.气体溶解度的影响因素
17.(2023•云南)夏季下雨之前,天气闷热,水中的含氧量降低,养鱼池中的鱼往往会浮出水面。
下列有关说法错误的是( )
A.氧气的溶解度会随压强的减小而减小
B.氧气的溶解度会随温度的升高而增大
C.为了增加养鱼池中的含氧量,可以向养鱼池中通入空气
D.为了增加养鱼池中的含氧量,可以把养鱼池的水喷向空中
考点七.晶体和结晶的概念与现象
18.(2023•花山区一模)为探究硝酸钾的溶解性,进行了如图所示实验,结合硝酸钾在不同温度
下的溶解度,判断下列说法不正确的是( )
温度/℃ 10 20 30 40 50 60
KNO 溶解 20.9 31.6 45.8 63.9 85.5 110.0
3
度/g
A.①③中的溶液均为不饱和溶液
B.②③中溶液的质量:③>②
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C.②③④中溶液的溶质质量分数:③>②>④
D.④中析出晶体的质量是9.9g
19.(2023•峰峰矿区校级模拟)为探究硝酸钾的溶解性,进行了如图所示实验,结合硝酸钾在不
同温度下的溶解度(下表),判断下列说法不正确的是( )
温度/℃ 10 20 30 40 50 60
KNO 溶解 20.9 31.6 45.8 63.9 85.5 110.0
3
度/g
A.①③中的溶液均为不饱和溶液
B.②③中溶液的质量:③>②
C.④中析出晶体的质量是10.7g
D.溶液的溶质质量分数:③>②>④
考点八.溶质的质量分数
20.(2023•滨州)下面是四位同学在小组学习群中的交流记录,其中错误的是( )
A.小云:硝酸铵溶于水后,溶液温度降低
B.小丁:饱和溶液的溶质质量分数不一定大于不饱和溶液的溶质质量分数
C.小丽:具有均一性稳定性的液体一定是溶液
D.小凯:利用洗洁精的乳化作用,可洗去餐具上的油污
一.选择题(共14小题)
1.(2023•合肥二模)王亚平在太空做了油和水“难分难舍”的神奇实验:她用力摇晃装有油和水
的瓶子,让油水充分混合、静置,发现油水不分层。下列说法不正确的是( )
A.在地面油水混合物会产生分层现象
B.太空中水的化学性质与地面不同
C.在不同环境中同一实验可能现象不同
D.在地面向油水混合物中加入洗涤剂会产生乳化现象
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
2.(2023•伊通县模拟)下列物质加入足量的水中能形成紫红色溶液的是( )
A.硫酸铜 B.植物油 C.氯化铁 D.高锰酸钾
3.(2023•佛冈县一模)关于100g 10%的硝酸钾溶液,下列叙述正确的是( )
A.100g水中溶有10g硝酸钾
B.溶液中硝酸钾与水的质量比为1:10
C.将硝酸钾和水按9:1的质量比配成的溶液
D.将10g硝酸钾溶于90g水中,可制得该溶液
4.(2023•江都区二模)KNO 的溶解度曲线如图所示。下列说法错误的是( )
3
A.0~60℃,KNO 的溶解度随温度升高而增大
3
B.60℃时的KNO 饱和溶液降温至20℃,有晶体析出
3
C.20℃时,100g水中最多能溶解31.6g KNO
3
D.60℃时,可配制溶质质量分数为60%的KNO 溶液
3
5.(2023•奉节县模拟)溶液用途广泛,与人们的生活息息相关。下列说法正确的是( )
A.溶液是由溶质和溶剂组成的
B.溶液都是无色透明的液体
C.溶液是具有均一性、稳定性的纯净物
D.饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液
6.(2023•曲江区校级模拟)在20℃时,某固体物质(不含结晶水)的水溶液,经历如图变化,下
列 说 法 正 确 ( )
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.溶液甲一定是饱和溶液
B.20℃时,该固体的溶解度是40g
C.20℃时,溶液丙若再蒸发10g水(不考虑蒸干),析出晶体总质量为8g
D.溶液质量分数:乙<丙
7.(2023•黑龙江二模)下列对实验结果的预判或结论中,正确的是( )
A.将1gCaO投入到99g水中,将得到溶质的质量分数大于1%的氢氧化钙溶液
B.常温下KNO 、Ca(OH) 的饱和溶液降温后,仍都是饱和溶液
3 2
C.将带火星的木条伸入集气瓶内,木条复燃,证明瓶内已集满氧气
D.在测定空气中氧气的体积分数时,测量结果偏低,可能是红磷量不足
8.(2023•青羊区校级模拟)为探究硝酸钾的溶解性,进行了如图所示实验(实验过程)
结合硝酸钾在不同温度下的溶解度,判断下列说法不正确的是( )
温度/℃ 10 20 30 40 50 60
KNO 溶解 20.9 31.6 45.8 63.9 85.5 110.0
3
度/g
A.①③中的溶液均为不饱和溶液
B.②③中溶液的质量:③>②
C.②③④中溶液的溶质质量分数:③>②>④
D.④中析出晶体的质量是0.9g
9.(2023•南海区校级模拟)如图为甲、乙两种固体物质在水中的溶解度曲线.下列说法正确的是
( )
A.甲物质的溶解度大于乙物质的溶解度
B.在t ℃时,甲、乙两物质溶液溶质质量分数相等
1
C.在t ℃时,H点表示乙物质的不饱和溶液
2
14关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
D.G点对应的甲物质溶液升温到t ℃时,溶质质量分数不变
2
10.(2023•顺义区二模)某实验小组进行了如图所示的实验。(已知:20℃时,KNO 的溶解度为
3
31.6g。实验中水的损失以及温度变化忽略不计)。下列说法不正确的是( )
A.a≥11.6g
B.溶质质量②=④
C.一定属于不饱和溶液的是①
D.实验范围内,KNO 的溶解度随温度升高而增大
3
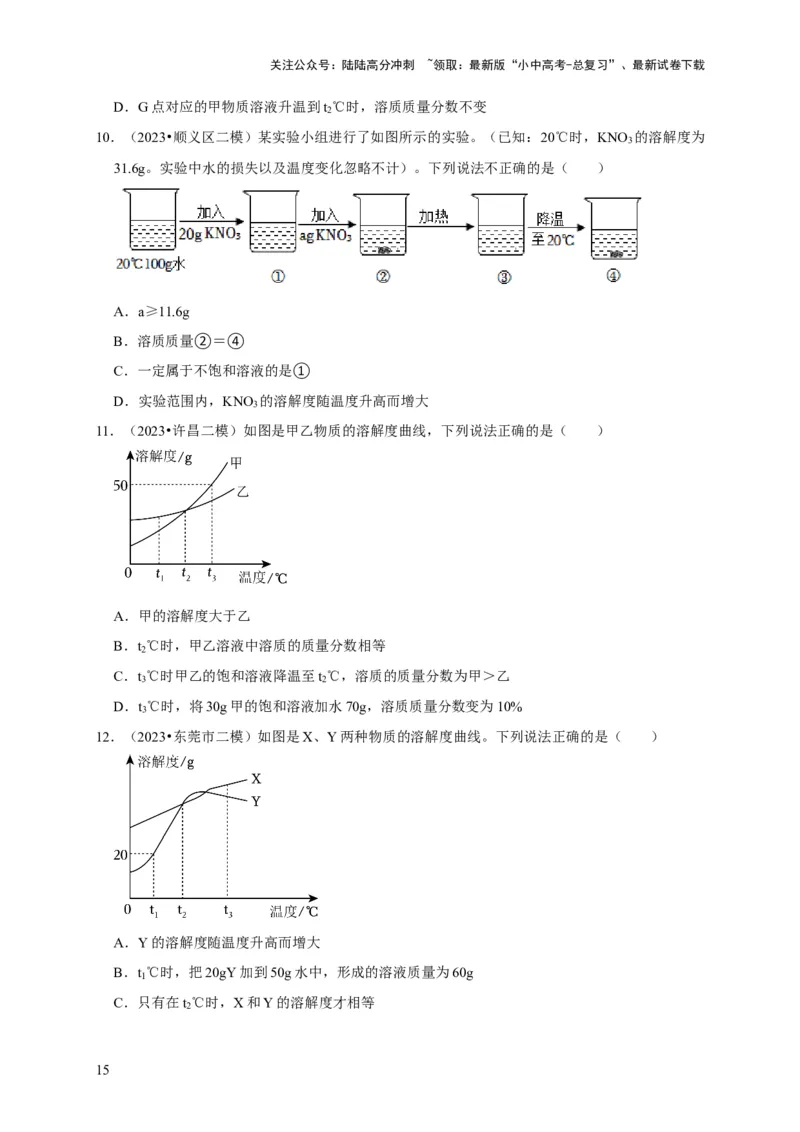
11.(2023•许昌二模)如图是甲乙物质的溶解度曲线,下列说法正确的是( )
A.甲的溶解度大于乙
B.t ℃时,甲乙溶液中溶质的质量分数相等
2
C.t ℃时甲乙的饱和溶液降温至t ℃,溶质的质量分数为甲>乙
3 2
D.t ℃时,将30g甲的饱和溶液加水70g,溶质质量分数变为10%
3
12.(2023•东莞市二模)如图是X、Y两种物质的溶解度曲线。下列说法正确的是( )
A.Y的溶解度随温度升高而增大
B.t ℃时,把20gY加到50g水中,形成的溶液质量为60g
1
C.只有在t ℃时,X和Y的溶解度才相等
2
15关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
D.t ℃时,Y物质的饱和溶液的溶质质量分数为20%
1
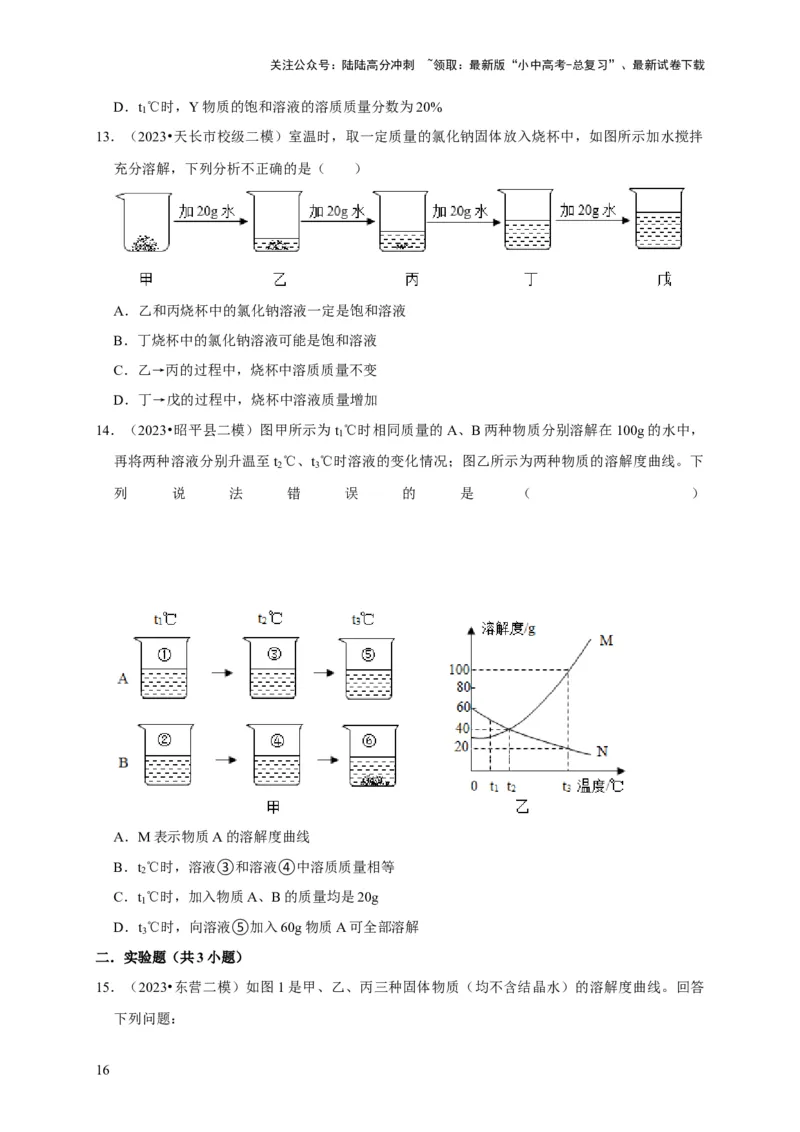
13.(2023•天长市校级二模)室温时,取一定质量的氯化钠固体放入烧杯中,如图所示加水搅拌
充分溶解,下列分析不正确的是( )
A.乙和丙烧杯中的氯化钠溶液一定是饱和溶液
B.丁烧杯中的氯化钠溶液可能是饱和溶液
C.乙→丙的过程中,烧杯中溶质质量不变
D.丁→戊的过程中,烧杯中溶液质量增加
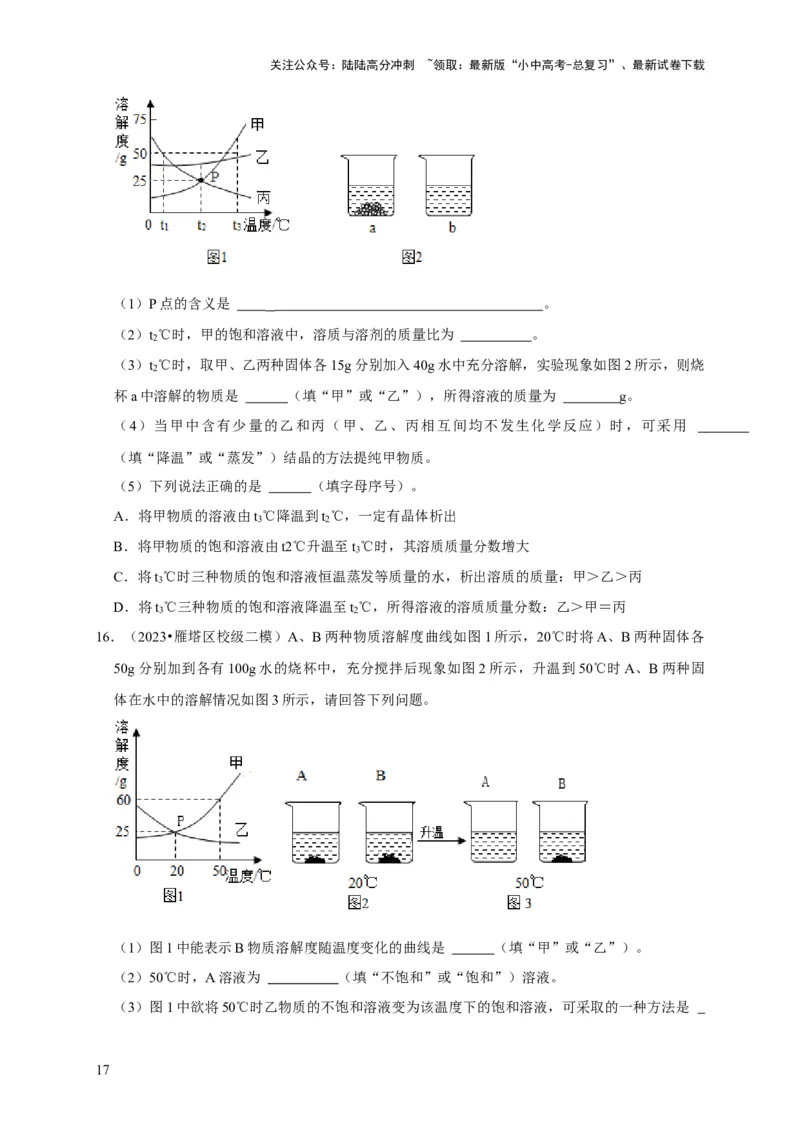
14.(2023•昭平县二模)图甲所示为t ℃时相同质量的A、B两种物质分别溶解在100g的水中,
1
再将两种溶液分别升温至t ℃、t ℃时溶液的变化情况;图乙所示为两种物质的溶解度曲线。下
2 3
列 说 法 错 误 的 是 ( )
A.M表示物质A的溶解度曲线
B.t ℃时,溶液③和溶液④中溶质质量相等
2
C.t ℃时,加入物质A、B的质量均是20g
1
D.t ℃时,向溶液⑤加入60g物质A可全部溶解
3
二.实验题(共3小题)
15.(2023•东营二模)如图1是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线。回答
下列问题:
16关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)P点的含义是 。
(2)t ℃时,甲的饱和溶液中,溶质与溶剂的质量比为 。
2
(3)t ℃时,取甲、乙两种固体各15g分别加入40g水中充分溶解,实验现象如图2所示,则烧
2
杯a中溶解的物质是 (填“甲”或“乙”),所得溶液的质量为 g。
(4)当甲中含有少量的乙和丙(甲、乙、丙相互间均不发生化学反应)时,可采用
(填“降温”或“蒸发”)结晶的方法提纯甲物质。
(5)下列说法正确的是 (填字母序号)。
A.将甲物质的溶液由t ℃降温到t ℃,一定有晶体析出
3 2
B.将甲物质的饱和溶液由t2℃升温至t ℃时,其溶质质量分数增大
3
C.将t ℃时三种物质的饱和溶液恒温蒸发等质量的水,析出溶质的质量:甲>乙>丙
3
D.将t ℃三种物质的饱和溶液降温至t ℃,所得溶液的溶质质量分数:乙>甲=丙
3 2
16.(2023•雁塔区校级二模)A、B两种物质溶解度曲线如图1所示,20℃时将A、B两种固体各
50g分别加到各有100g水的烧杯中,充分搅拌后现象如图2所示,升温到50℃时A、B两种固
体在水中的溶解情况如图3所示,请回答下列问题。
(1)图1中能表示B物质溶解度随温度变化的曲线是 (填“甲”或“乙”)。
(2)50℃时,A溶液为 (填“不饱和”或“饱和”)溶液。
(3)图1中欲将50℃时乙物质的不饱和溶液变为该温度下的饱和溶液,可采取的一种方法是
17关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
。
(4)分别将50℃时80g甲、乙的饱和溶液降温到20℃,以下说法正确的是 。
A.溶液的质量:甲<乙
B.溶剂的质量:甲=乙
C.溶质的质量分数:甲>乙
D.甲溶液析出的固体质量:35g
17.(2023•东方校级三模)甲、乙试管中各盛有10g水,向其中一支加入3gKNO 固体,另一支
3
加入3gNaCl固体,按图1进行实验。图2为KNO 和NaCl的溶解度曲线。据图回答问题:
3
(1)甲中加入的固体是 。
(2)20℃时,KNO 的溶解度为 31.6g,在 100g水中加入 50gKNO ,形成的溶液质量为
3 3
。
(3)将30℃时KNO 、NaCl两种物质的饱和溶液降温至20℃(其他条件不变),所得溶液的溶
3
质质量分数:KNO (填“>”、“<”或“=”)NaCl。
3
(4)KNO 中混有少量NaCl杂质,可用 的方法提纯KNO 。
3 3
三.解答题(共3小题)
18.(2023•嘉禾县校级二模)如图是硝酸钾(KNO )和氯化钾(KCl)的溶解度曲线,请回答下
3
列问题。
(1)10℃时,KNO 和KCl的溶解度大小关系是:KNO KCl(选填“>”、“<”或
3 3
“=”)。
(2)60℃时,将 60g KNO 固体放入 50g 水中,充分溶解后,所得溶液的质量为
3
g。
(3)据图,下列有关说法正确的是 。
18关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.KCl的不饱和溶液只能采用蒸发溶剂的方法才可变成饱和溶液
B.60℃时,KNO 溶液的溶质质量分数比KCl溶液的大
3
C.将60℃时KNO 和KCl两种溶液分别降温至10℃,析出晶体较多的是KNO 溶液
3 3
D.60℃时,从KNO 和KCl两种饱和溶液中获得等质量晶体,蒸发水较多的是KCl溶液
3
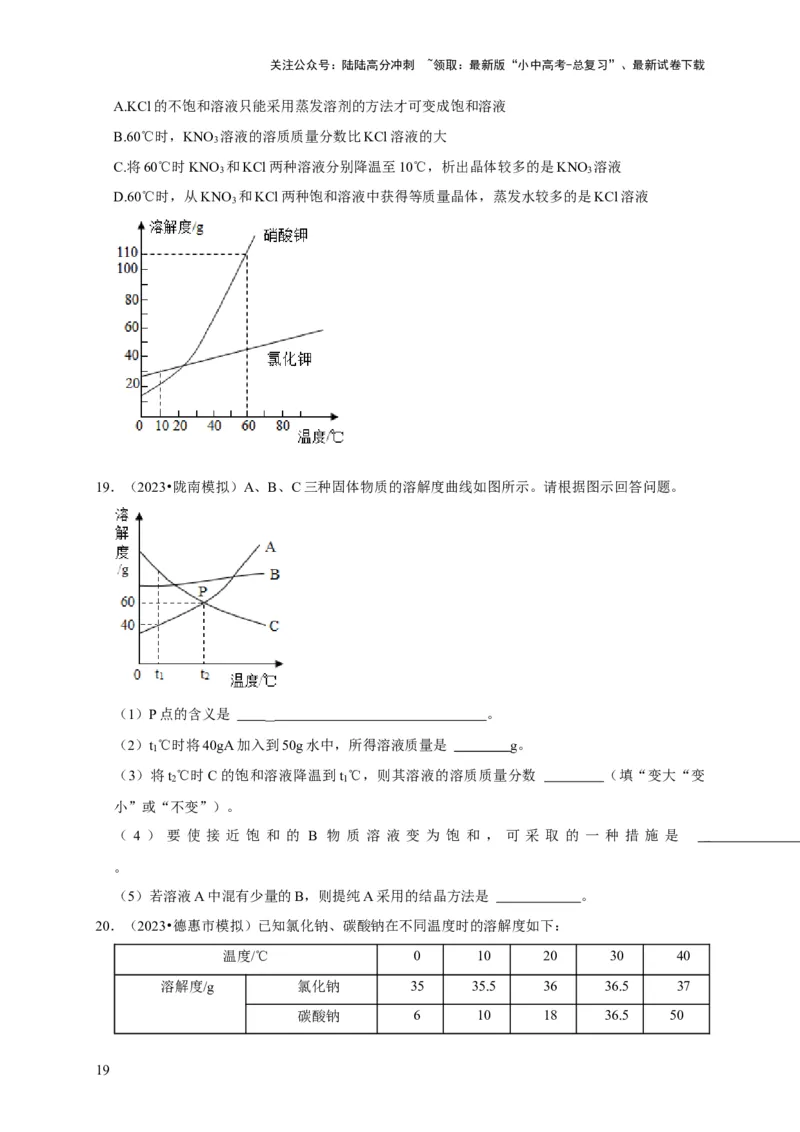
19.(2023•陇南模拟)A、B、C三种固体物质的溶解度曲线如图所示。请根据图示回答问题。
(1)P点的含义是 。
(2)t ℃时将40gA加入到50g水中,所得溶液质量是 g。
1
(3)将t ℃时C的饱和溶液降温到t ℃,则其溶液的溶质质量分数 (填“变大“变
2 1
小”或“不变”)。
( 4 ) 要 使 接 近 饱 和 的 B 物 质 溶 液 变 为 饱 和 , 可 采 取 的 一 种 措 施 是
。
(5)若溶液A中混有少量的B,则提纯A采用的结晶方法是 。
20.(2023•德惠市模拟)已知氯化钠、碳酸钠在不同温度时的溶解度如下:
温度/℃ 0 10 20 30 40
溶解度/g 氯化钠 35 35.5 36 36.5 37
碳酸钠 6 10 18 36.5 50
19关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
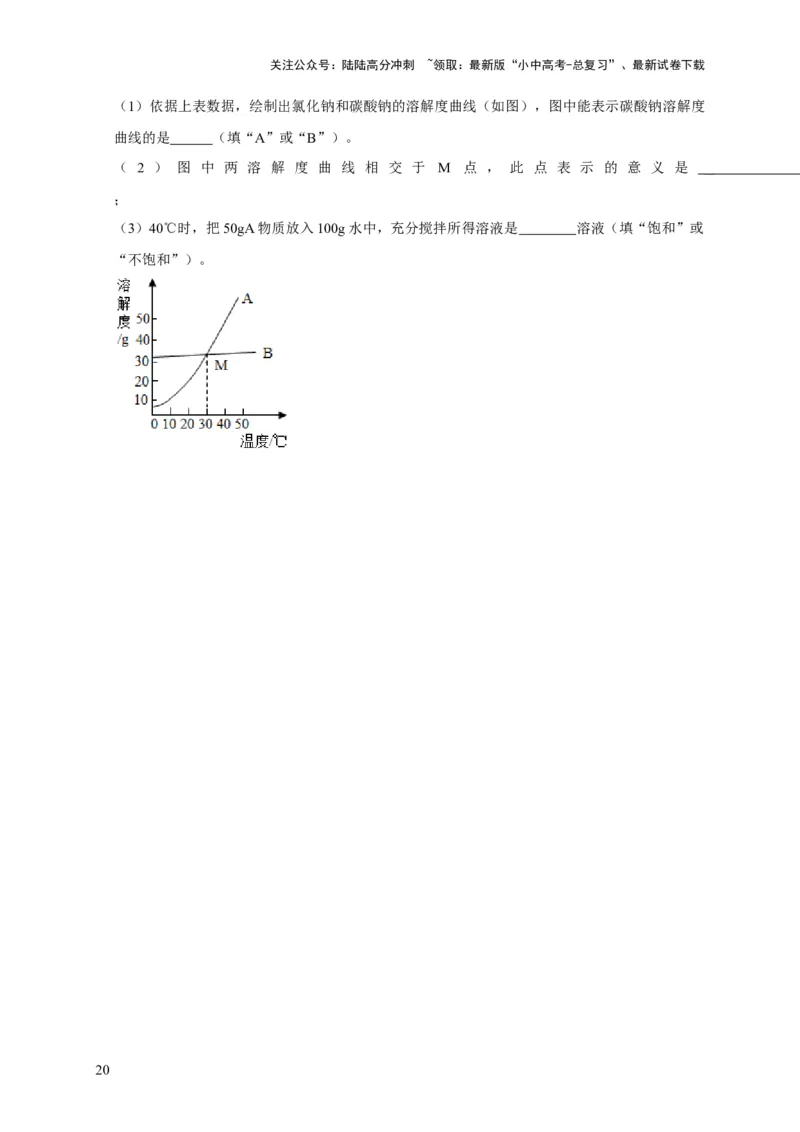
(1)依据上表数据,绘制出氯化钠和碳酸钠的溶解度曲线(如图),图中能表示碳酸钠溶解度
曲线的是 (填“A”或“B”)。
( 2 ) 图 中 两 溶 解 度 曲 线 相 交 于 M 点 , 此 点 表 示 的 意 义 是
;
(3)40℃时,把50gA物质放入100g水中,充分搅拌所得溶液是 溶液(填“饱和”或
“不饱和”)。
20