文档内容
2025年上海市高考化学试卷
一、碳酸丙烯酯的合成(20分)
1.(20分)碳酸丙烯酯(PC)是一种重要的有机化合物,在工业上有广泛应用。
(1) 中电负性最大的元素是 。
A.C
B.H
C.O
(2)1mol 分子中σ键的数目为 。
A.7N
A
B.12N
A
C.13N
A
D.14N
A
环氧丙烷与CO 催化合成法是生产碳酸丙烯酯(PC)的常用方法:
2
反应Ⅰ: (g)+CO (g)═ (l)ΔH =﹣125kJ•mol﹣1
2 1
反应Ⅱ:C(s)+O (g)═CO (g)ΔH =﹣393.5kJ•mol﹣1
2 2 2
反应Ⅲ:3H (g)+3C(s)+0.5O (g)═ (g)ΔH =﹣94.7kJ•mol﹣1
2 2 3
(3)反应Ⅳ:3H (g)+4C(s)+1.5O (g)═ (l)的热效应为ΔH = kJ•mol﹣1。
2 2 4
A.﹣613.2
B.613.2
C.395.2
D.﹣395.2
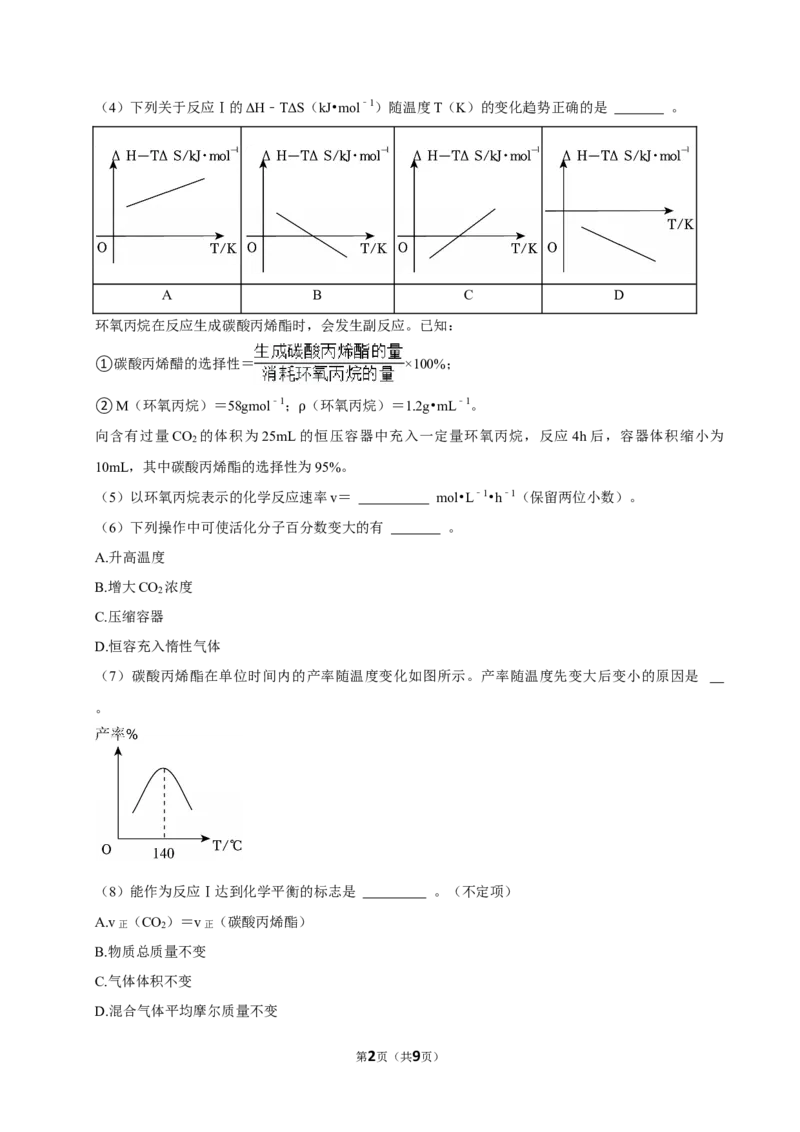
第1页(共9页)(4)下列关于反应Ⅰ的ΔH﹣TΔS(kJ•mol﹣1)随温度T(K)的变化趋势正确的是 。
A B C D
环氧丙烷在反应生成碳酸丙烯酯时,会发生副反应。已知:
①碳酸丙烯醋的选择性= ×100%;
②M(环氧丙烷)=58gmol﹣1; (环氧丙烷)=1.2g•mL﹣1。
向含有过量CO
2
的体积为25mLρ的恒压容器中充入一定量环氧丙烷,反应4h后,容器体积缩小为
10mL,其中碳酸丙烯酯的选择性为95%。
(5)以环氧丙烷表示的化学反应速率v= mol•L﹣1•h﹣1(保留两位小数)。
(6)下列操作中可使活化分子百分数变大的有 。
A.升高温度
B.增大CO 浓度
2
C.压缩容器
D.恒容充入惰性气体
(7)碳酸丙烯酯在单位时间内的产率随温度变化如图所示。产率随温度先变大后变小的原因是
。
(8)能作为反应Ⅰ达到化学平衡的标志是 。(不定项)
A.v正 (CO
2
)=v正 (碳酸丙烯酯)
B.物质总质量不变
C.气体体积不变
D.混合气体平均摩尔质量不变
第2页(共9页)(9)用光气COCl 与丙二醇反应也可以用于制备碳酸丙烯酯,从绿色化学角度写出三点传统环氧丙烷
2
与CO 催化合成法的优势 。
2
二、“重石头元素”——钨(20分)
2.(20分)钨属于有色金属,在高温下可以发出亮光。
(1)钨作灯丝与钨的 性质有关。
A.延展性
B.导电性
C.高熔点
D.高密度
(2)请从微观角度解释钨有金属光泽的原因: 。
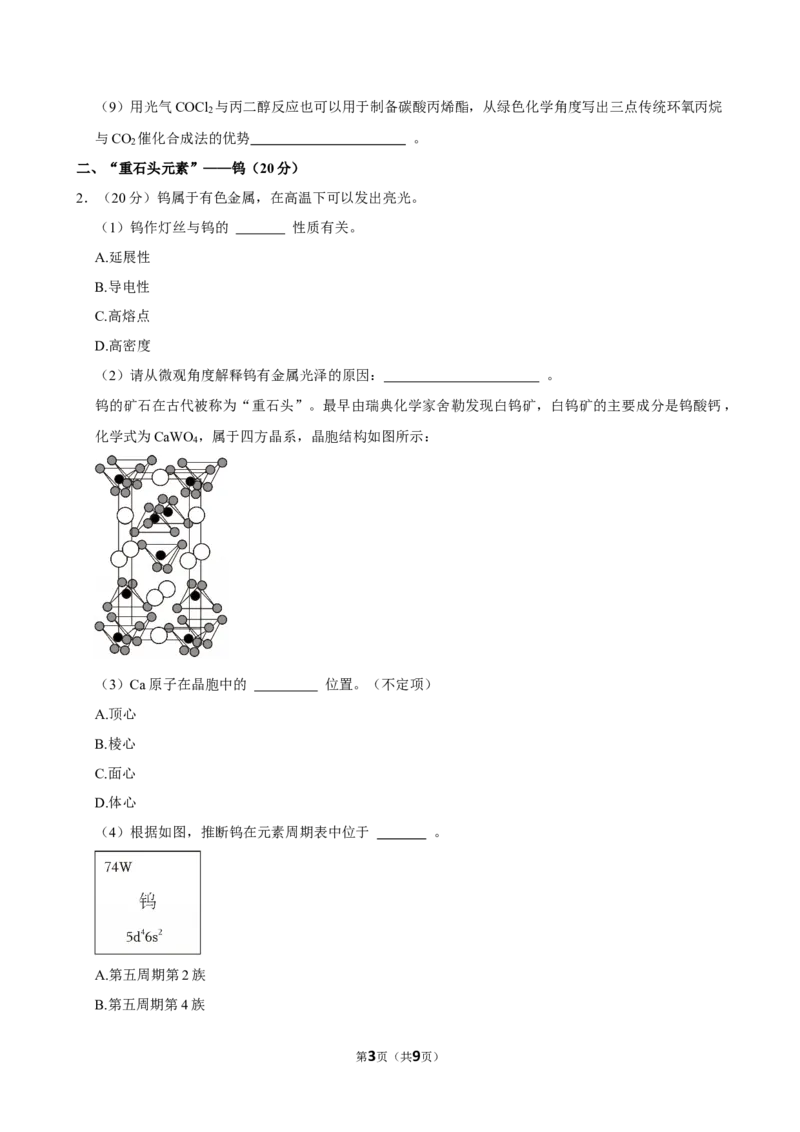
钨的矿石在古代被称为“重石头”。最早由瑞典化学家舍勒发现白钨矿,白钨矿的主要成分是钨酸钙,
化学式为CaWO ,属于四方晶系,晶胞结构如图所示:
4
(3)Ca原子在晶胞中的 位置。(不定项)
A.顶心
B.棱心
C.面心
D.体心
(4)根据如图,推断钨在元素周期表中位于 。
A.第五周期第2族
B.第五周期第4族
第3页(共9页)C.第六周期第4族
D.第六周期第6族
(5)根据价层电子对互斥理论, 的价层电子对数为 。
(6)若如图所示的晶胞中仅含1个完整的 四面体,则1~8号O原子中,组成该四面体的O编号
为 。
白钨矿通常与脉石、黄铁矿等伴生。已知白钨矿中各种矿石的密度如表所示:
矿石 脉石 黄铁矿 萤石 磷灰石
密度 (g•cm﹣3) 2.65 4.95 3.18 3.13
(7)已知ρ M(CaWO )=288g•mol﹣1、V(CaWO )=3.12×10﹣22cm3,则 (CaWO )=
4 4 4
g•cm﹣3。 ρ
结合数据说明钨酸钙矿石被称为“重石头”的原因: 。
CaWO 具有良好的光学性质,被广泛应用于光电陶瓷材料中,工业上可用电解法制备,电解装置如图
4
所示:
已知:K (CaWO )=8.7×10﹣9,K (CaCO )=2.7×10﹣8。
sp 4 sp 3
(8)写出电解池阳极的反应式: 。
(9)为获取高纯产物,制备时需要不断通入N 的原因是 。
2
三、福辛普利中间体合成(20分)
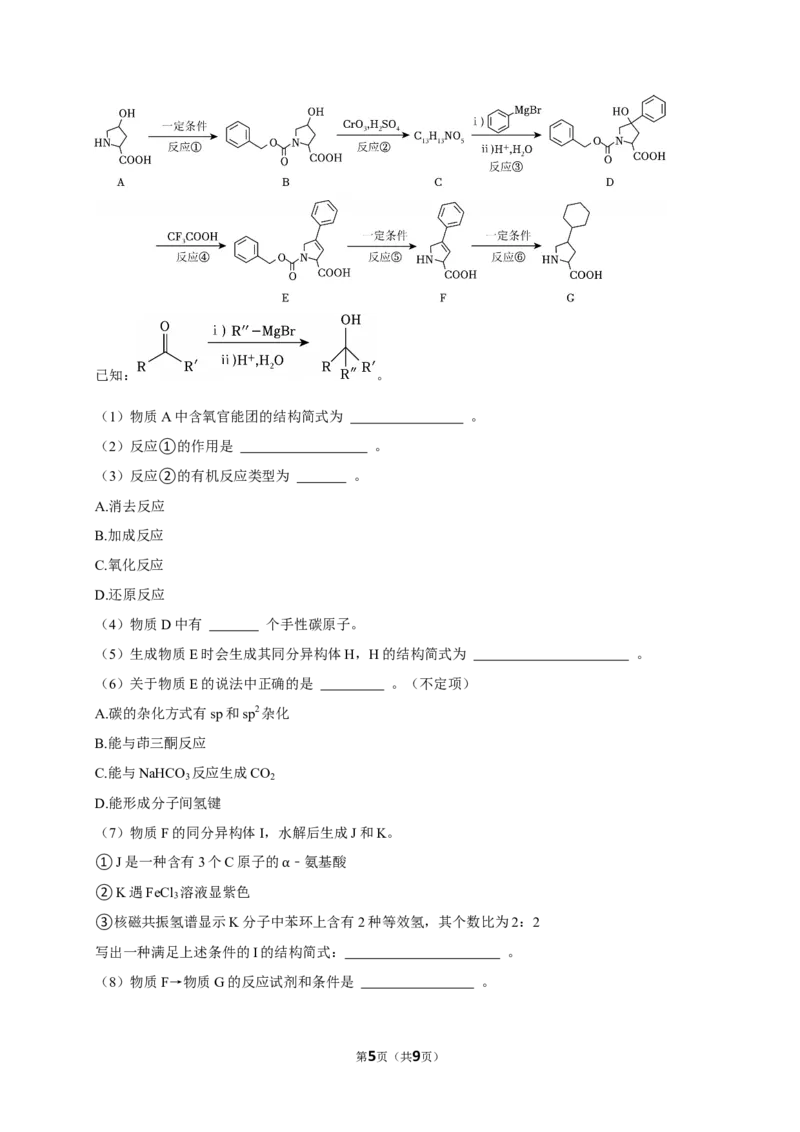
3 . ( 20 分 )
第4页(共9页)已知: 。
(1)物质A中含氧官能团的结构简式为 。
(2)反应①的作用是 。
(3)反应②的有机反应类型为 。
A.消去反应
B.加成反应
C.氧化反应
D.还原反应
(4)物质D中有 个手性碳原子。
(5)生成物质E时会生成其同分异构体H,H的结构简式为 。
(6)关于物质E的说法中正确的是 。(不定项)
A.碳的杂化方式有sp和sp2杂化
B.能与茚三酮反应
C.能与NaHCO 反应生成CO
3 2
D.能形成分子间氢键
(7)物质F的同分异构体I,水解后生成J和K。
①J是一种含有3个C原子的 ﹣氨基酸
②K遇FeCl 3 溶液显紫色 α
③核磁共振氢谱显示K分子中苯环上含有2种等效氢,其个数比为2:2
写出一种满足上述条件的I的结构简式: 。
(8)物质F→物质G的反应试剂和条件是 。
第5页(共9页)(9)结合信息,以HCHO和 为原料合成 。
(无机试剂任选)
四、锗的工业提取(20分)
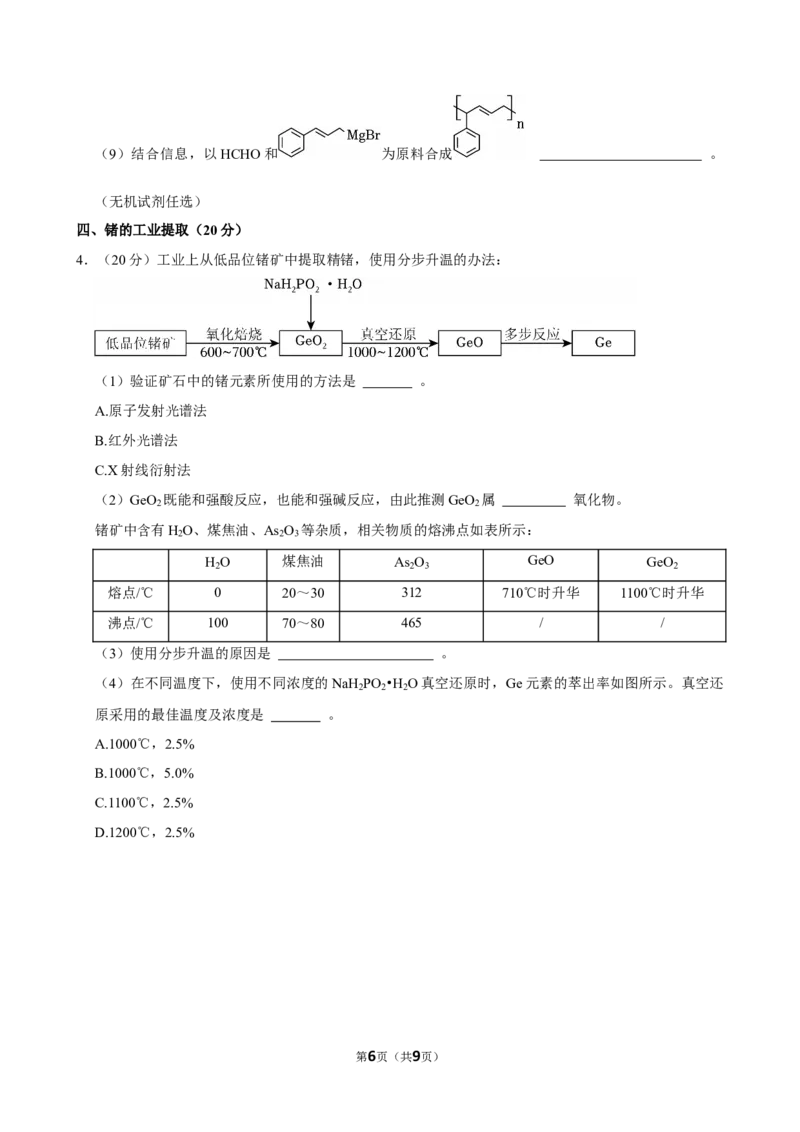
4.(20分)工业上从低品位锗矿中提取精锗,使用分步升温的办法:
(1)验证矿石中的锗元素所使用的方法是 。
A.原子发射光谱法
B.红外光谱法
C.X射线衍射法
(2)GeO 既能和强酸反应,也能和强碱反应,由此推测GeO 属 氧化物。
2 2
锗矿中含有H O、煤焦油、As O 等杂质,相关物质的熔沸点如表所示:
2 2 3
H O 煤焦油 As O GeO GeO
2 2 3 2
熔点/℃ 0 20~30 312 710℃时升华 1100℃时升华
沸点/℃ 100 70~80 465 / /
(3)使用分步升温的原因是 。
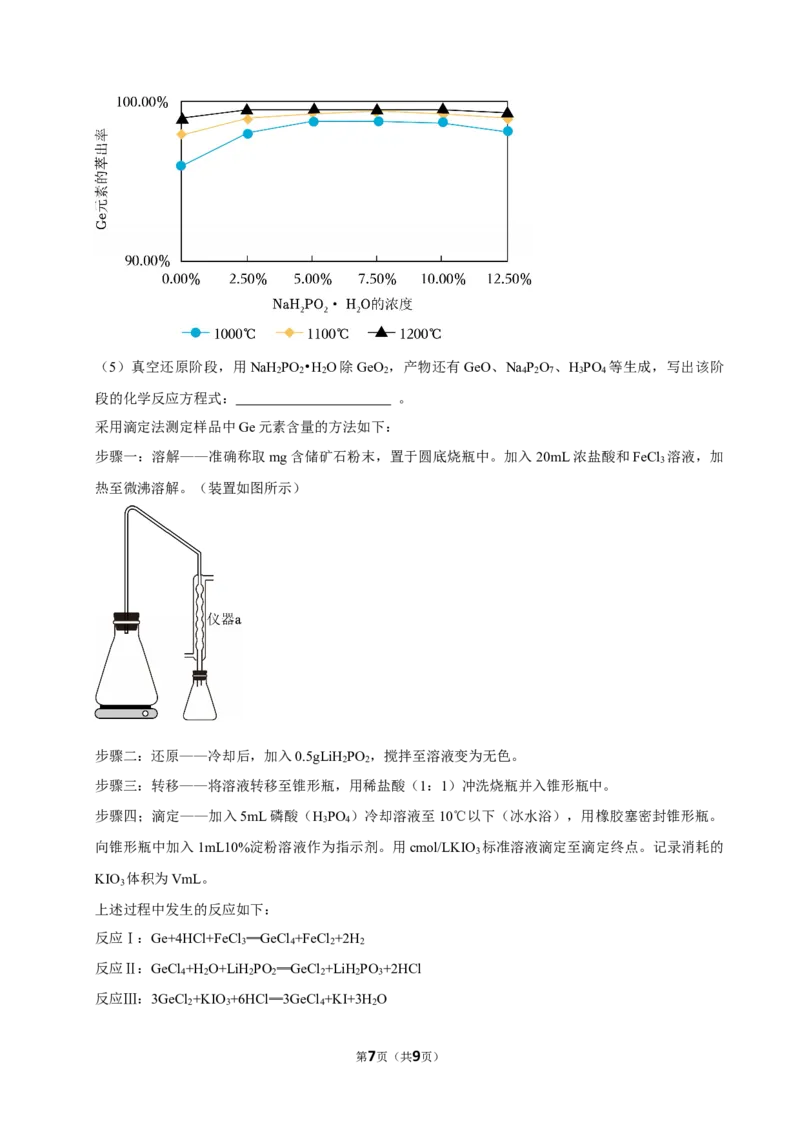
(4)在不同温度下,使用不同浓度的NaH PO •H O真空还原时,Ge元素的萃出率如图所示。真空还
2 2 2
原采用的最佳温度及浓度是 。
A.1000℃,2.5%
B.1000℃,5.0%
C.1100℃,2.5%
D.1200℃,2.5%
第6页(共9页)(5)真空还原阶段,用NaH PO •H O除GeO ,产物还有GeO、Na P O 、H PO 等生成,写出该阶
2 2 2 2 4 2 7 3 4
段的化学反应方程式: 。
采用滴定法测定样品中Ge元素含量的方法如下:
步骤一:溶解——准确称取mg含储矿石粉末,置于圆底烧瓶中。加入20mL浓盐酸和FeCl 溶液,加
3
热至微沸溶解。(装置如图所示)
步骤二:还原——冷却后,加入0.5gLiH PO ,搅拌至溶液变为无色。
2 2
步骤三:转移——将溶液转移至锥形瓶,用稀盐酸(1:1)冲洗烧瓶并入锥形瓶中。
步骤四;滴定——加入5mL磷酸(H PO )冷却溶液至10℃以下(冰水浴),用橡胶塞密封锥形瓶。
3 4
向锥形瓶中加入1mL10%淀粉溶液作为指示剂。用cmol/LKIO 标准溶液滴定至滴定终点。记录消耗的
3
KIO 体积为VmL。
3
上述过程中发生的反应如下:
反应Ⅰ:Ge+4HCl+FeCl ═GeCl +FeCl +2H
3 4 2 2
反应Ⅱ:GeCl +H O+LiH PO ═GeCl +LiH PO +2HCl
4 2 2 2 2 2 3
反应Ⅲ:3GeCl +KIO +6HCl═3GeCl +KI+3H O
2 3 4 2
第7页(共9页)反应Ⅳ:5KI+KIO +6HCl═3I +6KCl+3H O
3 2 2
(6)装置a的名称是 。
A.滴定管
B.恒压漏斗
C.冷凝管
D.蒸馏管
(7)到达滴定终点时,锥形瓶内液体的颜色由 色变 色,半分钟不改变。
(8)步骤四中滴定前,要用橡胶塞密封锥形瓶的原因是 。
(9)样品中Ge的质量分数 = 。(用含c、V、m的代数式表示)
(10)滴定结果偏大的可能原ω因是 。(不定项)
A.未用KIO 标准溶液润洗滴定管
3
B.未用HCl将样品从装置a中洗入锥形瓶
C.滴定结束后,在滴定管尖嘴处出现气泡
D.在室温下进行滴定
五、铁及其化合物(20分)
5.(20分)铁红是一种红色颜料。
(1)铁红的主要成分是 。
A.Fe S
2 3
B.Fe O
3 4
C.FeS
D.Fe O
2 3
(2)下列关于饱和FeCl 溶液的说法中正确的是 。
3
A.常温显中性
B.加铁粉变红褐色
C.遇沸水得到胶体
D.加氨水出现白色沉淀
(3)下列有关基态Fe的说法中正确的是 。(不定项)
A.电子处在4个不同能级
B.核外有5个未成对电子
C.核外电子占用15个原子轨道
D.核外有26种能量不同的电子
第8页(共9页)(4)混合铁粉和硫粉,在试管中加热,那么 。(不定项)
A.移开酒精灯后,固体仍保持红热
B.S作还原剂
C.主要的气体副产物是SO
3
D.最终得到黑色的Fe S
2 3
(5)配合物[Fe(SCN)(H O) ]Cl 内界为 ,配体有 种。
2 5 2
(6)在FeCl 溶液中存在平衡:Fe3+(aq)+xCl﹣(aq) [FeCl]3﹣x(aq)(x=1、2、3、4)。若加水
3
稀释溶液到原体积的两倍,则m(Fe3+) ;(⇌填“变大”、“不变”或“变小”)
请从浓度商Q、平衡常数K的大小关系角度解释原因 。
(7)已知Fe3+(aq)+xCl﹣(aq) [FeCl ]3﹣x(aq)的平衡常数K 如表所示。
x x
x 1 ⇌ 2 3 4
K 30.2 134.9 97.72 1.02
x
若 溶 液 中 [Cl﹣ ] = 12mol• L﹣ 1 , 则
= 。
(保留两位小数)
第9页(共9页)