文档内容
湖北省高中名校联盟 届高三第二次联合测评
2025
化学试卷参考答案与解析
一 选择题 本题共15小题 每小题3分 共45分
、 : , , 。
详解 越王勾践剑是春秋晚期青铜器 锡铜合金 正确 秦墓中出土的竹简 基本材料为
1.D 【 】A. ( ),A 。 B. ,
天然纤维素 正确 郧县直立人头骨化石 主要由硅酸盐构成 正确 东周彩漆二十八宿图衣
,B 。 C. , ,C 。 D.
箱为东周 战国早期 文物 所用的漆来源于天然漆树 综上所述 本题选
( ) , 。 , D。
详解 金属铍的金属性弱于镁并且与金属铝的性质相似 由此推测金属铍不能与水剧烈反应
2.A 【 】A. , ,
错误 聚四氟乙烯耐腐蚀耐高温 机械韧性好 正确 产生高温高压气体是推进剂的基本要
A 。 B. 、 ,B 。 C.
求 正确 钨 钼等金属是过渡元素 由元素周期律可知其熔点高 硬度大 正确 综上所述 本
,C 。 D. 、 , 、 ,D 。 ,
题选
A。
详解 氢碘酸属于强酸 电离方程式为 + - 错误 的 模型为四面
3.C 【 】A. , :HI H +I ,A 。 B.NCl3 VSEPR
体形 错误 过氧化氢电子式为 选项错误 综上所述 本题选
,B 。 D. :H O O H,D 。 , C。
详解 -中的共用电子对数目为 N 错误 为弱酸 在水溶液中会发生水解
4.D 【 】A.CN 3 A,A 。 B.HCN ,NaCN
导致 -的数目小于 N 错误 和 条件下 气体的体积约为
CN 0. 1 A,B 。 C. 25℃ 101 kPa ,1mol 24. 5L。
所含分子个数小于N 错误 综上所述 本题选
22.4 L Cl2 A,C 。 , B。
详解 产物应该是 错误 方程式未配平 应为 + -
5.C 【 】A. Fe3O4,A 。 B. , 2Na2O2+2H2O 4Na +4OH +
错误 氢氧化钠过量 产物为 - 正确 为弱酸 离子方程式中不应拆
O2↑,B 。 C. , [Al(OH)4] ,C 。 D.HClO ,
开 错误 综上所述 本题选
,D 。 , C。
详解 由图可知 为 为 为 为 为 为 为亚硝酸盐 以此解
6.A 【 】 ,a NH3,b N2H4,c N2,d NO,e NO2,f HNO3,g ,
题 催化氧化生成 得不到 错误 是 电子分子 正确 与水反应
。 A.NH3 NO, N2,A 。 B.N2H4 18 ,B 。 C.NO2
可得到 和 正确 亚硝酸钠是一种护色剂 可用于一些肉制品如腊肉 香肠等的生产
NO HNO3,C 。 D. , 、 。
综上所述 本题选
, A。
详解 氢氧化铁胶体可用于净水是因为胶体比表面积大 可吸附悬浮物质 错误
7.C 【 】A. , ,A 。 B. NaClO
溶液可用于杀菌消毒是因为可与空气中 反应产生强氧化性的 错误 乙酸的酸性弱于
CO2 HClO,B 。 C.
甲酸 是因为 是推电子基 推电子效应使羧基中羟基极性减小 正确 戊醇的水溶性弱于
, -CH3 , ,C 。 D.1-
乙醇 是因为疏水基团变大 错误 综上所述 本题选
, ,D 。 , C。
详解 该有机物结构简式含有腈基 羟基 碳碳双键 种官能团 正确 有机物 存在顺
8.C 【 】A. 、 、 3 ,A 。 B. M
反异构 正确 有机物 中腈基也可以被氢气加成 该物质最多可与 发生加成反
,B 。 C. M ,1 mol 6 mol H2
应 错误 有机物 中的腈基酸性条件下水解可得羧基 与酚羟基在一定条件下可以发生取代反
,C 。 D. M ,
应生成内酯 正确 综上所述 本题选
,D 。 , C。
化学试卷参考答案与解析 第 页 共 页
1 ( 6 )详解 导气管浸入液面之下使产生的气体无法导出并且应该用亚硫酸钠固体 不能达到相应
9.D 【 】A. ,A
实验目的 图示的装置中左侧小试管如果盛放氢氧化钠溶液会使收集到的乙酸乙酯发生水解而损
。 B.
失 不能达到相应实验目的 使用聚四氟乙烯活塞的滴定管为酸碱通用滴定管 可以达到相应
,B 。 D. ,D
实验目的 综上所述 本题选
。 , D。
详解 碘水和含铁离子的溶液均显黄色 无法证明是 2+先被氧化 不能得出相应结论
10.B 【 】A. , Fe ,A 。 B.
溴的四氯化碳溶液不能氧化乙醇 只会因为与丁烯发生加成反应而褪色 3+与 2-发生的是氧化
, 。 C.Fe S
还原反应 该现象证明的是羟基使苯环活化 不能得出相应结论 综上所述 本题选
。 D. ,D 。 , B。
详解 由题易知 分别为 据此作答 原子以 个 3 杂化轨道与配体
11.B 【 】 W、X、Y、Z Be、C、N、O, 。 A.Be 4 sp
-的氧原子形成 键 容纳 配体的孤电子对 正确 的第一电离能依次
CH3COO σ 、 NH3 ,A 。 B. Be、C、O、N
增大 错误 基态氧原子核外电子排布式为 2 2 4 核外电子占有 个原子轨道 故共有 种
,B 。 C. 1S 2S 2P , 5 , 5
不同的空间运动状态 正确 配体 的氮原子与中心原子 形成配位键 配体 -的端
,C 。 D. NH3 Be 、 CH3COO
氧与配体 的氢原子形成氢键 正确 综上所述 本题选
NH3 ,D 。 , B。
详解 红外光谱法可或得该分子中所含有的化学键或官能团的信息 错误 元素分析和
12.D 【 】A. ,A 。 B.
质谱法可确定该分子相对分子质量 错误 核磁共振氢谱法可获得该有机物分子中有几种不同
,B 。 C.
类型的氢原子以及它们的相对数目等信息 错误 射线衍射法可获得键长 键角等与分子结构
,C 。 D.X 、
有关的数据 正确 综上所述 本题选
,D 。 , D。
详解 根据均摊法则 一个晶胞中含有 个 个 由 化学式可知 代表氧离子
13.C 【 】A. , 8 Y,4 X。 CeO2 Y ,A
正确 位于 个 构成的正方体的体心 配位数为 正确 若 为晶胞的顶点 新晶胞中
。 B.X 8 Y , 8,B 。 C. Y (
位于所有的顶点 所有棱边的中心 所有面的面心 均摊后共有 个 新的晶胞其参数不变 故则一
Y 、 、 , 8 ), ,
个晶胞仍含有 个 错误 阿伏加德罗个晶胞中含有 其体积为 N a -9
4 X,C 。 D. 4×172 g CeO2, A×( ×10 ×
2 3 则 晶体的密度为4×172 21 -3 正确 综上所述 本题选
10 cm) , CeO2 a3 N ×10 g·cm ,D 。 , C。
× A
详解 该火星电池的放电反应为 放电时 正极反应为 +
14.B 【 】A. 3CO2+4Li=2Li2CO3+C。 , 3CO2+4Li +
- 正确 充电时 +向阴极迁移 错误 正极材料是碳纳米管负载二氧化
4e =2Li2CO3+C,A 。 B. ,Li ,B 。 C.
钌 碳纳米管有大的比表面积和空隙空间 二氧化钌是催化剂 正确 地球上的光合作用是
, , ,C 。 D. CO2
在叶绿体中氧化水生成氧气 电池放电时 做氧化剂氧化金属锂 正确 综上所述 本题选
, CO2 ,D 。 , B。
-3 -3
详解 由 点可知 的电离平衡常数K 10 ×10 -5 项正确 点所给的弱
15.C 【 】A. a HA a= =1.0×10 ,A 。 B.b
0.1
酸被滴定的百分数为 % 由电荷守恒和物料守恒可得 c - c - c c + 项正
50 。 2 (OH )+ (A )= (HA)+2 (H ),B
c + c -
确 点溶液的 K (H )· (A ) -5 将 c + -7 代入整理得 c -
。 C.c pH=7, a = c = 1. 0×10 , (H )= 10 (A )=
(HA)
c 项错误 点正好中和生成 水的电离受到促进 点水的电离刚好没有受到
100 (HA),C 。 D.d NaA, 。 c
影响 点弱酸 还未被滴定 其电离会抑制水的电离 点弱酸 被滴定了 % 但是溶液仍
。 a HA , 。 b HA 50 ,
显酸性 水的电离相比 点受抑制的程度稍小 点 过量 % 水的电离受的抑制比 点程度
, a 。 e NaOH 100 , a
更大 溶液中水的电离程度 项正确 综上所述 本题选
。 :d>c>b>a>e。 D 。 , C。
化学试卷参考答案与解析 第 页 共 页
2 ( 6 )二 非选择题 本题共4小题 共55分
、 : , 。
分
16.(14 )
四 分 分
(1) (1 ) VII B(1 )
分
(2)3Li2SO4+6NaOH+2H3PO4 2Li3PO4↓+6H2O+3Na2SO4(2 )
过滤 洗涤 干燥 分 无干燥操作仅得 分
(3) 、 、 (2 , 1 )
分 各 分
(4)Mn3(PO4)2、Fe3(PO4)2(2 , 1 )
使前驱体颗粒细化和分散 分
(5) (2 )
防止 2+ 2+被氧化 分
(6) Mn 、Fe (2 )
直接提高材料的导电性 分
(2 )
解析
【 】
元素位于元素周期表第四周期第 族
(1)Mn VII B 。
根据所给试剂 沉锂的过程是 三种溶液发生复分解反应 其反应的化学方
(2) , Li2SO4、6NaOH、2H3PO4 ,
程式为
3Li2SO4+6NaOH+2H3PO4 2Li3PO4↓+6H2O+3Na2SO4
(3)
前驱体
LiMn1- xFexPO4
的制备过程的原理是
Mn
2+
、Fe
2+在
Li3PO4
的表界面上发生溶解再沉淀的过
程 获得无水 前驱体则需要过滤 洗涤 干燥等过程
, LiMn1- xFexPO4 、 、 。
根据已知数据 和 的溶度积常数 K 远低于 溶液中的游离的 3-
(4) Fe3(PO4)2 Mn3(PO4)2 sp Li3PO4, PO4
更倾向于与 2+和 2+结合形成磷酸盐 随着 3- 的逐渐消耗 +和 3-的浓度乘积降至临界
Fe Mn 。 PO4 ,Li PO4
K 值以下 导致 的进一步溶解 这种 溶解 再沉淀 过程不断重复 直至 与
sp , Li3PO4 。 “ - ” , Me3(PO4)2
M
2+
(M=Fe,Mn)
之间达到平衡
,
最终与
Li3PO4
反应
,
形成
LiMn1- xFexPO4
材料
。
然而由于
Li3PO4
溶解
缓慢 在 尚未完全溶解的情况下 其表面易被 包覆形成包覆层 这一过程最终阻碍
, Li3PO4 , M3(PO4)2 ,
了 的彻底转化 抑制了前驱体材料的进一步形成
Li3PO4 , 。
球磨技术作为提高材料分散性的有效机械加工方法 通过球体与材料间的碰撞和摩擦作用 显著
(5) , ,
减少材料团聚现象 促进颗粒细化和分散 对于 前驱体材料 优化前驱体的分散性对
, 。 LiMn1- xFexPO4 ,
于实现与碳源的均匀混合至关重要 均匀且厚度适中的碳层结构有利于提高材料的导电性和锂离子
,
的迁移
。
原材料中涉及 2+ 2+易被氧化的离子 因此体系应保持惰性环境 通入 气和加入抗坏血酸
(6) Mn 、Fe , , Ar
的目的是排除反应体系中的空气
,
防止
Mn
2+
、Fe
2+被氧化
。 LiMn1- xFexPO4
材料由于电子电导率低和
锂离子扩散速率低的问题 解决此问题的有效方法是在材料表面构筑均匀地碳层 因此 采用葡萄糖
, , ,
作为碳源对材料进行改性的目的是提高材料的导电性
。
分
17.(13 )
还原反应 分
(1) (1 )
分
(2)16(1 )
化学试卷参考答案与解析 第 页 共 页
3 ( 6 )羰基 分
(3) (2 )
分 分 各 分
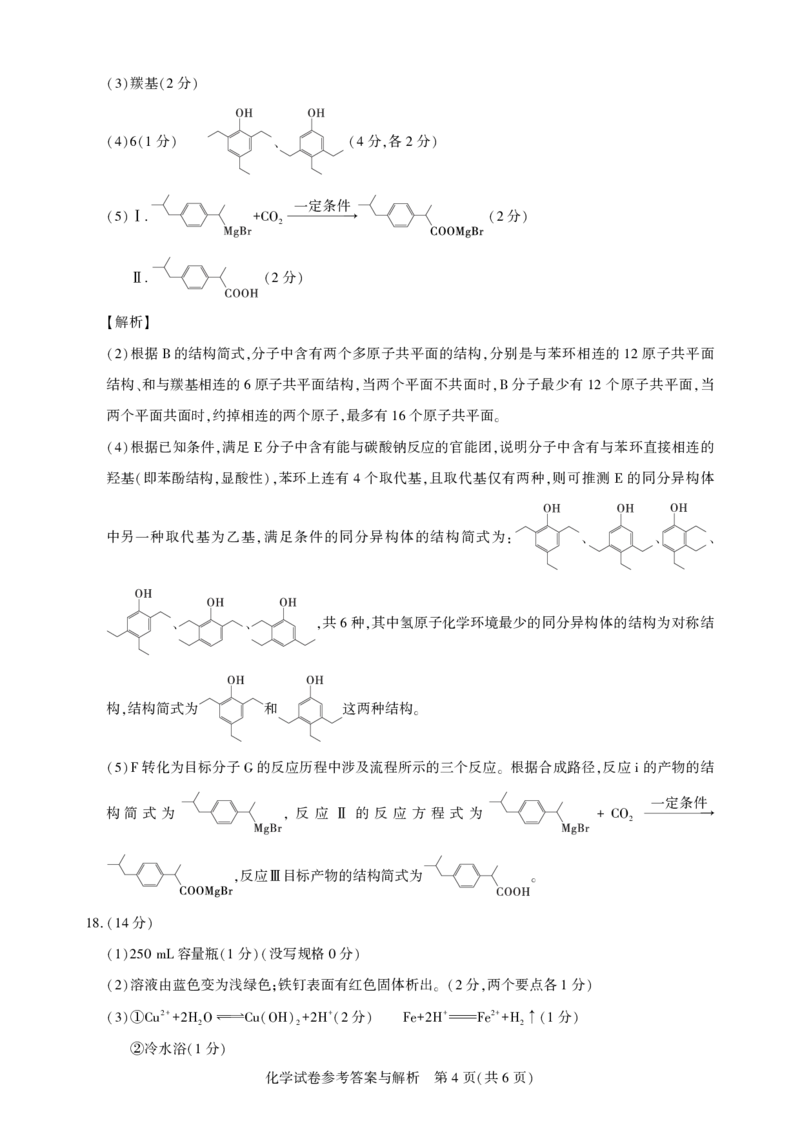
(4)6(1 ) 、 (4 , 2 )
一定条件
分
(5)Ⅰ. +CO2 → (2 )
分
Ⅱ. (2 )
解析
【 】
根据 的结构简式 分子中含有两个多原子共平面的结构 分别是与苯环相连的 原子共平面
(2) B , , 12
结构 和与羰基相连的 原子共平面结构 当两个平面不共面时 分子最少有 个原子共平面 当
、 6 , ,B 12 ,
两个平面共面时 约掉相连的两个原子 最多有 个原子共平面
, , 16 。
根据已知条件 满足 分子中含有能与碳酸钠反应的官能团 说明分子中含有与苯环直接相连的
(4) , E ,
羟基 即苯酚结构 显酸性 苯环上连有 个取代基 且取代基仅有两种 则可推测 的同分异构体
( , ), 4 , , E
中另一种取代基为乙基 满足条件的同分异构体的结构简式为
, : 、 、 、
共 种 其中氢原子化学环境最少的同分异构体的结构为对称结
、 、 , 6 ,
构 结构简式为 和 这两种结构
, 。
转化为目标分子 的反应历程中涉及流程所示的三个反应 根据合成路径 反应 的产物的结
(5)F G 。 , i
一定条件
构简 式 为 反 应 的 反 应 方 程 式 为
, Ⅱ + CO2 →
反应 目标产物的结构简式为
, Ⅲ 。
分
18.(14 )
容量瓶 分 没写规格 分
(1)250 mL (1 )( 0 )
溶液由蓝色变为浅绿色 铁钉表面有红色固体析出 分 两个要点各 分
(2) ; 。 (2 , 1 )
2+ + 分 + 2+ 分
(3)①Cu +2H2OCu(OH)2+2H (2 ) Fe+2H Fe +H2↑(1 )
冷水浴 分
② (1 )
化学试卷参考答案与解析 第 页 共 页
4 ( 6 )分 漏 个扣 分 漏 个或多选均给 分
③AD(2 , 1 1 , 2 0 )
2+ 胶体 + 分 没有写胶体或写沉淀符号给 分
④4Fe +O2+10H2O4Fe(OH)3( )+8H (2 , 1 )
玻璃搅拌器 分 分
(4) (1 ) -150.5(2 )
解析 与 溶液发生置换反应 预期实验现象为溶液由蓝色
【 】(2)Fe CuSO4 Fe+CuSO4 FeSO4+Cu,
水合铜离子 变为浅绿色 亚铁离子 铁钉表面有红色固体 铜单质 析出
( ) ( ); ( ) 。
为强酸弱碱盐 2+发生水解反应 2+ +使溶液呈酸性 出水
(3)①CuSO4 ,Cu Cu +2H2O Cu(OH)2+2H 。
解产生的 +与 2+发生竞争反应 + 2+ 释放出
H Cu Fe+2H Fe +H2↑ H2。
控制温度变量 需将试管放入冷水浴中反应 消除反应放热对水解的影响
② , , 。
乙同学用氧气含量传感器监测 发现反应过程中溶液气氧含量逐渐下降 说明硫酸铜溶液中确实存
③ , ,
在溶解氧气而且反应过程中被消耗 用激光笔照射取出反应完毕取出铁钉后的溶液 从侧面看到一条
; ,
光亮的通路 说明生成了胶体 该胶体只可能是 胶体 接着向试管中加入适量稀硫酸 振荡
, , Fe(OH)3 ; , ,
再滴入 溶液变红 或滴入苯酚溶液显紫色 结果均可证明有 3+存在
KSCN , , Fe 。
综合以上探究 溶液 下降的原因为氧气氧化了产生的亚铁离子生成铁离子 铁离子容易水解生
④ , pH ,
成了氢氧化铁胶体 并使溶液 下降 2+ 胶体 +
, pH :4Fe +O2+10H2O4Fe(OH)3( )+8H 。
计算反应热 比热容为 -3 -1 -1 注意热量单位转化为 溶液总质量为
(4) , 4.18×10 kJ∙g ∙℃ ( kJ), 1.0 g∙
-1 硫酸铜溶液过量 依据铁粉的量计算 铁粉为
mL ×100 mL=100 g, , , 0.01 mol。
H c m t n -3 -1 -1 -1
Δ =- ∙ ∙Δ / (Fe)= -4.18×10 kJ∙g ∙℃ ×100 g∙×3.6 ℃/0.01 mol=-150.5 kJ·mol 。
分
公众号:高中试卷君
19.(14 )
减 分 高温 低压 分 各 分
(1) (1 ) 、 (2 , 1 )
分
(2)①-90(1 )
a+b 分 4a 分
② (1 ) (2 )
2
2 b(3-3a-b)
分 写成 也给 分
③HCOO∗+H∗H2COO∗(2 , HCOO∗+5H∗H2COO∗+4H∗ 2 )
-4 -1 -1 分 无单位或数值算错均 分
(3)①3.0×10 mol·L ·min (1 , 0 )
% 分 分
②100 (1 ) 5(1 )
分
③8.5(2 )
解析
【 】
空气中 的化学捕获是 被溶液或固体物质反应而吸收 是熵减的反应 反应
(1) CO2 CO2 , 。 RNH2(s)+
H 是气体分子数减小的放热反应 根据平衡移动原理 在
CO2(g)+H2O(g)RNH3HCO3(s) Δ <0 , ,
干燥条件下加热并减小压强 有利于平衡逆移 使有机胺再生并释放出
, , CO2。
根据盖斯定律 故 H H H -1 -1 -1
(2)① ,Ⅲ=Ⅰ-Ⅱ, Δ 3=Δ 1-Δ 2=(-49 kJ·mol )-(+41 kJ·mol )=-90 kJ·mol 。
观察方程 水的物质的量等于 和 物质的量之和 n 故
② Ⅰ、Ⅱ: CH3OH CO 。 (H2O)= (a+b) mol,
化学试卷参考答案与解析 第 页 共 页
5 ( 6 )c -1 因为通入 和 达到平衡时 容器中 为a
(H2O)=(a+b)/2 mol·L 。 1 mol CO2 3 mol H2, , CH3OH mol,
为b 根据氢元素守恒 知n 故 c
CO mol,H2O(a+b)mol, , (H2)= 3-2a-(a+b)= 3-3a-b mol, (CH3OH)=
a/ -1 c b -1 c -1 代入反应 的平衡常数表达式
2 mol ·L , (CO)= /2 mol·L , (H2)=(3-3a-b)/2 mol·L , Ⅲ
中 得K 2
, =4a/[b(3-3a-b) ]。
第二步反应活化能最高 是决速步骤 其反应方程式为
③ , , HCOO∗+H∗==H2COO∗。
由反应 知
(3)① 2H2O2 2H2O+O2↑ :
v v -3 -1 -4 -1 -1
(O2)= (H2O2)/2=3.0×10 mol·L ÷5 min÷2=3.0×10 mol·L ·min 。
由 分子甲醛得到 分子的 二羟基丙酮 为加成反应 分子甲醛断开
② HCHO→DHA,3 1 1,3- (DHA), ,1
两个碳氢键分别加成另外两个甲醛分子的碳氧键形成两个羟甲基 故原子利用率为 % 环状葡萄
, 100 ;
糖中有 个碳原子 除不在环上的一个外 其余 个在六元环上的碳原子所连原子或原子团均各不相
6 , , 5
同 均为手性碳原子
, ;
本题考察合成效率的理解 从玉米合成淀粉的效率为 -4 -1 -1 的单位 合成效率
③ 。 1.548×10 mol·h ·g ,
的含义为每一克催化剂每小时生成的淀粉的物质的量 每个周期即 中每克催化剂能生产
。 4 h 5.28×
-3 淀粉 故人工合成效率为 -3 -1 -1 自然界中玉米合成淀粉的效率为
10 mol , 5. 28×10 ÷4 mol·h ·g ;
-4 -1 -1 该方法生产淀粉的效率是玉米的 -3 -4 倍
1.548×10 mol·h ·g , (5.28×10 ÷4)÷(1.548×10 )= 8.5 。
化学试卷参考答案与解析 第 页 共 页
6 ( 6 )