文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
专题八 计算题——中考二轮专题达标训练
1.某校学习小组的同学为了测定某大理石中碳酸钙的质量分数,将10 g该大理石样品加入烧
杯中,再把80 g稀盐酸分四次加入烧杯中,实验过程所得数据如表(已知大理石样品中含有
的杂质既不溶于水,也不与稀盐酸反应)。
实验次数 第1次 第2次 第3次 第4次
加入稀盐酸的质量/g 20 20 20 20
剩余固体的质量/g 7 4 2.6 m
分析表中数据,完成下列问题。
(1)表中m的数值为_________。
(2)该大理石样品中碳酸钙的质量分数为_________。
(3)计算第一次实验结束后所得溶液中溶质质量分数(计算结果精确到0.1%)。
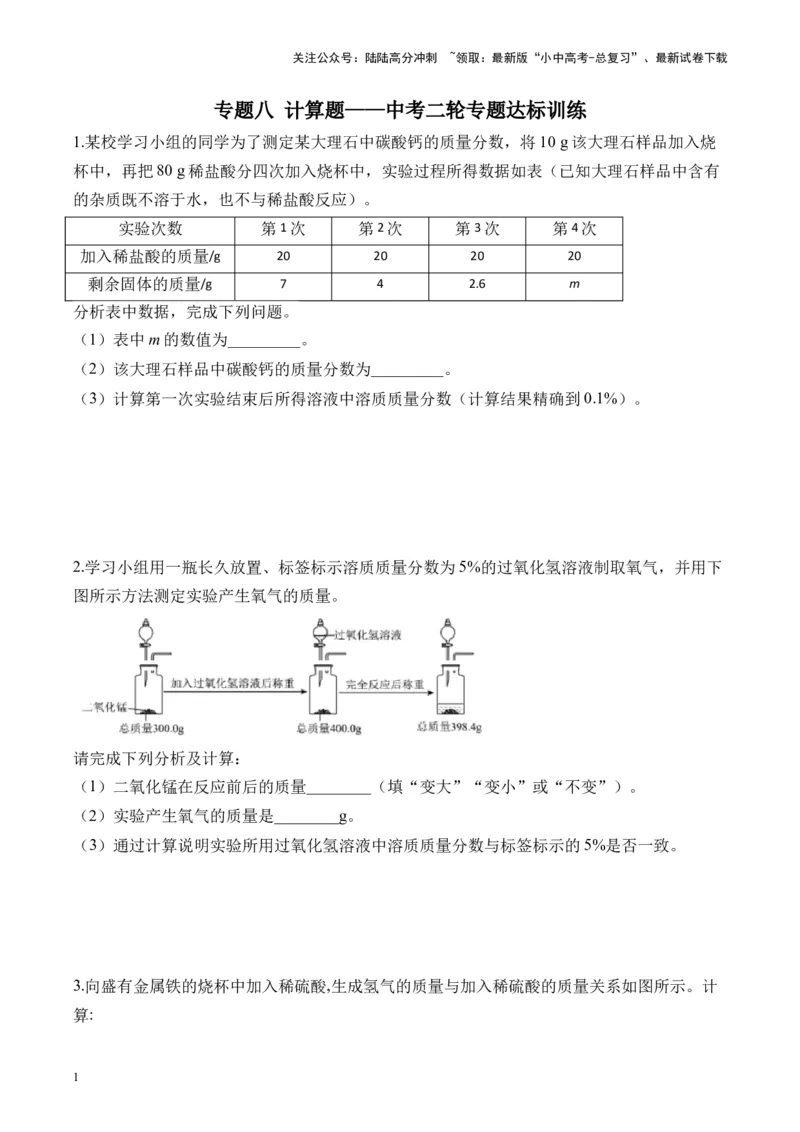
2.学习小组用一瓶长久放置、标签标示溶质质量分数为5%的过氧化氢溶液制取氧气,并用下
图所示方法测定实验产生氧气的质量。
请完成下列分析及计算:
(1)二氧化锰在反应前后的质量________(填“变大”“变小”或“不变”)。
(2)实验产生氧气的质量是________g。
(3)通过计算说明实验所用过氧化氢溶液中溶质质量分数与标签标示的5%是否一致。
3.向盛有金属铁的烧杯中加入稀硫酸,生成氢气的质量与加入稀硫酸的质量关系如图所示。计
算:
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)充分反应后生成氢气的质量是_______g。
(2)稀硫酸中溶质的质量分数。
(提示:铁和稀硫酸反应的化学方程式为 )
4.工业上,煅烧大理石可以制取生石灰和二氧化碳( )。请你计算煅
烧含碳酸钙50t的大理石可以制得氧化钙和二氧化碳的质量是多少?
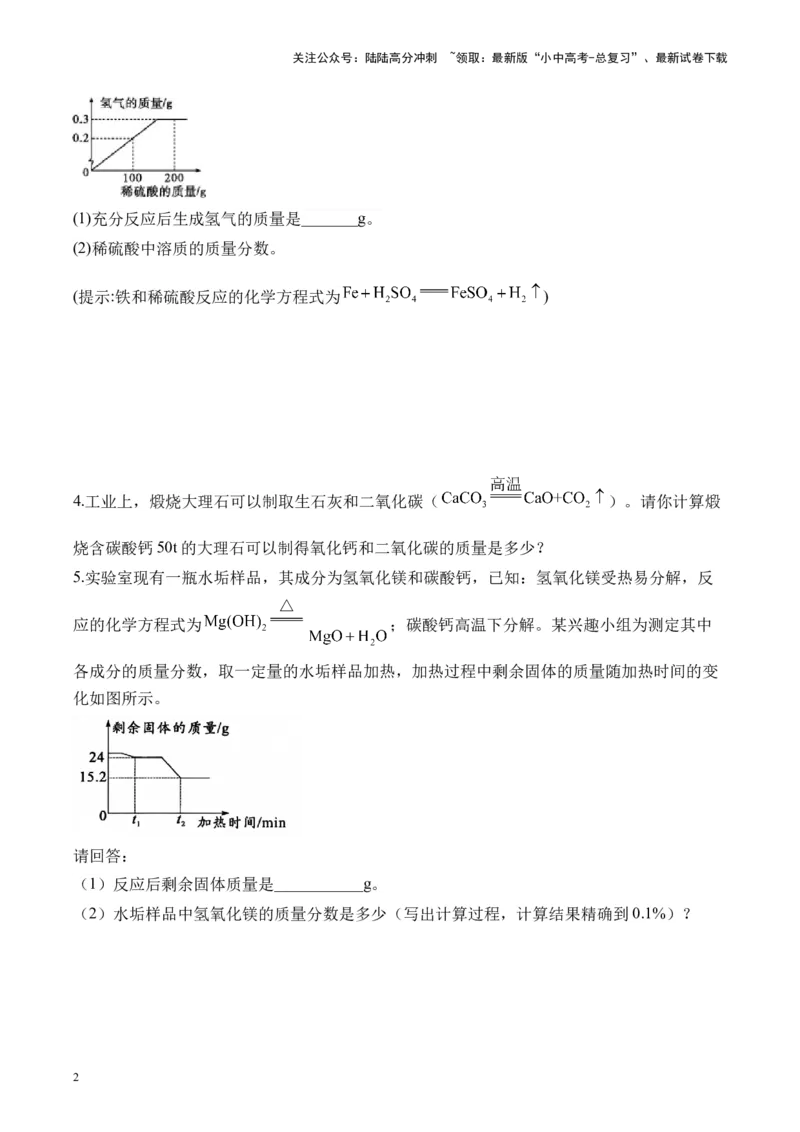
5.实验室现有一瓶水垢样品,其成分为氢氧化镁和碳酸钙,已知:氢氧化镁受热易分解,反
应的化学方程式为 ;碳酸钙高温下分解。某兴趣小组为测定其中
各成分的质量分数,取一定量的水垢样品加热,加热过程中剩余固体的质量随加热时间的变
化如图所示。
请回答:
(1)反应后剩余固体质量是___________g。
(2)水垢样品中氢氧化镁的质量分数是多少(写出计算过程,计算结果精确到0.1%)?
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
6.回答下列问题。
(1)为测定某胃药中碳酸氢钠的含量,向一锥形瓶中加入10 g该胃药,再逐渐加入一定溶
质质量分数的稀盐酸,当观察到_______时,说明碳酸氢钠已完全反应。此时消耗稀盐酸的质
量是50 g,测得锥形瓶内剩余物质质量是55.6 g(假设胃药中的其他成分不参与反应,不考
虑稀盐酸挥发,反应产生的气体全部逸出)。
(2)完全反应后,产生的二氧化碳的质量为_______g。
(3)计算该胃药中碳酸氢钠的质量分数(写出计算过程)。
7. 和 的固体混合物10g做如下实验。请根据图中实验及数据进行计算。
(1)计算混合物中 的质量(写出计算过程)。
(2)计算溶液B中 的质量分数(写出计算过程)。
(3)要配制与溶液B相同质量分数的 溶液200g,需要质量分数为24.4%的NaCl溶液的
质量是多少?(写出计算过程)
8.中华民族的发明创造为人类文明进步作出了巨大贡献。西汉时期的《淮南万毕术》中有
“曾青得铁则化为铜”之说,东汉的《神农本草经》、晋代的《抱朴子内篇》中也都有类似
的记载,同学们在实验室根据上述原理制取铜:取足量的硫酸铜溶液于烧杯中,向其中加入
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
5.6g铁,充分反应,计算可制得钢粉的质量?
9.实验室有一瓶含杂质的高锰酸钾,兴趣小组同学取10g该药品放入大试管中加热(杂质不
参加反应),并在不同时刻测定试管内剩余固体物质的质量,实验数据记录如下,请回答:
加热时间/min
剩余固体质量/g 10 10 9.24 9.16 9.04 9.04
(1)加热到 min时,_________(填“是”或“否”)完全反应。
(2)完全反应后,生成氧气的质量为_________g。
(3)计算10g药品中高锰酸钾的质量。
10.工业上可利用 的反应来冶炼铁。现用100t含四氧化三铁为
46.4%的某铁矿石冶炼金属铁。请完成下列问题,写出必要的计算过程。
(1)该铁矿石中含四氧化三铁的质量是多少?
(2)理论上可炼出含铁96%的生铁的质量是多少?
11.氢气作为燃料具有热值高、无污染的优点。某化学社团的同学们用20g废旧黄铜(铜锌合
金)和100g稀硫酸反应制取氢气(如图1),二者恰好完全反应,天平的示数随时间的变化
如图2(仪器质量不计算在内)。请计算。
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)生成氢气的质量为________g。
(2)该20g废旧黄铜中锌的质量分数。(写出计算过程)
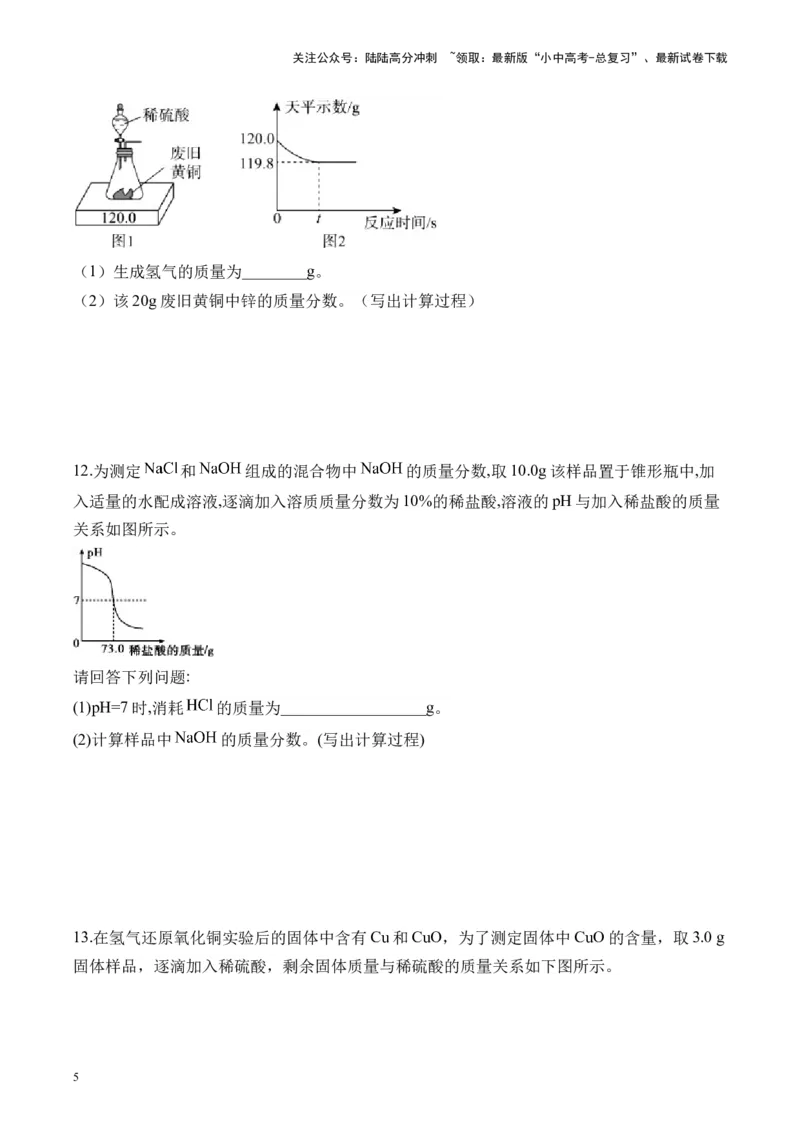
12.为测定 和 组成的混合物中 的质量分数,取10.0g该样品置于锥形瓶中,加
入适量的水配成溶液,逐滴加入溶质质量分数为10%的稀盐酸,溶液的pH与加入稀盐酸的质量
关系如图所示。
请回答下列问题:
(1)pH=7时,消耗 的质量为__________________g。
(2)计算样品中 的质量分数。(写出计算过程)
13.在氢气还原氧化铜实验后的固体中含有Cu和CuO,为了测定固体中CuO的含量,取3.0 g
固体样品,逐滴加入稀硫酸,剩余固体质量与稀硫酸的质量关系如下图所示。
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
已知: 。
(1)固体样品中CuO的质量为________g。
(2)固体样品与稀硫酸恰好完全反应时所得溶液的溶质质量分数为多少(写出计算过程)?
14.为测定某硫酸溶液的溶质质量分数,某实验小组设计了以下方案:在烧杯中加入该硫酸溶
液100 g,然后向烧杯中逐滴加入氢氧化钡溶液,滴加的氢氧化钡溶液质量与生成沉淀的质量
关系如图所示。请你帮其解决下列问题:
(1)恰好完全反应时,生成沉淀的质量为_______g。
(2)求该硫酸溶液中溶质的质量分数。(写出计算过程)
15.某化学实验小组为测定碳酸钾和氯化钾的固体混合物组成情况,同学们取20g固体混合物,
加入90g水使固体混合物全部溶解,再向该溶液中加入111g溶质质量分数为10%的氯化钙溶
液,恰好完全反应形成不饱和溶液。请计算下列问题:
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)固体混合物中碳酸钾的质量。
(2)恰好完全反应后所得溶液的溶质质量分数。
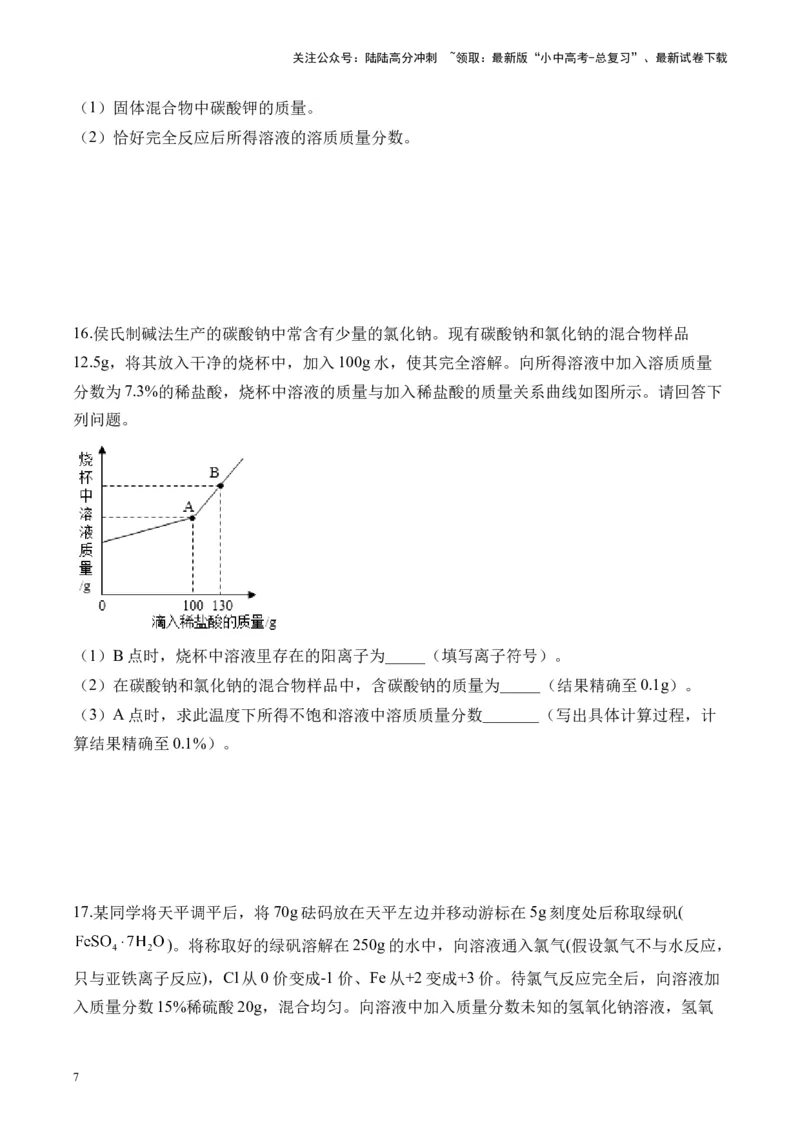
16.侯氏制碱法生产的碳酸钠中常含有少量的氯化钠。现有碳酸钠和氯化钠的混合物样品
12.5g,将其放入干净的烧杯中,加入100g水,使其完全溶解。向所得溶液中加入溶质质量
分数为7.3%的稀盐酸,烧杯中溶液的质量与加入稀盐酸的质量关系曲线如图所示。请回答下
列问题。
(1)B点时,烧杯中溶液里存在的阳离子为_____(填写离子符号)。
(2)在碳酸钠和氯化钠的混合物样品中,含碳酸钠的质量为_____(结果精确至0.1g)。
(3)A点时,求此温度下所得不饱和溶液中溶质质量分数_______(写出具体计算过程,计
算结果精确至0.1%)。
17.某同学将天平调平后,将70g砝码放在天平左边并移动游标在5g刻度处后称取绿矾(
)。将称取好的绿矾溶解在250g的水中,向溶液通入氯气(假设氯气不与水反应,
只与亚铁离子反应),Cl从0价变成-1价、Fe从+2变成+3价。待氯气反应完全后,向溶液加
入质量分数15%稀硫酸20g,混合均匀。向溶液中加入质量分数未知的氢氧化钠溶液,氢氧
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
化钠溶液的质量与沉淀物质量的关系图如图所示。
(1)溶液中通入氯气且氯气反应完全后,求氯化铁的质量分数。
(2)求x、y的值。
18.某课外兴趣小组在实验室发现了一瓶含杂质的熟石灰粉末(杂质不溶于水也不与稀盐酸反
应),为探究熟石灰的变质程度他们取六份样品,分别加稀盐酸反应测得部分数据如下,请
根据有关信息回答问题。
实验次数 1 3 4 5 6
取样品质量(g) 25.0 25.0 25.0 25.0 25.0
取稀盐酸质量(g) 50.0 120.0 140.0 160.0 205.0
产生气体质量(g) 0 a 2.2 3.3 4.4
(1)a的数值为______。
(2)第6次实验,所得溶液中溶质的化学式为______。
(3)计算25克样品中碳酸钙的质量分数______。
(4)列式计算所用盐酸的溶质质量分数(保留到0.1%)(写出解题过程)
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
19.取 和 的混合物 于烧杯中,向其中加入 一定溶质质量分数的稀盐酸,
恰好完全反应,反应后称得烧杯中溶液的质量为216.2g。请计算:
(1)混合物中 的质量分数。
(2)恰好完全反应时,所得溶液中溶质的质量分数(计算结果精确到 )。
20.请根据所示的实验过程和提供的信息作答:
(1)实验结束后溶液中的溶质为______。
(2)实验所用 溶液的溶质质量分数为______(精确至0.1%)。
(3)计算原混合液中 的质量分数。(写出计算过程,精确至0.1%)
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
答案以及解析
1.答案:(1)2.6
(2)74%
(3)解:设第一次实验中生成 的质量为x,生成 的质量为y。
所得溶液溶质质量分数为 。
答:第一次实验结束后所得溶液中溶质质量分数约为5.4%。
解析:(1)由第1、2次实验数据可知,20 g稀盐酸和3 g碳酸钙恰好完全反应,而第3次加
入20g稀盐酸,与其反应的碳酸钙的质量为4 g-2.6 g=1.4 g<3 g,说明碳酸钙已完全反应,剩
余的杂质是2.6 g,所以m的值为2.6。
(2)该石灰石样品中 的质量分数为 。
2.答案:(1)不变
(2)1.6
(3)解:设残疾反应的过氧化氢的质量为x,
x=3.4g
则实验所用过氧化氢溶液中溶质质量分数为 ≠5%,
答:实验所用过氧化氢溶液中溶质质量分数与标签标示的5%不一致。
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
解析:(1)过氧化氢在二氧化锰的催化下分解生成氧气和水,二氧化锰作为该反应的催化剂,
在反应前后质量不变;
(2)根据质量守恒定律,实验产生氧气的质量是400.0g-398.4g=1.6g;
(3)见答案。
3.答案:(1)0.3
(2)9.8%
解析:
(2)解:设产生0.2g氢气,需要硫酸的质量为x。
98 x
2 0.2g
x9.8g
9.8g
稀硫酸中溶质的质量分数为 100%9.8%
100g
答:稀硫酸中溶质的质量分数为9.8%。
4.答案:22t
解析:设可制得氧化钙和二氧化碳的质量分别为x、y,
答:煅烧含碳酸钙50t的大理石可以制得氧化钙的质量为28t,二氧化碳的质量是22t。
5.答案:(1)15.2
(2)解:反应后产生 的质量为
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
设水垢样品中 的质量为x。
反应中生成MgO的质量为
设水垢样品中 的质量为y。
水垢样品中 的质量分数为
答:水垢样品中 的质量分数约为 。
6.答案:(1)不再产生气泡
(2)4.4
(3)解:设10 g该胃药中碳酸氢钠的质量为x。
该胃药中碳酸氢钠的质量分数为 。
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
答:该胃药中 的质量分数为84%
解析:(1)碳酸氢钠与稀盐酸反应能产生二氧化碳,向一锥形瓶中加入10 g该胃药,再逐
渐加入一定溶质质量分数的稀盐酸,当观察到不再产生气泡时,说明碳酸氢钠已完全反应。
(2)由质量守恒定律可知,完全反应后,产生的二氧化碳的质量为10 g+50 g-55.6 g=4.4 g。
7.答案:(1)9.5g
(2)6.1%
(3)50g
解析:(1)设混合物中MgCl 的质量是x,反应生成氯化钠质量是y。
2
MgCl 2NaOH Mg(OH) 2NaCl
2 2
95 58 117
x 5.8g y
答:混合物中 的质量是9.5g。
(2)混合物中氯化钠质量是10g-9.5g=0.5g,溶液B中氯化钠质量是11.7g+0.5g=12.2g,
的质量分数是 。
(3)设要配制与溶液B相同质量分数的 溶液200g,需要质量分数为24.4%的 溶液
的质量是z,根据题意有24.4%x=12.2g,z=50g。
8.答案:6.4g
解析:设可制得铜粉的质量为x。
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
答:可制得铜粉的质量为6.4g。
9.答案:(1)是
(2)0.96
(3)9.48g
解析:(1)加热到 min时,剩余固体的质量不再减少,说明已完全反应。
(2)由表中的数据和质量守恒定律可知,生成氧气的质量为10g-9.04g=0.96g。
(3)设10g药品中高锰酸钾的质量为x。
答:10g药品中高锰酸钾的质量为9.48g。
10.答案:(1)该铁矿石中含四氧化三铁的质量是100t×46.4%=46.4t。
答:该铁矿石中含四氧化三铁的质量是46.4t。
(2)解:设理论上可炼出含铁96%的生铁的质量是x。
答:理论上可炼出含铁96%的生铁的质量是35 t。
11.答案:(1)0.2
(2)32.5%
解析:
(2)解:设废旧黄铜中锌的质量为x。
14关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
此样品中碳酸钙的质量分数为:
答:此样品中碳酸钙的质量分数为32.5%。
12.答案:(1)7.3
(2)80%
解析:(1)恰好完全反应时,溶液显中性,溶液的pH=7,则消耗稀盐酸中溶质的质量为
73.0g×10%=7.3g。
(2)解:设参加反应的氢氧化钠的质量为x。
样品中 的质量分数为
答:样品中 的质量分数为80%。
13.答案:(1)0.8
(2)解:设反应生成的硫酸铜质量为x。
CuOH SO CuSO H O
2 4 4 2
80 160
0.8g x
80 0.8g
160 x
x=1.6 g
15关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
1.6g
100%16%
固体样品与稀硫酸恰好完全反应时所得溶液的溶质质量分数为
0.8g9.2g
答:固体样品与稀硫酸恰好完全反应时所得溶液的溶质质量分数为16%。
14.答案:(1)23.3
(2)9.8%
解析:
(2)解:设该硫酸溶液中溶质的质量为x。
该硫酸溶液中溶质的质量分数为
答:该硫酸溶液中溶质的质量分数为9.8%。
15.答案:(1)13.8g
(2)10%
解析:(1)解:设固体混合物中碳酸钾的质量为x,则
111 111g10%
138 x
答:固体混合物中碳酸钾的质量为13.8g。
(2)解:设产生的碳酸钙沉淀的质量为y,则
CaCl + K CO CaCO + 2KCl
2 2 3 3
111 100
111g10% y
16关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
则所得溶液的溶质质量为
所得溶液的质量为
21.1g
所得溶液的溶质质量分数为 100%10%
211g
答:恰好完全反应后所得溶液的溶质质量分数为10%。
16.答案:(1) 、
(2)10.6g
(3)6.5%
解析:(1)由图可知,当滴入稀盐酸至B点时,加入的稀盐酸过量。烧杯中溶液里的溶质为
、 ,故存在的阳离子为 、 ;
(2)由图可知,当滴入稀盐酸至A点时,加入的稀盐酸恰好与碳酸钠完全反应。设样品中
碳酸钠的质量为x,生成氯化钠的质量为y,二氧化碳的质量为z。
x=10.6g
y=11.7g
z=4.4g
(3)当滴入稀盐酸至A点时,所得不饱和溶液中溶质质量为12.5g+11.7g-10.6g=13.6g;所得
不饱和溶液中溶质质量为100g+12.5g+100g-4.4g=208.1g;所得不饱和溶液中溶质质量分数为
。
17.答案:(1)39.2%
(2)124.5;25
解析:(1)砝码与药品位置放反了,则绿矾的质量为70g-5g=65g,绿矾中硫酸亚铁的质量为
17关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
152
65g× ×100%≈35.54g;
278
设参加反应的氯气质量为m,生成氯化铁的质量为n,
6FeSO 3Cl 2FeCl 2Fe SO
4 2 3 2 4 3
912 213 325
35.54g m n
912 35.54g 912 35.54g
,
213 m 325 n
,
溶液中通入氯气且氯气反应完全后,氯化铁的质量分数为 ×100%≈39.2%;
(2)解:加入氢氧化钠溶液,氢氧化钠先与硫酸反应,再与氯化铁、硫酸铁反应生成氢氧化
铁沉淀,设氢氧化钠溶液中溶质的质量分数为z,
由反应的化学方程式6FeSO +3Cl =2FeCl +2Fe (SO ) 、FeCl +3NaOH=Fe(OH) ↓+3NaCl、
4 2 3 2 4 3 3 3
Fe (SO ) +6NaOH=2Fe(OH) ↓+3Na SO ,可得出关系式FeSO ~3NaOH~Fe(OH)
2 4 3 3 2 4 4 3
答:氯化铁的质量分数为39.2%;x、y的值124.5、25。
18.答案:(1)1.1
(2) 和
18关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(3)40.0%
(4)3.4%
解析:变质的氢氧化钙中常含有碳酸钙,加入稀盐酸时,稀盐酸与氢氧化钙反应生成氯化钙
和水,氢氧化钙完全反应后,稀盐酸再与碳酸钙反应生成二氧化碳气体。由表中的数据可知,
每20g的稀盐酸完全反应生成二氧化碳的质量为1.1g,由此可知a的值为1.1g;第6次加入
45g的稀盐酸生成二氧化碳的质量为1.1q,说明了盐酸有剩余,25g的样品完全反应生成二氧
化碳的总质量为4.4g。
(1)由上述分析可知,a的数值为1.1。
(2)第6次实验,盐酸有剩余,所得溶液中溶质的化学式为: 和 。
(3)解:设25克样品中碳酸钙的质量为x
故碳酸钙的质量分数为:
答:25克样品中碳酸钙的质量分数为40.0%。
(4)解:生成3.3g气体所需的盐酸的质量为y,则
故所用盐酸的溶质质量分数为:
答:所用盐酸的溶质质量分数为3.4%。
19.答案:(1)80%
(2)12.6%
19关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
解析:(1)解:设混合物中CaCO 的质量为x,反应后生成CaCl 的质量为y
3 2
由题目可知生成二氧化碳的质量为200g25g216.2g 8.8g
CaCO 2HCl CaCl H OCO
3 2 2 2
100 111 44
x y 8.8g
100 x 111 y
= , =
44 8.8g 44 8.8g
解得
混合物中 的质量分数:
(2)恰好完全反应时,所得溶液中溶质的质量分数
答:混合物中碳酸钙的质量分数为 80%,恰好完全反应后所得氯化钙的溶质质量分数为
12.6%。
20.答案:(1)氯化钾、碳酸钾( 、 )
(2)13.8%
(3)11.1%
解析:(1)第一次加入50g碳酸钾,生成了2.5g沉淀,说明混合液中稀盐酸已经被完全反应,
接着第二次加入50g碳酸钾,生成了7.5g-2.5g=5g沉淀,说明每50g碳酸钾能够生成5g沉淀,
那么按照理论,再次加入30g碳酸钾能够生成了3g沉淀,但实验数据只生成了10g-7.5g=2.5g
沉淀,说明混合液中氯化钙已经被完全反应,且碳酸钾过量,所以实验结束后溶液中的溶质
为氯化钾(碳酸钾和氯化钙反应生成碳酸钙沉淀和氯化钾,稀盐酸与碳酸钾反应生成氯化钾、
水和二氧化碳)和过量的碳酸钾。
(2)设:实验所用 溶液的溶质质量为y。
20关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
答:实验所用 溶液的溶质质量分数为13.8%。
(3)设原混合液中 的质量为x。
原混合液中 的质量分数为: 。
答:原混合液中CaCl 的质量分数为11.1%。
2
21关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
22