文档内容
雅礼中学 2025 届高三月考试卷(二)
化学
命题人:吴建新 审题人:刘思朋
本试题卷分选择题和非选择题两部分,共8页。时量75分钟,满分100分。
可能用到的相对原子质量:
H~1 C~12 N~14 O~16 Na~23 S~32 Cl~35.5 K~39 Fe~56 Br~80 Ba~137
第Ⅰ卷(选择题共42分)
一、选择题(本题共14小题,每小题3分,共42分,每小题只有一个选项符合题意。)
1.人类生活品质的提升离不开科技的进步。下列说法正确的是( )
A.作为纳米荧光材料的碳量子点属于胶体
B.食品脱氧剂使用后,其中的铁粉转化成
C.“大数据中心”的电子设备芯片使用的材料是二氧化硅
D.环型碳 、环型碳 和金刚石均是碳元素的同素异形体
2.下列说法不正确的是( )
A. 和 分别与Fe反应生成 和
B.分别向 溶液和饱和 溶液中通入过量的 ,均可析出白色沉淀
C.新制氯水和浓硝酸在光照下可产生同种气体
D.将等物质的量的Al和Si分别加入足量NaOH溶液中,生成气体的物质的量之比为4∶3
3.下列方程式与所给事实不相符的是( )
A.工业上海水提溴常用 作氧化剂:
B.铝粉和氧化铁组成的铝热剂用于焊接钢轨:
C.在稀硝酸中加入过量的铁粉: (稀)
D.用石灰乳吸收泄漏的氯气:
4.硫及其化合物部分转化关系如图。设 为阿伏加德罗常数的值,下列说法正确的是( )
A.标准状况下,11.2 L 中原子总数为B.100 mL 0.1 mol⋅L 溶液中, 数目为
C.反应①每消耗3.4 g ,生成物中硫原子数目为
D.反应②每生成1 mol还原产物,转移电子数目为
5.实验是探究元素化合物性质的重要方法。利用下列实验装置和试剂能实现相应元素不同价态间转化的
是( )
试剂
选项 元素不同价态间的转化
a b c
A 70%硫酸 亚硫酸钠 新制氯水
B 稀硫酸 硫化亚铁 氯化铁溶液
C 浓硝酸 铜片 水
D 浓盐酸 高锰酸钾 溴化钾溶液
6.某溶液只含有 , , , 、 、 和 中的几种。取该溶液100 mL,加入过
量NaOH溶液,加热,得到0.02 mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到 1.6 g固体;
向上述滤液中加入足量 溶液,得到4.66 g不溶于盐酸的沉淀。由此可知原溶液中( )
A.至少存在5种上述离子
B. 一定存在,且 mol⋅L
C. , 一定存在, 可能不存在
D. 、 一定不存在, 可能存在
7.为达到实验目的,下列对应的实验方法正确或实验操作规范的是( )
选项 实验目的 实验方法或操作
称取1.4625 g NaCl置于250 mL容量瓶中,加水至刻
A 配制250 mL 0.1000 mol·L NaCl溶液
度线
向某稀溶液中加入NaOH溶液,能产生使湿润的蓝色
B
检验溶液中含有 石蕊试纸变红的气体向4 mL 0.1 mol·L KI溶液中滴加1 mL新制的氯
C 探究Cl和Ⅰ的非金属性强弱 水,振荡,若溶液变成棕黄色,则Cl的非金属性强
于I
D 验证 具有氧化性 向少量酸性 溶液中滴加少量 溶液,再
滴加2滴KSCN溶液
8.钧瓷是宋代五大名瓷之一,其中红色钧瓷的发色剂为 。为探究 的性质,取少许等量
分别加入甲、乙两支试管,进行如下实验。下列说法不正确的是( )
实验操作及现象
试管甲 滴加过量0.3 mol·L 溶液并充分振荡,砖红色沉淀转化为另一颜色沉淀,溶液显浅
蓝色;倾倒溶液,滴加浓硝酸,沉淀逐渐消失
滴加过量6 mol·L 氨水并充分振荡,沉淀逐渐溶解,溶液颜色为无色;静置一段时间
试管乙
后,溶液颜色变为深蓝色
A.试管甲中新生成的沉淀为金属Cu
B.试管甲中沉淀的变化说明过程中浓、稀硝酸的作用不一样
C.试管乙实验可证明Cu(Ⅰ)与 形成无色配合物
D.上述两个实验表明 为两性氧化物
9.高铁酸钠( )是一种新型绿色消毒剂,主要用于饮用水处理。某化学兴趣小组用废铁屑(主
要成分为Fe,杂质有Al、C及油脂)制备高铁酸钠的主要流程如下。下列说法错误的是( )
A.“碱浸”可以除去废铁屑表面的油脂
B.“滤渣”的主要成分是Al和C
C.“操作Ⅰ”通入的空气可以用 溶液代替
D.若流程改为先“氧化”后“调pH”,可能会生成
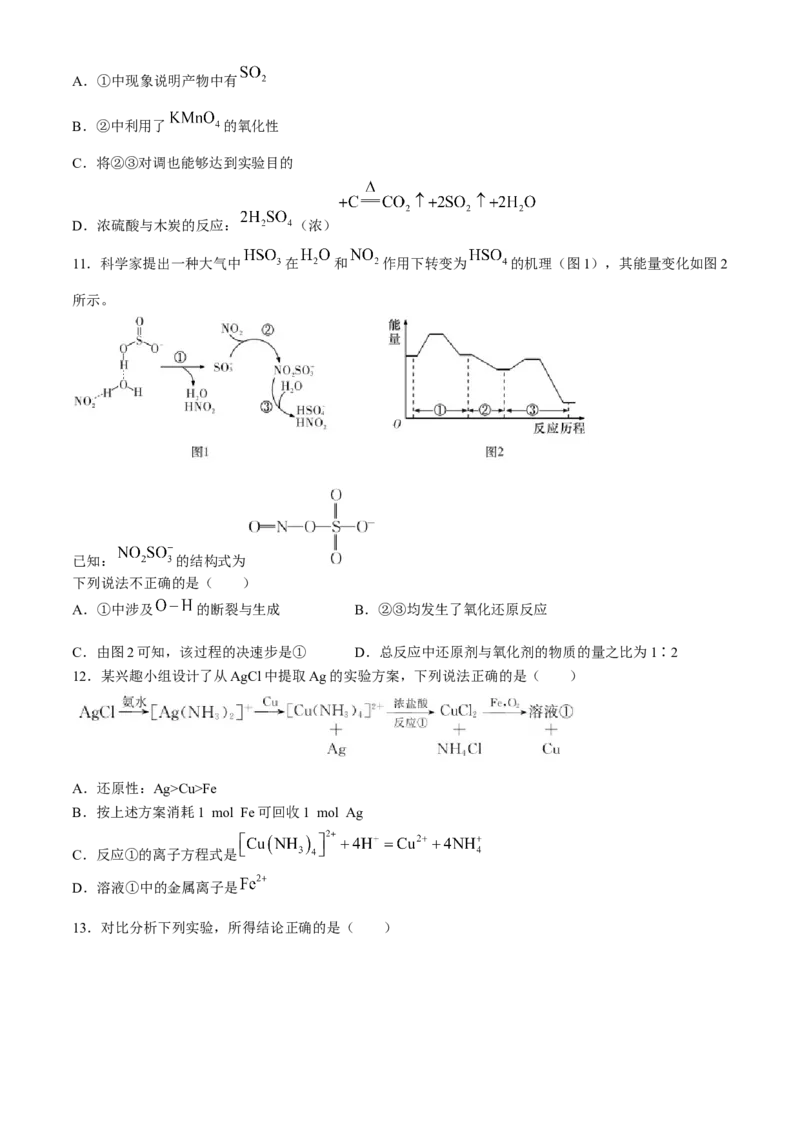
10.用如图装置检验浓硫酸与木炭在加热条件下反应的产物 和 。
下列说法不正确的是( )A.①中现象说明产物中有
B.②中利用了 的氧化性
C.将②③对调也能够达到实验目的
D.浓硫酸与木炭的反应: (浓)
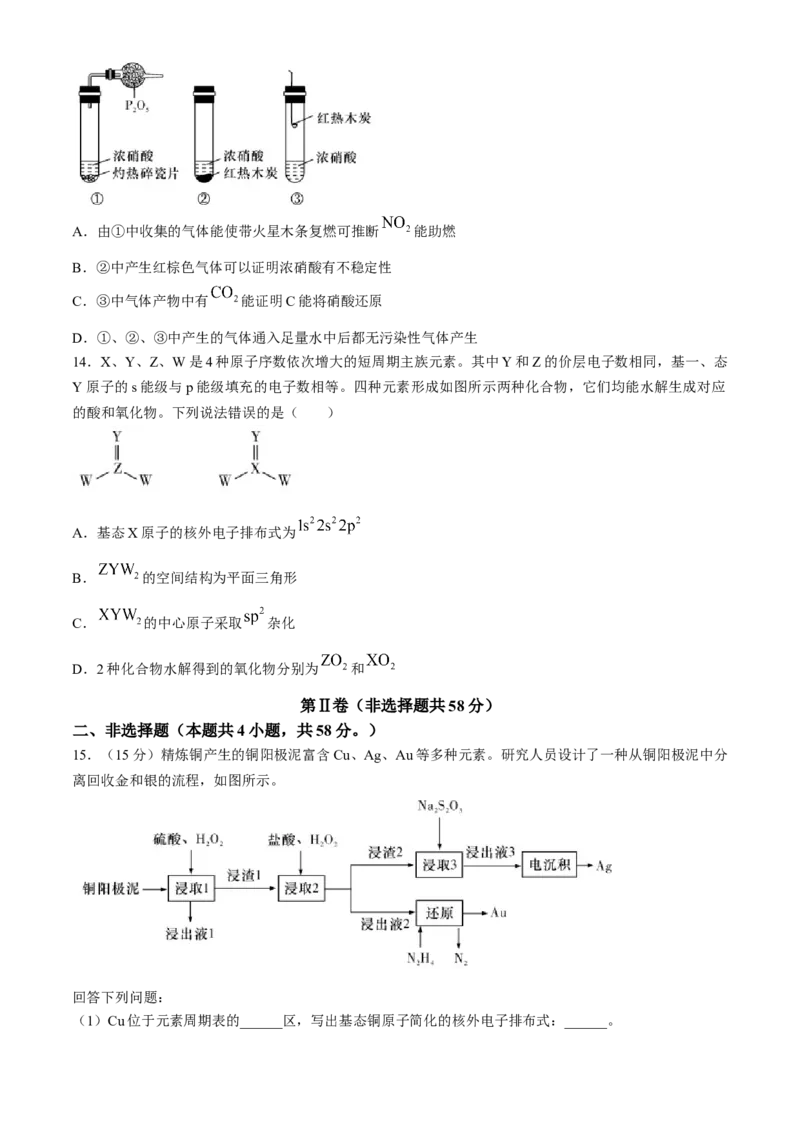
11.科学家提出一种大气中 在 和 作用下转变为 的机理(图1),其能量变化如图2
所示。
已知: 的结构式为
下列说法不正确的是( )
A.①中涉及 的断裂与生成 B.②③均发生了氧化还原反应
C.由图2可知,该过程的决速步是① D.总反应中还原剂与氧化剂的物质的量之比为1∶2
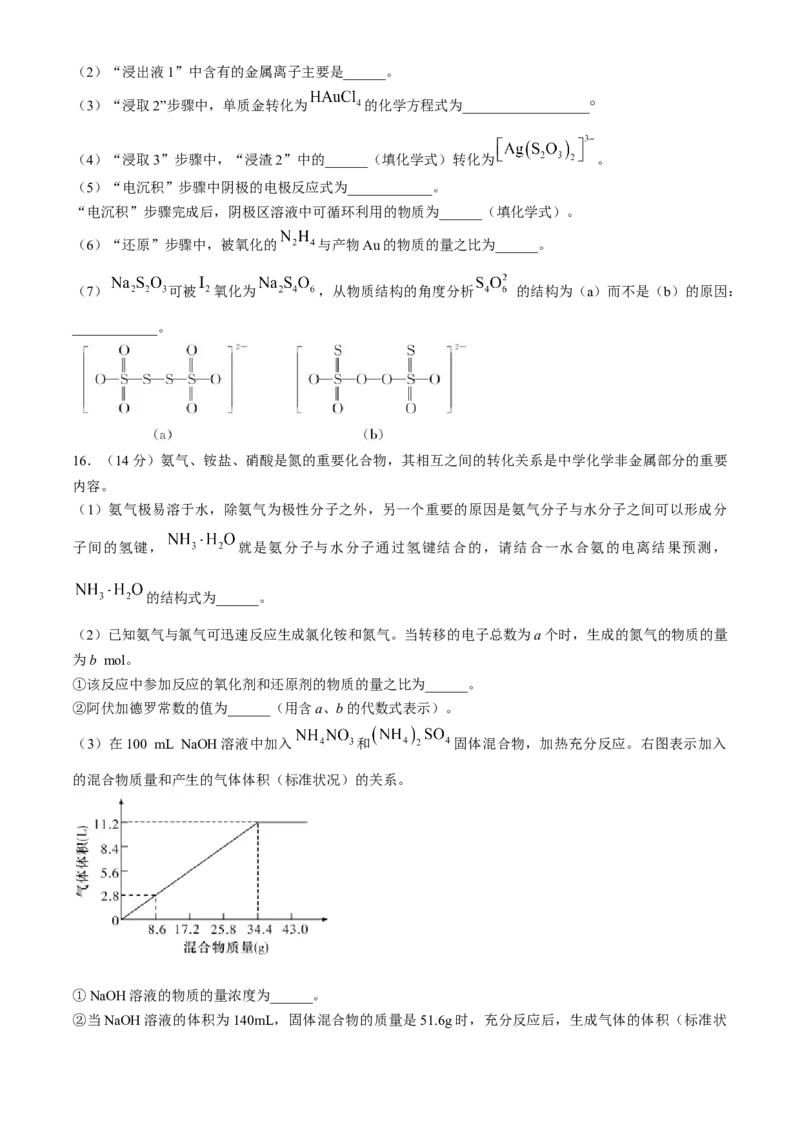
12.某兴趣小组设计了从AgCl中提取Ag的实验方案,下列说法正确的是( )
A.还原性:Ag>Cu>Fe
B.按上述方案消耗1 mol Fe可回收1 mol Ag
C.反应①的离子方程式是
D.溶液①中的金属离子是
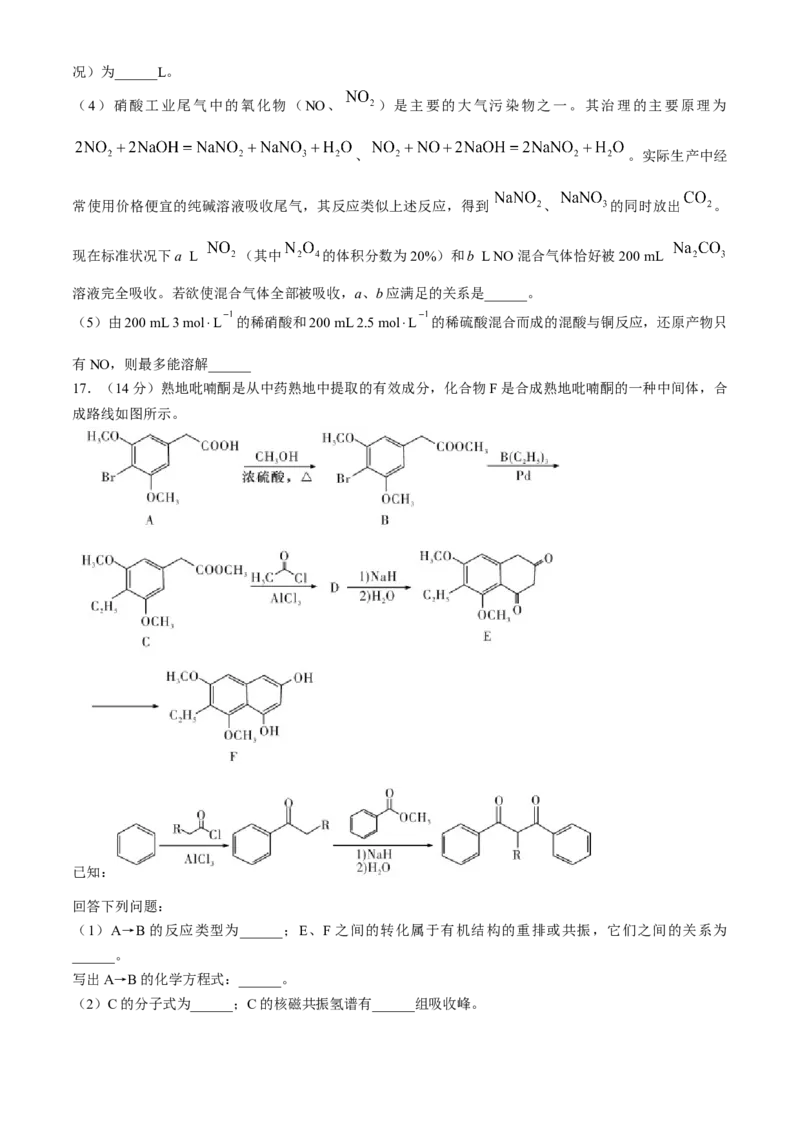
13.对比分析下列实验,所得结论正确的是( )A.由①中收集的气体能使带火星木条复燃可推断 能助燃
B.②中产生红棕色气体可以证明浓硝酸有不稳定性
C.③中气体产物中有 能证明C能将硝酸还原
D.①、②、③中产生的气体通入足量水中后都无污染性气体产生
14.X、Y、Z、W是4种原子序数依次增大的短周期主族元素。其中Y和Z的价层电子数相同,基一、态
Y原子的s能级与p能级填充的电子数相等。四种元素形成如图所示两种化合物,它们均能水解生成对应
的酸和氧化物。下列说法错误的是( )
A.基态X原子的核外电子排布式为
B. 的空间结构为平面三角形
C. 的中心原子采取 杂化
D.2种化合物水解得到的氧化物分别为 和
第Ⅱ卷(非选择题共58分)
二、非选择题(本题共4小题,共58分。)
15.(15分)精炼铜产生的铜阳极泥富含Cu、Ag、Au等多种元素。研究人员设计了一种从铜阳极泥中分
离回收金和银的流程,如图所示。
回答下列问题:
(1)Cu位于元素周期表的______区,写出基态铜原子简化的核外电子排布式:______。(2)“浸出液1”中含有的金属离子主要是______。
(3)“浸取2”步骤中,单质金转化为 的化学方程式为__________________°
(4)“浸取3”步骤中,“浸渣2”中的______(填化学式)转化为 。
(5)“电沉积”步骤中阴极的电极反应式为____________。
“电沉积”步骤完成后,阴极区溶液中可循环利用的物质为______(填化学式)。
(6)“还原”步骤中,被氧化的 与产物Au的物质的量之比为______。
(7) 可被 氧化为 ,从物质结构的角度分析 的结构为(a)而不是(b)的原因:
____________。
16.(14分)氨气、铵盐、硝酸是氮的重要化合物,其相互之间的转化关系是中学化学非金属部分的重要
内容。
(1)氨气极易溶于水,除氨气为极性分子之外,另一个重要的原因是氨气分子与水分子之间可以形成分
子间的氢键, 就是氨分子与水分子通过氢键结合的,请结合一水合氨的电离结果预测,
的结构式为______。
(2)已知氨气与氯气可迅速反应生成氯化铵和氮气。当转移的电子总数为a个时,生成的氮气的物质的量
为b mol。
①该反应中参加反应的氧化剂和还原剂的物质的量之比为______。
②阿伏加德罗常数的值为______(用含a、b的代数式表示)。
(3)在100 mL NaOH溶液中加入 和 固体混合物,加热充分反应。右图表示加入
的混合物质量和产生的气体体积(标准状况)的关系。
①NaOH溶液的物质的量浓度为______。
②当NaOH溶液的体积为140mL,固体混合物的质量是51.6g时,充分反应后,生成气体的体积(标准状况)为______L。
(4)硝酸工业尾气中的氧化物(NO、 )是主要的大气污染物之一。其治理的主要原理为
、 。实际生产中经
常使用价格便宜的纯碱溶液吸收尾气,其反应类似上述反应,得到 、 的同时放出 。
现在标准状况下a L (其中 的体积分数为20%)和b L NO混合气体恰好被200 mL
溶液完全吸收。若欲使混合气体全部被吸收,a、b应满足的关系是______。
(5)由200 mL 3 mol⋅L 的稀硝酸和200 mL 2.5 mol⋅L 的稀硫酸混合而成的混酸与铜反应,还原产物只
有NO,则最多能溶解______
17.(14分)熟地吡喃酮是从中药熟地中提取的有效成分,化合物F是合成熟地吡喃酮的一种中间体,合
成路线如图所示。
已知:
回答下列问题:
(1)A→B的反应类型为______;E、F之间的转化属于有机结构的重排或共振,它们之间的关系为
______。
写出A→B的化学方程式:______。
(2)C的分子式为______;C的核磁共振氢谱有______组吸收峰。(3)F中含氧官能团的名称是______。
(4)D的结构简式是______。
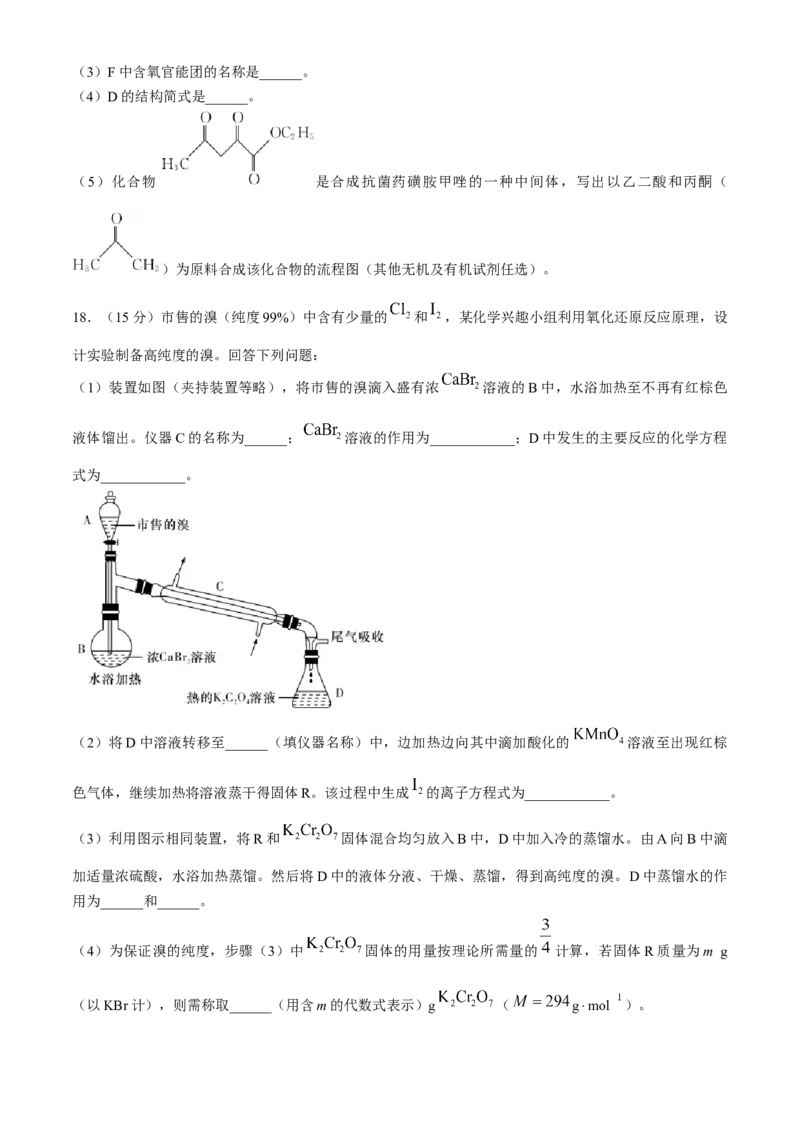
(5)化合物 是合成抗菌药磺胺甲唑的一种中间体,写出以乙二酸和丙酮(
)为原料合成该化合物的流程图(其他无机及有机试剂任选)。
18.(15分)市售的溴(纯度99%)中含有少量的 和 ,某化学兴趣小组利用氧化还原反应原理,设
计实验制备高纯度的溴。回答下列问题:
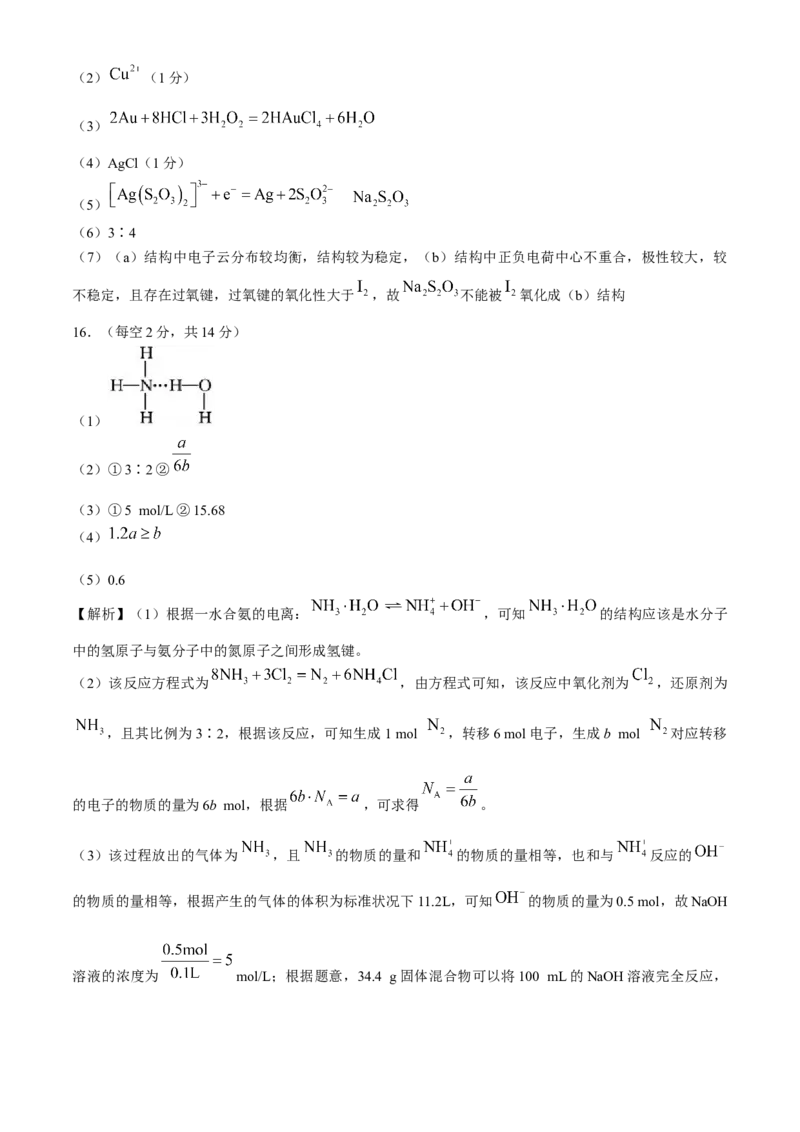
(1)装置如图(夹持装置等略),将市售的溴滴入盛有浓 溶液的B中,水浴加热至不再有红棕色
液体馏出。仪器C的名称为______; 溶液的作用为____________;D中发生的主要反应的化学方程
式为____________。
(2)将D中溶液转移至______(填仪器名称)中,边加热边向其中滴加酸化的 溶液至出现红棕
色气体,继续加热将溶液蒸干得固体R。该过程中生成 的离子方程式为____________。
(3)利用图示相同装置,将R和 固体混合均匀放入B中,D中加入冷的蒸馏水。由A向B中滴
加适量浓硫酸,水浴加热蒸馏。然后将D中的液体分液、干燥、蒸馏,得到高纯度的溴。D中蒸馏水的作
用为______和______。
(4)为保证溴的纯度,步骤(3)中 固体的用量按理论所需量的 计算,若固体R质量为m g
(以KBr计),则需称取______(用含m的代数式表示)g ( g⋅mol )。(5)本实验所用钾盐试剂均经重结晶的方法纯化。其中趁热过滤的具体操作为漏斗下端管口紧靠烧杯内
壁,转移溶液时用____________,滤液沿烧杯壁流下。雅礼中学 2025 届高三月考试卷(二)
化学参考答案
一、选择题(本题共14小题,每小题3分,共42分,每小题只有一个选项符合题意。)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 D D C D D B C D B C B C A B
1.D【解析】纳米荧光材料的碳量子点颗粒大小在胶体的范围内,但是没有分散剂,不能叫做胶体,故A
错误;食品脱氧剂使用后,其中的铁粉与空气中的氧气反应转化成 ,故B错误;芯片使用的材料是
单质硅,故C错误;环型碳 、环型碳 和金刚石都是碳元素的单质,均是碳元素的同素异形体,故
D正确。
2.D【解析】结合得失电子守恒,将等物质的量的 Al和Si分别加入足量NaOH溶液中,生成气体的物质
的量之比为3∶4。
3.C【解析】过量铁粉会和硝酸铁发生归中反应,最终溶液中的成分为硝酸亚铁: (稀)
。
4.D【解析】标准状况下 为气体,11.2 L 为0.5 mol,其中含有1.5 mol原子,原子总数为 ,
A错误; 为弱酸阴离子,其在水中易发生水解,因此,100 mL 0.1 mol⋅L 溶液中 数
目小于 ,B错误;反应①的方程式为 ,反应中每生成3 mol S消耗2 mol
,3.4 g 为0.1 mol,故可以生成0.15 mol S,生成物中硫原子数目为 ,C错误;反应②的
方程式为 ,反应的还原产物为 ,每生成2 mol 共转移4 mol电
子,因此,每生成1 mol ,转移2 mol电子,数目为 ,D正确。
5.D【解析】70%硫酸和亚硫酸钠反应生成 ,没有发生氧化还原反应,S的化合价没有变化,故A错
误;稀硫酸和硫化亚铁反应生成 ,Fe的化合价没有变化,故B错误;浓硝酸和铜片反应生成 ,
N从+5价转化为+4价, 和水反应生成 和NO,N的化合价从+4价变为+5价和+2价,故C错误;浓盐酸和高锰酸钾反应生成 ,Cl的化合价从—1价变为0价, 和溴化钾溶液反应生成KCl,Cl
的化合价从0价变为-1价,故D正确。
6.B【解析】根据加入过量NaOH溶液,加热,得到0.02 mol气体,说明有 ,且为0.02 mol,同时产
生红褐色沉淀,说明有 ,且为0.02 mol,则没有 ,根据得到不溶于盐酸的4.66g沉淀,说明有
,且为0.02 mol,则根据电荷守恒可知一定有 ,至少有0.04 mol,B正确。
7.C【解析】配制250 mL 0.1000 mol⋅L NaCl溶液时,称取的NaCl固体应先在烧杯中溶解,再转移至
容量瓶中定容,A错误;将某稀溶液加热浓缩,然后加入浓NaOH溶液,并加热,若能产生使湿润的红色
石蕊试纸变蓝的气体,该气体是 ,说明溶液中含有 ,由于题目没有加热,溶液是稀溶液,试纸
是蓝色石蕊试纸,因此不能看到湿润的红色石蕊试纸变蓝,实验操作及现象均有误,B错误;溶液变成棕
黄色,说明新制氯水能将碘离子氧化为碘单质,新制氯水中含有 ,该反应属于置换反应,证明Cl和I
的非金属性前者更强,C正确; 具有还原性,可以被酸性KMnO₄溶液氧化为 , 与 作
用使溶液变为红色,证明 具有还原性,而不是氧化性,D错误。
8.D【解析】 中滴加过量0.3 mol/L 溶液并充分振荡,砖红色沉淀转化为另一颜色沉淀,溶
液显浅蓝色,说明 转化成 ,Cu的化合价由+1价升至+2价,根据氧化还原反应的特点知,Cu
的化合价还有由+1价降至0价,新生成的沉淀为金属Cu,A项正确; 与0.3 mol/L 发生的反
应为 ,该过程中 表现酸性,后滴加浓硝酸发生的反应为
(浓) ,该过程中 表现氧化性和酸性,B项正确;
中滴加过量6 mol/L氨水并充分振荡,沉淀逐渐溶解得到无色溶液,静置一段时间后无色溶液变为
深蓝色,说明 与 形成的无色配合物易被空气中的 氧化成深蓝色 ,C项正确;
既能与酸反应生成盐和水、又能与碱反应生成盐和水的氧化物为两性氧化物, 溶于6 mol/L氨水形
成的是配合物, 不属于两性氧化物,D项错误。9.B【解析】“碱浸”可以除去废铁屑表面的油脂,A正确;“滤渣”的主要成分是单质C,B错误;
“操作Ⅰ”的目的是将 氧化为 ,也可以用 做氧化剂,不会引入杂质,因此“操作Ⅰ”通入
的空气可以用H₂O₂溶液代替,C正确;若先“氧化”,溶液呈酸性,NaClO溶液能将盐酸中的 氧化为
,D正确。
10.C【解析】②中的酸性高锰酸钾溶液颜色变浅,既能检验二氧化硫,也能除去二氧化硫,还能进一步
确认已除尽二氧化硫,从而确保③中的澄清石灰水变浑浊是二氧化碳产生的结果,②③对调达不到实验目
的。
11.B【解析】由 和 发生反应②生成 ,存在化合价的变化,为氧化还原反应;但发生
的反应③为水解反应,化合价没有变化,不属于氧化还原反应。
12.C【解析】从实验方案可知,氨水溶解了氯化银,然后用铜置换出银,滤液中加入浓盐酸后得到氯化
铜和氯化铵的混合液,向其中加入铁,铁置换出铜,过滤出铜可以循环利用,并通入氧气可将亚铁离子氧
化为铁离子。金属活动性越强,金属的还原性越强,而且由题中的实验方案能得到证明,还原性从强到弱
的顺序为Fe>Cu>Ag,A不正确;由电子守恒可知,1 mol Fe可以置换1 mol Cu,而1 mol Cu可以置换
2 mol Ag,因此,按实验方案消耗1 mol Fe可回收2 mol Ag,B不正确;反应①中,氯化四氨合铜溶液
与浓盐酸反应生成氯化铜和氯化铵,该反应的离子方程式是 ,C正
确;向氯化铜和氯化铵的混合液中加入铁,铁置换出铜后生成 ,然后 被通入的氧气氧化为 ,
氯化铁和氯化铵水解均使溶液呈酸性,二者可共存,因此,溶液①中的金属离子是 ,D不正确。
13.A【解析】①中发生反应 (浓) ,收集的气体中 的百分含量为
20%,与空气中 的百分含量(约21%)接近,而空气不能使带火星的木条复燃,由此可推断 能助
燃,A正确;浓硝酸能与红热的木炭反应生成 ,不能证明浓硝酸具有不稳定性,B错误;红热的木炭
与试管中的氧气反应也能生成二氧化碳,C错误;②、③中生成的 溶于水后生成 和NO,NO
属于污染性气体,D错误。
14.B
二、非选择题(本题共4小题,共58分。)
15.(除标注外,其余每空2分,共15分)
(1)ds(1分)(2) (1分)
(3)
(4)AgCl(1分)
(5)
(6)3∶4
(7)(a)结构中电子云分布较均衡,结构较为稳定,(b)结构中正负电荷中心不重合,极性较大,较
不稳定,且存在过氧键,过氧键的氧化性大于 ,故 不能被 氧化成(b)结构
16.(每空2分,共14分)
(1)
(2)①3∶2②
(3)①5 mol/L②15.68
(4)
(5)0.6
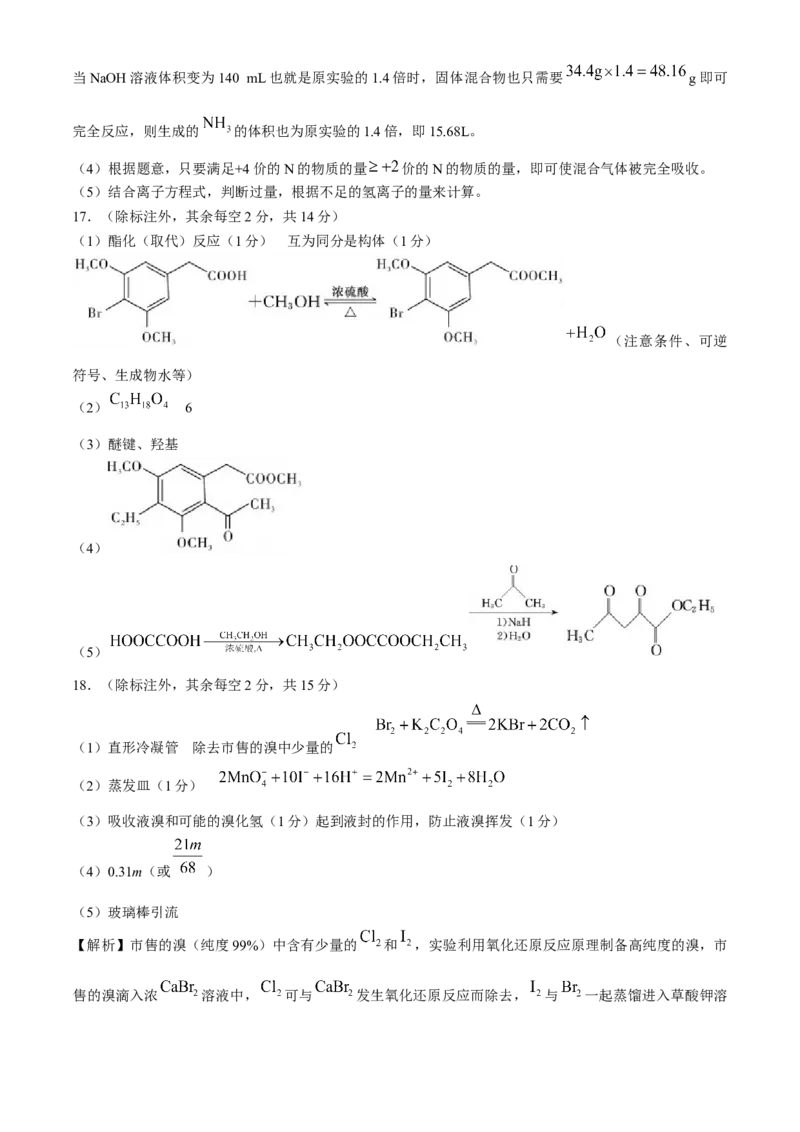
【解析】(1)根据一水合氨的电离: ,可知 的结构应该是水分子
中的氢原子与氨分子中的氮原子之间形成氢键。
(2)该反应方程式为 ,由方程式可知,该反应中氧化剂为 ,还原剂为
,且其比例为3∶2,根据该反应,可知生成1 mol ,转移6 mol电子,生成b mol 对应转移
的电子的物质的量为6b mol,根据 ,可求得 。
(3)该过程放出的气体为 ,且 的物质的量和 的物质的量相等,也和与 反应的
的物质的量相等,根据产生的气体的体积为标准状况下11.2L,可知 的物质的量为0.5 mol,故NaOH
溶液的浓度为 mol/L;根据题意,34.4 g固体混合物可以将100 mL的NaOH溶液完全反应,当NaOH溶液体积变为140 mL也就是原实验的1.4倍时,固体混合物也只需要 g即可
完全反应,则生成的 的体积也为原实验的1.4倍,即15.68L。
(4)根据题意,只要满足+4价的N的物质的量 价的N的物质的量,即可使混合气体被完全吸收。
(5)结合离子方程式,判断过量,根据不足的氢离子的量来计算。
17.(除标注外,其余每空2分,共14分)
(1)酯化(取代)反应(1分) 互为同分是构体(1分)
(注意条件、可逆
符号、生成物水等)
(2) 6
(3)醚键、羟基
(4)
(5)
18.(除标注外,其余每空2分,共15分)
(1)直形冷凝管 除去市售的溴中少量的
(2)蒸发皿(1分)
(3)吸收液溴和可能的溴化氢(1分)起到液封的作用,防止液溴挥发(1分)
(4)0.31m(或 )
(5)玻璃棒引流
【解析】市售的溴(纯度99%)中含有少量的 和 ,实验利用氧化还原反应原理制备高纯度的溴,市
售的溴滴入浓 溶液中, 可与 发生氧化还原反应而除去, 与 一起蒸馏进入草酸钾溶液中,并被草酸钾还原为 、 ,向溶液中滴加高锰酸钾溶液氧化 ,加热蒸干主要得KBr固体,将
KBr固体和 固体混合均匀,D中加入冷的蒸馏水,同时滴加适量浓硫酸,水浴加热蒸馏,得到的
液体分液、干燥、蒸馏,可得高纯度的溴。