文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
模块一 知识主题
热点突破 溶解度及溶解度曲线
01考情透视·目标导航
02知识导图·思维引航
03核心精讲·题型突破
考点一 溶解度曲线 小温度范围
【真题研析】 ►考法03 溶解度与溶解性
►考法01 改变温度时溶液发生的变化 ►考法04 溶解度与溶质质量分数关系
►考法02 比较溶液中各种量的关系 【核心精讲】
►考法03 判断物质提纯与结晶的方法 ►知识点一 溶解度与溶解性
►考法04 饱和与不饱和溶液的判断和转化 ►知识点二 溶解度与溶质质量分数
►考法05 气体溶解度 【命题探究】
【核心精讲】 考点三 实物(操作)图
►知识点一 溶解度曲线 【真题研析】
►知识点二 气体溶解度 ►考法01 饱和与不饱和溶液的判断
►知识点三 饱和与不饱和溶液 ►考法02 饱和溶液中溶质质量分数计算
【命题探究】 【核心精讲】
考点二 溶解度表 ►知识点一 饱和与不饱和溶液的判断
【真题研析】 ►知识点二 饱和溶液中溶质质量分数计算
►考法01 判断对应的溶解度曲线 【命题探究】
►考法02 判断两种物质的溶解度相等的最
考点要求 课标要求 命题预测
了解饱和溶液和溶解度的含义;查阅溶 本专题的内容是中考常考的考点。常以选
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
解度数据,绘制溶解度曲线;认识结晶现 择题和填空与简答题的形式进行考查,考查的
象。 命题点有:饱和与不饱和溶液的转化方法、溶
解度随温度的变化情况、某温度下,溶解度大
认识溶质质量分数的含义,学习计算溶 小的判断及比较、溶解度曲线上的点的含义、
质质量分数。 判断物质提纯的方法、计算或比较溶液中溶质
质量分数的大小等。
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
考点一 溶解度曲线
考法 01 根据溶解度曲线判断 改变温度时溶液发生的变化
1.(2024·四川广元·中考真题)甲、乙、丙三种固体的溶解度曲线如图1所示,如图2是选用图1中某种
固体进行实验时的情况。下列说法正确的是
A.图2试管中固体对应图1中的丙
B.t℃时,甲、乙两饱和溶液中溶质质量相等
2
C.t℃时,将40g甲加入到50g水中,所得溶液的溶质质量分数为80%
3
D.将等质量的甲、乙、丙饱和溶液从t℃降温到t℃,得到溶液的质量:丙>乙>甲
2 1
【答案】D
【详解】A、氢氧化钠固体溶于水放热,使温度升高,试管内的原来剩余的固体完全溶解,说明该物质的
溶解度随着温度的升高而增大,图2试管中固体对应的不可能是图1中的丙,故A错误;
B、选项说法没有指明饱和溶液的质量,则t℃时甲、乙两饱和溶液中溶质质量不一定相等,故B错误;
2
C、t℃时,甲的溶解度为80g,将40g甲加入到50g水中,最多能溶解40g,所得溶液的溶质质量分数为:
3
,故C错误;
D、将等质量的甲、乙、丙饱和溶液从t℃降温到t℃,甲、乙的溶解度减小,有晶体析出,t℃时乙的溶
2 1 1
解度大于甲,甲析出晶体的质量大于乙,丙的溶解度随温度的降低而增大,没有晶体析出,则得到溶液的
质量:丙>乙>甲,故D正确。
故选:D。
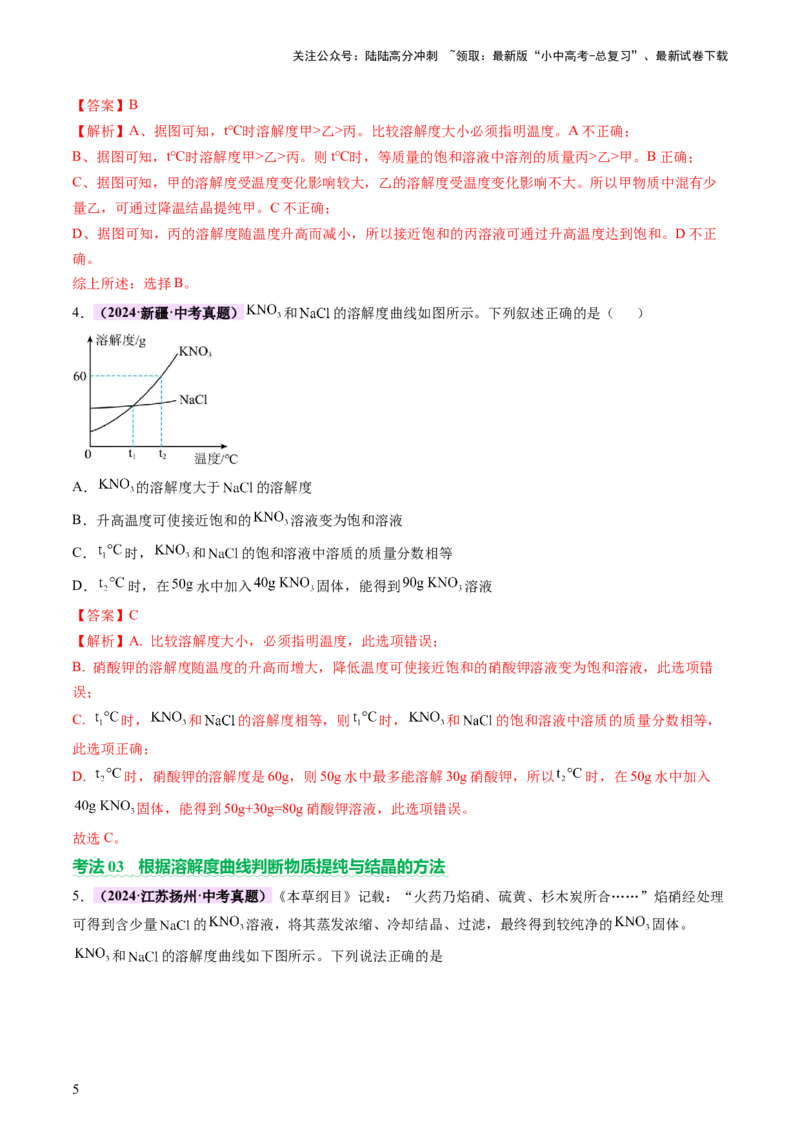
2.(2024·山东威海·中考真题)如图是硝酸钾和氯化钾的溶解度曲线,下列说法正确的是( )
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.t℃时,将60g硝酸钾加入50g水中,充分溶解,所得溶液的质量是100g
2
B.t℃时,将等质量的两种物质的饱和溶液降温至t℃,析出晶体的质量:硝酸钾>氯化钾
2 1
C.将t℃氯化钾的饱和溶液升温至t℃,溶液的溶质质量分数变大
1 2
D.相同温度下,硝酸钾的溶解度大于氯化钾的溶解度
【答案】B
【解析】A、因为t℃时,硝酸钾的溶解度为110g,即在50g水中最多溶解55g硝酸钾,所以将60g硝酸钾
2
加入50g水中,充分溶解,所得溶液的质量是105g,该项错误;
B、因为从t℃降温到t℃时,硝酸钾的溶解度比氯化钾的溶解度减少的多,所以将等质量的两种物质的饱
2 1
和溶液从t℃降温至t℃,析出晶体的质量:硝酸钾>氯化钾,该项正确;
2 1
C、将t℃氯化钾的饱和溶液升温至t℃,虽然溶解度增大,但溶液中溶质和溶剂的质量没变,溶质质量分
1 2
数不变,该项错误;
D、在t℃时,氯化钾和硝酸钾的溶解度相等,所以该项错误;
1
故选B。
考法 02 根据溶解度曲线 比较溶液中各种质量关系
3.(2024·四川巴中·中考真题)甲、乙、丙三种固体物质的溶解度曲线如图所示,下列说法正确的是(
)
A.溶解度甲>乙>丙
B.t℃时,等质量的饱和溶液中溶剂的质量丙>乙>甲
C.甲物质中混有少量乙,可通过蒸发结晶提纯甲
D.接近饱和的丙溶液可通过降低温度达到饱和
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【答案】B
【解析】A、据图可知,t℃时溶解度甲>乙>丙。比较溶解度大小必须指明温度。A不正确;
B、据图可知,t℃时溶解度甲>乙>丙。则t℃时,等质量的饱和溶液中溶剂的质量丙>乙>甲。B正确;
C、据图可知,甲的溶解度受温度变化影响较大,乙的溶解度受温度变化影响不大。所以甲物质中混有少
量乙,可通过降温结晶提纯甲。C不正确;
D、据图可知,丙的溶解度随温度升高而减小,所以接近饱和的丙溶液可通过升高温度达到饱和。D不正
确。
综上所述:选择B。
4.(2024·新疆·中考真题) 和 的溶解度曲线如图所示。下列叙述正确的是( )
A. 的溶解度大于 的溶解度
B.升高温度可使接近饱和的 溶液变为饱和溶液
C. 时, 和 的饱和溶液中溶质的质量分数相等
D. 时,在 水中加入 固体,能得到 溶液
【答案】C
【解析】A. 比较溶解度大小,必须指明温度,此选项错误;
B. 硝酸钾的溶解度随温度的升高而增大,降低温度可使接近饱和的硝酸钾溶液变为饱和溶液,此选项错
误;
C. 时, 和 的溶解度相等,则 时, 和 的饱和溶液中溶质的质量分数相等,
此选项正确;
D. 时,硝酸钾的溶解度是60g,则50g水中最多能溶解30g硝酸钾,所以 时,在50g水中加入
固体,能得到50g+30g=80g硝酸钾溶液,此选项错误。
故选C。
考法 0 3 根据溶解度曲线判断物质提纯与结晶的方法
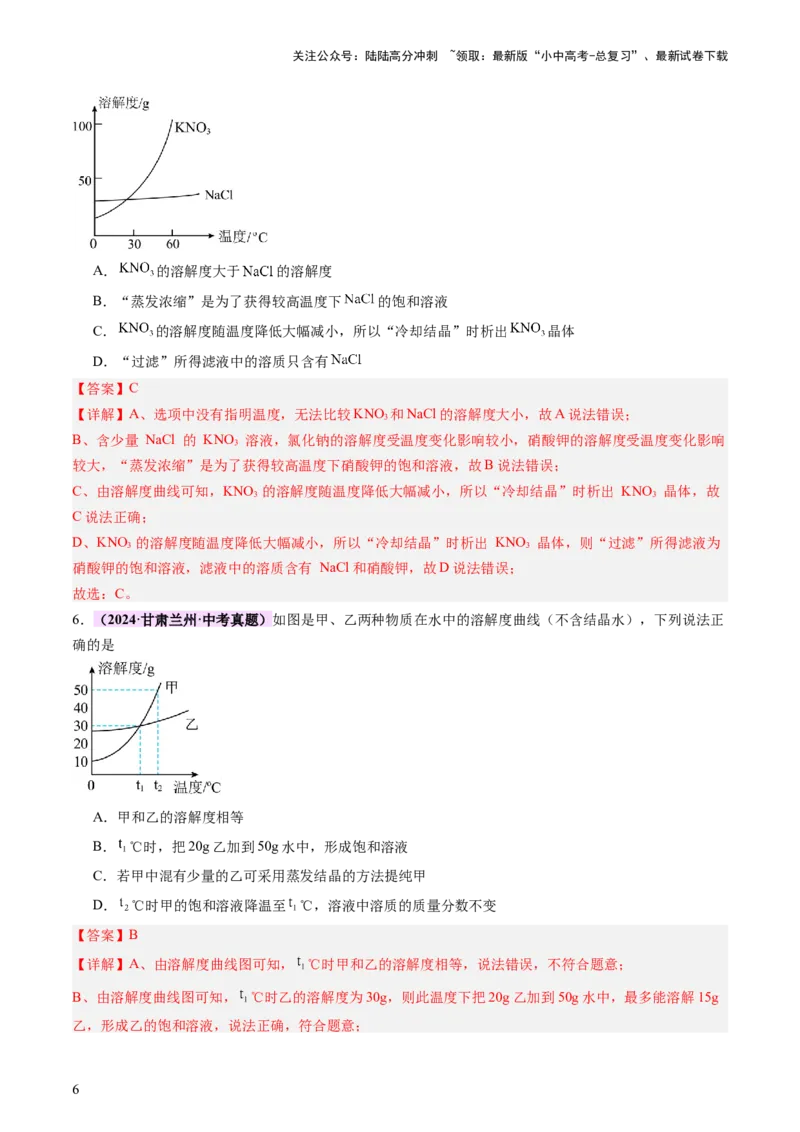
5.(2024·江苏扬州·中考真题)《本草纲目》记载:“火药乃焰硝、硫黄、杉木炭所合……”焰硝经处理
可得到含少量 的 溶液,将其蒸发浓缩、冷却结晶、过滤,最终得到较纯净的 固体。
和 的溶解度曲线如下图所示。下列说法正确的是
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A. 的溶解度大于 的溶解度
B.“蒸发浓缩”是为了获得较高温度下 的饱和溶液
C. 的溶解度随温度降低大幅减小,所以“冷却结晶”时析出 晶体
D.“过滤”所得滤液中的溶质只含有
【答案】C
【详解】A、选项中没有指明温度,无法比较KNO 和NaCl的溶解度大小,故A说法错误;
3
B、含少量 NaCl 的 KNO 溶液,氯化钠的溶解度受温度变化影响较小,硝酸钾的溶解度受温度变化影响
3
较大,“蒸发浓缩”是为了获得较高温度下硝酸钾的饱和溶液,故B说法错误;
C、由溶解度曲线可知,KNO 的溶解度随温度降低大幅减小,所以“冷却结晶”时析出 KNO 晶体,故
3 3
C说法正确;
D、KNO 的溶解度随温度降低大幅减小,所以“冷却结晶”时析出 KNO 晶体,则“过滤”所得滤液为
3 3
硝酸钾的饱和溶液,滤液中的溶质含有 NaCl和硝酸钾,故D说法错误;
故选:C。
6.(2024·甘肃兰州·中考真题)如图是甲、乙两种物质在水中的溶解度曲线(不含结晶水),下列说法正
确的是
A.甲和乙的溶解度相等
B. ℃时,把20g乙加到50g水中,形成饱和溶液
C.若甲中混有少量的乙可采用蒸发结晶的方法提纯甲
D. ℃时甲的饱和溶液降温至 ℃,溶液中溶质的质量分数不变
【答案】B
【详解】A、由溶解度曲线图可知, ℃时甲和乙的溶解度相等,说法错误,不符合题意;
B、由溶解度曲线图可知, ℃时乙的溶解度为30g,则此温度下把20g乙加到50g水中,最多能溶解15g
乙,形成乙的饱和溶液,说法正确,符合题意;
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C、由溶解度曲线图可知,甲的溶解度受温度变化影响较大,乙的溶解度受温度变化影响较小,若甲中混
有少量的乙可采用降温结晶的方法提纯甲,说法错误,不符合题意;
D、 ℃时甲的饱和溶液降温至 ℃,甲的溶解度减小,有晶体析出,甲的饱和溶液仍为饱和溶液,但溶
液中溶质质量分数变为 ℃时甲的饱和溶液的溶质质量分数,因此降温后溶液的溶质质量分数减小,说法
错误,不符合题意。
故选:B。
考法 0 4 饱和与不饱和溶液的判断和转化
7.(2024·江苏连云港·中考真题)我国盐湖地区有“夏天晒盐(NaCl),冬天捞碱(NaCO)”的做法。
2 3
NaCl、NaCO 的溶解度曲线如图所示。下列说法中正确的是
2 3
A.20℃时NaCO 的饱和溶液,升温到40℃时仍是饱和溶液
2 3
B.30℃时,在100g水中加入40g NaCl,形成不饱和溶液
C.NaCl的溶解度比NaCO 的大
2 3
D.“夏天晒盐”经过蒸发结晶过程,“冬天捞碱”经过降温结晶过程
【答案】D
【详解】A、20℃时,碳酸钠的饱和溶液升温至40℃,升温后,碳酸钠的溶解度增加,变为不饱和溶液,
不符合题意;
B、30℃时,氯化钠的溶解度小于40g,则该温度下,在100g水中加入40g氯化钠,氯化钠部分溶解,形
成的是饱和溶液,不符合题意;
C、溶解度比较,应指明温度,否则无法比较,不符合题意;
D、由图可知,碳酸钠和氯化钠的溶解度均随温度的升高而增加,碳酸钠的溶解度受温度影响较大,氯化
钠的溶解度受温度影响较小,故“夏天晒盐”通过蒸发结晶获得氯化钠,“冬天捞碱”通过降温结晶得到
碳酸钠,符合题意。
故选D。
8.(2024·西藏·中考真题)温度是影响固体溶解度的因素之一。氯化钠、硝酸钾两种物质的溶解度随温度
变化情况如图所示。下列说法中正确的是( )
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.氯化钠和硝酸钾的溶解度大小相等
B.氯化钠和硝酸钾的溶解度随温度的升高而增大
C.20℃时,15g氯化钠放入50g水中能形成饱和溶液
D.将接近饱和的硝酸钾溶液升高温度,可变为饱和溶液
【答案】B
【解析】A、溶解度比较,应指明温度,否则无法比较,不符合题意;
B、由图可知,氯化钠和硝酸钾的溶解度均随温度的升高而增大,符合题意;
C、由图可知,20℃时,氯化钠的溶解度大于30g,该温度下,将15g氯化钠放入50g水中,氯化钠能全部
溶解,形成不饱和溶液,不符合题意;
D、硝酸钾的溶解度随温度的升高而增加,将接近饱和的硝酸钾溶液升高温度,得到的仍是不饱和溶液,
将接近饱和的硝酸钾溶液降低温度,可得到饱和溶液,不符合题意。
故选B。
考法 0 5 气体溶解度
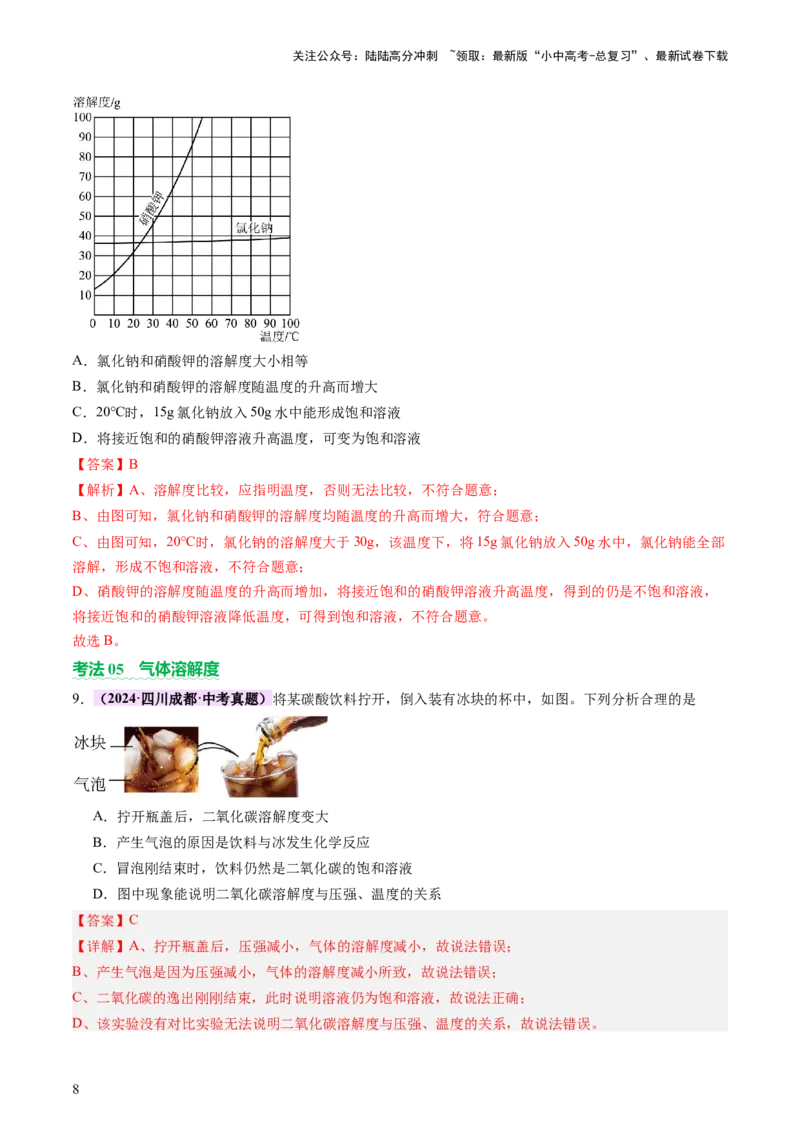
9.(2024·四川成都·中考真题)将某碳酸饮料拧开,倒入装有冰块的杯中,如图。下列分析合理的是
A.拧开瓶盖后,二氧化碳溶解度变大
B.产生气泡的原因是饮料与冰发生化学反应
C.冒泡刚结束时,饮料仍然是二氧化碳的饱和溶液
D.图中现象能说明二氧化碳溶解度与压强、温度的关系
【答案】C
【详解】A、拧开瓶盖后,压强减小,气体的溶解度减小,故说法错误;
B、产生气泡是因为压强减小,气体的溶解度减小所致,故说法错误;
C、二氧化碳的逸出刚刚结束,此时说明溶液仍为饱和溶液,故说法正确;
D、该实验没有对比实验无法说明二氧化碳溶解度与压强、温度的关系,故说法错误。
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
故选C。
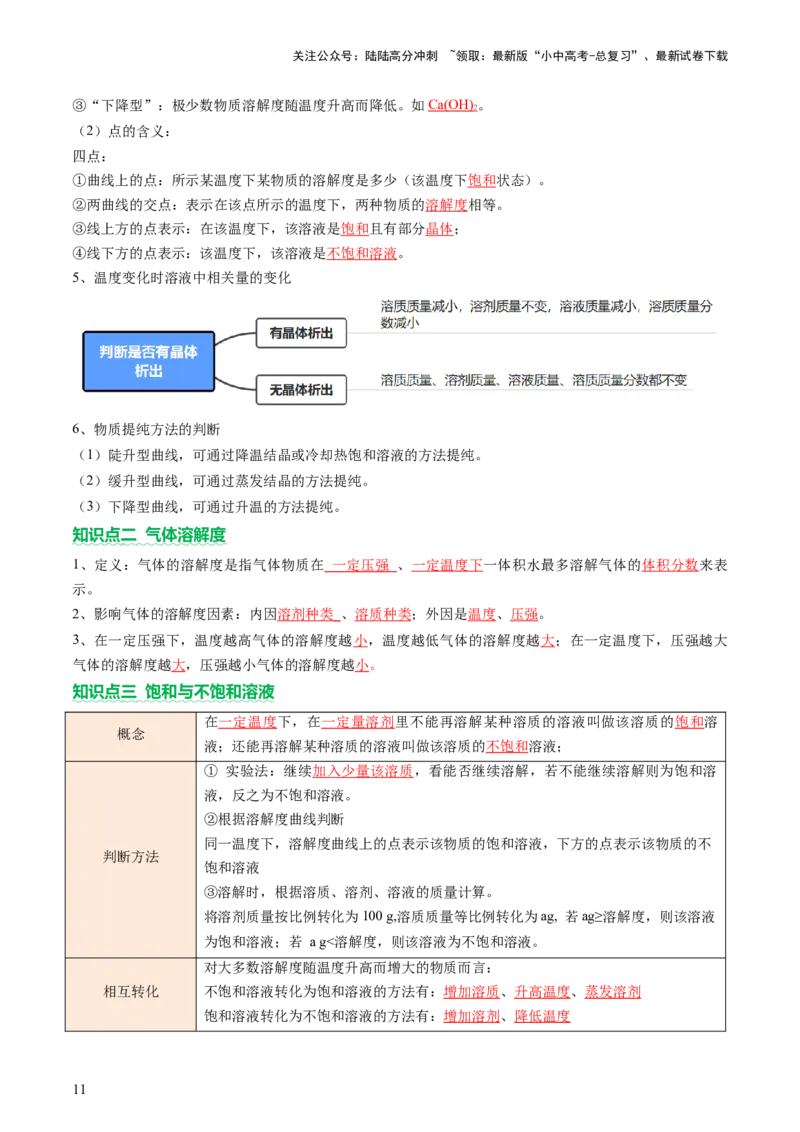
10.(2023·四川乐山·中考真题)气体的溶解度通常指压强为101 kPa和一定温度时,在1体积水里溶解达
到饱和状态时的气体体积。如图是甲、乙两种气体在101 kPa时的溶解度曲线,下列说法正确的是
A.甲的溶解度大于乙的溶解度 B.两种气体的溶解度都随温度升高而增大
C.甲气体的溶解度受温度的影响小于乙 D.T℃时,气体乙的溶解度为2 g
【答案】C
【详解】A、溶解度比较,应指明温度,否则无法比较,不符合题意;
B、由图可知,两种气体的溶解度都随温度升高而减小,不符合题意;
C、由图可知,两种气体的溶解度都随温度升高而减小,且甲的溶解度受温度影响比乙小,符合题意;
D、气体的溶解度通常指压强为101 kPa和一定温度时,在1体积水里溶解达到饱和状态时的气体体积,单
位不是“g”,不符合题意。
故选C。
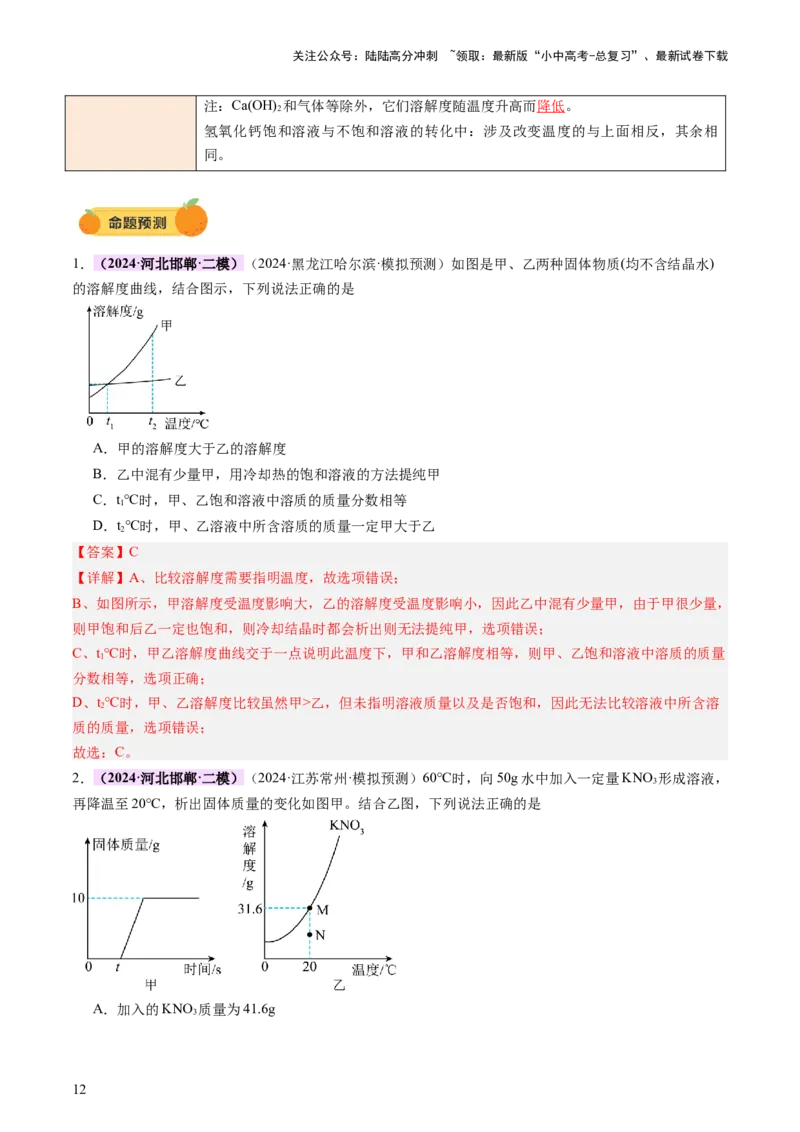
11.(2022·四川广元·中考真题)下列图像不能正确反映对应关系的是
A.加热一定质量 与 的混合物
B.等质量、等浓度的稀盐酸分别与足量的Mg、Fe反应
C.向一定质量的氢氧化钡溶液中加入稀硫酸
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
D.气体溶解度与温度、压强的关系
【答案】B
【详解】A、氯酸钾在二氧化锰催化作用下受热分解生成氯化钾和氧气,等一会儿,反应才会发生,随着
反应进行,氧气逸出,根据质量守恒定律,固体质量减小,二氧化锰作为催化剂,质量不变,因此二氧化
锰质量分数增大,完全反应后固体质量不再变化,二氧化锰质量分数也不再变化,图像正确;
B、等质量、等浓度的稀盐酸分别与足量的Mg、Fe反应,金属与酸反应时氢气来源于酸中的氢元素,因
为酸的量相同,金属过量,故生成的氢气应该相等;根据化学方程式Mg+2HCl═MgCl +H ↑,
2 2
Fe+2HCl═FeCl +H ↑可知,同样生成2份质量氢气,Mg需要24份质量,Fe需要56份质量,则生成等质量
2 2
的氢气,消耗的Fe的质量多,Mg的质量少,图像错误;
C、氢氧化钡和硫酸反应生成硫酸钡沉淀和水,所以向一定质量的氢氧化钡溶液中不断加入稀硫酸,溶质
质量逐渐减小,恰好完全反应时,溶质质量为零,继续滴加稀硫酸,溶质质量逐渐增大,图像正确;
D、在压强一定的条件下,气体物质温度越高,溶解度越小;在温度一定的条件下,气体物质压强越大,
溶解度越大,图像正确;
故选B。
知识点一 固体溶解度及曲线
1、概念:固体物质溶解度指的是在 一定温度下 ,某固态物质在 100g 溶剂 里达到饱和状态时所溶解的
质量。
2、影响固体物质的溶解度因素:内因溶剂种类、溶质种类;外因是温度。
3、溶解度的意义
20℃时,氯化钠溶解度为36g:
①在20℃时,100g水中最多能溶解(即达饱和)36gNaCl。
②在20℃时,100g水中溶解36g氯化钠形成饱和溶液。
③在20℃时,要完全溶解36g氯化钠,最少需要水100g。
④在20℃时,136g氯化钠溶液中有100g水,36g氯化钠。
4、溶解度曲线
(1)线的含义:
三线:①“陡升型” :大多数固体物的溶解度随温度升高而升高。如KNO;
3
② “缓升型”:少数固体物质的溶解度受温度的影响很小。如NaCl;
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
③“下降型”:极少数物质溶解度随温度升高而降低。如Ca(OH) 。
2
(2)点的含义:
四点:
①曲线上的点:所示某温度下某物质的溶解度是多少(该温度下饱和状态)。
②两曲线的交点:表示在该点所示的温度下,两种物质的溶解度相等。
③线上方的点表示:在该温度下,该溶液是饱和且有部分晶体;
④线下方的点表示:该温度下,该溶液是不饱和溶液。
5、温度变化时溶液中相关量的变化
6、物质提纯方法的判断
(1)陡升型曲线,可通过降温结晶或冷却热饱和溶液的方法提纯。
(2)缓升型曲线,可通过蒸发结晶的方法提纯。
(3)下降型曲线,可通过升温的方法提纯。
知识点 二 气体溶解度
1、定义:气体的溶解度是指气体物质在 _ 一定压强 _ 、一定温度下一体积水最多溶解气体的体积分数来表
示。
2、影响气体的溶解度因素:内因 溶剂种类 _、溶质种类;外因是温度、压强。
3、在一定压强下,温度越高气体的溶解度越小,温度越低气体的溶解度越大;在一定温度下,压强越大
气体的溶解度越大,压强越小气体的溶解度越小。
知识点 三 饱和与不饱和溶液
在一定温度下,在一定量溶剂里不能再溶解某种溶质的溶液叫做该溶质的饱和溶
概念
液;还能再溶解某种溶质的溶液叫做该溶质的不饱和溶液;
① 实验法:继续加入少量该溶质,看能否继续溶解,若不能继续溶解则为饱和溶
液,反之为不饱和溶液。
②根据溶解度曲线判断
同一温度下,溶解度曲线上的点表示该物质的饱和溶液,下方的点表示该物质的不
判断方法
饱和溶液
③溶解时,根据溶质、溶剂、溶液的质量计算。
将溶剂质量按比例转化为100 g,溶质质量等比例转化为ag, 若ag≥溶解度,则该溶液
为饱和溶液;若 a g<溶解度,则该溶液为不饱和溶液。
对大多数溶解度随温度升高而增大的物质而言:
相互转化 不饱和溶液转化为饱和溶液的方法有:增加溶质、升高温度、蒸发溶剂
饱和溶液转化为不饱和溶液的方法有:增加溶剂、降低温度
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
注:Ca(OH) 和气体等除外,它们溶解度随温度升高而降低。
2
氢氧化钙饱和溶液与不饱和溶液的转化中:涉及改变温度的与上面相反,其余相
同。
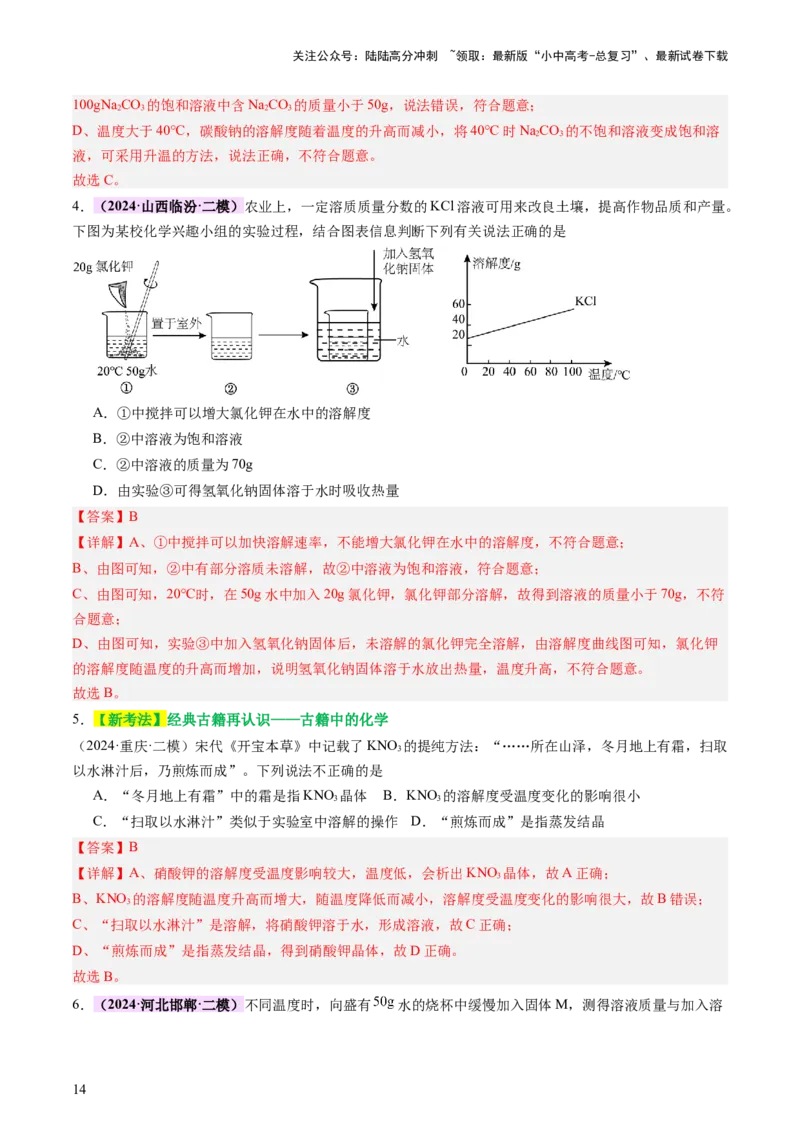
1.(2024·河北邯郸·二模)(2024·黑龙江哈尔滨·模拟预测)如图是甲、乙两种固体物质(均不含结晶水)
的溶解度曲线,结合图示,下列说法正确的是
A.甲的溶解度大于乙的溶解度
B.乙中混有少量甲,用冷却热的饱和溶液的方法提纯甲
C.t℃时,甲、乙饱和溶液中溶质的质量分数相等
1
D.t℃时,甲、乙溶液中所含溶质的质量一定甲大于乙
2
【答案】C
【详解】A、比较溶解度需要指明温度,故选项错误;
B、如图所示,甲溶解度受温度影响大,乙的溶解度受温度影响小,因此乙中混有少量甲,由于甲很少量,
则甲饱和后乙一定也饱和,则冷却结晶时都会析出则无法提纯甲,选项错误;
C、t℃时,甲乙溶解度曲线交于一点说明此温度下,甲和乙溶解度相等,则甲、乙饱和溶液中溶质的质量
1
分数相等,选项正确;
D、t℃时,甲、乙溶解度比较虽然甲>乙,但未指明溶液质量以及是否饱和,因此无法比较溶液中所含溶
2
质的质量,选项错误;
故选:C。
2.(2024·河北邯郸·二模)(2024·江苏常州·模拟预测)60℃时,向50g水中加入一定量KNO 形成溶液,
3
再降温至20℃,析出固体质量的变化如图甲。结合乙图,下列说法正确的是
A.加入的KNO 质量为41.6g
3
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
B.t时刻,KNO 溶液的溶质质量分数约为34.0%
3
C.20℃时加溶剂可以将N点的溶液转化成M点的溶液
D.60℃降温到20℃过程中由不饱和变为饱和,溶质质量分数变大
【答案】B
【详解】A、由图2可知,20℃时,硝酸钾的溶解度为31.6g,即该温度下,100g水中最多能溶解31.6g硝
酸钾,50g水中最多能溶解15.8g硝酸钾,所以60℃时,向50g水中加入一定量KNO 形成溶液,再降温至
3
20℃,共析出10g硝酸钾,说明加入硝酸钾的质量为15.8g+10g=25.8g,故A不符合题意;
B、t时刻,溶液刚好达到饱和,由A可知此时50g水中溶解了25.8g硝酸钾,故溶质质量分数为
,故B符合题意;
C、M点为20℃时,硝酸钾的饱和溶液,N点为20℃时,硝酸钾的不饱和溶液,所以增加溶剂可将M点的
溶液转化到N点,故C不符合题意;
D、由图2可知,硝酸钾的溶解度随温度的升高而增大,由图1可知,降温过程中,一开始没有溶质析出,
说明一开始是不饱和溶液,变为饱和溶液后,有溶质析出,所以降温过程中KNO 溶液由不饱和溶液变为
3
饱和溶液,降温过程达饱和前,溶质不变,溶剂不变,溶质质量分数不变,故D不符合题意。
故选B。
3.【新考法】化学与生活
(2024·广东深圳·二模)如图是市面上一种“果蔬洗盐”的说明书和配料中两种物质的溶解度曲线,下列
说法错误的是
A.按使用方法,若用500g水配制果蔬洗盐的溶液,需要果蔬洗盐7.5g
B.20℃时,按说明书配制果蔬洗盐的溶液,可继续溶解NaCl固体
C.40℃时,100gNaCO 的饱和溶液中含NaCO 的质量为50g
2 3 2 3
D.欲将40℃时NaCO 的不饱和溶液变成饱和溶液,可采用升温的方法
2 3
【答案】C
【详解】A、由使用方法,15g果蔬洗盐加入1000g水中配成溶液,若用500g水配制果蔬洗盐的溶液,需
要果蔬洗盐7.5g,说法正确,不符合题意;
B、由图可知,20℃时,NaCl的溶解度约为34g,说明20℃时100g水中最多溶解约34gNaCl,则1000g水
中最多溶解约340gNaCl,故15g“果蔬洗盐”加入1000g20℃的水中形成的溶液是NaCl的不饱和溶液,可
以继续溶解氯化钠,说法正确,不符合题意;
C、40°C时,碳酸钠的溶解度为50g,该温度下,100g水中最多能溶解50g氯化钠,则40℃时,
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
100gNaCO 的饱和溶液中含NaCO 的质量小于50g,说法错误,符合题意;
2 3 2 3
D、温度大于40°C,碳酸钠的溶解度随着温度的升高而减小,将40°C时NaCO 的不饱和溶液变成饱和溶
2 3
液,可采用升温的方法,说法正确,不符合题意。
故选C。
4.(2024·山西临汾·二模)农业上,一定溶质质量分数的KCl溶液可用来改良土壤,提高作物品质和产量。
下图为某校化学兴趣小组的实验过程,结合图表信息判断下列有关说法正确的是
A.①中搅拌可以增大氯化钾在水中的溶解度
B.②中溶液为饱和溶液
C.②中溶液的质量为70g
D.由实验③可得氢氧化钠固体溶于水时吸收热量
【答案】B
【详解】A、①中搅拌可以加快溶解速率,不能增大氯化钾在水中的溶解度,不符合题意;
B、由图可知,②中有部分溶质未溶解,故②中溶液为饱和溶液,符合题意;
C、由图可知,20℃时,在50g水中加入20g氯化钾,氯化钾部分溶解,故得到溶液的质量小于70g,不符
合题意;
D、由图可知,实验③中加入氢氧化钠固体后,未溶解的氯化钾完全溶解,由溶解度曲线图可知,氯化钾
的溶解度随温度的升高而增加,说明氢氧化钠固体溶于水放出热量,温度升高,不符合题意。
故选B。
5.【新考法】经典古籍再认识——古籍中的化学
(2024·重庆·二模)宋代《开宝本草》中记载了KNO 的提纯方法:“……所在山泽,冬月地上有霜,扫取
3
以水淋汁后,乃煎炼而成”。下列说法不正确的是
A.“冬月地上有霜”中的霜是指KNO 晶体 B.KNO 的溶解度受温度变化的影响很小
3 3
C.“扫取以水淋汁”类似于实验室中溶解的操作 D.“煎炼而成”是指蒸发结晶
【答案】B
【详解】A、硝酸钾的溶解度受温度影响较大,温度低,会析出KNO 晶体,故A正确;
3
B、KNO 的溶解度随温度升高而增大,随温度降低而减小,溶解度受温度变化的影响很大,故B错误;
3
C、“扫取以水淋汁”是溶解,将硝酸钾溶于水,形成溶液,故C正确;
D、“煎炼而成”是指蒸发结晶,得到硝酸钾晶体,故D正确。
故选B。
6.(2024·河北邯郸·二模)不同温度时,向盛有 水的烧杯中缓慢加入固体M,测得溶液质量与加入溶
14关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
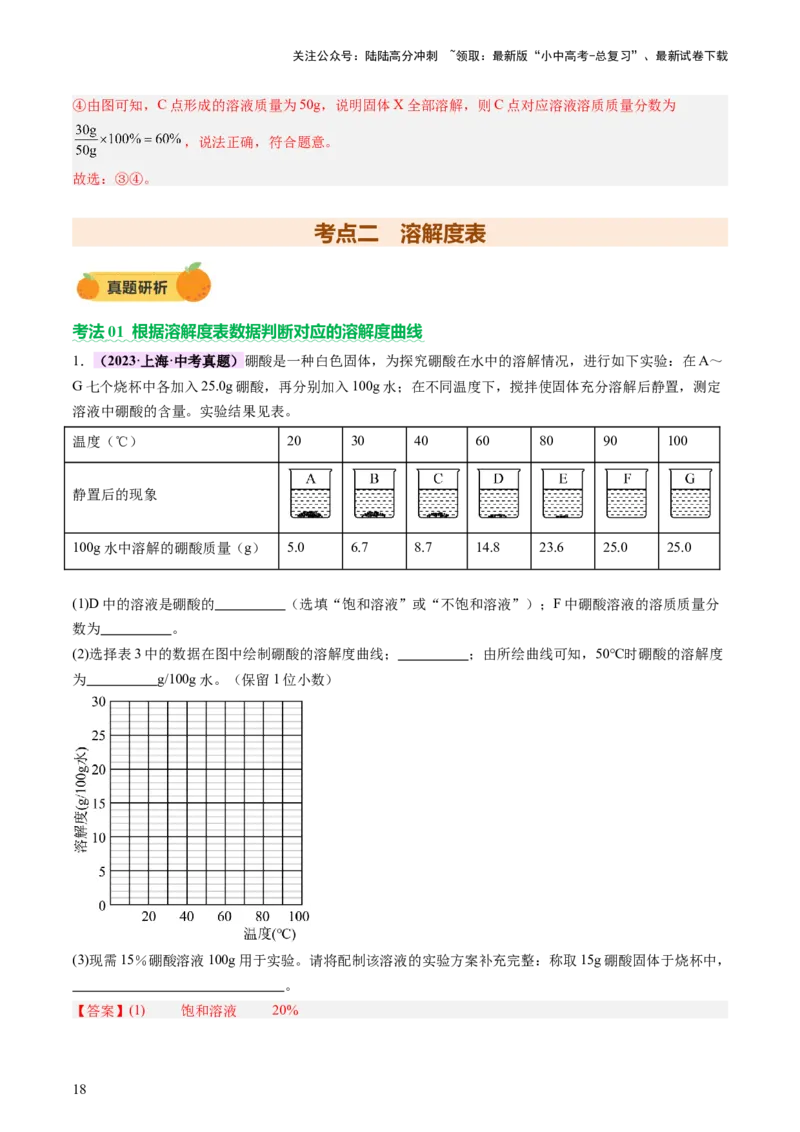
质M的质量的变化关系如图。下列说法不正确的是
A.由图象可知,M物质的溶解度随温度的升高而降低
B. 时,A、B、C三点所示溶液中属于饱和溶液的是C
C. 时,M物质的溶解度是
D.B、D点所示溶液的溶质质量分数相同
【答案】C
【详解】A、在不同温度下,向盛有50g水的烧杯中缓慢加入固体M,至B、C点溶液质量不再发生改变,
20℃时得到饱和溶液的质量>30℃时得到饱和溶液的质量,说明20℃50g水中达到饱和状态溶解的固体的
质量>30℃50g水中达到饱和状态溶解的固体的质量,说明溶质M的溶解度随着温度升高而降低,故选项
说法正确;
B、20℃时,A、B、C三点溶液中至C点溶液质量不再发生改变,则属于饱和溶液的是C,A、B对应溶
液不属于饱和溶液,故选项说法正确;
C、20℃时,至C点溶液质量不再发生改变,则属于饱和溶液,则20℃50g水中达到饱和状态溶解的固体
的质量为30g,则20℃50g水中达到饱和状态溶解的固体的质量为60g,说明20°C时,M物质的溶解度是
60g,故选项说法不正确;
D、30℃时,至B点溶液质量不再发生改变,则属于饱和溶液,则30℃时50g水中达到饱和状态溶解的固
体的质量为20g,继续加入M,不会继续溶解,则B和D点均表示在30℃时的饱和溶液,溶质质量分数相
同,故选项说法正确;
故选:C。
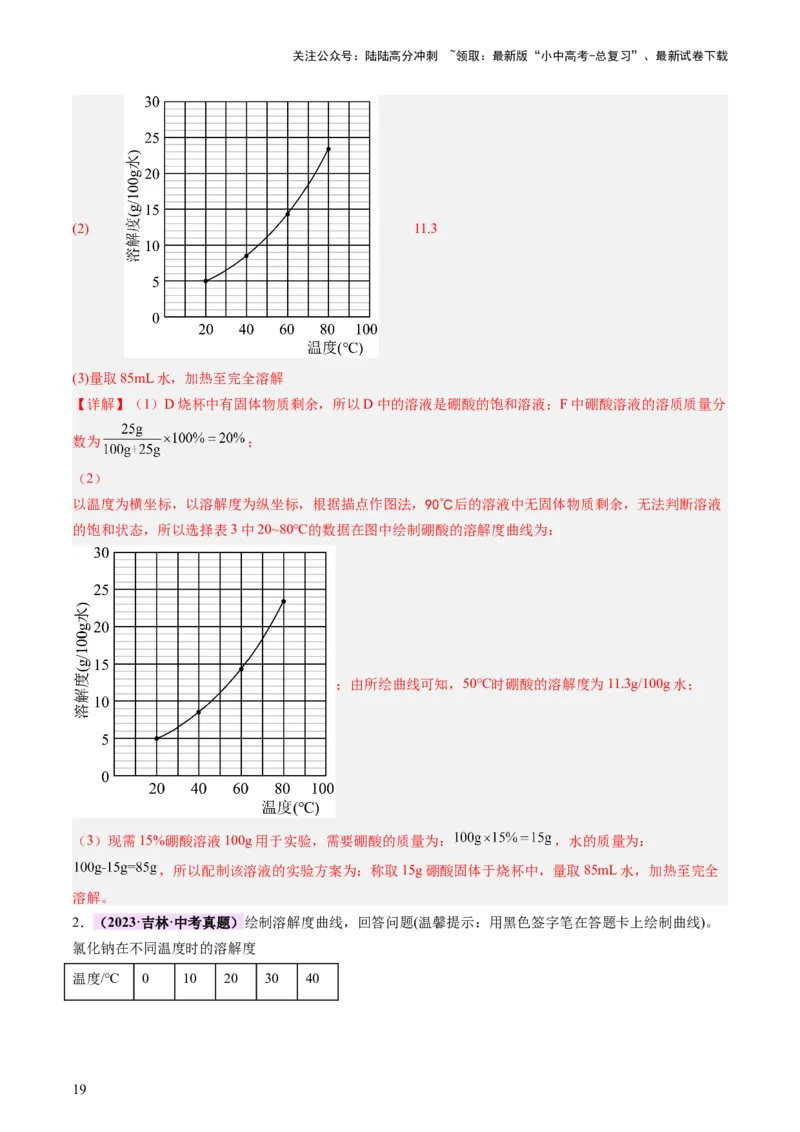
7.(2024·江苏常州·二模) 与 在水中的溶解度曲线如图一所示。
(1) ℃时,将25g 加入到50g水中,充分搅拌后所得溶液的质量为 ;
15关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(2)氯化铵样品混有少量硝酸钾,可采用 方法提纯氯化铵;
(3) ℃时将等质量的 和 的饱和溶液均降到 ℃,析出晶体的质量关系正确的是( 析出
晶体的质量为a, 析出晶体的质量为b)______(填字母):
A.ab D.不能确定
(4) ℃时,将一定量的 和 溶液分别进行恒温蒸发,蒸发水的质量与溶液质量之间的关系如图
二所示,下列说法正确的是 。(填序号)
①甲溶液是 溶液,乙溶液是 溶液
②蒸发前乙溶液为不饱和溶液
③a点对应溶液的溶质质量分数约为45.7%
④b点溶液的溶质质量分数和c点溶液溶质质量分数相等
【答案】(1)70g
(2)蒸发结晶
(3)C
(4)①②③
【详解】(1)由图可知,t℃时,硝酸钾的溶解度为40g,即该温度下,100g水中最多可溶解40g硝酸钾,
1
则该温度下,将25g硝酸钾加入到50g水中,只能溶解20g,充分搅拌后所得溶液的质量为:
20g+50g=70g;
(2)由图可知,硝酸钾、氯化铵的溶解度均随温度的升高而增加,硝酸钾的溶解度受温度影响较大,氯
化铵的溶解度受温度影响较小,故氯化铵样品中混有少量硝酸钾,可采用蒸发结晶的方法提纯氯化铵;
(3)t℃时将等质量的 KNO 和 NH Cl 的饱和溶液均降到t℃,降温后,硝酸钾和氯化铵的溶解度均减
2 3 4 1
小,均有溶质析出,且硝酸钾的溶解度受温度影响比氯化铵大,故硝酸钾析出的晶体多,即a>b。
故选C;
(4)①t℃时,将一定量的KNO 和NH Cl溶液分别进行恒温蒸发,乙溶液蒸发过程中,出现拐点,说明
2 3 4
乙溶液一开始蒸发,无晶体析出,待蒸发一定量溶剂后,开始析出晶体,故一开始乙溶液是该温度下的不
饱和溶液,而甲溶液,随着水分的蒸发,溶液质量呈直线下降,故一开始甲为该温度下的饱和溶液,由图
可知,b点时,甲溶液中溶剂质量为:60g-10g=50g,溶质质量为:75g-50g=25g,即该温度下,50g水中最
多可溶解25g甲,则t℃时,甲的溶解度为50g,则甲溶液是NH Cl溶液,乙溶液是KNO 溶液,符合题意;
2 4 3
②由①的分析可知,蒸发前乙溶液为不饱和溶液,符合题意;
③乙溶液是KNO 溶液,a点对应溶液为该温度下的饱和溶液,a点溶液中水的质量为:60g-10g=50g,溶
3
质质量为:102g-60g=42g,则a点对应溶液的溶质质量分数为: ,符合题意;
④b、c点的溶液分别为该温度下的饱和溶液,t℃时,硝酸钾的溶解度大于氯化铵,则b点氯化铵溶液的
2
溶质质量分数小于c点硝酸钾溶液溶质质量分数,不符合题意。
故选①②③。
8.(2024·陕西西安·模拟预测)将30g固体物质X(不含结晶水)投入盛有20g水的烧杯中,搅拌,测得溶
液的质量分别如图中A、B、C、D点所示。回答下列问题:
16关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)0℃时,物质X的溶解度是 。
(2)A、B、C、D四点对应的溶液中,一定属于饱和溶液的是 (填字母编号)。
(3)下列说法正确的是 (填序号)。
①t℃时,若向B点对应的烧杯中再加入30g水,搅拌,所得溶液为不饱和溶液
1
②若要从D点对应的溶液中得到全部固体X,可采用降温结晶的方法
③可依次通过蒸发浓缩、降温结晶的方法,从D点对应的溶液中提纯得到固体X
④C点对应溶液溶质质量分数为60%
【答案】(1)20g
(2)A、B
(3)③④
【详解】(1)将30g固体物质X(不含结晶水)投入盛有20g水的烧杯中,由图可知,0℃时溶液质量为
24g,则此温度下20g水最多能溶解物质X的质量是 ,则此温度下100g水中最多能溶解物质
X的质量是 ,因此0℃时,物质X的溶解度是20g;
(2)将30g固体物质X(不含结晶水)投入盛有20g水的烧杯中,由图可知,A、B点形成的溶液质量均小
于50g,说明固体X均有剩余,因此A、B点对应的溶液均为饱和溶液;C、D点形成的溶液质量均为
50g,说明固体X全部溶解,没有固体剩余,因此无法确定溶液是不是饱和溶液,因此A、B、C、D四点
对应的溶液中,一定属于饱和溶液的是A、B;
(3)①由图可知,t℃时20g水能形成32g溶液,则此温度下20g水中最多能溶解X的质量为
1
,则剩余固体的质量为 ,要使剩余固体全部溶解,至少需要水的质量为
,因此t℃时,若向B点对应的烧杯中再加入30g水,搅拌,所得溶液恰好为饱和溶液,
1
说法错误,不符合题意;
②若要从D点对应的溶液中得到全部固体X,需将水分全部蒸干,可采用蒸发结晶的方法,说法错误,不
符合题意;
③0℃时物质X的溶解度是20g,t℃时物质X的溶解度是 ,说明X的溶解度受温度变化影
1
响较大,则可依次通过蒸发浓缩、降温结晶的方法,从D点对应的溶液中提纯得到固体X,说法正确,符
合题意;
17关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
④由图可知,C点形成的溶液质量为50g,说明固体X全部溶解,则C点对应溶液溶质质量分数为
,说法正确,符合题意。
故选:③④。
考点二 溶解度表
考法 0 1 根据溶解度表数据判断对应的溶解度曲线
1.(2023·上海·中考真题)硼酸是一种白色固体,为探究硼酸在水中的溶解情况,进行如下实验:在A~
G七个烧杯中各加入25.0g硼酸,再分别加入100g水;在不同温度下,搅拌使固体充分溶解后静置,测定
溶液中硼酸的含量。实验结果见表。
温度(℃) 20 30 40 60 80 90 100
静置后的现象
100g水中溶解的硼酸质量(g) 5.0 6.7 8.7 14.8 23.6 25.0 25.0
(1)D中的溶液是硼酸的 (选填“饱和溶液”或“不饱和溶液”);F中硼酸溶液的溶质质量分
数为 。
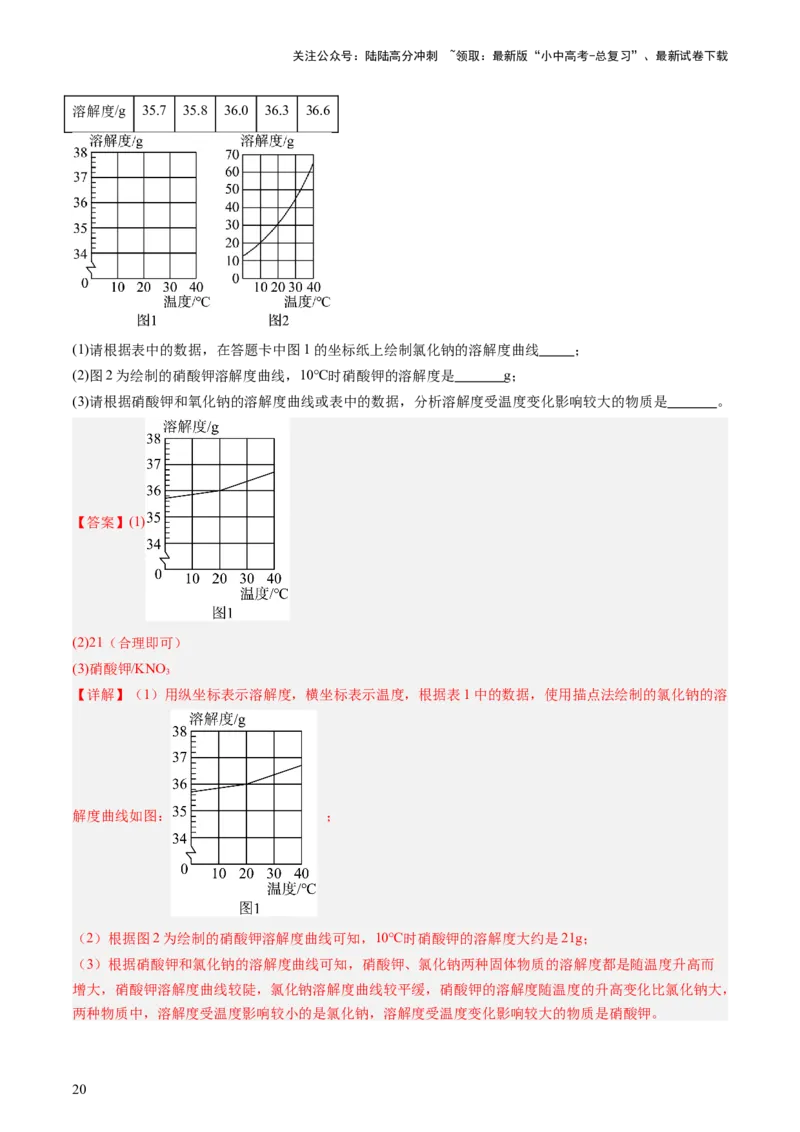
(2)选择表3中的数据在图中绘制硼酸的溶解度曲线; ;由所绘曲线可知,50℃时硼酸的溶解度
为 g/100g水。(保留1位小数)
(3)现需15%硼酸溶液100g用于实验。请将配制该溶液的实验方案补充完整:称取15g硼酸固体于烧杯中,
。
【答案】(1) 饱和溶液 20%
18关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(2) 11.3
(3)量取85mL水,加热至完全溶解
【详解】(1)D烧杯中有固体物质剩余,所以D中的溶液是硼酸的饱和溶液;F中硼酸溶液的溶质质量分
数为 ;
(2)
以温度为横坐标,以溶解度为纵坐标,根据描点作图法,90℃后的溶液中无固体物质剩余,无法判断溶液
的饱和状态,所以选择表3中20~80℃的数据在图中绘制硼酸的溶解度曲线为:
;由所绘曲线可知,50℃时硼酸的溶解度为11.3g/100g水;
(3)现需15%硼酸溶液100g用于实验,需要硼酸的质量为: ,水的质量为:
,所以配制该溶液的实验方案为:称取15g硼酸固体于烧杯中,量取85mL水,加热至完全
溶解。
2.(2023·吉林·中考真题)绘制溶解度曲线,回答问题(温馨提示:用黑色签字笔在答题卡上绘制曲线)。
氯化钠在不同温度时的溶解度
温度/℃ 0 10 20 30 40
19关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
溶解度/g 35.7 35.8 36.0 36.3 36.6
(1)请根据表中的数据,在答题卡中图1的坐标纸上绘制氯化钠的溶解度曲线 ;
(2)图2为绘制的硝酸钾溶解度曲线,10℃时硝酸钾的溶解度是 g;
(3)请根据硝酸钾和氧化钠的溶解度曲线或表中的数据,分析溶解度受温度变化影响较大的物质是 。
【答案】(1)
(2)21(合理即可)
(3)硝酸钾/KNO
3
【详解】(1)用纵坐标表示溶解度,横坐标表示温度,根据表1中的数据,使用描点法绘制的氯化钠的溶
解度曲线如图: ;
(2)根据图2为绘制的硝酸钾溶解度曲线可知,10℃时硝酸钾的溶解度大约是21g;
(3)根据硝酸钾和氯化钠的溶解度曲线可知,硝酸钾、氯化钠两种固体物质的溶解度都是随温度升高而
增大,硝酸钾溶解度曲线较陡,氯化钠溶解度曲线较平缓,硝酸钾的溶解度随温度的升高变化比氯化钠大,
两种物质中,溶解度受温度影响较小的是氯化钠,溶解度受温度变化影响较大的物质是硝酸钾。
20关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
考法 0 2 判断两种物质的溶解度相等的最小温度范围
3.(2023·黑龙江绥化·中考真题))KCl和KNO 的溶解度(见下表)和溶解度曲线(如图)。
3
温度/度 0 10 20 30 40 50 60
KNO 13.3 20.9 31.6 45.8 63.9 85.5 110
3
溶解度/g
KCl 27.6 31.0 34.0 37.0 40.0 42.6 45.5
(1)40℃时KCl饱和溶液的溶质质量分数是 (精确到0.1%)。
(2)代表KC1溶解度曲线的是 (选填“甲”或“乙”)。
(3)KC1和KNO 溶解度相等的温度范围是_______。
3
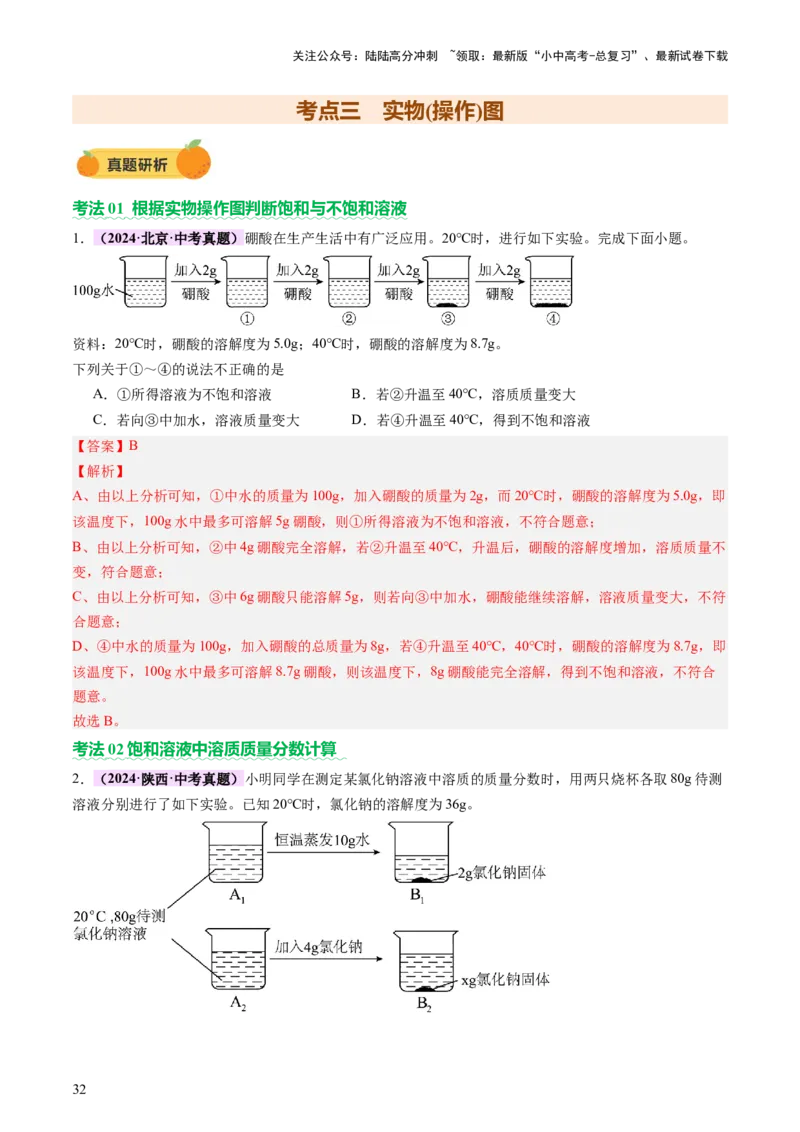
A.10度范围 B.20℃10 易溶
(1)NaCl属于 (填“易溶”或“可溶”)物质。
(2)10℃时,NaCl饱和溶液的溶质质量分数为 (列出计算式即可)。
22关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(3)生产时,向盐矿中注水制成溶液,再通过管道输回地面。冬天地面温度低于地下温度,需要输回的溶液
中NaCl的质量分数略低于地面其饱和溶液的溶质质量分数,否则易结晶导致管道堵塞(忽略管道中水分
的损失),原因是 。
(4) 又称无水芒硝,是重要的化工原料。40℃时,输回地面的溶液分离出NaCl后,剩余溶液适宜采
用 方法获得硫酸钠晶体,实现“盐硝联产”,增效环保。
【答案】(1)易溶
(2)
(3)氯化钠溶解度随温度降低而减小,降温后会从饱和溶液中析出
(4)降温结晶
【详解】(1)如图所示,20℃时氯化钠的溶解度大于10g,因此属于易容物质;
(2)根据饱和溶液的溶质质量分数= ,故10℃的氯化钠饱和溶液中溶质质量分数=
;
(3)如图所示,氯化钠的溶解度随温度的降低而减小,地面温度低,输回的氯化钠溶液到地表后氯化钠
的溶解度减小,高于地面的溶质质量分数则会导致氯化钠析出,从而会堵塞管道。故填:氯化钠溶解度随
温度降低而减小,降温后会从饱和溶液中析出;
(4)如图所示,硫酸钠的溶解度在低于40℃时受温度影响大,在分离出氯化钠后,可采用降温结晶的方
法使其大量析出。
6.(2022·重庆·中考真题)20℃时溶解度和溶解性的关系如下表,a、b、c三种物质的溶解度曲线如下图。
溶解度S 溶解性
S≥10g 易溶
10g>S≥lg 可溶
1g>S≥0.0lg 微溶
S<0.01g 难溶
(1)20℃时a、b两物质的溶解性均为 溶。
(2)c在水中的溶解度随温度的变化趋势与_______相似(填序号)。
23关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.KNO B.NaCl C.Ca(OH)
3 2
(3)某温度时,将b的饱和溶液升温 (填“一定”或“不一定”)能形成不饱和溶液。
(4)关于a、b溶液说法正确的是 (填序号)。
A. 20℃时可配制质量分数为25%的a溶液
B.使60℃的a饱和溶液析出晶体的方法不止一种
C.阴影区域(不包括b曲线上的点)对应的b溶液为饱和溶液
【答案】(1)易
(2)C
(3)不一定
(4)B
【详解】(1)由图可知,20℃时,a、b两物质的溶解度均为25g,均大于10g,溶解性均为易溶;
(2)由图可知,c的溶解度随温度的升高而减小,硝酸钾和氯化钠的溶解度均随温度的升高而增加,氢氧
化钙的溶解度随温度的升高而减小。
故选C;
(3)由图可知,b的溶解度随温度的升高先增大后减小,故某温度时,将b的饱和溶液升温,不一定能形
成不饱和溶液;
(4)A、20℃时,a的溶解度为25g,该温度下,a的饱和溶液的溶质质量分数为:
,不可能配制质量分数为25%的a溶液,不符合题意;
B、a的溶解度随温度的升高而增加,使60℃的a饱和溶液析出晶体,可采取恒温蒸发溶剂、降低温度的方
法,符合题意;
C、阴影区域(不包括b曲线上的点)在b的溶解度曲线的下方,对应的b溶液为不饱和溶液,不符合题意。
故选B。
考法 0 4 溶解度与溶质质量分数关系
7.(2024·四川内江·中考真题)表格是KNO 在不同温度下的溶解度。下列理解正确的是
3
温度/℃ 0 10 20 30 40 50
溶解度/g 13.3 20.9 31.6 45.8 63.9 85.5
A.KNO 的溶解度随温度升高而增大
3
B.稀溶液一定是不饱和溶液
C.KNO 饱和溶液的溶质质量分数一定比KNO 不饱和溶液大
3 3
D.20℃时,KNO 饱和溶液的溶质质量分数为31.6%
3
【答案】A
【详解】A、根据表格信息,KNO 的溶解度随温度升高而增大,A选项正确;
3
B、溶液的浓稀与是否饱和不存在特定关系,稀溶液不一定是不饱和溶液,B选项错误;
C、溶液的溶质质量分数大小与溶质的溶解度、溶液是否处于饱和状态这两个因素有关,所以KNO 饱和溶
3
液的溶质质量分数不一定比KNO 不饱和溶液大。根据表格信息,10℃时KNO 的溶解度为20.9g,此时饱
3 3
24关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
和KNO 溶液的溶质质量分数为 ,而50℃时KNO 的溶解度为85.5g,此时
3 3
KNO 饱和溶液的溶质质量分数为 ,则50℃时KNO 不饱和溶液的溶质质量分
3 3
数小于46.1%,但有可能大于10℃时KNO 饱和溶液的溶质质量分数,C选项错误;
3
D、根据表格信息,20℃时,KNO 的溶解度为31.6g,此时KNO 饱和溶液的溶质质量分数为
3 3
,D选项错误。
故选:A。
8.(2024·重庆·中考真题)已知KCl的溶解度随温度升高而增大,在40℃时KCl的溶解度为40g,在该温
度下,依据下表所示的数据,进行KCl溶于水的实验探究。下列说法中正确的是
实验编号 ① ② ③
KCl的质量/g 10 20 30
水的质量/g 50 60 70
A.在上述实验所得的溶液中,溶质质量分数①>②
B.实验③所得溶液中,溶质与溶剂的质量比为3:7
C.将实验②、③的溶液分别降温,一定都有晶体析出
D.将实验①、③的溶液按一定比例混合可得到与②浓度相等的溶液
【答案】D
【详解】A、在40℃时KCl的溶解度为40g,即100g水中最多能溶解40g氯化钾,则50g水中最多能溶解
氯化钾,60g水中最多能溶解 氯化钾,①中水的质量为50g,加入氯化钾
的质量为10g,可以完全溶解,得到不饱和溶液,溶质质量分数为: ,②中水的
质量为60g,加入氯化钾的质量为20g,可以完全溶解,得到不饱和溶液溶质质量分数为:
,故溶质质量分数①<②,故A说法错误;
B、在40℃时KCl的溶解度为40g,即100g水中最多能溶解40g氯化钾,则70g水中最多能溶解
氯化钾,③中水的质量为70g,加入氯化钾的质量为30g>28g,只能溶解28g氯化钾,得
到饱和溶液,则实验③所得溶液中,溶质与溶剂的质量比为28g:70g=2:5,故B说法错误;
C、由上可知,②为该温度下的不饱和溶液,③为该温度下的饱和溶液,KCl的溶解度随温度升高而增大,
将实验②、③的溶液分别降温,②不一定有晶体析出,③一定有晶体析出,故C说法错误;
D、将实验①、③的溶液按一定比例混合,即按照1:1混合,则得到的溶液中水的质量为
50g+70g=120g,加入氯化钾的质量为10g+30g=40g,可以完全溶解,溶质与溶剂的质量比为40g:
120g=1:3,②中溶质与溶剂的质量比也为20g:60g=1:3,即将实验①、③的溶液按一定比例(1:1)混
25关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
合可得到与②浓度相等的溶液,故D说法正确;
故选:D。
9.(2024·天津·中考真题)溶液与人类的生产、生活密切相关。
(1)下列物质分别放入水中,能形成溶液的是______(填序号)。
A.食盐 B.面粉 C.泥沙
(2)氯化铵和硝酸钾在不同温度时的溶解度如表。
温度/℃ 10 20 30 40 50 60 70
NH Cl 33.3 37.2 41.4 45.8 50.4 55.2 60.2
4
溶解度/g
KNO 20.9 31.6 45.8 63.9 85.5 110 138
3
①10℃时,氯化铵的溶解度为 g。
②20℃时,将20g氯化铵加入到100g水中,充分搅拌后所得溶液为 溶液(填“饱和”或“不饱和”)。
③60℃时,将60g硝酸钾溶于50g水中,充分溶解后,所得溶液的质量为 g。
④将60℃相同质量的氯化铵饱和溶液和硝酸钾饱和溶液分别降温至20℃时,析出晶体的质量:氯化铵
硝酸钾(填“大于”、“等于”或“小于”)。
⑤20℃时,向50g质量分数为12%的硝酸钾溶液中加入5g硝酸钾固体,完全溶解,所得溶液中溶质的质量
分数为 。
【答案】(1)A
(2) 33.3 不饱和 105 小于 20%
【详解】(1)A、食盐溶于水,形成溶液,故A正确;
B、面粉不溶于水,形成悬浊液,故B错误;
C、泥沙不溶于水,形成悬浊液,故C错误;
故选A;
(2)①从表中可知:10℃时,氯化铵的溶解度为33.3g;
②20℃时,氯化铵的溶解度为37.2g,即100g水中最多能溶解氯化铵37.2g,将20g氯化铵加入到100g水
中,得到不饱和溶液;
③60℃时,氯化铵的溶解度为110g,即100g水中最多能溶解氯化铵110g,将60g氯化铵加入到50g水中,
最多能溶解55g,所得溶液的质量为55g+50g=105g;
④从表中可知,硝酸钾的溶解度受温度影响变化较大,氯化铵的溶解度受温度影响变化较小,故将60℃相
同质量的氯化铵饱和溶液和硝酸钾饱和溶液分别降温至20℃时,析出晶体的质量:氯化铵小于硝酸钾;
⑤所得溶液中溶质的质量分数为 。
知识点 一 溶解度与溶解性
溶解性 易溶物质 可溶物质 微溶物质 难溶物质
26关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
20℃溶解度(g) 大于10g 10g-1g 1g-0.01g 小于0.01g
【易混易错】
物质的溶解性,是指根据20℃时的溶解度来区分,记准那分界的那三个数,10g、1g和0.01g。
知识点 二 溶解度与溶质质量分数
溶质质量分数的计算与比较
第一步:判断溶液是否饱和。
第二步:代入公式计算。
溶解度
(2)溶液饱和时其溶质质量分数: ×100%
溶解度+100g
饱和溶液中溶质的质量分数
(3)溶解度: ×100g
1−饱和溶液中溶质的质量分数
1.(2024·吉林长春·三模)2021年和2022年宇航员进行了两次太空授课,解答同学们的疑问,传播和普
及科学知识,凸显了我国蓬勃发展的航天事业!
(1)“冰雪实验”是运用结晶的原理。乙酸钠在不同温度时的溶解度如下表所示,从表中数据发现乙酸钠溶
解度的主要特点是 。
温度(℃) 10 20 30 40 50 60 70 80
溶解度(g) 40.88 46.5 54.55 65.5 83 139 153 170
(2)60℃时,向盛有50g水的烧杯中加入 g乙酸钠固体,搅拌,恰好形成饱和溶液,将其饱和溶液降温
到20℃时,可观察到的现象是 。
【答案】(1)随温度升高而增大
(2) 69.5 有固体析出
【详解】(1)由表格数据可知,乙酸钠的溶解度随温度的升高而不断增大。
(2)由表格数据可知,60℃时,乙酸钠的溶解度为139g,所以在60℃时,向盛有100g水的烧杯中加入
139g乙酸钠固体,搅拌,恰好形成饱和溶液;因乙酸钠的溶解度随温度的升高而增大,则60℃时的饱和溶
液降温到20℃时,溶解度降低,可观察到有晶体析出。
2.(2024·陕西渭南·三模)航天员在空间站进行栽培植物研究时只能是无土栽培。某无土栽培液是由硝酸
钾、硝酸钙等物质溶于水得到。下表是 在不同温度时的溶解度:
温度 0 20 40 60
27关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
13.3 31.6 63.9 110
溶解度
102 129 189 359
(1) 时,向 水中加入 固体,充分搅拌后,所得溶液中溶质与溶剂的质量比为
(填最简整数比)。
(2) 时,等质量 和 的饱和溶液, (填“ ”或“ ”)中
所含溶剂的质量较多。
(3) 时,某栽培液中物质的含量如表。该栽培液是硝酸钙的 (填“饱和”或“不饱
和”)溶液,栽培液中硝酸钾的质量分数为 。
物质 水 硝酸钾 硝酸钙 其他钾盐
5
每 栽培液所含质量 10 30 10
0
【答案】(1)3:5
(2)KNO
3
(3) 不饱和 10%
【详解】(1)40℃,硝酸钾的溶解度为63.9g,则向100g水中加入60g硝酸钾固体,硝酸钾全部溶解,则
所得溶液中溶质与溶剂的质量比为60g:100g=3:5。
(2)60℃时,溶解度:硝酸钾<硝酸钙,则等质量的饱和溶液中,硝酸钙饱和溶液中所含溶质质量较多,
则硝酸钾饱和溶液中所含溶剂较多。
(3)20℃时,硝酸钙的溶解度为139g,则50g水中最多可溶解硝酸钙的质量为 >30g,
则该栽培液是硝酸钙的不饱和溶液;
栽培液中硝酸钾的质量分数为 。
3.(2024·重庆长寿·模拟预测)溶液与人们的生活息息相关。下表是两种物质在不同温度时的溶解度:
温度/℃ 0 10 20 30 40 50
氯化钾 27.6 31.0 34.0 37.0 40.0 42.6
溶解度/g
次氯酸
22.7 26.7 34.8 50.0 52.4 56.5
钠
(1)0℃时,50g水里最多只能溶解 g氯化钾。
(2)30℃时,将30g次氯酸钠加入到装有50g水的烧杯中,充分溶解后,所得溶液的质量是 g。
(3)50℃时,将氯化钾和次氯酸钠的饱和溶液各100g分别降温至20℃,两溶液中溶质的质量大小关系是:
28关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
氯化钾 次氯酸钠(填“大于”“等于”或“小于”)。
(4)我们常用含次氯酸钠的“84”消毒液定期对教室消毒。配制1000g质量分数为0.05%的消毒液,需要质量
分数为10%的“84”消毒液 g。
【答案】(1)13.8
(2)75
(3)大于
(4)5
【详解】(1)根据表格信息,0℃时,氯化钾的溶解度为27.6g,则100g水里最多可溶解27.6g氯化钾,
所以50g水里最多只能溶解13.8g氯化钾。
(2)30℃时,次氯酸钠的溶解度为50g,则100g水中最多可溶解50g次氯酸钠,50g水中最多可溶解25g
次氯酸钠,将30g次氯酸钠加入到装有50g水的烧杯中,充分溶解后,只能溶解25g,所得溶液的质量是
。
(3)50℃时,氯化钾、次氯酸钠的溶解度分别是42.6g、56.5g,此时100g氯化钾饱和溶液中氯化钾的质
量为 ,则水的质量为 ;100g次氯酸钠溶液中次氯酸
钠的质量为 ,则水的质量为 。降温至20℃,氯化钾、
次氯酸钠的溶解度分别是34.0g、34.8g,二者溶解度都减小,都有溶质析出,所得溶液仍是饱和溶液,而
溶剂质量不变,则此时氯化钾溶液中溶质质量为 ,次氯酸钠溶液中溶质质量为
,故填:大于。
(4)稀释过程溶质质量不变,设需要的质量分数为10%的“84”消毒液质量为x,则有
,解得x=5g。
4.(2024·陕西西安·模拟预测)已知硝酸钾和氯化钠在不同温度时的溶解度如下表,请回答下列问题。
温度/℃ 0 20 40 60
溶解度
110
(1)40℃时,用 氯化钠恰好配制成氯化钠饱和溶液,需要 水,硝酸钾溶液中混有少量的氯化
钠杂质,提纯方法为 。
(2)40℃时,等质量的氯化钠和硝酸钾的饱和溶液分别降温至20℃,所得溶液中溶剂质量较大的是
(填“硝酸钾”、“氯化钠”或“无法判断”)。
(3)60℃时,对一定量的 溶液进行如图所示的操作:则烧杯 溶液中的溶质质量是 。
29关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【答案】(1) 50 冷却热饱和溶液
(2)氯化钠
(3)121
【详解】(1)40℃时,氯化钠的溶解度为36.6g,100g水中加入36.6g氯化钠形成饱和溶液,故用18.3g
氯化钠恰好配制成氯化钠饱和溶液需要50g水;
因为两物质中硝酸钾的溶解度受温度变化影响较大,氯化钠的溶解度受温度变化影响较小,硝酸钾溶液中
含有少量氯化钠杂质,提纯的方法是冷却热饱和溶液;
(2)40℃时,氯化钠的溶解度为36.6g,硝酸钾的溶解度为63.9g,饱和溶液的溶质质量分数=
,固体溶解度越大,则其饱和溶液的溶质质量分数越大,故40℃时,等质量的氯化
钠和硝酸钾的饱和溶液中,溶质质量:硝酸钾大于氯化钠,溶液质量相等,溶剂质量:氯化钠大于硝酸钾,
40℃时,等质量的氯化钠和硝酸钾的饱和溶液分别降温至20℃,两种溶液均有晶体析出,但溶剂质量不变,
故所得溶液中溶剂质量较大的是氯化钠;
(3)A烧杯溶液恒温蒸发20g水得到11g晶体和B溶液,故B溶液为60℃时KNO 饱和溶液,对B溶液降
3
温至40℃时析出46.1g晶体,60℃时硝酸钾的溶解度为110g,40℃时硝酸钾的溶解度为63.9g,
110g-63.9g=46.1g,故B烧杯内含有100g水,B烧杯内溶液质量为210g,B烧杯中溶质质量为
210g-100g=110g,A烧杯中的溶质质量为:110g+11g=121g。
5.(2024·江苏南通·模拟预测)硝酸钾和氯化钠的不同温度下的溶解度如下表。某实验残渣中含168g硝
酸钾和18g氯化钠,为回收其中的硝酸钾晶体,进行如图实验。
温度/℃ 0 20 80
硝酸钾 13.3 31.6 169.0
溶解度/g
氯化钠 35.7 36.0 38.4
有关上述实验分析不正确的是
A.溶液Z为硝酸钾的饱和溶液
B.若冷却至10℃,也能达成实验目的
C.操作a滤出的硝酸钾质量约为136.4g
30关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
D.冷却至20℃时,所得溶液中硝酸钾质量分数的计算式为:31.6g/(100g+31.6g)
【答案】D
【详解】A、20℃时,硝酸钾的溶解度为31.6g,滤液Z中水的质量为100g,氯化钠的质量为168g,则滤
液Z为硝酸钾的饱和溶液,A选项正确;
B、0℃时氯化钠的溶解度为35.7g,若冷却至10℃,所得溶液仍为氯化钠的不饱和溶液,析出的晶体只有
硝酸钾,也能达成实验目的,B选项正确;
C、由表格可知,20℃时,硝酸钾的溶解度为31.6g,氯化钠的溶解度为36.0g,冷却至20℃时得到的溶液
为氯化钠的不饱和溶液,此时100g水中只能够溶液31.6g硝酸钾,则得到的晶体是硝酸钾,质量
=168g-31.6g=136.4g,C选项正确;
D、冷却至20℃时,所得溶液为硝酸钾的饱和溶液,但氯化钠溶于水中,则其中硝酸钾质量分数的计算式
为 ,D选项错误。
故选:D。
6.(2024·河北张家口·三模)硝酸钾的溶解度如下表所示,将硝酸钾按照图3的操作进行实验,下列说法
错误的是
温度/℃ 10 20 30 40 50 60
硝酸钾溶解度/g 20.9 31.6 45.8 63.9 85.5 110.0
A.①中溶液的溶质与溶剂的质量比为31.6:100
B.将②中溶液恒温蒸发10g水后,仍为不饱和溶液
C.将③中溶液降温,一定会有硝酸钾晶体析出
D.溶液中溶质的质量分数大小关系为①<②<③
【答案】B
【详解】A、20℃时,硝酸钾的溶解度为31.6g,即20℃时,100g水中最多溶解31.6g硝酸钾,所以溶液①
是100g的水溶解了31.6g的硝酸钾,溶质与溶剂的质量比为31.6:100,故说法正确;
B、40℃时,硝酸钾的溶解度为63.9g,即40℃时,100g水中最多可以溶解63.9g硝酸钾,经等比例计算,
90g水最多可溶解57.51g硝酸钾。溶液②中加入了60g的硝酸钾,故蒸发10g水后,溶液会变为饱和溶液,
故说法错误;
C、根据实验流程,溶液③为40℃,100g的水中共计加入了63.9g的硝酸钾,为恰好饱和的状态,所以降
温一定会有晶体析出,故说法正确;
D、①②③溶液中均含100g水,分别溶解了31.6g、60g、63.9g硝酸钾,所以溶质质量分数的大小关系为
①<②<③,故说法正确。
故选B。
31关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
考点三 实物(操作)图
考法 01 根据实物操作图判断饱和与不饱和溶液
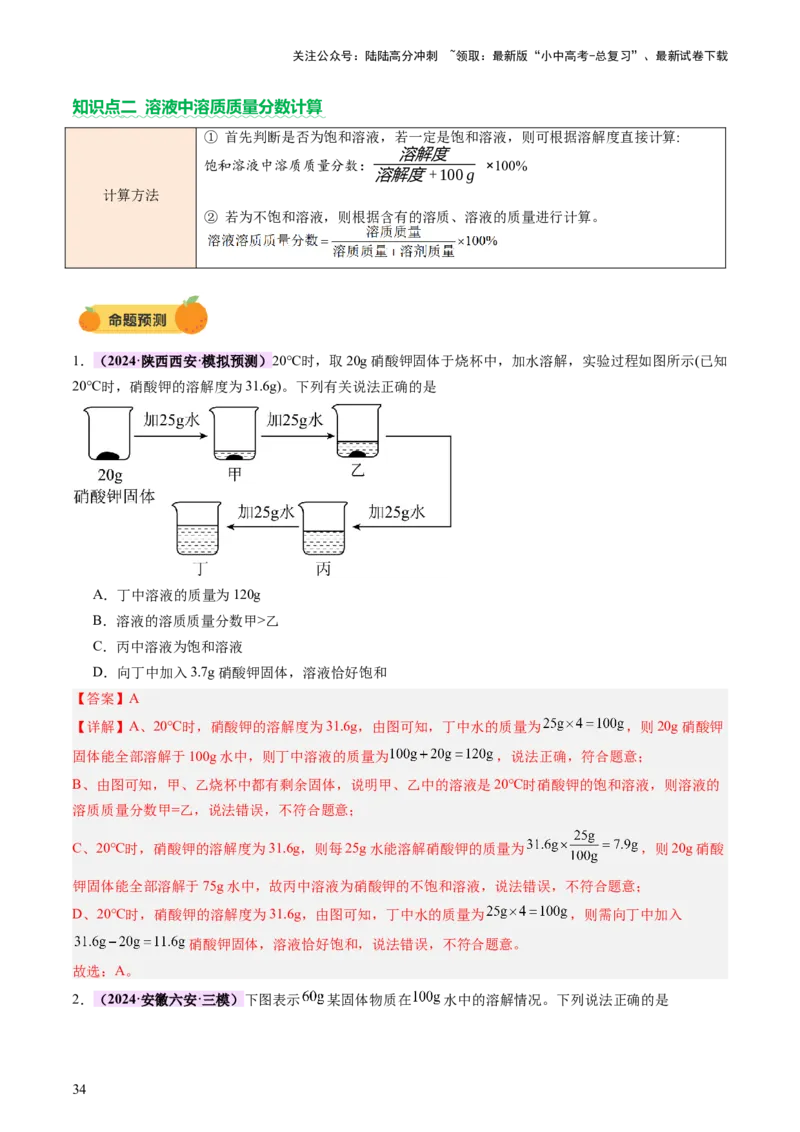
1.(2024·北京·中考真题)硼酸在生产生活中有广泛应用。20℃时,进行如下实验。完成下面小题。
资料:20℃时,硼酸的溶解度为5.0g;40℃时,硼酸的溶解度为8.7g。
下列关于①~④的说法不正确的是
A.①所得溶液为不饱和溶液 B.若②升温至40℃,溶质质量变大
C.若向③中加水,溶液质量变大 D.若④升温至40℃,得到不饱和溶液
【答案】B
【解析】
A、由以上分析可知,①中水的质量为100g,加入硼酸的质量为2g,而20℃时,硼酸的溶解度为5.0g,即
该温度下,100g水中最多可溶解5g硼酸,则①所得溶液为不饱和溶液,不符合题意;
B、由以上分析可知,②中4g硼酸完全溶解,若②升温至40℃,升温后,硼酸的溶解度增加,溶质质量不
变,符合题意;
C、由以上分析可知,③中6g硼酸只能溶解5g,则若向③中加水,硼酸能继续溶解,溶液质量变大,不符
合题意;
D、④中水的质量为100g,加入硼酸的总质量为8g,若④升温至40℃,40℃时,硼酸的溶解度为8.7g,即
该温度下,100g水中最多可溶解8.7g硼酸,则该温度下,8g硼酸能完全溶解,得到不饱和溶液,不符合
题意。
故选B。
考法 0 2 饱和溶液中溶质质量分数计算
2.(2024·陕西·中考真题)小明同学在测定某氯化钠溶液中溶质的质量分数时,用两只烧杯各取80g待测
溶液分别进行了如下实验。已知20℃时,氯化钠的溶解度为36g。
32关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)20℃时,100g水中最多溶解氯化钠的质量是 g。
(2)20℃时, 、 中的溶液是氯化钠的 (填“饱和”或“不饱和”)溶液。
(3) 、 中的溶液溶质与溶剂的质量比 (填“相等”或“不相等”)。
(4)x的值等于 。
(5)由上述实验可得出待测氯化钠溶液中溶质质量分数为 。
【答案】(1)36
(2)不饱和
(3)相等
(4)2.4g
(5)25%
【详解】(1)20℃时,氯化钠的溶解度为36g,根据溶解度概念可知,20℃时,100g水中最多溶解氯化
钠的质量是36g;
(2)20℃时,氯化钠的溶解度为36g,若A 是饱和溶液,则蒸发的10g水与析出的氯化钠固体会形成饱
1
和溶液,则析出的氯化钠固体质量= ,3.6g>2g,则A 中溶液是不饱和溶液,溶液具有均
1
一性,A 中溶液也是不饱和溶液;
2
(3)根据图示可知,B 、B 中溶液中都存在没有溶解的固体,则B 、B 都是饱和溶液,B 、B 中的溶液
1 2 1 2 1 2
溶质与溶剂的质量比相等;
(4)B 溶液的质量=80g-10g-2g=68g,则该饱和溶液中氯化钠质量= ,水的质量
1
=68g-10g=50g;则A 溶液中水的质量=50g+10g=60g,氯化钠固体质量=18g+2g=20g;溶液具有均一性,A
1 1
与A 中溶液的溶质、溶剂质量相等,20℃时,60g水最多溶解氯化钠质量= ,x的值
2
=20g+4g-21.6g=2.4g;
(5)根据第(4)小题分析可知,A 溶液中水的质量=60g,氯化钠固体质量=20g,待测氯化钠溶液中溶质
1
质量分数= 。
知识点 一 饱和与不饱和溶液的判断
① 溶液中有剩余固体,是饱和溶液;若没有剩余固体,则不一定是不饱和溶液,
也可能是刚好饱和的溶液。
判断方法
② 同一温度下,都有剩余固体,则两者溶液都为饱和溶液,且溶液中溶质的质量
分数相同。
33关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
知识点 二 溶液中溶质质量分数计算
① 首先判断是否为饱和溶液,若一定是饱和溶液,则可根据溶解度直接计算:
溶解度
饱和溶液中溶质质量分数: ×100%
溶解度+100g
计算方法
② 若为不饱和溶液,则根据含有的溶质、溶液的质量进行计算。
1.(2024·陕西西安·模拟预测)20℃时,取20g硝酸钾固体于烧杯中,加水溶解,实验过程如图所示(已知
20℃时,硝酸钾的溶解度为31.6g)。下列有关说法正确的是
A.丁中溶液的质量为120g
B.溶液的溶质质量分数甲>乙
C.丙中溶液为饱和溶液
D.向丁中加入3.7g硝酸钾固体,溶液恰好饱和
【答案】A
【详解】A、20℃时,硝酸钾的溶解度为31.6g,由图可知,丁中水的质量为 ,则20g硝酸钾
固体能全部溶解于100g水中,则丁中溶液的质量为 ,说法正确,符合题意;
B、由图可知,甲、乙烧杯中都有剩余固体,说明甲、乙中的溶液是20℃时硝酸钾的饱和溶液,则溶液的
溶质质量分数甲=乙,说法错误,不符合题意;
C、20℃时,硝酸钾的溶解度为31.6g,则每25g水能溶解硝酸钾的质量为 ,则20g硝酸
钾固体能全部溶解于75g水中,故丙中溶液为硝酸钾的不饱和溶液,说法错误,不符合题意;
D、20℃时,硝酸钾的溶解度为31.6g,由图可知,丁中水的质量为 ,则需向丁中加入
硝酸钾固体,溶液恰好饱和,说法错误,不符合题意。
故选:A。
2.(2024·安徽六安·三模)下图表示 某固体物质在 水中的溶解情况。下列说法正确的是
34关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.该物质的溶解度随温度升高而减小
B.Ⅱ中溶液为该温度下的不饱和溶液
C. 时,该物质的溶解度为
D.Ⅱ中溶液溶质质量分数比Ⅲ中的小
【答案】D
【详解】A、比较Ⅱ和Ⅲ可知,在100g水中,温度越高,该物质溶解的质量越多(Ⅱ中有部分物质未溶解,
Ⅲ中物质全部溶解),所以该物质的溶解度随温度升高而增大,故选项说法错误;
B、观察图示可知,Ⅱ中有部分该物质未溶解,所以Ⅱ中的溶液是该物质在该温度(20°C)下的饱和溶液,
故选项说法错误;
C、根据图示可知,如果Ⅲ为饱和溶液,则该物质在50°C时的溶解度为60 g,如果Ⅲ为不饱和溶液,则该
物质在50°C时的溶解度大于60g,由于根据图示无法判段Ⅲ是否为饱和溶液,所以无法确定该物质在50°C
时的溶解度,故选项说法错误;
D、比较Ⅱ和Ⅲ可知,Ⅱ和Ⅲ中含有溶剂的质量相等(都为100g),Ⅱ中含有溶质的质量小于Ⅲ中含有溶
质的质量(Ⅱ中溶质质量<60 g,Ⅲ中溶质质量=60 g),所以Ⅱ中溶质质量分数比Ⅲ的小,故选项说法正
确;
故选:D。
3.(2024·湖北十堰·二模)试管内盛有20℃的饱和硝酸钾溶液,其上漂浮一小木块。如下图所示,将试管
插入烧杯内的冰水混合物中,一段时间后,下列有关说法不正确的是
A.试管内有固体析出 B.试管内溶液的质量分数变小
C.试管内溶剂的质量不变 D.小木块浸入溶液内的体积变小
【答案】D
【详解】A、硝酸钾的溶解度随着温度的降低而减小,将盛有硝酸钾饱和溶液试管插入盛有冰水混合物的
烧杯中,温度降低,硝酸钾的溶解度减小,有硝酸钾晶体析出,说法正确;
B、硝酸钾的溶解度随着温度的降低而减小,温度下降,硝酸钾溶解度下降,为降低温度后的饱和硝酸钾
溶液,此时饱和溶液的溶质质量分数减小,说法正确;
C、硝酸钾的溶解度随着温度的降低而减小,将盛有硝酸钾饱和溶液试管插入盛有冰水混合物的烧杯中,
温度降低,硝酸钾的溶解度减小,有硝酸钾晶体析出,试管内溶液中溶质的质量减小,溶剂的质量不变,
说法正确;
35关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
D、硝酸钾的溶解度随着温度的降低而减小,温度下降,硝酸钾溶解度下降,晶体析出,溶液中溶质质量
降低,溶液密度减小,根据浮力公式 ,溶液密度减小,小木块浸入溶液内的体积变大,说法错误;
故选:D。
4.(2024·陕西·三模)将粉末状白色硫酸铜晶体( )加入盛有100mL 热水的烧杯中,直至不
能继续溶解为止,得到该温度下的蓝色溶液M,接着将一小块蓝色硫酸铜晶体( )浸入烧
杯中的硫酸铜溶液中(如图所示),自然冷却至室温,观察现象(已知:硫酸铜的溶解度随温度的降低而
减小)。下列有关该实验的描述中,不合理的是
A.60℃时,蓝色溶液M 是硫酸铜的饱和溶液
B.随着温度的降低,硫酸铜溶液的质量不断减少
C.冷却至室温后,此时溶液为该温度下的不饱和溶液
D.在降温过程中,小块硫酸铜晶体N所受的浮力越来越小
【答案】C
【详解】A、将粉末状白色硫酸铜晶体(CuSO )加入盛有100mL60°C热水的烧杯中,直至不能继续溶解
4
为止,得到该温度下的蓝色溶液M,因为固体不再溶解,所以M 是硫酸铜的饱和溶液。A合理,不符合
题意;
B、由于硫酸铜的溶解度随温度的降低而减小,所以随着温度的降低,溶液M中会有晶体析出,即随着温
度的降低,硫酸铜溶液的质量不断减少。B合理,不符合题意;
C、由于硫酸铜的溶解度随温度的降低而减小,将一小块蓝色硫酸铜晶体( CuSO ⋅5HO)浸入烧杯中的
4 2
硫酸铜溶液中,自然冷却至室温,随着温度的降低,溶液M中会有晶体析出,此时溶液仍为该温度下的饱
和溶液。C不合理,符合题意;
D、由于硫酸铜的溶解度随温度的降低而减小,将一小块蓝色硫酸铜晶体( CuSO ⋅5HO)浸入烧杯中的
4 2
硫酸铜溶液中,自然冷却至室温,随着温度的降低,溶液M中会有晶体析出,在降温过程中,小块硫酸铜
晶体N质量增大,硫酸铜溶液密度变小,所受的浮力越来越小。D合理,不符合题意。
综上所述:选择C。
5.【新考法】化学与生活
(2024·辽宁抚顺·模拟预测)KNO 的溶解度随温度升高而增大。图甲是一种简易的天气预报瓶,瓶内装有
3
一定量的水和KNO 晶体,20℃环境下出现的现象如图乙所示。随外界温度的变化也会出现如图丙和丁所
3
示的现象(忽略水分的蒸发),则下列判断正确的是
36关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.从乙到丁溶质的质量逐渐变大
B.图丙中溶液一定是硝酸钾的不饱和溶液
C.乙丙丁三种情况下,外界温度最低的是丙
D.溶液中溶质的质量分数大小关系是丙>乙>丁
【答案】D
【详解】A、瓶中硝酸钾和水的质量是一定的,由图可知,丁中析出晶体最多,乙中析出晶体较少,丙中
无晶体析出,故溶液中溶质质量:丙>乙>丁,不符合题意;
B、丙中无晶体析出,可能是硝酸钾的不饱和溶液,也可能恰好饱和,不符合题意;
C、硝酸钾的溶解度随温度的升高而增大,丁中析出晶体最多,乙中析出晶体较少,丙中无晶体析出,故
乙丙丁三种情况下,外界温度最低的是丁,不符合题意;
D、由A的分析可知,溶液中溶质质量:丙>乙>丁,溶剂质量相等,则溶质质量分数:丙>乙>丁,符
合题意。
故选D。
6.(2024·山东淄博·二模)已知20℃时CuSO 的溶解度为32g。20℃时,取一定质量某CuSO 溶液于烧杯
4 4
中,按如图进行实验(整个过程中忽略溶剂损失),下列说法不正确的是
A.丁溶液一定是饱和溶液
B.CuSO 50℃时的溶解度比20℃时的大
4
C.丙中溶液溶质与溶剂的质量比为8:25
D.溶液中溶质质量分数的大小关系为丁> 丙>甲
【答案】A
【详解】A、丁中溶质完全溶解,丁可能恰好饱和,也可能是不饱和溶液,故说法错误
B、完全加热到50℃时,丙中未溶解的硫酸铜完全溶解,说明升温后,溶解度增加,故50℃时CuSO 的溶
4
解度比20℃时的大,故说法正确;
C、丙中有溶质未溶解,则丙溶液是20℃时的饱和溶液,20℃时CuSO 的溶解度为32g,故丙中溶液溶质
4
与溶剂的质量比为32g:100g=8:25,故说法正确;
D、等质量的水中,丁中溶质的质量最多,丙中其次,甲中溶质的质量最少,则溶液中溶质质量分数的大
小关系为丁>丙>甲,故说法正确。
37关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
故选A。
7.【新考法】化学与生活
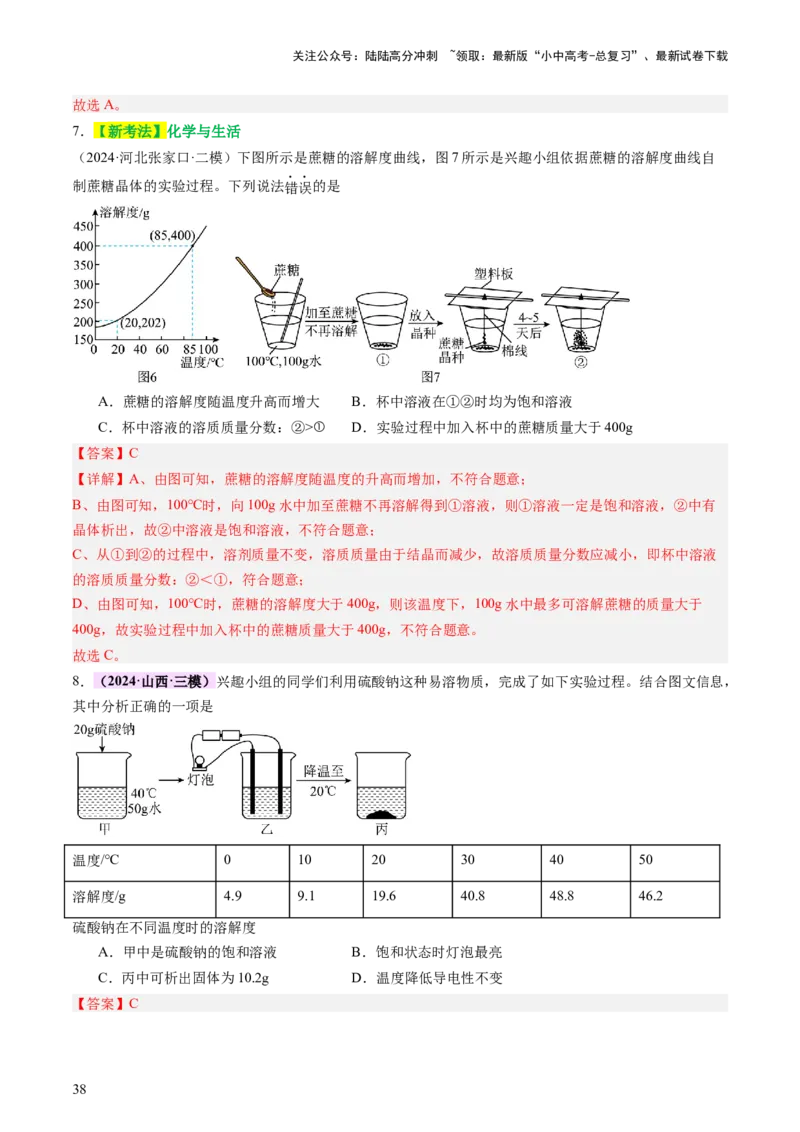
(2024·河北张家口·二模)下图所示是蔗糖的溶解度曲线,图7所示是兴趣小组依据蔗糖的溶解度曲线自
制蔗糖晶体的实验过程。下列说法错误的是
A.蔗糖的溶解度随温度升高而增大 B.杯中溶液在①②时均为饱和溶液
C.杯中溶液的溶质质量分数:②>① D.实验过程中加入杯中的蔗糖质量大于400g
【答案】C
【详解】A、由图可知,蔗糖的溶解度随温度的升高而增加,不符合题意;
B、由图可知,100℃时,向100g水中加至蔗糖不再溶解得到①溶液,则①溶液一定是饱和溶液,②中有
晶体析出,故②中溶液是饱和溶液,不符合题意;
C、从①到②的过程中,溶剂质量不变,溶质质量由于结晶而减少,故溶质质量分数应减小,即杯中溶液
的溶质质量分数:②<①,符合题意;
D、由图可知,100℃时,蔗糖的溶解度大于400g,则该温度下,100g水中最多可溶解蔗糖的质量大于
400g,故实验过程中加入杯中的蔗糖质量大于400g,不符合题意。
故选C。
8.(2024·山西·三模)兴趣小组的同学们利用硫酸钠这种易溶物质,完成了如下实验过程。结合图文信息,
其中分析正确的一项是
温度/℃ 0 10 20 30 40 50
溶解度/g 4.9 9.1 19.6 40.8 48.8 46.2
硫酸钠在不同温度时的溶解度
A.甲中是硫酸钠的饱和溶液 B.饱和状态时灯泡最亮
C.丙中可析出固体为10.2g D.温度降低导电性不变
【答案】C
38关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【详解】A、40℃时,硫酸钠的溶解度为48.8g,根据溶解度概念可知,50g水需溶解24.4g硫酸钠,达到
饱和状态,甲中水的质量是50g,硫酸钠质量是20g,得到硫酸钠的不饱和溶液,该选项分析不正确;
B、灯泡的亮度与溶液浓度有关系,浓度越大,灯泡越亮,浓度的多少与溶解度有关,该选项没有说明饱
和溶液的温度,该选项分析错误;
C、20℃时,硫酸钠的溶解度为19.6g,根据溶解度概念可知,50g水最多溶解9.8g硫酸钠,丙中析出固体
的质量=20g-9.8g=10.2g,该选项分析正确;
D、温度降低,硫酸钠的溶解度下降,有晶体析出,溶液中溶质质量减少,故导电性减弱,该选项分析错
误;
故选C。
9.(2024·山东淄博·二模)20℃时氯化钠的溶解度为36g。下图为配制某氯化钠溶液的过程,有关分析正
确的一项是
A.图1中搅拌可增大氯化钠的溶解度 B.图2中溶液为20℃氯化钠的不饱和溶液
C.图2溶液中溶质的质量分数为10% D.图2溶液由 、 构成
【答案】B
【详解】A、氯化钠的溶解度与温度有关,搅拌不能增大氯化钠的溶解度,错误;
B、20℃时,氯化钠的溶解度为36.0g,即20℃时,100g水中溶解36.0g氯化钠达到饱和状态,20℃时,图
2中溶液中,100g水中溶解了10g氯化钠,则图2中溶液为20℃氯化钠的不饱和溶液,正确;
C、图2中溶液中氯化钠的质量分数为 ×100%≈9.1%,错误;
D、氯化钠溶液中的微粒是钠离子、氯离子和水分子,错误。
故选B。
10.(2024·天津滨海新·一模)溶液与人类生产、生活密切相关。
(1)下列少量物质分别放入水中,充分搅拌,可以得到溶液的是______(填序号)。
A.植物油 B.面粉 C.食盐
(2)下列有关说法正确的是______(填序号)。
A.均一、稳定的液体都是溶液
B.某溶液中可能含有多种溶质
C.溶液均为无色透明的混合物
(3)室温下小明做了如图所示对比实验,发现B中固体消失而A中几乎没有溶解,由此可知影响溶解性的因
素有 。
39关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(4)实验室用 的硝酸银溶液配制 溶质质量分数为 的硝酸银溶液。
①配制过程有以下步骤: 。混匀 。计算 。量取 。装入试剂瓶并贴上标签,正确的操作顺序是
(填序号)。
A.bcad B.bacd C.abcd
②需要取用溶质质量分数为 的硝酸银溶液 。
(5)在室温下 实验小组按如图所示进行探究。
由此可知,图中所示A、B、C中一定为不饱和溶液的是 (填序号)。
【答案】(1)C
(2)B
(3)溶质的性质(或溶质种类)
(4) A 250
(5)C
【详解】(1)A、植物油难溶于水,不能和水形成均一、稳定的混合物,即不能够形成溶液,故选项错误;
B、面粉难溶于水,不能和水形成均一、稳定的混合物,即不能够形成溶液,故选项错误;
C、食盐易溶于水,形成均一、稳定的混合物,能形成溶液,故选项正确;
故选:C;
(2)A、均一、稳定的液体不一定都是溶液,如水是均一的、稳定的液体,但不是混合物,不是溶液,故
选项说法错误;
B、一种或几种物质分散到另一种物质中,形成均一的、稳定的混合物叫做溶液,则某溶液中可能含有多
种溶质,故选项说法正确;
C、溶液不一定均为无色透明的混合物,有些溶液是带有颜色的,如硫酸铜溶液是蓝色的,故选项说法错
误;
故选:B;
(3)图中实验,溶剂相同,溶质种类不同,发现B中固体消失而A中几乎没有溶解,说明影响溶解性的
因素是溶质的种类(或溶质的性质);
(4)①实验室用12%的硝酸银溶液配制500g溶质质量分数为6%的硝酸银溶液,采用的是加水稀释的方
法,其操作步骤是计算、量取、混匀,最后装入试剂瓶并贴上标签,故正确的操作顺序是A;
40关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
②设需要取用溶质质量分数为12%的硝酸银溶液的质量为x,根据溶液稀释前后溶质的质量不变,则
500g×6%=x×12%,x=250g;
(5)20℃时,向100g水中加入34g氯化钾,氯化钾全部溶解,则A溶液可能是恰好饱和的溶液,也可能
是不饱和溶液;再加入6g氯化钾,有氯化钾固体剩余,则B溶液为20℃时氯化钾的饱和溶液;再加入20g
水,若A溶液可能是恰好饱和的溶液,则20g水中最多能溶解氯化钾的质量为34g× =6.8g,C溶液为
不饱和溶液;若A溶液是不饱和溶液,则20g水中最多能溶解氯化钾的质量大于6.8g,C溶液为不饱和溶
液;则A、B、C中一定为不饱和溶液的是C。
41