文档内容
2025 年普通高中学业水平选择性考试
化学
可能用到的相对原子质量:H—1 C—12 N—14 O—16 F—19 S—32 Co—59 I—127
Sm—150 Pb—207
一、选择题:本题共 14小题,每小题 3分,共 42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1. 河北省古建筑数量大,历史跨度长,种类齐全,在我国建筑史上占有非常重要的地位。下列古建筑组件
主要成分属于有机物的是
A.基石 B.斗拱 C.青瓦 D.琉璃
A.A B.B C.C D.D
2. 下列不符合实验安全要求的是
A. 酸、碱废液分别收集后直接排放 B. 进行化学实验时需要佩戴护目镜
C. 加热操作时选择合适的工具避免烫伤 D. 乙醇应存放在阴凉通风处,远离火种
3. 高分子材料在生产、生活中得到广泛应用。下列说法错误的是
A.ABS高韧性工程塑料用于制造汽车零配件 B. 聚氯乙烯微孔薄膜用于制造饮用水分离膜
C. 聚苯乙烯泡沫用于制造建筑工程保温材料 D. 热固性酚醛树脂用于制造集成电路的底板
4. 设N 是阿伏加德罗常数的值,下列说法错误的是
A
A. 18gH O晶体内氢键的数目为2N
2 A
B. 1L1molL1的NaF溶液中阳离子总数为N
A
C.28g环己烷和戊烯的混合物中碳原子的数目为2N
A
D. 铅酸蓄电池负极增重96g,理论上转移电子数为2N
A
5. 下列化学用语表述正确的是
第1页/共12页
学科网(北京)股份有限公司A. 中子数为12的氖核素:22Ne B. 氯化镁的电子式:
12
C. 甲醛分子的球棍模型: D. CO2的价层电子对互斥模型:
3
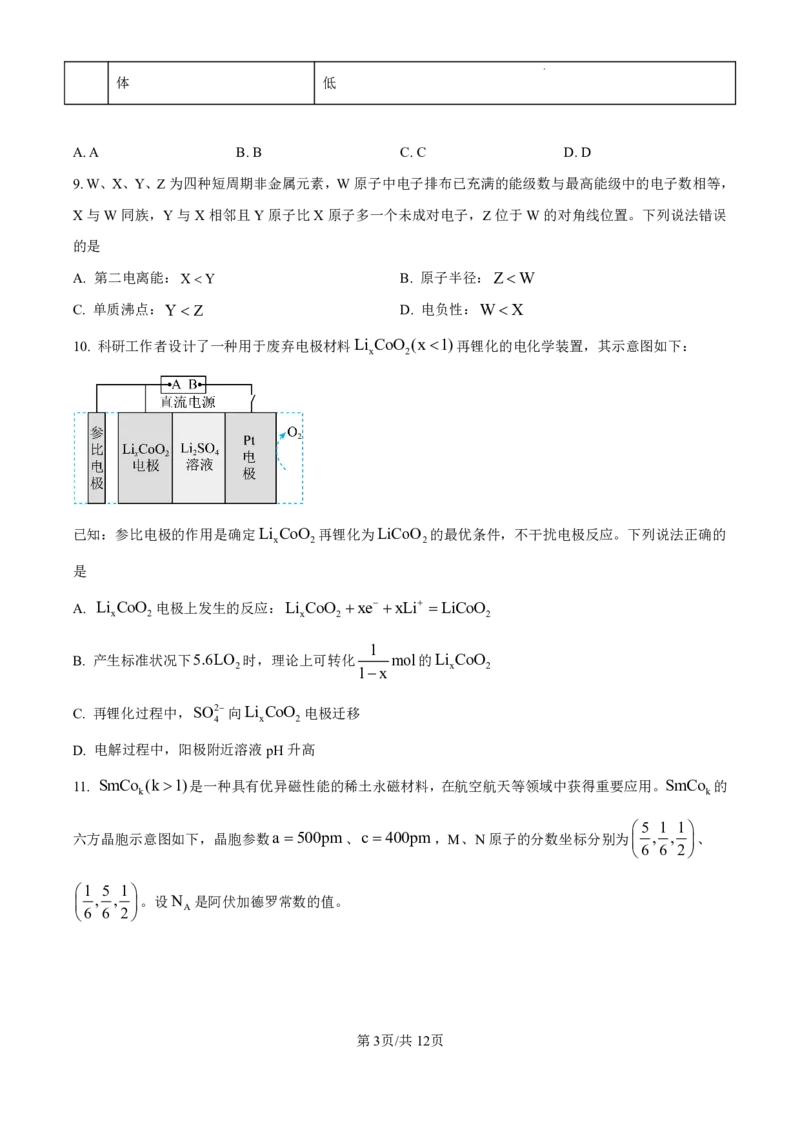
6. 丁香挥发油中含丁香色原酮(K)、香草酸(M),其结构简式如下:
下列说法正确的是
A.K中含手性碳原子 B.M中碳原子都是sp2杂化
C K、M均能与NaHCO 反应 D.K、M共有四种含氧官能团
. 3
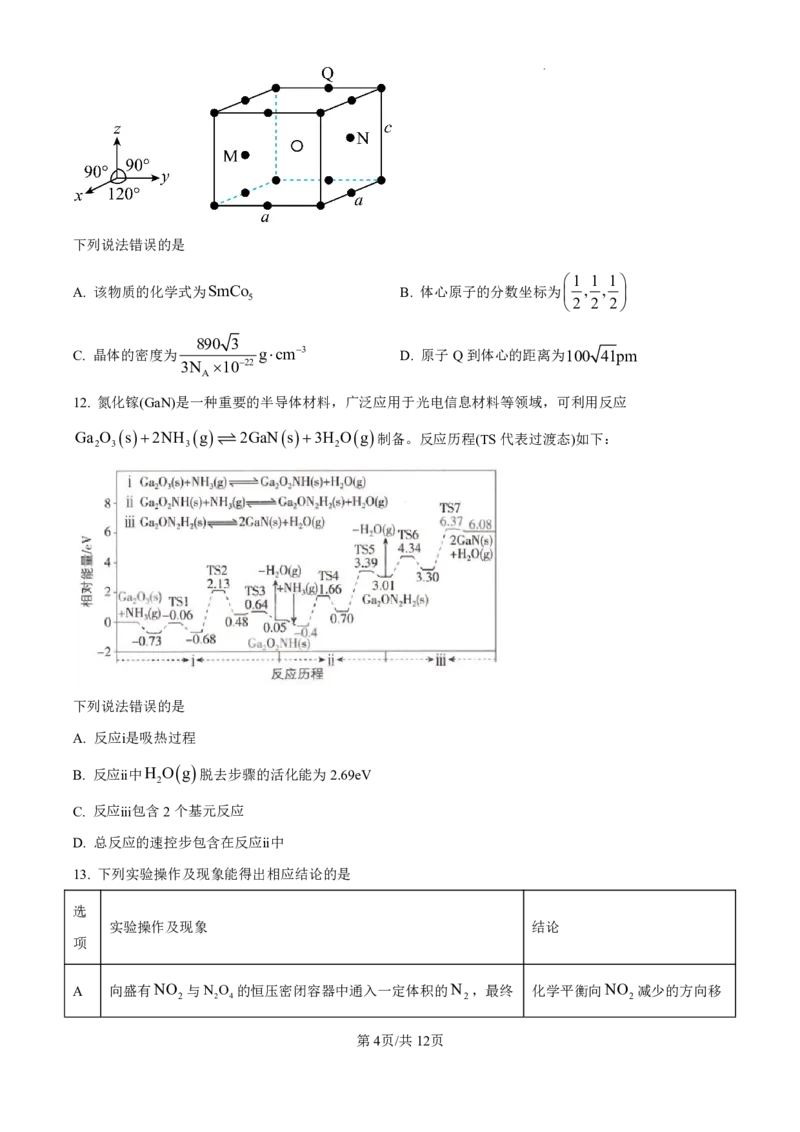
7. 如图所示装置(加热、除杂和尾气处理装置任选)不能完成相应气体的制备和检验的是
A. 电石与饱和NaCl溶液 B. Na SO 固体与70%的浓H SO
2 3 2 4
C. 大理石与稀HCl D. Al S 固体与水
2 3
8. 化学研究应当注重宏观与微观相结合。下列宏观现象与微观解释不符的是
选
宏观现象 微观解释
项
A 氮气稳定存在于自然界中 氮分子中存在氮氮三键,断开该共价键需要较多的能量
B 苯不能使溴的CCl 溶液褪色 苯分子中碳原子形成了稳定的大π键
4
C 天然水晶呈现多面体外形 原子在三维空间里呈周期性有序排列
D 氯化钠晶体熔点高于氯化铝晶 离子晶体中离子所带电荷数越少,离子半径越大,离子晶体熔点越
第2页/共12页
学科网(北京)股份有限公司体 低
A.A B.B C.C D.D
9.W、X、Y、Z为四种短周期非金属元素,W原子中电子排布已充满的能级数与最高能级中的电子数相等,
X与W同族,Y与X相邻且Y原子比X原子多一个未成对电子,Z位于W的对角线位置。下列说法错误
的是
A. 第二电离能:XY B. 原子半径:ZW
C. 单质沸点:Y Z D. 电负性:WX
10. 科研工作者设计了一种用于废弃电极材料Li CoO (x1)再锂化的电化学装置,其示意图如下:
x 2
已知:参比电极的作用是确定Li CoO 再锂化为LiCoO 的最优条件,不干扰电极反应。下列说法正确的
x 2 2
是
A. Li CoO 电极上发生的反应:Li CoO xe xLi LiCoO
x 2 x 2 2
1
B. 产生标准状况下5.6LO 时,理论上可转化 mol的Li CoO
2 1x x 2
C. 再锂化过程中,SO2向Li CoO 电极迁移
4 x 2
D. 电解过程中,阳极附近溶液pH升高
11. SmCo (k1)是一种具有优异磁性能的稀土永磁材料,在航空航天等领域中获得重要应用。SmCo 的
k k
5 1 1
六方晶胞示意图如下,晶胞参数a 500pm、c400pm,M、N原子的分数坐标分别为 , , 、
6 6 2
1 5 1
, , 。设N 是阿伏加德罗常数的值。
6 6 2 A
第3页/共12页
学科网(北京)股份有限公司下列说法错误的是
1 1 1
A. 该物质的化学式为SmCo B. 体心原子的分数坐标为 , ,
5 2 2 2
890 3
C. 晶体的密度为 gcm3 D. 原子Q到体心的距离为100 41pm
3N 1022
A
12. 氮化镓(GaN)是一种重要的半导体材料,广泛应用于光电信息材料等领域,可利用反应
Ga O
s
2NH
g
2GaN
s
3H
O
g
制备。反应历程(TS代表过渡态)如下:
2 3 3 2
下列说法错误的是
A. 反应ⅰ是吸热过程
B. 反应ⅱ中H O g 脱去步骤的活化能为2.69eV
2
C. 反应ⅲ包含2个基元反应
D. 总反应的速控步包含在反应ⅱ中
13. 下列实验操作及现象能得出相应结论的是
选
实验操作及现象 结论
项
A 向盛有NO 与N O 的恒压密闭容器中通入一定体积的N ,最终 化学平衡向NO 减少的方向移
2 2 4 2 2
第4页/共12页
学科网(北京)股份有限公司气体颜色变浅 动
以K CrO 为指示剂,用AgNO 标准溶液滴定溶液中的Cl,先
B
2 4 3
K
AgCl
K
Ag CrO
sp sp 2 4
出现白色沉淀,后出现砖红色沉淀
向盛有2mLFeCl 溶液的试管中加入过量铁粉,充分反应后静置,
3
C 滴加KSCN溶液无明显变化;静置,取上层清液滴加几滴氯水,溶 Fe2具有还原性
液变红
向盛有2mL饱和Na SO 溶液的试管中滴加鸡蛋清溶液,振荡,
2 4
D 蛋白质沉淀后活性改变
有沉淀析出;加蒸馏水稀释,再振荡,沉淀溶解
A.A B.B C.C D.D
14. 已知Cu2和L3结合形成两种配离子 CuL 和 CuL 4 常温下,0.100molL1的H L和
2 3
0.002molL1的CuSO 混合溶液中,HL2和L3的浓度对数lgc(实线)、含铜微粒的分布系数δ(虚线)[例
4
c
Cu2
如δ
Cu2
c Cu2 c CuL c CuL
4]与溶液pH的关系如图所示:
2
下列说法错误的是
A
Cu2 L3 [CuL],K109.4
.
B. HL2 H L3,K 1011.6
C. 图中a点对应的pH 4.2
第5页/共12页
学科网(北京)股份有限公司D. 当pH6.4时,体系中c HL2 c CuL 4 c CuL c L3
2
二、非选择题:本题共 4题,共 58分。
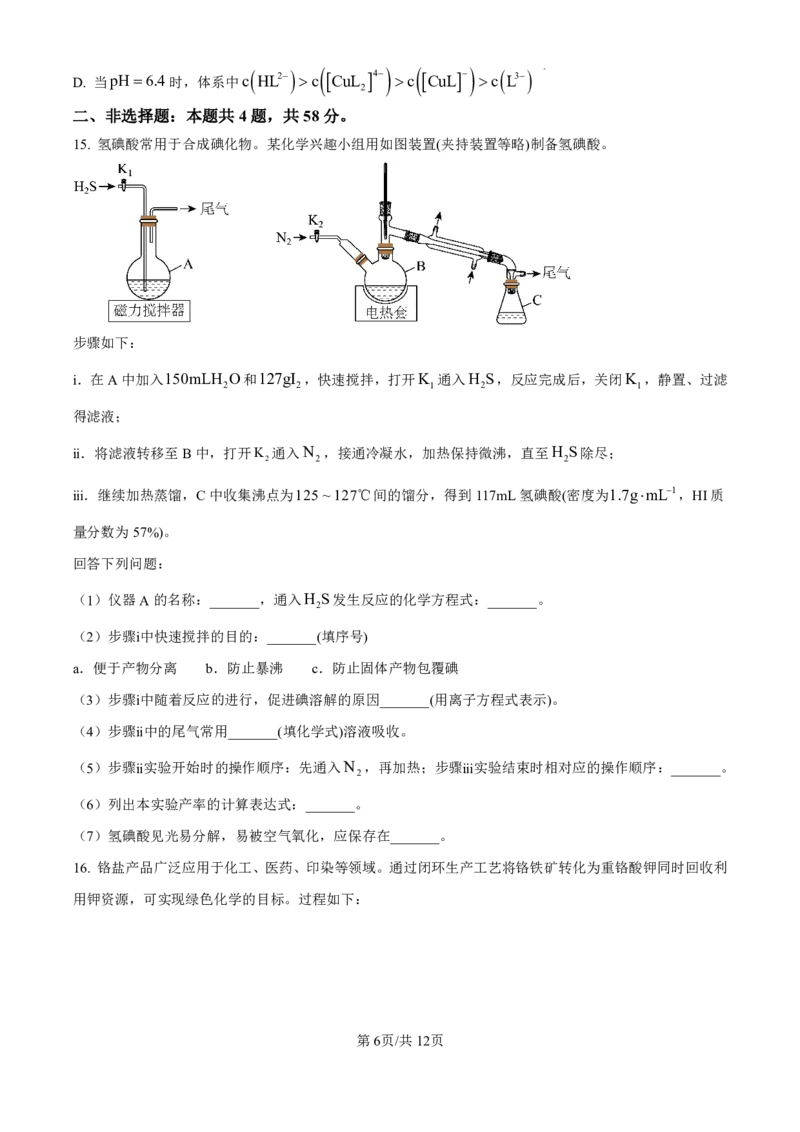
15. 氢碘酸常用于合成碘化物。某化学兴趣小组用如图装置(夹持装置等略)制备氢碘酸。
步骤如下:
ⅰ.在A中加入150mLH O和127gI ,快速搅拌,打开K 通入H S,反应完成后,关闭K ,静置、过滤
2 2 1 2 1
得滤液;
ⅱ.将滤液转移至B中,打开K 通入N ,接通冷凝水,加热保持微沸,直至H S除尽;
2 2 2
ⅲ.继续加热蒸馏,C中收集沸点为125~127℃间的馏分,得到117mL氢碘酸(密度为1.7gmL1,HI质
量分数为57%)。
回答下列问题:
(1)仪器A的名称:_______,通入H S发生反应的化学方程式:_______。
2
(2)步骤ⅰ中快速搅拌的目的:_______(填序号)
a.便于产物分离 b.防止暴沸 c.防止固体产物包覆碘
(3)步骤ⅰ中随着反应的进行,促进碘溶解的原因_______(用离子方程式表示)。
(4)步骤ⅱ中的尾气常用_______(填化学式)溶液吸收。
(5)步骤ⅱ实验开始时的操作顺序:先通入N ,再加热;步骤ⅲ实验结束时相对应的操作顺序:_______。
2
(6)列出本实验产率的计算表达式:_______。
(7)氢碘酸见光易分解,易被空气氧化,应保存在_______。
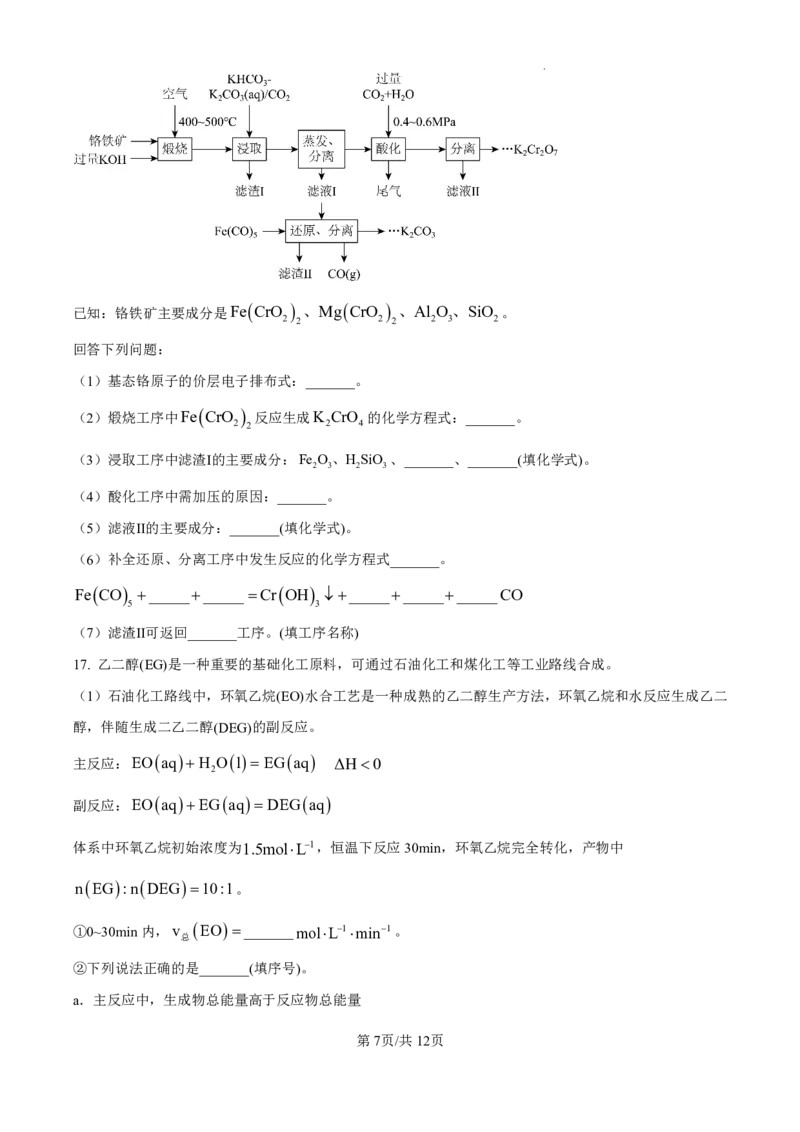
16. 铬盐产品广泛应用于化工、医药、印染等领域。通过闭环生产工艺将铬铁矿转化为重铬酸钾同时回收利
用钾资源,可实现绿色化学的目标。过程如下:
第6页/共12页
学科网(北京)股份有限公司已知:铬铁矿主要成分是Fe CrO 、Mg CrO 、Al O、SiO 。
2 2 2 2 2 3 2
回答下列问题:
(1)基态铬原子的价层电子排布式:_______。
(2)煅烧工序中Fe CrO 反应生成K CrO 的化学方程式:_______。
2 2 2 4
(3)浸取工序中滤渣Ⅰ的主要成分:Fe O、H SiO 、_______、_______(填化学式)。
2 3 2 3
(4)酸化工序中需加压的原因:_______。
(5)滤液Ⅱ的主要成分:_______(填化学式)。
(6)补全还原、分离工序中发生反应的化学方程式_______。
Fe CO __________ Cr OH _______________CO
5 3
(7)滤渣Ⅱ可返回_______工序。(填工序名称)
17. 乙二醇(EG)是一种重要的基础化工原料,可通过石油化工和煤化工等工业路线合成。
(1)石油化工路线中,环氧乙烷(EO)水合工艺是一种成熟的乙二醇生产方法,环氧乙烷和水反应生成乙二
醇,伴随生成二乙二醇(DEG)的副反应。
主反应:EO
aq
H
O
l
EG
aq
ΔH0
2
副反应:EO
aq
EG
aq
DEG
aq
体系中环氧乙烷初始浓度为1.5molL1,恒温下反应30min,环氧乙烷完全转化,产物中
n
EG
:n
DEG
10:1。
①0~30min内,v
EO
_______molL1min1。
总
②下列说法正确的是_______(填序号)。
a.主反应中,生成物总能量高于反应物总能量
第7页/共12页
学科网(北京)股份有限公司b.0~30min内,v
EO
v
EG
总 总
c.0~30min内,v
EG
:v
DEG
11:1
主 副
d.选择适当催化剂可提高乙二醇的最终产率
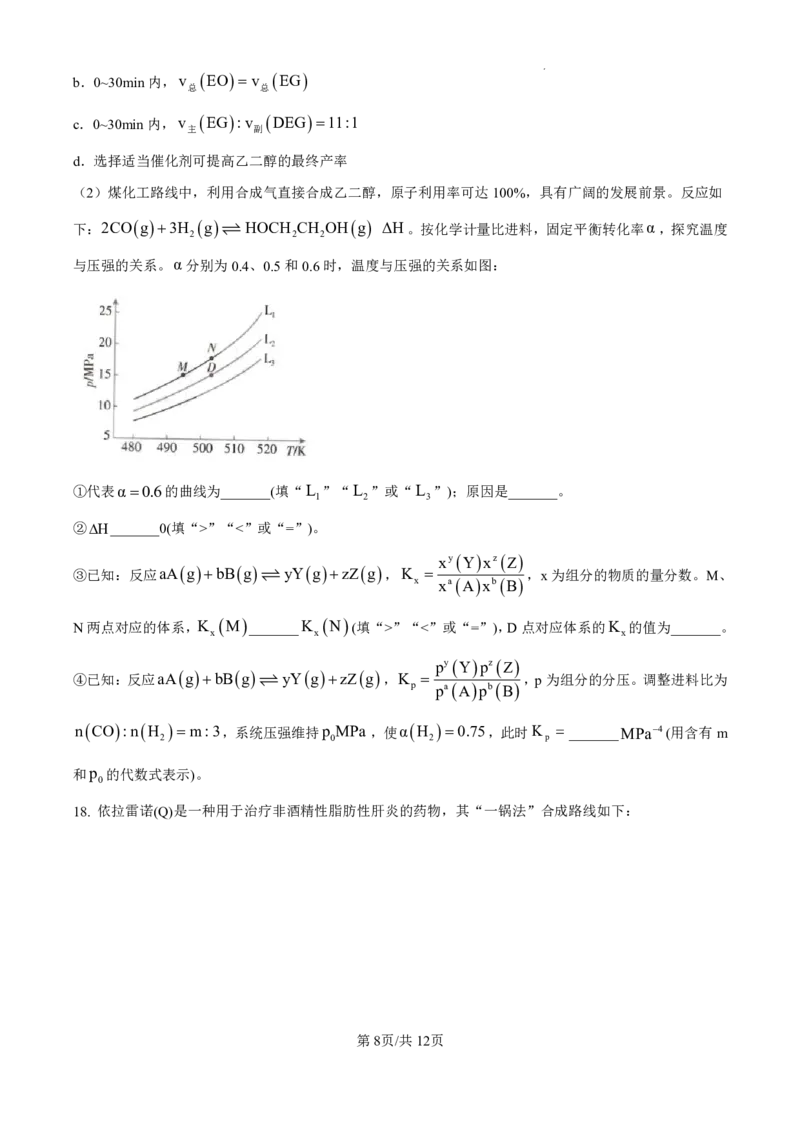
(2)煤化工路线中,利用合成气直接合成乙二醇,原子利用率可达100%,具有广阔的发展前景。反应如
下:2CO g 3H g HOCH CH OH g ΔH。按化学计量比进料,固定平衡转化率α,探究温度
2 2 2
与压强的关系。α分别为0.4、0.5和0.6时,温度与压强的关系如图:
①代表α0.6的曲线为_______(填“L ”“L ”或“L ”);原因是_______。
1 2 3
②H_______0(填“>”“<”或“=”)。
xy
Y
xz
Z
③已知:反应aA g bB g yY g zZ g ,K ,x为组分的物质的量分数。M、
x xa A xb B
N两点对应的体系,K M _______K N (填“>”“<”或“=”),D点对应体系的K 的值为_______。
x x x
py
Y
pz
Z
④已知:反应aA g bB g yY g zZ g ,K ,p为组分的分压。调整进料比为
p pa A pb B
n CO :n H m:3,系统压强维持p MPa ,使α H 0.75,此时K _______MPa4(用含有m
2 0 2 p
和p 的代数式表示)。
0
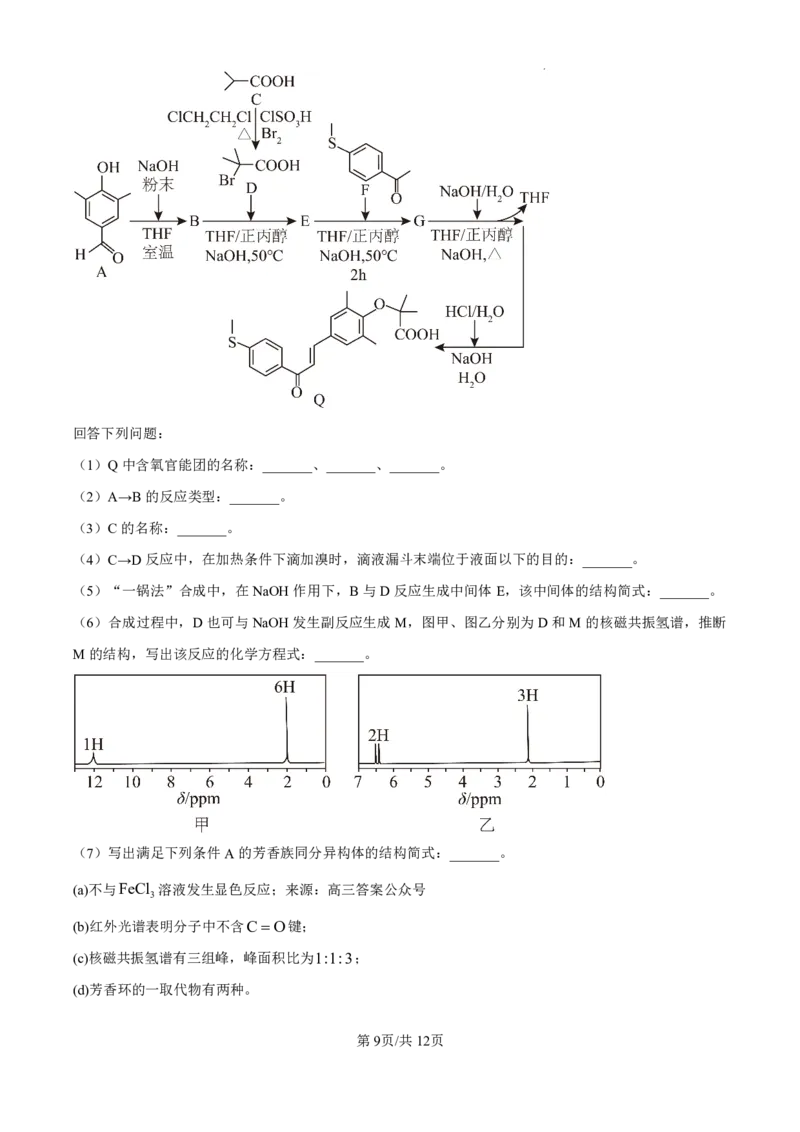
18. 依拉雷诺(Q)是一种用于治疗非酒精性脂肪性肝炎的药物,其“一锅法”合成路线如下:
第8页/共12页
学科网(北京)股份有限公司回答下列问题:
(1)Q中含氧官能团的名称:_______、_______、_______。
(2)A→B的反应类型:_______。
(3)C的名称:_______。
(4)C→D反应中,在加热条件下滴加溴时,滴液漏斗末端位于液面以下的目的:_______。
(5)“一锅法”合成中,在NaOH作用下,B与D反应生成中间体E,该中间体的结构简式:_______。
(6)合成过程中,D也可与NaOH发生副反应生成M,图甲、图乙分别为D和M的核磁共振氢谱,推断
M的结构,写出该反应的化学方程式:_______。
(7)写出满足下列条件A的芳香族同分异构体的结构简式:_______。
(a)不与FeCl 溶液发生显色反应;来源:高三答案公众号
3
(b)红外光谱表明分子中不含CO键;
(c)核磁共振氢谱有三组峰,峰面积比为1:1:3;
(d)芳香环的一取代物有两种。
第9页/共12页
学科网(北京)股份有限公司2025 年普通高中学业水平选择性考试
化学
可能用到的相对原子质量:H—1 C—12 N—14 O—16 F—19 S—32 Co—59 I—127
Sm—150 Pb—207
一、选择题:本题共 14小题,每小题 3分,共 42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
【1题答案】
【答案】B
【2题答案】
【答案】A
【3题答案】
【答案】B
【4题答案】
【答案】B
【5题答案】
【答案】C
【6题答案】
【答案】D
【7题答案】
【答案】C
【8题答案】
【答案】D
【9题答案】
【答案】A
【10题答案】
【答案】B
【11题答案】
【答案】D
【12题答案】
【答案】D
【13题答案】
第10页/共12页
学科网(北京)股份有限公司【答案】C
【14题答案】
【答案】C
二、非选择题:本题共 4题,共 58分。
【15题答案】
【答案】(1) ①. 圆底烧瓶 ②.I +H S=S+2HI
2 2
(2)c (3)I +I- I-
2 3
(4)NaOH (5)先停止加热,再通一段时间的N 后关闭K
2 2
1171.757
(6) %
128
(7)密封的棕色细口瓶中,并放在避光低温处
【16题答案】
【答案】(1)3d54s1
400500℃
(2)4Fe CrO +7O+16KOH 2Fe O +8K CrO +8H O
2 2 2 2 3 2 4 2
(3) ①. Al OH ②.MgO
3
(4)增大CO 的溶解度,保证酸化反应充分进行
2
(5)KHCO
3
(6)Fe CO K CrO 4H OCr OH Fe OH 2KOH5CO
5 2 4 2 3 3
(7)煅烧
【17题答案】
【答案】(1) ①. 0.05molL1min1 ②.cd
(2) ①. L ②. 该反应为气体体积减小的反应,温度相同时,增大压强,平衡正向移动,平衡转
1
1
化率增大 ③.< ④.= ⑤.12 ⑥. m-1.5 2 0.75 2
p MPa p MPa
m 0 m 0
【18题答案】
【答案】(1) ①. 羰基 ②. 醚键 ③. 羧基 (2)取代反应
(3)异丁酸或2-甲基丙酸
(4)溴易挥发,减少损失,提高利用率
第11页/共12页
学科网(北京)股份有限公司50°C
(5) (6) 2NaOH NaBr+2H O+
THF/正丙醇 2
(7)
第12页/共12页
学科网(北京)股份有限公司