文档内容
【基础知识】原子结构与性质
考点一 原子结构
【必备知识】
一、原子结构
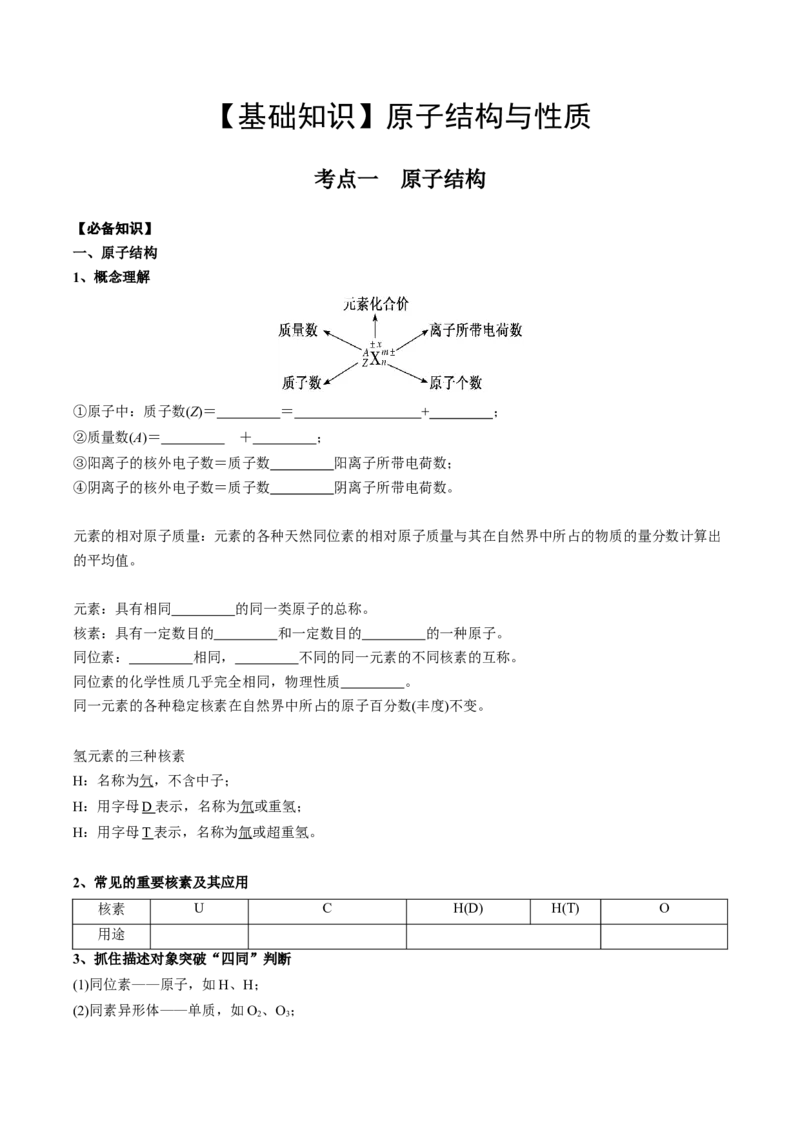
1、概念理解
①原子中:质子数(Z)= = + ;
②质量数(A)= + ;
③阳离子的核外电子数=质子数 阳离子所带电荷数;
④阴离子的核外电子数=质子数 阴离子所带电荷数。
元素的相对原子质量:元素的各种天然同位素的相对原子质量与其在自然界中所占的物质的量分数计算出
的平均值。
元素:具有相同 的同一类原子的总称。
核素:具有一定数目的 和一定数目的 的一种原子。
同位素: 相同, 不同的同一元素的不同核素的互称。
同位素的化学性质几乎完全相同,物理性质 。
同一元素的各种稳定核素在自然界中所占的原子百分数(丰度)不变。
氢元素的三种核素
H:名称为氕,不含中子;
H:用字母D 表示,名称为氘或重氢;
H:用字母T 表示,名称为氚或超重氢。
2、常见的重要核素及其应用
核素 U C H(D) H(T) O
用途
3、抓住描述对象突破“四同”判断
(1)同位素——原子,如H、H;
(2)同素异形体——单质,如O、O;
2 3(3)同系物——化合物,如CHCH、CHCHCH;
3 3 3 2 3
(4)同分异构体——化合物,如正戊烷、新戊烷。
【注意】
1、1H、2H 即不是同位素,也不同素异形体,是同种物质。
2 2
2、核变化 化学变化。
例1、完成下列表格
HO DO TO
2 2 2
相对分子质量
质子数
中子数
电子数
例2、现有下列9种微粒:H、H、C、C、N、Fe2+、Fe3+、O、O。按要求完成以下各题:
2 3
(1)H、H分别是氢元素的一种________,它们互称为________。
(2)互为同素异形体的微粒是________。
(3)Fe2+的中子数为________,核外电子数为_______________________________________。
(4)上述9种微粒中有________种核素,含有________种元素。
二、核外电子排布
1、电子排布
电子排布规则
每层最多容纳的电子数为 ,最外层不超过 个(K层为最外层时不超过 个),次外层不
超过 个。
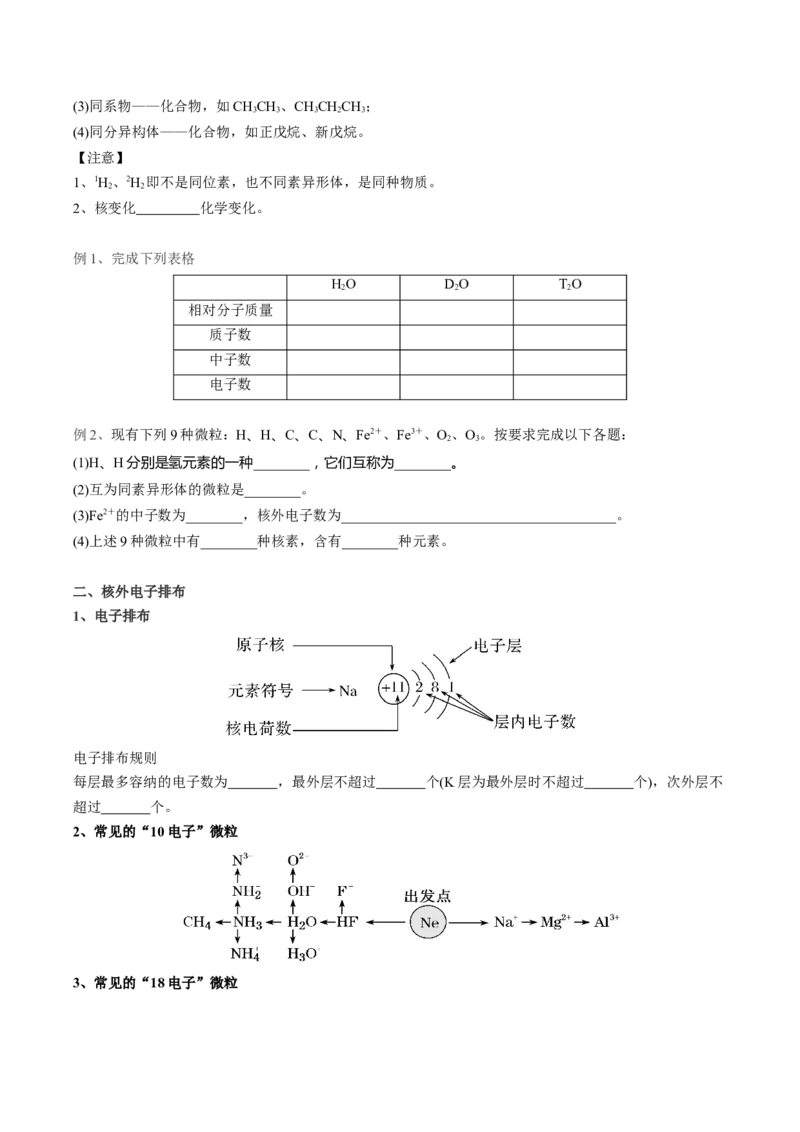
2、常见的“10电子”微粒
3、常见的“18电子”微粒例2、A+、B+、C-、D、E五种粒子(分子或离子)中,每个粒子均有10个电子,已知:
①A++C-===D+E↑;②B++C-===2D。
回答下列问题:
(1)C-的电子式是________。
(2)分别写出A+和D反应、B+和E反应的离子方程式:_____________________、_______________。
(3)除D、E外,请再写出两种含10个电子的分子的分子式:______________________。
(4)除A+、B+外,请再写出两种含10个电子的阳离子:________________________。
4、1~20号元素原子核外电子排布的特点与规律
(1)原子核中无中子的原子: 。
(2)最外层只有一个电子的原子: ;
最外层有两个电子的原子: 。
(3)最外层电子数等于次外层电子数的原子: ;
最外层电子数是次外层电子数2倍的原子: ;
最外层电子数是次外层电子数3倍的原子: 。
(4)电子层数与最外层电子数相等的原子: ;
最外层电子数是电子层数2倍的原子: ;
最外层电子数是电子层数3倍的原子: 。
(5)次外层电子数是最外层电子数2倍的原子: 。
(6)内层电子总数是最外层电子数2倍的原子: 。
(7)次外层电子数是其他各层电子总数2倍的原子: ;
(8)次外层电子数与其他各层电子总数相等的元素: 。
【易错辨析】
1、一种元素可以有多种核素,也可能只有一种核素,有多少种核素就有多少种原子。( )
2、所有原子核内一定都有中子。( )
3、质量数就是元素的相对原子质量。( )
4、质子数相同的微粒一定属于同一种元素。( )
5、核外电子数相同的微粒,其质子数一定相同。( )
6、核聚变如H+H―→He+n,因为有新微粒生成,所以该变化是化学变化。( )7、氢的三种核素形成的单质有6种,它们物理性质有所不同,但化学性质几乎完全相同。( )
8、14C可由中子轰击14N产生,14C与14N的化学性质相同。( )
9、M层电子为奇数的所有主族元素所在族的序数与该元素原子的M层电子数相等。( )
【跟踪练习】
1、《格物探源》中提到:“天地万物皆以六十四种元质配合而成,如金银铜铁养轻淡炭等皆是元质,皆
由微渺而造”,“微渺”即现代之“原子”。下列说法错误的是( )
A.“元质”即现代之“元素”,现在人类发现的化学元素已超过六十四种
B.“养、轻、淡”即“氧、氢、氮”三种元素,均为短周期主族元素
C.上文中提到的八种“元质”中,有四种金属“元质”
D.“微渺”是组成物质的基本微粒,不可再分
2、下列表示或说法正确的是( )
A.Mg2+的结构示意图: (2016·江苏) B.氯离子(Cl-)的结构示意图: (2015·江苏)
C.硫离子S2-的结构示意图: (2014·江苏) D.核外电子排布相同的微粒化学性质也相同(2014·山
东)
3、下列物质之间的相互关系不正确的是( )
A. 与 为同一种物质 B.C 、C 、金刚石、石墨互为同素异形体
60 70
C.HO、HO、HO互为同位素 D.CH 与CHCHCH 是同系物
2 2 2 4 3 2 3
4、已知R2+离子核外有a个电子,核内有b个中子.下列表示R原子符号正确的是( )
5、(2021·北京,2)下列有关放射性核素氚(H)的表述不正确的是( )
A.H原子核外电子数为1 B.H原子核内中子数为3
C.H 与H 化学性质基本相同 D.HO具有放射性
2 2 2
6、全氮类物质具有高密度、超高能量及爆轰产物清洁无污染等优点。中国科学家成功合成全氮阴离子
N,N是制备全氮类物质NN的重要中间体。下列说法中不正确的是( )
A.全氮类物质属于绿色能源 B.每个N中含有35个质子
C.每个N中含有35个电子 D.NN结构中含共价键7、(2023届河北全过程纵向评价)科学家以氘原子撞击铜的一种同位素Cu,产生了一种镍的同位素Ni,其
核反应可表示为H+Cu →Ni+α。下列说法正确的是( )
A.α粒子为He B.Cu与Ni中子数相差2
C.Ni元素的相对原子质量为61 D.1H 与2H 互为同素异形体
2 2
8、(2022·山东,3)O、O的半衰期很短,自然界中不能稳定存在。人工合成反应如下:
O+He―→O+X;O+He―→O+Y。下列说法正确的是( )
A.X的中子数为2 B.X、Y互为同位素
C.O、O可用作示踪原子研究化学反应历程 D.自然界不存在O、O 分子是因其化学键不稳定
2 2
9、(2020全国Ⅰ卷)1934年约里奥-居里夫妇在核反应中用α粒子(即氦核He)轰击金属原子X,得到核素
Y,开创了人造放射性核素的先河:X+He―→Y+n。
其中元素X、Y的最外层电子数之和为8。下列叙述正确的是( )
A.X的相对原子质量为26 B.X、Y均可形成三氯化物
C.X的质子数大于Y的 D.Y仅有一种含氧酸
10、设X、Y、Z代表元素周期表中前4周期的三种元素,已知X+和Y-具有相同的电子层结构;Z元素的
原子核内质子数比Y元素的原子核内质子数少9;Y和Z两种元素可形成含4个原子核、42个电子的负一
价阴离子。下列说法不正确的是( )
A.元素Z的气态氢化物分子中含有10个电子 B.元素Y的气态氢化物分子中含有18个电子
C.元素Z与元素X形成的化合物XZ中离子都达到稳定结构
2
D.元素Y、Z组成的化合物属于离子化合物
11、短周期主族元素X、Y、Z、R的原子序数依次增大,核电荷数之和为36;X、Z原子的最外层电子数
之和等于Y原子的次外层电子数;R原子的质子数是Y原子质子数的两倍。下列有关这四种元素的相关叙
述正确的是( )
A.X的三种核素中均含有质子和中子 B.X与R组成的化合物溶于水呈碱性
C.R的离子结构示意图为 D.Y与Z可形成两种氧化物
12、X、Y、Z、W 是四种短周期非金属元素,原子序数依次增大。 Y 、Z 原子核外 L 层的电子数之比
为3:4, 且Z 的原子半径比 Y 大, Y、Z、W 的最外层电子数之和为 16。X 的简单离子 X- 能与水反应
生成X。下列说法正确的是( )
2
A.阴离子的还原性X>Y B.最简单氢化物的沸点: W>Y
C.X与 Y 形成的化合物只有极性键 D.最高价氧化物对应的水化物酸性: Z>W13、现有五种1~18号元素X、Y、Z、M、N的性质或原子结构如下表所示:
元素编号 元素性质或原子结构
X 电子层数=最外层电子数=原子序数
Y 原子最外层电子数为a,次外层电子数为b
Z 原子L层电子数为a+b,M层电子数为a-b
M 其某种同素异形体在自然界中的硬度最大
N M层电子数是K层电子数的3倍
请回答下列问题
(1)写出X、Y、Z、N四种元素的名称:X Y Z N
(2)由X、Y、Z、M、N五种元素两两组成的分子中,许多分子含有的电子数相等,写出符合下列要求
的分子式:
①含10e-且呈正四面体结构的分子: ;②含14e-的双原子分子: ;
③含16e-且能使溴水褪色的分子: ;④含18e-且常温下呈液态的分子: 。
14、现有部分元素的原子结构特点如下表所示:
X L层电子数是K层电子数的3倍
Y 核外电子层数等于原子序数
Z L层电子数是K层和M层电子数之和
G 最外层电子数是次外层电子数的2.5倍
(1)画出G原子结构示意图:____________________________________________________。
(2)元素X与元素Z相比,非金属性较强的是______________________________________
(填元素名称),写出一个能表示X、Z非金属性强弱关系的化学方程式:_______________。
(3)X、Y、Z、G 四种元素形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为
_____________________________________________________________________________。
(4)元素X和元素Y以原子个数比为1∶1形成的化合物Q,元素G和元素Y化合形成的化合物M,Q和M
的电子总数相等。以M为燃料,Q为氧化剂,可作火箭推进剂,最终生成无毒的,且在自然界中稳定存在
的物质,写出该反应的化学方程式:________。