文档内容
(四)物质结构与性质
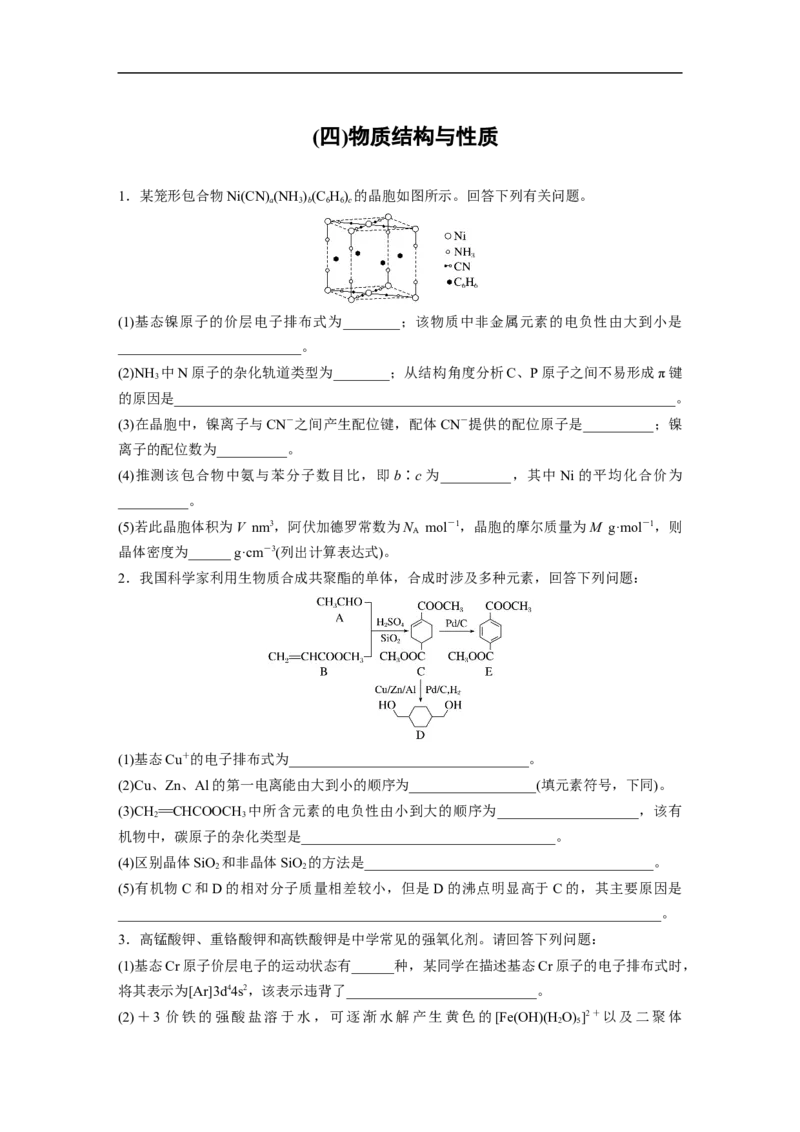
1.某笼形包合物Ni(CN) (NH )(C H) 的晶胞如图所示。回答下列有关问题。
a 3 b 6 6 c
(1)基态镍原子的价层电子排布式为________;该物质中非金属元素的电负性由大到小是
__________________________。
(2)NH 中N原子的杂化轨道类型为________;从结构角度分析C、P原子之间不易形成π键
3
的原因是_______________________________________________________________________。
(3)在晶胞中,镍离子与CN-之间产生配位键,配体CN-提供的配位原子是__________;镍
离子的配位数为__________。
(4)推测该包合物中氨与苯分子数目比,即 b∶c为__________,其中Ni的平均化合价为
__________。
(5)若此晶胞体积为V nm3,阿伏加德罗常数为N mol-1,晶胞的摩尔质量为M g·mol-1,则
A
晶体密度为______ g·cm-3(列出计算表达式)。
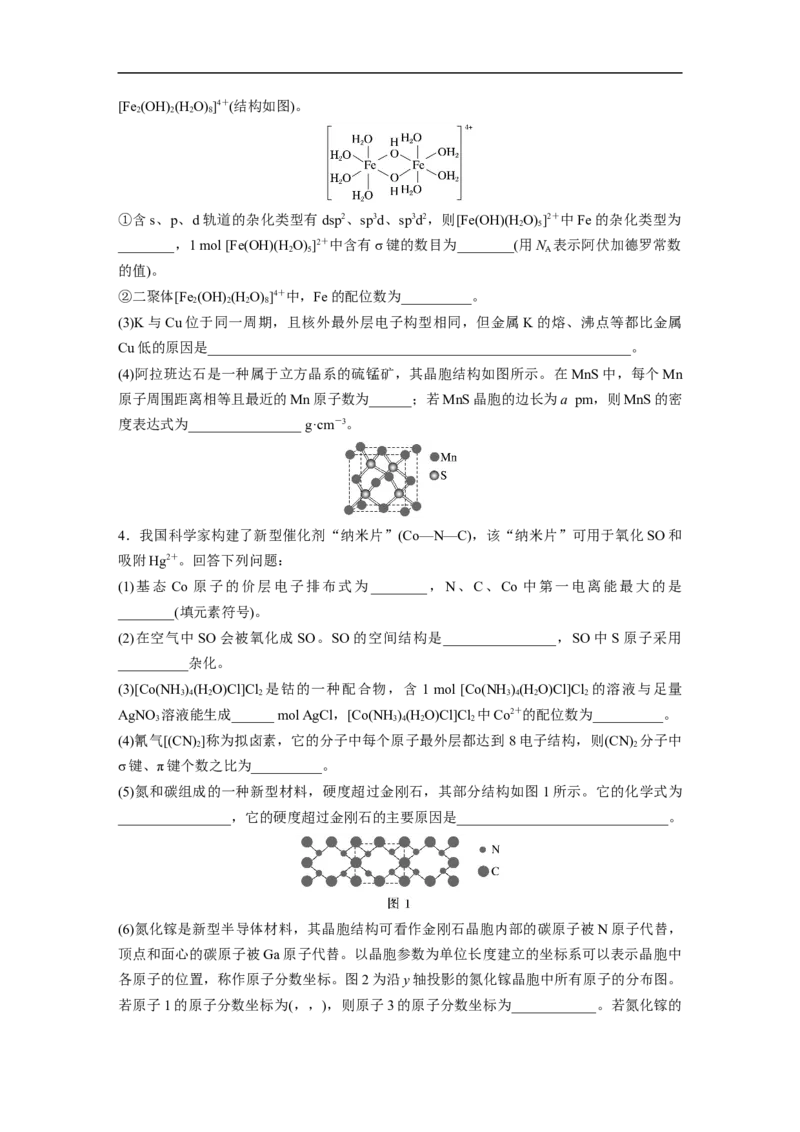
2.我国科学家利用生物质合成共聚酯的单体,合成时涉及多种元素,回答下列问题:
(1)基态Cu+的电子排布式为__________________________________。
(2)Cu、Zn、Al的第一电离能由大到小的顺序为__________________(填元素符号,下同)。
(3)CH ==CHCOOCH 中所含元素的电负性由小到大的顺序为____________________,该有
2 3
机物中,碳原子的杂化类型是____________________________________。
(4)区别晶体SiO 和非晶体SiO 的方法是_________________________________________。
2 2
(5)有机物C和D的相对分子质量相差较小,但是D的沸点明显高于C的,其主要原因是
_____________________________________________________________________________。
3.高锰酸钾、重铬酸钾和高铁酸钾是中学常见的强氧化剂。请回答下列问题:
(1)基态Cr原子价层电子的运动状态有______种,某同学在描述基态Cr原子的电子排布式时,
将其表示为[Ar]3d44s2,该表示违背了___________________________。
(2)+3 价铁的强酸盐溶于水,可逐渐水解产生黄色的[Fe(OH)(H O) ]2+以及二聚体
2 5[Fe (OH) (H O) ]4+(结构如图)。
2 2 2 8
①含s、p、d轨道的杂化类型有dsp2、sp3d、sp3d2,则[Fe(OH)(H O) ]2+中Fe的杂化类型为
2 5
________,1 mol [Fe(OH)(H O) ]2+中含有σ键的数目为________(用N 表示阿伏加德罗常数
2 5 A
的值)。
②二聚体[Fe (OH) (H O) ]4+中,Fe的配位数为__________。
2 2 2 8
(3)K与Cu位于同一周期,且核外最外层电子构型相同,但金属K的熔、沸点等都比金属
Cu低的原因是____________________________________________________________。
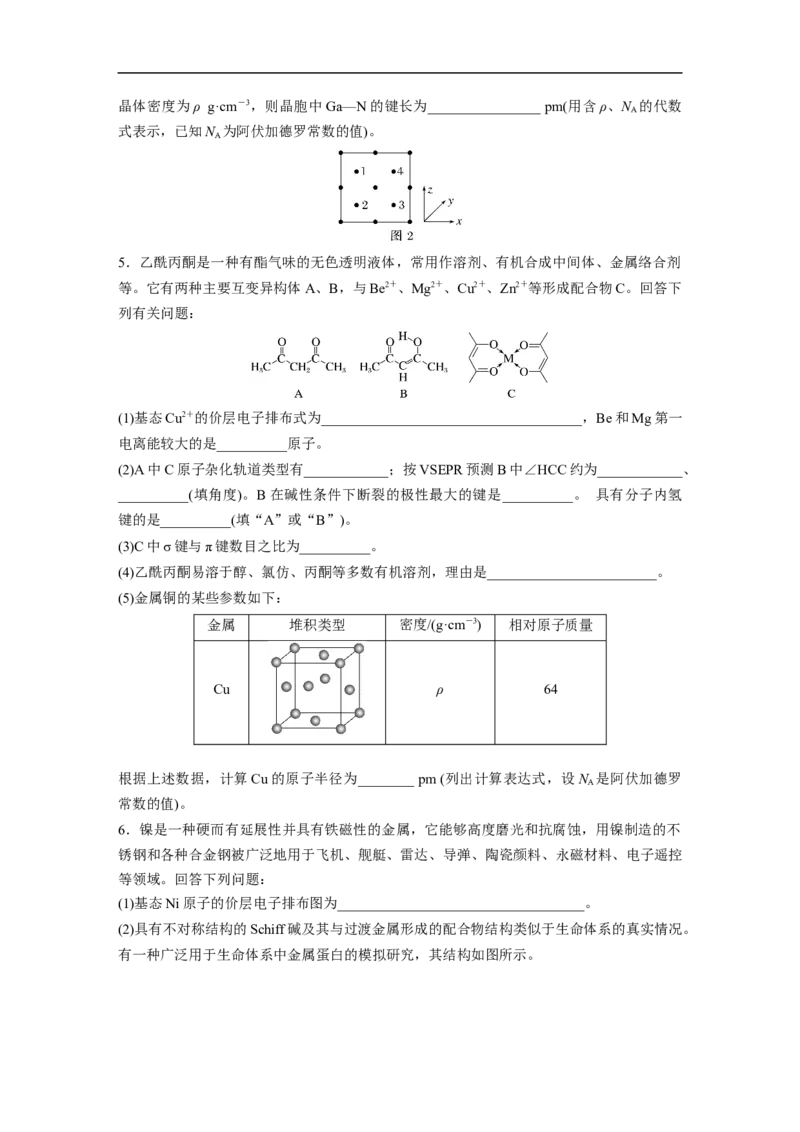
(4)阿拉班达石是一种属于立方晶系的硫锰矿,其晶胞结构如图所示。在 MnS中,每个Mn
原子周围距离相等且最近的Mn原子数为______;若MnS晶胞的边长为a pm,则MnS的密
度表达式为________________ g·cm-3。
4.我国科学家构建了新型催化剂“纳米片”(Co—N—C),该“纳米片”可用于氧化SO和
吸附Hg2+。回答下列问题:
(1)基态 Co 原子的价层电子排布式为________,N、C、Co 中第一电离能最大的是
________(填元素符号)。
(2)在空气中SO会被氧化成SO。SO的空间结构是________________,SO中S原子采用
__________杂化。
(3)[Co(NH )(H O)Cl]Cl 是钴的一种配合物,含 1 mol [Co(NH )(H O)Cl]Cl 的溶液与足量
3 4 2 2 3 4 2 2
AgNO 溶液能生成______ mol AgCl,[Co(NH )(H O)Cl]Cl 中Co2+的配位数为__________。
3 3 4 2 2
(4)氰气[(CN) ]称为拟卤素,它的分子中每个原子最外层都达到 8电子结构,则(CN) 分子中
2 2
σ键、π键个数之比为__________。
(5)氮和碳组成的一种新型材料,硬度超过金刚石,其部分结构如图1所示。它的化学式为
________________,它的硬度超过金刚石的主要原因是______________________________。
(6)氮化镓是新型半导体材料,其晶胞结构可看作金刚石晶胞内部的碳原子被N原子代替,
顶点和面心的碳原子被Ga原子代替。以晶胞参数为单位长度建立的坐标系可以表示晶胞中
各原子的位置,称作原子分数坐标。图2为沿y轴投影的氮化镓晶胞中所有原子的分布图。
若原子1的原子分数坐标为(,,),则原子3的原子分数坐标为____________。若氮化镓的晶体密度为ρ g·cm-3,则晶胞中Ga—N的键长为________________ pm(用含ρ、N 的代数
A
式表示,已知N 为阿伏加德罗常数的值)。
A
5.乙酰丙酮是一种有酯气味的无色透明液体,常用作溶剂、有机合成中间体、金属络合剂
等。它有两种主要互变异构体A、B,与Be2+、Mg2+、Cu2+、Zn2+等形成配合物C。回答下
列有关问题:
(1)基态Cu2+的价层电子排布式为_____________________________________,Be和Mg第一
电离能较大的是__________原子。
(2)A中C原子杂化轨道类型有____________;按VSEPR预测B中∠HCC约为____________、
__________(填角度)。B在碱性条件下断裂的极性最大的键是__________。 具有分子内氢
键的是__________(填“A”或“B”)。
(3)C中σ键与π键数目之比为__________。
(4)乙酰丙酮易溶于醇、氯仿、丙酮等多数有机溶剂,理由是________________________。
(5)金属铜的某些参数如下:
金属 堆积类型 密度/(g·cm-3) 相对原子质量
Cu ρ 64
根据上述数据,计算Cu的原子半径为________ pm (列出计算表达式,设N 是阿伏加德罗
A
常数的值)。
6.镍是一种硬而有延展性并具有铁磁性的金属,它能够高度磨光和抗腐蚀,用镍制造的不
锈钢和各种合金钢被广泛地用于飞机、舰艇、雷达、导弹、陶瓷颜料、永磁材料、电子遥控
等领域。回答下列问题:
(1)基态Ni原子的价层电子排布图为___________________________________。
(2)具有不对称结构的Schiff碱及其与过渡金属形成的配合物结构类似于生命体系的真实情况。
有一种广泛用于生命体系中金属蛋白的模拟研究,其结构如图所示。该配合物中C原子的杂化方式为______________________________;该配合物中除H之外
的组成元素的第一电离能由小到大的顺序是_______________________________________。
(3)二氧化硒主要用于电解锰行业,其中一种制备方法为 2NiSeO=====2NiSeO +O↑、
4 3 2
NiSeO=====NiO + SeO 。 下 列 分 子 或 离 子 的 VSEPR 模 型 为 平 面 三 角 形 的 是
3 2
____________(填字母)。
A.SeO B.SeO
C.NiO D.SeO
2
(4)草酸镍可用于制镍粉和镍的催化剂等,加热分解的化学方程式为NiC O=====NiO+CO↑
2 4
+CO↑,属于非极性分子的产物是__________,等物质的量的CO(C≡O)与CO 分子中的
2 2
π键数目之比为____________,与CO 互为等电子体(等电子体是指价电子数和原子数相同
2
的分子、离子或原子团)的阴离子为________________________(任写一种)。
(5)氢能是一种重要的二次能源,其独有的优势和丰富的资源引起人类广泛的兴趣,然而氢
的储存是目前氢能利用的一大难题,现有La、Ni合金是较为理想的储氢材料,其晶胞结构
如图所示:
①该储氢材料的化学式为__________________________________。
②已知晶胞参数边长为a nm,高为b nm,设阿伏加德罗常数的值为N ,一个晶胞内可以
A
储存18个氢原子,储氢后的晶胞密度为___________________________________g·cm-3。