文档内容
【基础知识】晶体结构与性质
考点六 常见晶体类型
【知识清单】
一、金属晶体
1、三维堆积方式
堆积模型 简单立方堆积 体心立方堆积 六方最密堆积 面心立方最密堆积
晶胞
配位数 6 8 12 12
原子半径(r)
和晶胞边长
(a)的关系
2r=a 4r=a 4r=a
一个晶胞内
1 2 2 4
原子数目
常见金属 Po Na、K、Fe Mg、Zn、Ti Cu、Ag、Au
空间利用率 52.36% 68.05% 74.05% 74.05%
2、电子气理论
金属原子脱落下来的价电子形成遍布整块晶体的“电子气”,被所有原子共用,从而把所有金属原子维系
在一起。
3、金属通性(用电子气理论解释)
通性 解释
导电性 通常情况下金属晶体内部电子的运动是自由的,但在外加电场的作用下会定向移动形成电
流。
导热性 金属受热时,自由电子与金属离子(金属原子)的碰撞频率增加,自由电子把能量传给金属
离子(或金属原子)从而把能量从温度高的区域传到温度低得区域。
延展性 由于金属键没有方向性,在外力作用下,金属原子之间发生相对滑动以后,各层金属原子仍可保持这种相互作用,发生形变也不易断裂。
有金属 当光线投射到金属表面时,自由电子吸收可见光,然后又把各种波长的光大部分再反射出
光泽 来,使绝大多数金属呈现银灰色或银白色光泽。而金属在粉末状态时,金属原子的取向杂
乱,排列不规则,吸收可见光后不能再反射出来,所以金属粉末常呈暗灰色或黑色。
思考1:为什么合金的硬度比纯金属大?
解析:纯金属内原子排列十分规整,当向金属晶体中掺入不同的金属或非金属原子,合金原子层之间相对
滑动变得困难。
思考2:为什么加热后金属电阻变大?
解析:加热后金属原子热运动加快,对自由电子的移动造成阻碍,故电阻变大。
二、离子晶体
常见晶体类型
晶体类型 晶胞模型 考点
①在晶体中,每个Na+同时吸引6 个Cl-,每个Cl-
同时吸引6 个Na+,配位数为6。
NaCl晶胞 ②每个晶胞含4 个Na+和4 个Cl-。
①在晶体中,每个Cl-吸引8 个Cs+,每个Cs+吸引
8 个Cl-,配位数为8。
CsCl晶胞
②每个晶胞中实际拥有的Cs+有1 个,Cl-有1 个。
①在晶体中,每个Ca2+吸引8 个F-,每个F-吸引
4 个Ca2+。
CaF 晶胞 ②每个晶胞含4 个Ca2+,8 个F-。
2
①每个Zn2+周围距离最近的S2-有4 个,每个S2-周
围距离最近的Zn2+有4 个。
ZnS晶胞
②每个晶胞中实际拥有的Zn2+有4 个,S2-有4 个。
例、如图是从NaCl或CsCl晶体结构图中分割出来的部分结构图,其中属于从NaCl晶体中分割出来的结
构图是( )A.图①和图③ B.图②和图③
C.图①和图④ D.只有图④
【答案】 C
三、分子晶体
1、分子常见堆积方式
分子间作用力 堆积方式 实例
范德华力 采用密堆积,每个分子周围有12 个紧邻的分子 如C 、干冰、I、O
60 2 2
范德华力、氢键 采用非密堆积,每个分子周围紧邻的分子少于12个 如HF、NH 、冰
3
2、常见分子晶体结构分析
晶体类型 晶胞模型 考点
①冰晶体中,氢键有方向性,它的存在迫使每
个水分子与四面体顶角方向的 个相邻水分
冰的结构
子相互吸引。
模型
②1 mol H O 的冰中,最多可形成 2 mol 氢
2
(分子非
键。
密堆积形
③氢键H-O···H较长,分子间距离增大并在水
式)
分子中间留有空隙,所以固态水的密度比液态
水的小。
干冰的晶 ①每个晶胞中有4 个CO 分子,12 个原子。
2
胞 ②干冰晶体中,每个CO 分子周围等距且紧邻
2
(分子密 的CO 分子有12 个。
2
堆积形
式)
例、C 晶体的晶胞结构如图所示,下列说法正确的是( )
60
A、该晶体熔化时需克服共价键 B、晶体中1个C 分子有12个紧邻的C 分子,属于分子密堆积类型
60 60
C、1个晶胞中含有8个C 分子 D、晶体中C 分子间以范德华力结合,故C 分子的热稳定性较差
60 60 60
【答案】 B四、共价晶体
(1)金刚石
①碳原子采取 sp 3 杂化,键角为109°28′。每个碳原子与周围紧邻的4个碳原子以共价键结合成正四面体结
构,向空间伸展形成 空间网状结构 , 碳的配位数为4。
②金刚石晶胞的每个顶点和面心均有1个C原子,晶胞内部有4 个C原子,内部的C在晶胞的体对角线的
处,每个金刚石晶胞中含有8 个C原子。
③最小碳环由6 个碳原子组成,每个碳原子被12 个六元环共用。六元环中最多有4 个碳原子在同一平面。
晶体中每个碳原子数目与C-C数目之比为1:2。
(2)二氧化硅晶体。
二氧化硅是自然界含量最高的固态二元氧化物,有多种结构,最常见的是低温石英(αSiO)。低温石英的结
2
构中有顶角相连的硅氧四面体形成螺旋上升的长链,没有封闭的环状结构,这一结构决定了它具有手性。
①Si原子采取sp3杂化,正四面体内O—Si—O键角为109°28′。
②每个Si原子与4 个O原子形成4个共价键,Si原子位于正四面体的中心,O原子位于正四面体的顶点,
同时每个O原子被2 个硅氧正四面体共用,晶体中Si原子与O原子个数比为1∶2,硅的配位数4,氧的配
位数2。
③最小环上有12 个原子,包括6 个O原子和6 个Si原子。
③1 mol SiO 晶体中含Si—O数目为 4 N 。
2 A
④SiO 晶胞中有8 个Si原子位于立方晶胞的顶点,有6 个Si原子位于立方晶胞的面心,还有4 个Si原子与
2
16 个O原子在晶胞内构成4个硅氧四面体。每个SiO 晶胞中含有8 个Si原子和16 个O原子。
2
(3)碳化硅晶体①碳、硅原子都采取sp3杂化,Si—C—Si键角为109°28′。
②每个硅(碳)原子与周围紧邻的4 个碳(硅)原子以共价键结合成正四面体结构,向空间伸展形成空间网状结
构。硅或碳的配位数为4。
③最小碳环由6 个原子组成且不在同一平面内,其中包括3 个C原子和3 个Si原子。
④每个SiC晶胞中含有4 个C原子和4 个Si原子。
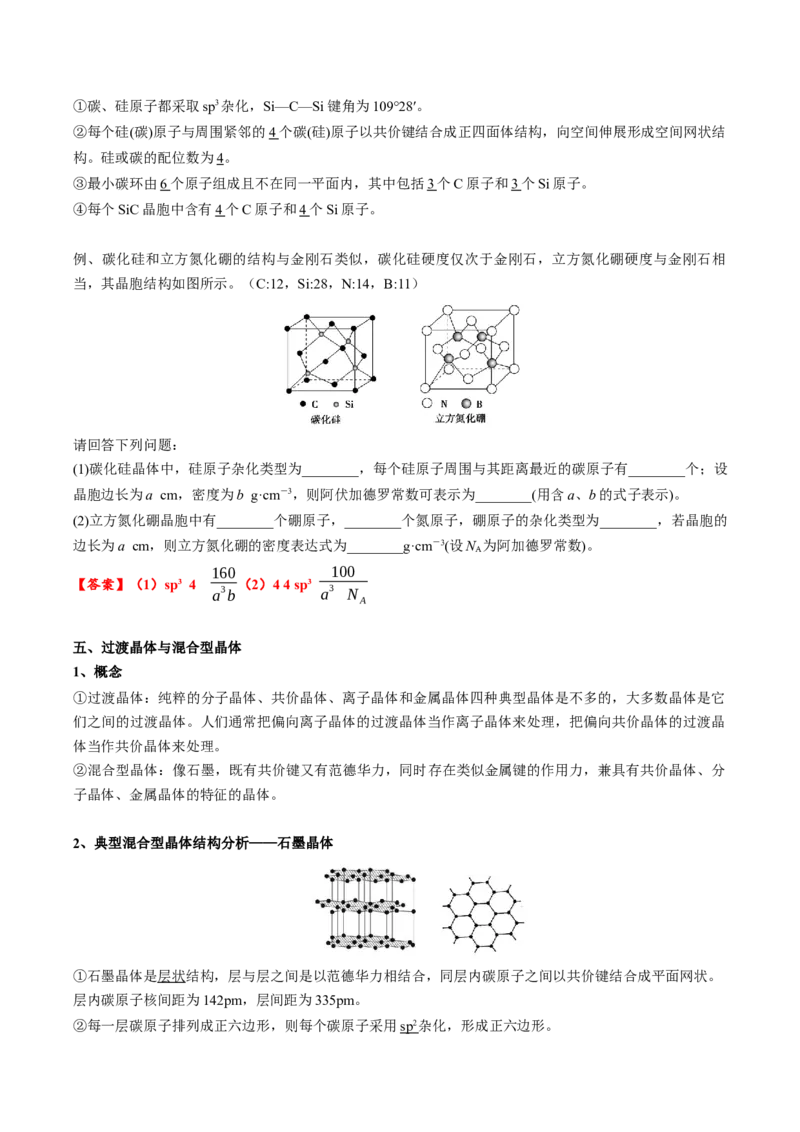
例、碳化硅和立方氮化硼的结构与金刚石类似,碳化硅硬度仅次于金刚石,立方氮化硼硬度与金刚石相
当,其晶胞结构如图所示。(C:12,Si:28,N:14,B:11)
请回答下列问题:
(1)碳化硅晶体中,硅原子杂化类型为________,每个硅原子周围与其距离最近的碳原子有________个;设
晶胞边长为a cm,密度为b g·cm-3,则阿伏加德罗常数可表示为________(用含a、b的式子表示)。
(2)立方氮化硼晶胞中有________个硼原子,________个氮原子,硼原子的杂化类型为________,若晶胞的
边长为a cm,则立方氮化硼的密度表达式为________g·cm-3(设N 为阿加德罗常数)。
A
160 100
【答案】(1)sp3 4 (2)4 4 sp3
a3b a3 N
A
五、过渡晶体与混合型晶体
1、概念
①过渡晶体:纯粹的分子晶体、共价晶体、离子晶体和金属晶体四种典型晶体是不多的,大多数晶体是它
们之间的过渡晶体。人们通常把偏向离子晶体的过渡晶体当作离子晶体来处理,把偏向共价晶体的过渡晶
体当作共价晶体来处理。
②混合型晶体:像石墨,既有共价键又有范德华力,同时存在类似金属键的作用力,兼具有共价晶体、分
子晶体、金属晶体的特征的晶体。
2、典型混合型晶体结构分析——石墨晶体
①石墨晶体是层状结构,层与层之间是以范德华力相结合,同层内碳原子之间以共价键结合成平面网状。
层内碳原子核间距为142pm,层间距为335pm。
②每一层碳原子排列成正六边形,则每个碳原子采用 sp 2 杂化,形成正六边形。③所有p轨道相互平行且相互重叠,形成离域大π键,使p轨道中的电子可在事个碳原子平面中运动,而
电子不能从一个平面跳跃到另一个平面,所以石墨的导电性只能沿石墨平面的方向。
④石墨晶体中每个正六边形含有的C原子数为2,含有的C-C键数为3。
例、氮化硼(BN)晶体有多种结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作
高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如图所示。
(1)关于这两种晶体的说法,正确的是 (填序号)。
A.立方相氮化硼含有σ键和π键,所以硬度大
B.六方相氮化硼层间作用力小,所以质地软
C.两种晶体中B-N键均为共价键
D.两种晶体均为分子晶体
(2)六方相氮化硼晶体层内一个硼原子与相邻氮原子构成的空间构型为 ,其结构与石
墨相似却不导电,原因是 。
(3)立方相氮化硼晶体,硼原子的杂化轨道类型为 。该晶体的天然矿物在青藏高原地下
约300 km在古地壳中被发现。根据这一矿物形成事实,推断实验室由六方相氮化硼合成立方相氮化硼需
要的条件应是 。
(4)NH BF(氟硼酸铵)是合成氮化硼纳米管的原料之一。1 molNH BF 含有 mol配位
4 4 4 4
键。
【答案】(1)BC (2)平面三角形 层状结构中没有自由移动的电子 (3)sp3 高温高压 (4)2
【概念辨析】
1、分子晶体不导电,溶于水后也都不导电( )
2、第三周期主族元素从左到右,最高价氧化物中离子键的百分数逐渐增大( )
3、大多数晶体是过渡晶体( )
4、共价晶体的熔点一定比离子晶体的高( )
5、金属导电是因为在外加电场作用下产生自由电子( )
6、金属具有光泽是因为金属阳离子吸收并放出可见光( )
7、过渡晶体是指某些物质的晶体通过改变条件,转化为另一种晶体( )
8、NaO是纯粹的离子晶体,SiO 纯粹的共价晶体( )
2 29、自由电子属于整块金属( )
10、金属的物理性质和金属固体的形成都与金属键有关( )
11、有阳离子的晶体一定有阴离子( )
12、金属晶体与共价晶体一样,是一种“巨分子”( )
13、金属阳离子与自由电子之间的强烈的相互作用,在一定外力作用下,不会因形变而消失( )
14、温度越高,自由电子的运动速率越快,金属的导电性越强( )
15、具有共价键的晶体叫共价晶体( )
16、金属一般具有金属光泽,是物理性质,与金属键无关( )
17、晶格能由大到小:NaF<NaCl<NaBr<NaI( )
18、高硬度、高熔点是许多有共价键三维骨架结构的共价晶体的特性( )
19、固态和熔融时易导电,熔点在1 000 ℃左右的晶体可能是金属晶体( )
20、因金属性K>Na,故金属钾的熔点高于金属钠( )
21、金属(除汞外)在常温下都是晶体,称其为金属晶体( )
【答案】 1.× 2.× 3.√ 4.× 5.× 6.× 7.× 8.× 9.√ 10.√ 11.× 12.√ 13.√ 14.× 15.× 16.×
17.× 18.√ 19.√ 20.× 21.√
【跟踪练习】
1、(2023·北京卷)中国科学家首次成功制得大面积单晶石墨炔,是碳材料科学的一大进步。
下列关于金刚石、石墨、石墨炔的说法正确的是( )
A.三种物质中均有碳碳原子间的 键 B.三种物质中的碳原子都是 杂化
C.三种物质的晶体类型相同 D.三种物质均能导电
【答案】A
【解析】A.原子间优先形成 键,三种物质中均存在 键,A项正确;
B.金刚石中所有碳原子均采用 杂化,石墨中所有碳原子均采用 杂化,石墨炔中苯环上的碳原子采
用 杂化,碳碳三键上的碳原子采用 杂化,B项错误;
C.金刚石为共价晶体,石墨炔为分子晶体,石墨为混合晶体,C项错误;
D.金刚石中没有自由移动电子,不能导电,D项错误。
2、(2021·辽宁1月适应性测试,6)我国科学家合成了富集11B的非碳导热材料立方氮化硼晶体,晶胞结构
如图。下列说法正确的是( )A.11BN和10BN的性质无差异 B.该晶体具有良好的导电性
C.该晶胞中含有14个B原子,4个N原子 D.N原子周围等距且最近的N原子数为12
【答案】 D
【解析】 11B和10B互为同位素,形成的化合物在化学性质上无差异,但其物理性质不同,A错误;该晶
体结构中无自由移动的电子,不具有导电性,B错误;由图可知,该晶胞含4个N原子,B原子位于晶胞
的顶角和面心,故B原子的数量为8×+6×=4,C错误;由晶胞示意图,1个N原子与4个B原子成键,1
个B原子可以和3个N原子成键,这些N原子距中心N原子等距离且最近,总数为12,D正确。
3、(2021·辽宁,7)单质硫和氢气在低温高压下可形成一种新型超导材料,其晶胞如图。下列说法错误的是(
)
A.S位于元素周期表p区 B.该物质的化学式为HS
3
C.S位于H构成的八面体空隙中 D.该晶体属于分子晶体
【答案】 D
【解析】S位于H构成的八面体空隙中,如图 ,C正确。该晶体为新型超导材料,说明由阴阳
离子构成,是离子晶体,D错误。
4、钒的某种氧化物的立方晶胞结构如图所示,晶胞参数为a pm。下列说法错误的是( ) (V:51 O:16)
A.该钒的氧化物的化学式为VO B.V原子在该晶体中的堆积方式为体心立方
2
C.V原子的配位数与O原子的配位数之比为1∶2 D.该晶胞的密度为 g·cm-3
【答案】 C
【解析】 晶胞中V原子位于顶角和体心,数目为1+8×=2;O原子位于上下面上和体内,数目为2+4×
=4,二者原子数目之比为1∶2,故氧化物的化学式为VO ,故A正确;晶胞V原子位于顶角和体心,符合
2
体心立方的堆积方式,故B正确;体心V原子的配位数为6,O原子的配位数为3,所以V原子的配位数与O原子的配位数之比为2∶1,故C错误;m= g,V=a3 pm3=(a×10-10)3cm3,ρ== g·cm-3,故D正
确。
5、金刚石和石墨是碳元素形成的两种单质,下列说法正确的是( )
A.金刚石和石墨晶体中最小的环均含有6个碳原子
B.在金刚石中每个C原子连接4个六元环,石墨中每个C原子连接3个六元环
C.金刚石与石墨中碳原子的杂化方式均为sp2
D.金刚石中碳原子数与C—C数之比为1∶4,而石墨中碳原子数与C—C数之比为1∶3
【答案】 A
【解析】 金刚石中每个C原子连接12个六元环,石墨中每个C原子连接3个六元环,B项错误;金刚石
中碳原子采取sp3杂化,而石墨中碳原子采取sp2杂化,C项错误;金刚石中每个碳原子与周围其他4个碳
原子形成共价键,而每个共价键为2个碳原子所共有,则每个碳原子平均形成的共价键数为 4×=2,故碳
原子数与C—C数之比为1∶2;石墨晶体中每个碳原子与周围其他3个碳原子形成共价键,同样可求得每个
碳原子平均形成的共价键数为3×=1.5,故碳原子数与C—C数之比为2∶3,D项错误。
6、如图是金属晶体内部的电子气理论示意图。电子气理论可以用来解释金属的性质,其中正确的是( )
A.金属能导电是因为金属阳离子在外加电场作用下定向移动
B.金属能导热是因为自由电子在热的作用下相互碰撞,从而发生热的传导
C.金属具有延展性是因为在外力的作用下,金属中各原子层间会出现相对滑动,但自由电子可以起到润
滑剂的作用,使金属不会断裂
D.合金与纯金属相比,由于增加了不同的金属或非金属,使电子数目增多,所以合金的延展性比纯金属
强,硬度比纯金属小
【答案】 C
【解析】 金属能导电是因为自由电子在外加电场作用下定向移动,A错误;自由电子在热的作用下与金
属阳离子发生碰撞,实现热的传导,B错误;在外力的作用下,金属中各原子层间会出现相对滑动,而自
由电子与金属阳离子之间的电性作用仍然存在,使得金属不会断裂,C正确;合金与纯金属相比,由于增
加了不同的金属或非金属,相当于填补了金属阳离子之间的空隙,所以一般情况下合金的延展性比纯金属
弱,硬度比纯金属大,D错误。
7、碳化硅(SiC)晶体具有多种结构,其中一种晶体的晶胞(如图所示)与金刚石的类似。下列判断正确的是(
)A.该晶体属于分子晶体
B.该晶体中存在极性键和非极性键
C.该晶体中Si的化合价为-4
D.该晶体中C的杂化类型为sp3
【答案】 D
【解析】 与金刚石类似,该晶体属于共价晶体,A错误;根据该晶体的晶胞结构图可知,该晶体只存在
Si—C极性共价键,B错误;Si—C中,C的电负性更强,共用电子对偏向 C原子,所以Si的化合价为+
4,C错误;每个C原子与4个Si原子形成4个σ键,C原子没有孤电子对,所以C的杂化类型为sp3,D
正确。
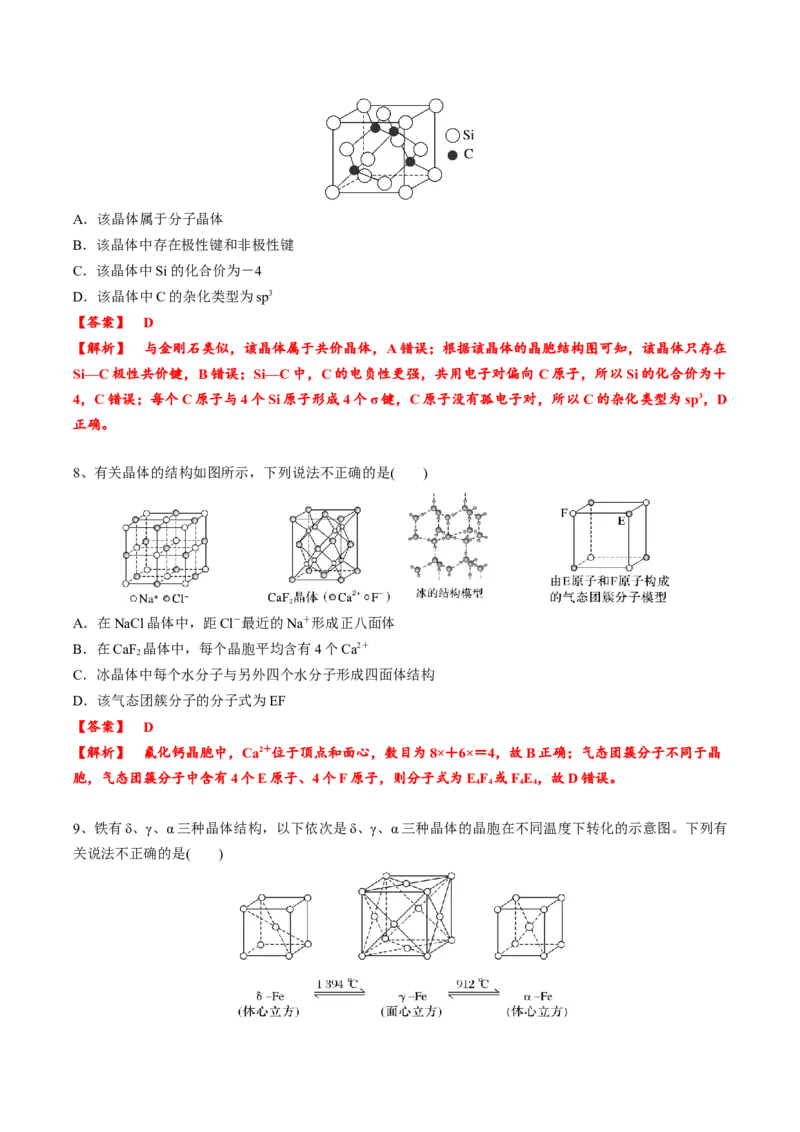
8、有关晶体的结构如图所示,下列说法不正确的是( )
A.在NaCl晶体中,距Cl-最近的Na+形成正八面体
B.在CaF 晶体中,每个晶胞平均含有4个Ca2+
2
C.冰晶体中每个水分子与另外四个水分子形成四面体结构
D.该气态团簇分子的分子式为EF
【答案】 D
【解析】 氟化钙晶胞中,Ca2+位于顶点和面心,数目为8×+6×=4,故B正确;气态团簇分子不同于晶
胞,气态团簇分子中含有4个E原子、4个F原子,则分子式为E F 或FE ,故D错误。
4 4 4 4
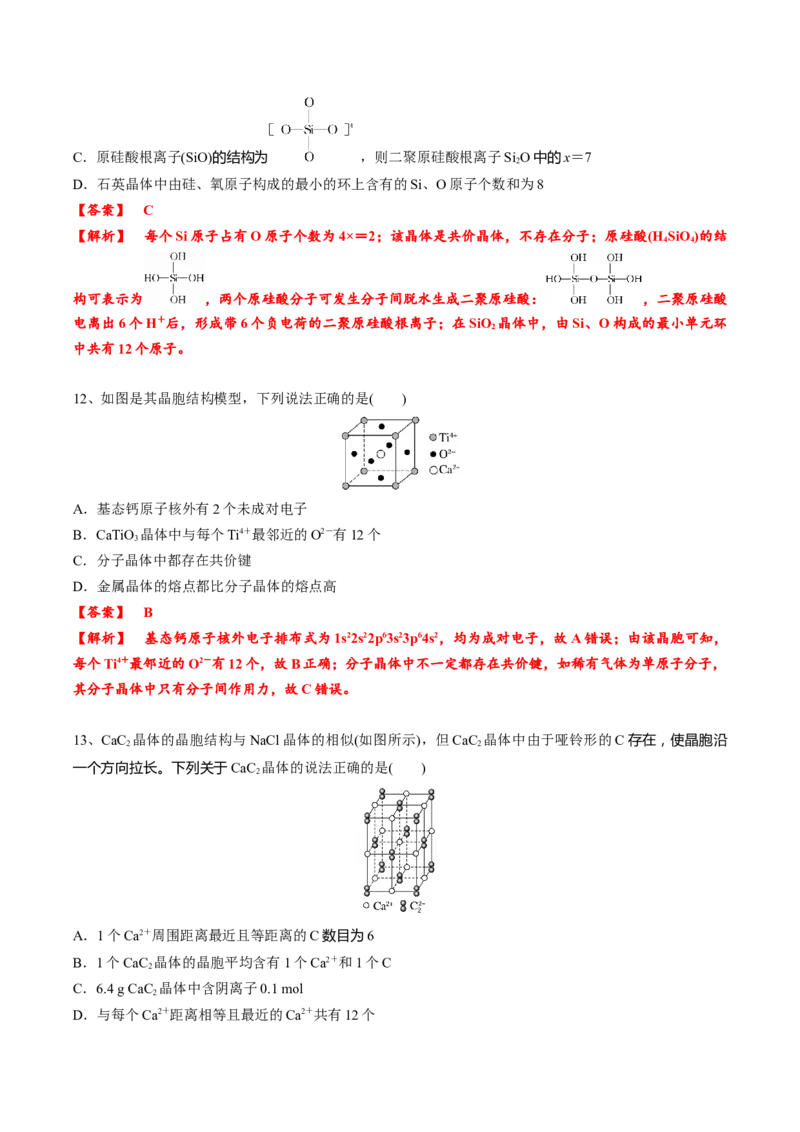
9、铁有δ、γ、α三种晶体结构,以下依次是δ、γ、α三种晶体的晶胞在不同温度下转化的示意图。下列有
关说法不正确的是( )A.每个δ-Fe晶体中有2个铁原子 B.γ-Fe晶体中与每个铁原子距离相等且最近的铁原子有12个
C.每个γ-Fe晶胞中含有14个铁原子
D.将铁加热到1 500 ℃分别急速冷却和缓慢冷却,得到的晶体类型不相同
【答案】 C
【解析】 根据切割法,一个δ-Fe晶胞中含有铁原子个数为×8+1=2,A正确;γ-Fe位于顶角的Fe原
子,被晶胞的三个平面共有,每个平面上有四个铁原子与顶角处铁原子距离最短,则共有 3×4=12个,B
正确;根据切割法,一个γ-Fe晶胞含有铁原子个数为×8+×6=4,C错误;依据得到晶体的条件可知,在
急速冷却时(立即降温到912 ℃)得到α-Fe,缓慢冷却时(缓慢冷却到1 394 ℃)得到γ-Fe,两种晶体类型不
同,D正确。
10、钡在氧气中燃烧时得到一种钡的氧化物晶体,其结构如图所示,下列有关说法正确的是( )
A.该晶体属于分子晶体 B.晶体的化学式为Ba O
2 2
C.该晶体晶胞结构与CsCl相似 D.与Ba2+距离相等且最近的Ba2+共有12个
【答案】 D
【解析】 该晶胞是由金属阳离子钡离子和阴离子过氧根离子构成的,属于离子晶体,A错误;该晶胞中
Ba2+个数为 8×+6×=4,O个数为 1+12×=4,则钡离子和过氧根离子个数之比为 1∶1,其化学式为
BaO ,B错误;该晶胞中钡离子配位数是6,过氧根离子配位数是6,氯化铯晶体中离子配位数是8,C错
2
误。
11、石英晶体的平面示意图如图,它实际上是立体的网状结构(可以看作是晶体硅中的每个Si—Si中插入一
个O),其中硅、氧原子数比是m∶n,下列有关叙述正确的是( )
A.m∶n=2∶1
B.6 g该晶体中含有0.1N 个分子
AC.原硅酸根离子(SiO)的结构为 ,则二聚原硅酸根离子Si O中的x=7
2
D.石英晶体中由硅、氧原子构成的最小的环上含有的Si、O原子个数和为8
【答案】 C
【解析】 每个Si原子占有O原子个数为4×=2;该晶体是共价晶体,不存在分子;原硅酸(H SiO )的结
4 4
构可表示为 ,两个原硅酸分子可发生分子间脱水生成二聚原硅酸: ,二聚原硅酸
电离出6个H+后,形成带6个负电荷的二聚原硅酸根离子;在SiO 晶体中,由Si、O构成的最小单元环
2
中共有12个原子。
12、如图是其晶胞结构模型,下列说法正确的是( )
A.基态钙原子核外有2个未成对电子
B.CaTiO 晶体中与每个Ti4+最邻近的O2-有12个
3
C.分子晶体中都存在共价键
D.金属晶体的熔点都比分子晶体的熔点高
【答案】 B
【解析】 基态钙原子核外电子排布式为1s22s22p63s23p64s2,均为成对电子,故A错误;由该晶胞可知,
每个Ti4+最邻近的O2-有12个,故B正确;分子晶体中不一定都存在共价键,如稀有气体为单原子分子,
其分子晶体中只有分子间作用力,故C错误。
13、CaC 晶体的晶胞结构与NaCl晶体的相似(如图所示),但CaC 晶体中由于哑铃形的C存在,使晶胞沿
2 2
一个方向拉长。下列关于CaC 晶体的说法正确的是( )
2
A.1个Ca2+周围距离最近且等距离的C数目为6
B.1个CaC 晶体的晶胞平均含有1个Ca2+和1个C
2
C.6.4 g CaC 晶体中含阴离子0.1 mol
2
D.与每个Ca2+距离相等且最近的Ca2+共有12个【答案】 C
【解析】 A项,依据晶胞示意图可以看出,晶胞的一个平面的长与宽不相等,再由图中体心可知,1个
Ca2+周围距离最近且相等的C有4个,错误;C项,6.4 g CaC 为0.1 mol,则含阴离子0.1 mol,正确;D
2
项,与每个Ca2+距离相等且最近的Ca2+有4个,错误。14、将石墨置于熔融的钾或气态钾中,石墨吸收钾形成名称为钾石墨的物质,其组成可以是 C K、C K、
8 12
C K、C K、C K、C K等。下列分析正确的是( )
24 36 48 60
A.题干中所列举的6种钾石墨属于有机高分子
B.钾石墨中碳原子的杂化方式是sp3杂化
C.若某钾石墨的原子分布如图所示,则它所表示的是C K
12
D.最近两个K原子之间距离为石墨中C—C键长的2倍
【答案】D
【解析】题干中列举的6种物质是石墨吸收钾形成的,不属于有机物,而是无机化合物,A项错误;钾石
墨是石墨吸收钾形成的化合物,其中的碳原子形成了键角约为 120°的三条共价键,因此采用的是 sp2杂
化,B项错误;由该种钾石墨的结构可知, 可选择图中虚线框选的部分作为该钾石墨的晶
胞,碳原子位于晶胞的内部共有8个,钾原子位于晶胞的4个顶点上,因此均摊法计算该钾石墨的化学式
为CK,C项错误;由该种钾石墨的结构可知,钾原子排列在每个六边形单元格中心位置,并且间隔 1个
8
六边形单元格填充,因此钾原子之间的最短距离等于相邻的 2个六边形单元格中心连线的长度的2倍,即
C—C键长的2倍,D项正确。