文档内容
2022 届高三化学二轮复习晶体结构与性质专题练习
一、选择题(共17题)
1.25℃,一个大气压下呈气态的化合物、降温使其固化得到的晶体属于
A.分子晶体 B.原子晶体
C.离子晶体 D.何种晶体无法判断
2.下列有关化学用语使用正确的是
A.石英的分子式:SiO
2
B.NH Cl的电子式:
4
C.Cr原子的基态简化电子排布式为 [Ar]3d54s1
D.基态碳原子最外层的电子排布图为
3.如图是从NaCl或CaF 晶体结构图中分割出来的部分结构图,其中属于从CaF 晶体中分割出来的结构
2 2
图是
A.图 和图 B.图 和图 C.只有图 D.只有图
4.下列晶体在相同条件下熔点由低到高排列正确的是
A.金刚石 碳化硅 晶体硅 B.HF HCl HBr
C.金属钾 金属钠 金属锂 D.二氧化硅 氯化钠 干冰
5.下列与等离子体无关的是( )
A.等离子体显示器 B.日光灯和霓虹灯
C.把温度升高到几千摄氏度时水蒸气发生的变化 D.液晶显示器
6.下列物质所属晶体类型分类正确的是
选项 A B C D
原子晶体 石墨 生石灰 碳化硅 金刚石分子晶体 冰 固态氨 氯化铯 干冰
离子晶体 氮化铝 食盐 明矾 氧化铝
金属晶体 铜 汞 铝 铁
A.A B.B C.C D.D
7.下列物质的熔点或沸点比较正确的是( )
A.沸点:HO>HS>HSe
2 2 2
B.熔点:F>Cl>Br
2 2 2
C.沸点:CH>SiH >GeH
4 4 4
D.熔点:Li>Na>K
8.下列各组物质中化学键类型与晶体类型均相同的是
A.HCl NaCl B.SiO CO
2 2
C.NaCO KClO D.HO Na O
2 3 3 2 2 2 2
9.下面的排序中,不正确的是
A.熔点由高到低:Rb>K>Na
B.熔点由高到低:GeH >SiH>CH
4 4 4
C.硬度由大到小:金刚石>碳化硅>晶体硅
D.晶格能由大到小: AlF>MgF >NaF
3 2
10.检验溴乙烷与NaOH乙醇溶液共热生成的气体中是否含有乙烯,装置如图1所示。下列说法不正确的
是
A.装置①的作用是除去乙醇
B.装置②的现象是高锰酸钾酸性溶液紫色褪去
C.将生成的气体直接通入溴的四氯化碳溶液也可以达到实验目的
D.图2所示NaBr晶胞中,每个Na+周围距离最近的Na+数目为4个
11.下列判断中不正确的是A.熔融态能够导电的晶体一定是离子晶体
B.不同族元素氧化物可形成同类晶体
C.同族元素氧化物可形成不同类型晶体
D.氯化铵固体属于离子晶体,加热使其分解时破坏了离子键和共价键
12.下列性质符合分子晶体的是
A.熔点1070℃,易熔于水,水溶液能导电
B.熔点是10.31℃,液体不导电,水溶液能导电
C.熔点97.81℃,质软,能导电,密度是0.97g/cm3
D.熔点973℃,熔化时能导电,水溶液也能导电
13.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.124 g P 含有P—P键的个数为4N
4 A
B.12 g石墨烯(单层石墨)中含有C-C键的数目为3N
A
C.60gSiO 中含Si—O键的个数为2N
2 A
D.六方最密堆积的配位数是12,空间利用率是74%
14.《天工开物》记载:“凡火药以硝石、硫黄为主,草木灰为辅……而后火药成声”。其中涉及的主要
反应为: 。下列说法正确的是
A.电负性: B. 分子中C原子为 杂化
C.单质硫属于共价晶体 D. 中化学键只有 键
15.下列说法不正确的是
A.NCl 中N—Cl键的键长比CCl 中C—C1键的键长短
3 4
B. 离子的空间结构是V形
C.Fe成为阳离子时首先失去能量最高的3d轨道电子
D.区分晶体、准晶体及非晶体的最可靠方法是对固体进行X射线衍射实验
16.原子序数小于18的八种连号元素,它们单质的熔点随原子序数增大而变化的趋势如图所示。图中X
元素应属A.ⅢA族 B.ⅣA族 C.ⅤA族 D.ⅥA族
17.设N 为阿伏伽德罗常数的值,下列叙述不正确的是
A
A.含16g氧原子的二氧化硅晶体中含有的σ键数目为2N
A
B.1mol甲基(—CH)所含电子数为9N
3 A
C.12克石墨中含有的共价键数目为1.5N
A
D.2molSO 和1molO 在一定条件下反应所得混合气体分子数等于2N
2 2 A
二、综合题(共6题)
18.某同学设计了如图所示的装置,可比较HNO、HCO、HSiO 的酸性强弱,进而比较氮、碳、硅元素
3 2 3 2 3
非金属性强弱。供选择的试剂:稀硝酸、稀硫酸、碳酸钙固体、碳酸钠固体、硅酸钠溶液、澄清石灰水、
饱和碳酸氢钠溶液
(1)仪器a的名称:___________。
(2)锥形瓶中装有某可溶性正盐,a中所盛试剂为___________。
(3)装置B所盛试剂是___________,其作用是___________。
(4)装置C所盛试剂是___________,C中反应的离子方程式是___________。
(5)通过实验证明碳、氮、硅的非金属性由强到弱的顺序是___________。
(6)写出碳、氮、硅三元素的简单气态氢化物的稳定性由强到弱的顺序是(写化学式)___________。
(7)写出碳、氮、硅三元素的简单气态氢化物的沸点由高到低的顺序是(写化学式)___________。
19.锌是人体必需的微量元素之一,起着极其重要的作用,回答下列问题:(1)请写出Zn2+的核外电子排布式_____________________。
(2)ZnCl 熔点为275 ℃,而CaCl 的熔点为782 ℃,请分析熔点不同的原因:_________。
2 2
(3)Zn2+能与多种微粒形成配合物,如Zn2+与CNO−可形成[Zn(CNO) ]2−,[Zn(CNO) ]2−中配位原子为
4 4
__________,[Zn(CNO) ]2−的组成中非金属元素的电负性大小顺序为____________;Zn2+与CN−可形成
4
[Zn(CN) ]2−,[Zn(CN) ]2−中σ键、π键和配位键的个数比为________;配合物Zn(NH )CO 中阴离子的空间
4 4 3 4 3
构型为____________,N原子的杂化方式为____________。
(4)Zn与S所形成化合物的晶胞如图1所示,图2为晶胞沿y轴的投影1∶1平面图:
①晶胞中S原子的配位数为_________。
②晶胞中最近的两个S原子之间的距离为_______pm。
③设阿伏加德罗常数的值为N ,则该晶胞的密度是__________g·cm−3(列出计算表达式)。
A
哌替啶盐酸盐G有镇痛作用,其合成路线如下。回答下列问题:
(1)写出A的结构简式:________;B中含有碳碳双键,则B的名称为_____________。
(2)G中含氧官能团名称为____________;B→C的反应类型为_________________。
(3)E的结构简式为_____________。
(4)写出C→D的化学方程式:_______________________________________。
(5)M与E互为同分异构体,符合下列条件的M有______种。①属于芳香α-氨基酸;
②含有两个六元环。
其中一种同分异构体,—NH 被H原子取代后,除苯基上H原子外,其他核磁共振氢谱的峰面积比为
2
4∶4∶1∶1∶1,该同分异构体的结构简式为______________。
(6)请结合以上合成路线,写出以HCNHCH Cl和CH=CHCl及上述流程中出现的物质为原料合成
3 2 2
的路线______________________。
20.有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,
B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在
水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价
氧化物中含D的质量分数为 40%,且其核内质子数等于中子数。R是由A、D两元素形成的离子化合物,
其中A+与D2-离子数之比为2∶1。请回答下列问题:
(1)B-的电子排布式为__________,在CB 分子中C元素原子的原子轨道发生的是__________杂化。
3
(2)C的氢化物的空间构型为__________,其氢化物在同族元素所形成的氢化物中沸点最高的原因是
__________。
(3)B元素的电负性__________D元素的电负性(填“>”、“<”或“=”),用一个化学方程式说明B、D
两元素形成的单质的氧化性强弱:__________。
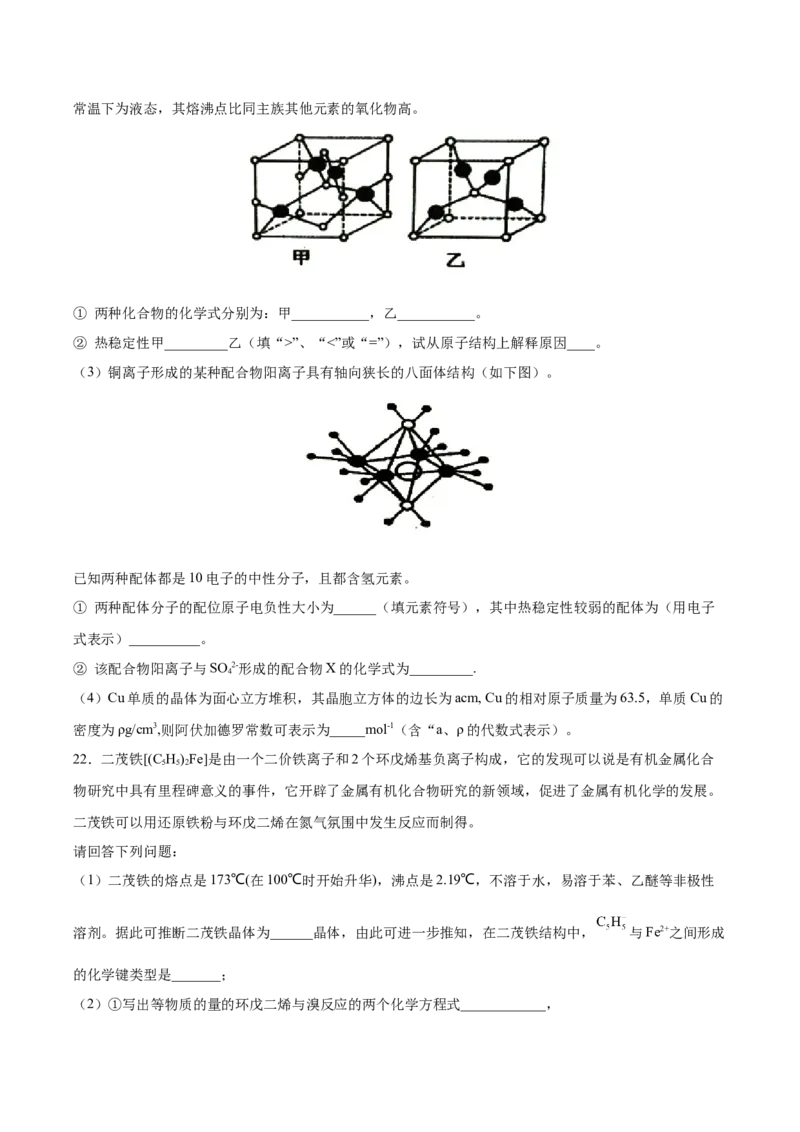
(4)如图所示是R形成的晶体的晶胞,设晶胞的棱长为a cm。 试计算R晶体的密度为__________。(阿伏加
德罗常数用N 表示)
A
21.铜是人类最早使用的金属之一。
(1)铜元素基态原子的价电子排布式为_______,其核外能级能量的高低3d______4s(填“>”、“<”或
“=”)
(2)Cu与元素A能形成如下图所示的两种化合物甲和乙。元素A是短周期非金属元素,A的常见氧化物常温下为液态,其熔沸点比同主族其他元素的氧化物高。
① 两种化合物的化学式分别为:甲___________,乙___________。
② 热稳定性甲_________乙(填“>”、“<”或“=”),试从原子结构上解释原因____。
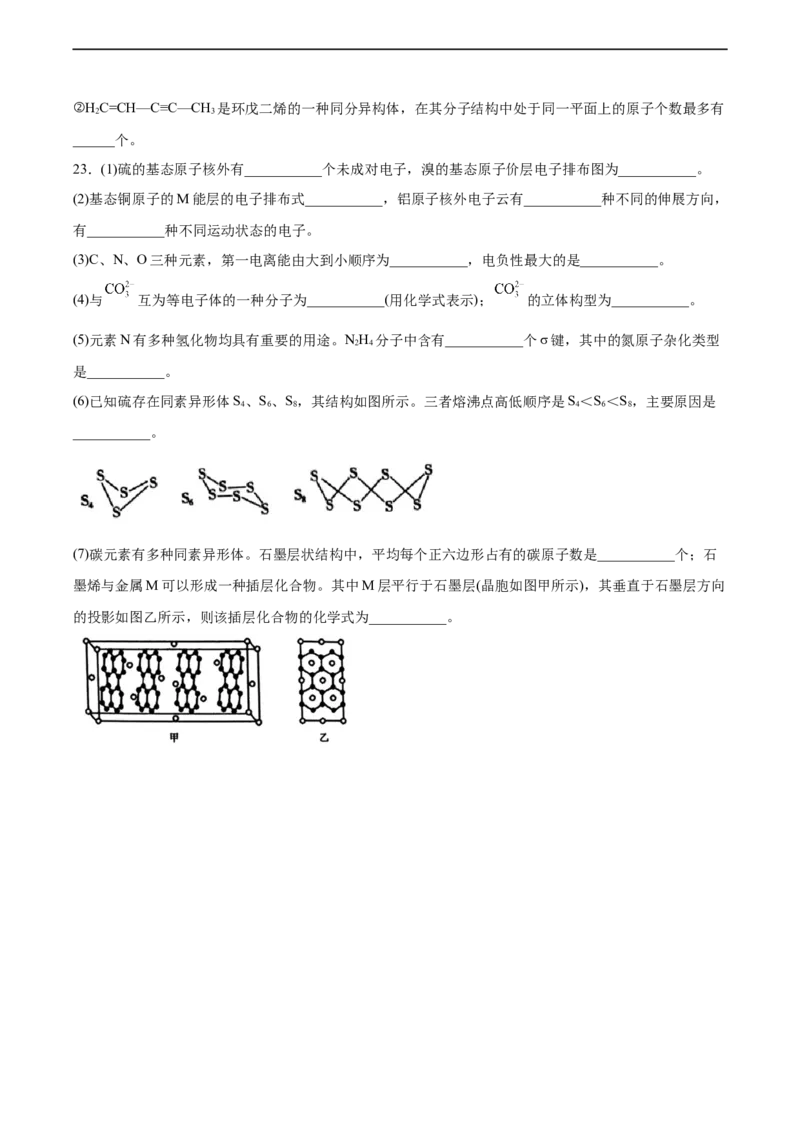
(3)铜离子形成的某种配合物阳离子具有轴向狭长的八面体结构(如下图)。
已知两种配体都是10电子的中性分子,且都含氢元素。
① 两种配体分子的配位原子电负性大小为______(填元素符号),其中热稳定性较弱的配体为(用电子
式表示)__________。
② 该配合物阳离子与SO 2-形成的配合物X的化学式为_________.
4
(4)Cu单质的晶体为面心立方堆积,其晶胞立方体的边长为acm, Cu的相对原子质量为63.5,单质Cu的
密度为ρg/cm3,则阿伏加德罗常数可表示为_____mol-1(含“a、ρ的代数式表示)。
22.二茂铁[(C H)Fe]是由一个二价铁离子和2个环戊烯基负离子构成,它的发现可以说是有机金属化合
5 5 2
物研究中具有里程碑意义的事件,它开辟了金属有机化合物研究的新领域,促进了金属有机化学的发展。
二茂铁可以用还原铁粉与环戊二烯在氮气氛围中发生反应而制得。
请回答下列问题:
(1)二茂铁的熔点是173℃(在100℃时开始升华),沸点是2.19℃,不溶于水,易溶于苯、乙醚等非极性
溶剂。据此可推断二茂铁晶体为______晶体,由此可进一步推知,在二茂铁结构中, 与Fe2+之间形成
的化学键类型是_______;
(2)①写出等物质的量的环戊二烯与溴反应的两个化学方程式____________,②H C=CH—C≡C—CH 是环戊二烯的一种同分异构体,在其分子结构中处于同一平面上的原子个数最多有
2 3
______个。
23.(1)硫的基态原子核外有___________个未成对电子,溴的基态原子价层电子排布图为___________。
(2)基态铜原子的M能层的电子排布式___________,铝原子核外电子云有___________种不同的伸展方向,
有___________种不同运动状态的电子。
(3)C、N、O三种元素,第一电离能由大到小顺序为___________,电负性最大的是___________。
(4)与 互为等电子体的一种分子为___________(用化学式表示); 的立体构型为___________。
(5)元素N有多种氢化物均具有重要的用途。NH 分子中含有___________个σ键,其中的氮原子杂化类型
2 4
是___________。
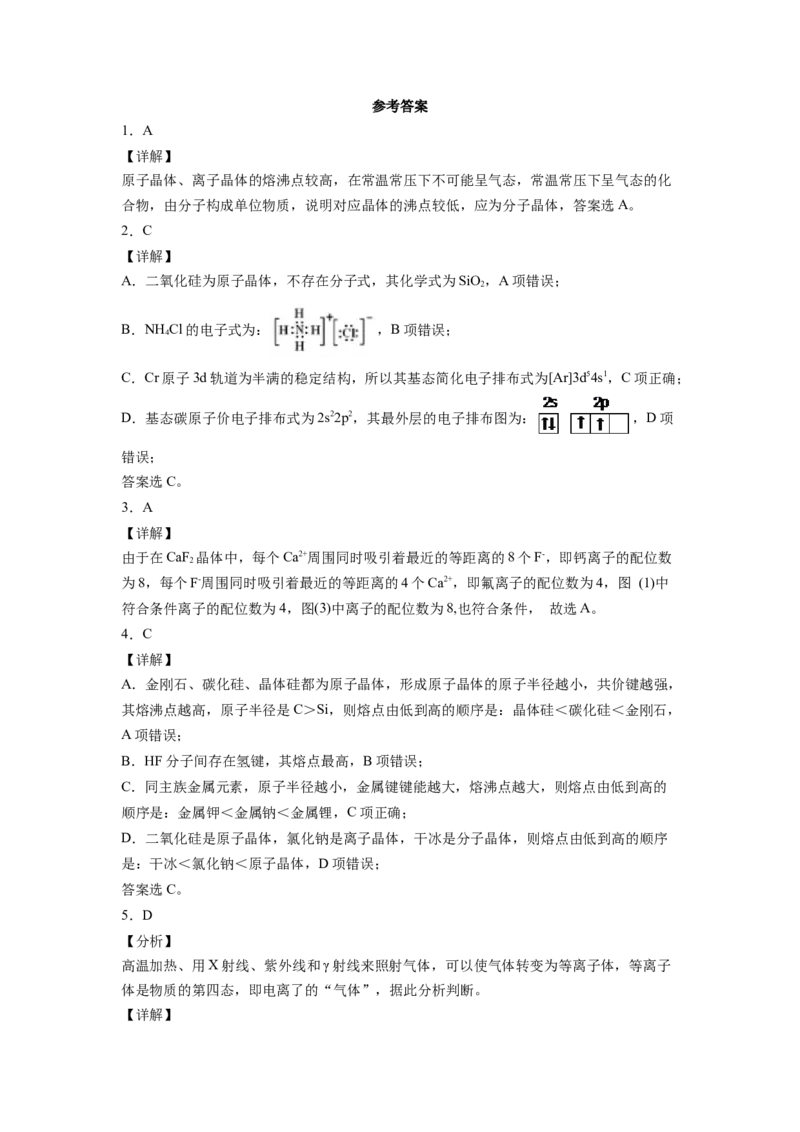
(6)已知硫存在同素异形体S、S、S,其结构如图所示。三者熔沸点高低顺序是S<S<S,主要原因是
4 6 8 4 6 8
___________。
(7)碳元素有多种同素异形体。石墨层状结构中,平均每个正六边形占有的碳原子数是___________个;石
墨烯与金属M可以形成一种插层化合物。其中M层平行于石墨层(晶胞如图甲所示),其垂直于石墨层方向
的投影如图乙所示,则该插层化合物的化学式为___________。参考答案
1.A
【详解】
原子晶体、离子晶体的熔沸点较高,在常温常压下不可能呈气态,常温常压下呈气态的化
合物,由分子构成单位物质,说明对应晶体的沸点较低,应为分子晶体,答案选A。
2.C
【详解】
A.二氧化硅为原子晶体,不存在分子式,其化学式为SiO,A项错误;
2
B.NH Cl的电子式为: ,B项错误;
4
C.Cr原子3d轨道为半满的稳定结构,所以其基态简化电子排布式为[Ar]3d54s1,C项正确;
D.基态碳原子价电子排布式为2s22p2,其最外层的电子排布图为: ,D项
错误;
答案选C。
3.A
【详解】
由于在CaF 晶体中,每个Ca2+周围同时吸引着最近的等距离的8个F-,即钙离子的配位数
2
为8,每个F-周围同时吸引着最近的等距离的4个Ca2+,即氟离子的配位数为4,图 (1)中
符合条件离子的配位数为4,图(3)中离子的配位数为8,也符合条件, 故选A。
4.C
【详解】
A.金刚石、碳化硅、晶体硅都为原子晶体,形成原子晶体的原子半径越小,共价键越强,
其熔沸点越高,原子半径是C>Si,则熔点由低到高的顺序是:晶体硅<碳化硅<金刚石,
A项错误;
B.HF分子间存在氢键,其熔点最高,B项错误;
C.同主族金属元素,原子半径越小,金属键键能越大,熔沸点越大,则熔点由低到高的
顺序是:金属钾<金属钠<金属锂,C项正确;
D.二氧化硅是原子晶体,氯化钠是离子晶体,干冰是分子晶体,则熔点由低到高的顺序
是:干冰<氯化钠<原子晶体,D项错误;
答案选C。
5.D
【分析】
高温加热、用X射线、紫外线和γ射线来照射气体,可以使气体转变为等离子体,等离子
体是物质的第四态,即电离了的“气体”,据此分析判断。
【详解】A.等离子体显示器是通过等离子体显示图像和文字,与等离子体有关,故A不选;
B.日光灯和霓虹灯中气体被电离形成了等离子体,与等离子体有关,故B不选;
C.把温度升高到几千摄氏度时,水蒸气被电离形成了等离子体,与等离子体有关,故C
不选;
D.液晶显示器是通过液晶显示图像和文字,与等离子体无关,故D选;
故选D。
6.D
【详解】
A.生石灰为CaO,为离子晶体,故A错误;B.氯化铯为活泼金属的氯化物,为离子晶体,
故B错误;C.氮化铝常用作砂轮及耐高温的材料,熔融时不导电为共价化合物,熔点高、
硬度大,为原子晶体,故C错误;D.金刚石为原子晶体,干冰为分子晶体,氧化铝为离
子晶体,Fe为金属单质为金属晶体,故D正确,故选D。
7.D
【详解】
A.水分子间含有氢键,沸点最高。一般来说,组成与结构相似的分子晶体,相对分子质量
越大,沸点越高,则沸点:HSe>H S,故A错误;
2 2
B. 一般来说,组成与结构相似的分子晶体,相对分子质量越大,熔点越高,则熔点
Br >Cl>F ,故B错误;
2 2 2
C. CH、SiH、GeH 均为分子晶体,则沸点:GeH >SiH >CH ,故C错误;
4 4 4 4 4 4
D.金属键越强,熔点越高,则熔点:Li>Na>K,故D正确;
故答案选:D。
8.C
【分析】
一般非金属元素之间形成共价键,金属元素与非金属元素形成离子键,由分子构成的晶体
为分子晶体,由离子构成的晶体为离子晶体,由金属原子和自由电子构成的为金属晶体,
由原子构成的且为空间网状结构的晶体为原子晶体,以此来解答。
【详解】
A.HCl属于分子晶体,氢原子和氯原子之间形成的是共价键;NaCl属于离子晶体,钠离子
和氯离子之间存在离子键,故A错误;
B.SiO 是原子晶体,硅原子和氧原子之间通过共价键形成空间网状结构;CO 属于分子晶
2 2
体,碳原子与氧原子之间形成的是共价键,故B错误;
C.Na CO KClO 均为离子晶体,均存在离子键,故C正确;
2 3 3
D.HO 属于分子晶体,氢原子和氧原子之间形成的是共价键;NaO 属于离子晶体,钠离
2 2 2 2
子和过氧根离子之间存在离子键,故D错误;
答案:C
9.A
【解析】【详解】
A.钠、钾、铷属于金属晶体,熔点与金属键的强弱有关,金属离子的电荷越多、离子半径
越小,金属键越强,熔点越高。钠、钾、铷离子的电荷相同,半径由大到小的顺序为Rb>
K>Na,沸点由低到高的顺序为RbSiH >CH ,故B项正确;
4 4 4
C.原子晶体中,原子半径越小,化学键越短,键能越大,化学键越强,硬度越大。所以硬
度由大到小:金刚石>碳化硅>晶体硅,故C项正确;
D.离子晶体中离子所带电荷越多、半径越小,晶格能越大,晶格能由大到小:AlF>MgF
3 2
>NaF,故D项正确;
综上所述,本题正确答案为A。
10.D
【分析】
溴乙烷与NaOH乙醇溶液共热发生消去反应生成乙烯,由于乙醇易挥发,生成的乙烯中会
混有乙醇,据此分析。
【详解】
A.乙醇与水互溶,乙烯难溶于水,所以可以用水除去混有的乙醇,A正确;
B.生成的气体中含有乙烯,乙烯可以还原酸性高锰酸钾溶液使其褪色,B正确;
C.乙烯可以和溴的四氯化碳溶液发生加成反应使其褪色,而挥发出的乙醇不能使溴的四
氯化碳溶液褪色,C正确;
D.以体心钠离子为例,距离最近的钠离子棱心上,所以有12个,D错误;
综上所述答案为D。
11.A
【详解】
A.熔融态能够导电的晶体不一定是离子晶体,可能是金属晶体,A错误;
B.不同族元素氧化物可形成同类晶体,例如氧化钠、氧化镁等均是离子晶体,B正确;
C.同族元素氧化物可形成不同类型晶体,例如二氧化硅是共价晶体,二氧化碳是分子晶
体,C正确;
D.氯化铵是离子化合物,氯化铵固体属于离子晶体,氯化铵中存在离子键和共价键,加
热使其分解时生成氨气和氯化氢,破坏了离子键和共价键,D正确;
答案选A。
12.B
【详解】
分子晶体具有熔沸点低、符合相似相溶原理,自身一般不导电,溶于水后导电的性质:
A.熔点1070℃,易熔于水,水溶液能导电,沸点较高,是离子晶体的性质,A错误;
B.熔点是10.31℃,液体不导电,水溶液能导电,是分子晶体的性质,B正确;
C.熔点97.81℃,质软,能导电,密度是0.97g/cm3,分子晶体不导电,是金属晶体,C错误;
D.熔点973℃,熔化时能导电,水溶液也能导电,是离子晶体,D错误;
答案选B。
13.D
【详解】
A、n(P )= = =1mol,1个P 分子含有6个P-P键,因此124g P 含有的P-P键
4 4 4
的物质的量为6mol,P-P键的个数为6N ,故A错误;
A
B、12g石墨中含有碳原子的物质的量n= = =1mol,在石墨晶体中一个碳原子
形成3个C-C键,每个C-C键由2个碳原子构成,因此12g石墨中含有C-C键的物质的量
为1mol×3× =1.5mol,C-C键的个数为1.5N ,故B正确;
A
C、n( SiO )= = =1mol,在二氧化硅晶体中,每个硅原子形成4个Si-O键,因
2
此60g SiO 中含Si-O键的物质的量为4mol,Si-O键的个数为4N ,故C错误;
2 A
D、六方最密堆积和面心立方最密堆积是空间利用率最高的结构,空间利用率均为74%,
故D正确;
故选D。
【点晴】
本题考查阿伏伽德罗常数的有关计算,侧重于分子晶体、原子晶体、混合晶体结构的考查,
掌握物质的晶体结构是解题的关键。如NaO 是由Na+和O2-构成,而不是有Na+和O2-构成;
2 2 2
SiO、SiC都是原子晶体,其结构中只有原子没有分子,SiO 是正四面体结构,1molSiO 中
2 2 2
含有的共价键为4N ,1molP 含有的共价键为6N 等。
A 4 A
14.B
【详解】
A.O的非金属性大于N,所以电负性N<O,故A错误;
B.CO 分子为直线型对称结构,C原子为sp杂化,故B正确;
2
C.单质硫是由分子通过分子间作用力结合而成,属于分子晶体,故C错误;
D.KNO 中既含离子键又含共价键,故D错误;
3
故选B。
15.C
【详解】
A.C原子的原子半径大于N原子的原子半径,则NCl 中N—Cl键的键长比CCl 中C—C1
3 4
键的键长短,故A正确;
B.I 离子与ClO 离子具有相同的原子个数和价电子数,互为等电子体,等电子体具有相
同的空间结构,ClO 离子氯原子的价层电子对数为4,孤对电子对数为2,ClO 离子的空间结构是V形,则I 离子的空间结构也是V形,故B正确;
C.铁原子形成阳离子时首先失去最外层4s轨道上的电子,故C错误;
D.对固体进行X射线衍射实验可以准确的区分固体是否为晶体、准晶体及非晶体,故D
正确;
故选C。
16.B
【详解】
根据图像可知,X的熔点最高,在短周期元素中,应该是第ⅣA族的碳元素形成的金刚石,
所以答案选B。
17.D
【解析】A,在二氧化硅晶体中,每个氧原子与邻近的2个硅原子形成共价键,16g氧原子
的物质的量为1mol,所以含有的σ键数目为2N ,A正确。B,甲基中含1个碳原子和3个
A
氢原子,碳原子有6个电子,氢原子有1个电子,所以甲基共有9个电子,所以1mol甲基
(—CH)所含电子数为9N ,B正确。C,石墨晶体中,每个碳原子与邻近的3个碳原子形
3 A
成共价键,形成一个共价键需要2个碳原子,所以平均每个碳原子可形成1.5个共价键,
12g石墨含碳原子1mol,所以含有的共价键数目为1.5N
A
,C正确。D,2molSO 和1molO 在一定条件下发生的反应是一个可逆反应,并不能完全
2 2
转化为2mol SO ,反应所得混合气体分子数小于2 N ,所以D不正确。
3 A
18.
(1)分液漏斗
(2)稀硝酸
(3) 饱和碳酸氢钠溶液 吸收气体中硝酸
(4) 硅酸钠溶液 SiO +CO+HO=HSiO↓+CO
2 2 2 3
(5)N>C>Si
(6)NH >CH>SiH
3 4 4
(7)NH >SiH>CH
3 4 4
【分析】
a中装有硝酸,装置A中装有碳酸钠溶液,硝酸与碳酸钠发生强酸制取弱酸的反应生成二
氧化碳,装置B中为饱和碳酸氢钠溶液,可以除去挥发的硝酸,装置C中装有硅酸钠溶液,
二氧化碳与硅酸钠发生强酸制取弱酸的反应生成硅酸沉淀,由此比较出酸性:HNO>
3
HCO>HSiO。
2 3 2 3
(1)
由图可知,仪器a为分液漏斗;
(2)
由分析可知,a中所盛试剂为稀硝酸;
(3)由分析可知,装置B所盛试剂是饱和碳酸氢钠溶液,可以除去二氧化碳中的硝酸;
(4)
由分析可知,装置C中装有硅酸钠溶液,二氧化碳与硅酸钠溶液发生反应生成硅酸沉淀,
离子方程式为SiO +CO+HO=HSiO↓+CO ;
2 2 2 3
(5)
元素的非金属性越强,其最高价氧化物对应水化物的酸性越强,酸性:HNO>HCO>
3 2 3
HSiO,则非金属性:N>C>Si;
2 3
(6)
元素的非金属性越强,对其氢化物的稳定性越强,则碳、氮、硅三元素的简单气态氢化物
的稳定性由强到弱的顺序为NH >CH>SiH;
3 4 4
(7)
NH 中含有氢键,其沸点较高,CH 和SiH 都是分子晶体,相对分子质量越大,沸点越高,
3 4 4
则沸点:NH >SiH>CH。
3 4 4
19.1s22s22p63s23p63d10(或[Ar]3d10)(1分) CaCl 为典型的离子化合物,而ZnCl 虽
2 2
为离子化合物,但有明显的共价性(1分) O(1分) O > N >C(1分) 2∶2∶1
(2分) 平面三角形(2分) sp3(1分) ①4(1分) ②2a(2分)
③ (3分) CH≡CH(1分) 氯乙烯(1-氯乙烯)(1分) 酯
基(1分) 加成反应(1分) (2分)
(2分) 3(1
分) (2分)
(4分)
【详解】
[化学——选修3:物质结构与性质]
(1)Zn的原子序数为30,其核外电子排布式为[Ar]3d104s2,Zn2+是锌原子失去2个电子所
形成的,Zn2+的核外电子排布式为1s22s22p63s23p63d10或[Ar]3d10。(2)Ca的金属性比Zn的强,Ca、Zn与氯形成CaCl 、ZnCl,其中CaCl 为典型的离子化
2 2 2
合物,熔点比较高,而ZnCl 虽为离子化合物,但因Zn的活泼性比较弱,形成的ZnCl 有
2 2
明显的共价性,使ZnCl 熔点比CaCl 低。
2 2
(3)配位原子必须能提供孤电子对,而CNO−结构中,O能提供孤电子对,故配位原子为
O原子,[Zn(CNO) ]2−中非金属元素为C、N、O,同一周期从左至右,电负性逐渐增大,
4
它们的电负性大小顺序为O> N>C,一个[Zn(CN) ]2−中Zn与4个CN−间有4个配位键即4个
4
σ键,每个CN之间存在一个σ键和2个π键,σ与π和配位键的个数为8、8、4,比值为
2∶2∶1。Zn(NH )CO 中阴离子为 ,是平面三角形,NH 中的N是sp3杂化。
3 4 3 3
(4)①根据图可看出每一个S周围有4个Zn,配位数为4。②最近的两个S原子之间的距
离是面对角线的一半,根据图2可知面对角线长为4a pm。最近的两个S原子之间的距离
是2a pm。③晶胞中Zn的个数为顶点8× =1,面心6× =3,共4个,S在内部,共4个,
化学式为ZnS,式量为65+32,设晶胞边长为d pm, =4a,d= ,
ρd3N =4(65+32),ρ = g·cm−3。
A
[化学——选修5:有机化学基础]
(1)根据A→B→C,可看出A与HCl和HCNH 发生连续加成反应,所以A含有碳碳叁
3 2
键,为乙炔,结构简式为CH≡CH,B中含有碳碳双键,是A与HCl加成所得,所以B为
氯乙烯。
(2)根据合成路线可知,G中含氧官能团为酯基,B生成C,发生加成反应。
(3)根据D、F的结构,可知E中含羧基,得出E的结构简式为 。
(4)C生成 D发生了取代反应,方程式为:
。
(5)苯环在1,2,3位时都满足条件,即 ,
中—NH 被H代替后为 ,除苯
2
环外,其他C原子上的H原子个数如下: ,核磁共振氢谱峰
面积比正好为4∶4∶1∶1∶1。(6)利用题干B→C→D→E→F的反应原理,B→C为双加成反应,而所设计的合成路线
中为单加成反应,题干中C→D和所设计合成路线中一样均为双取代反应,题干中
D→E→F与所设计合成路线中一样均为水解、酯化反应,所以合成路线为:
20.ls22s22p63s23p6或者[Ne]3s23p6 sp3 三角锥形 氨分子间形成氢键,所以氨气比
同族其它元素形成的氢化物沸点高 > Cl +Na S=2NaCl+S↓ g·
2 2
【分析】
B原子得一个电子填入3p轨道后,3p轨道已充满,B为Cl元素;B-离子为Cl-离子,A+比
B-少一个电子层,A+为Na+离子;C原子的p轨道中有3个未成对电子,C原子的外围电子
排布为ns2np3,是第ⅤA族元素,其气态氢化物在水中的溶解度在同族元素所形成的氢化
物中最大,所以为N元素;D的最高化合价和最低化合价的代数和为4,为第ⅥA族元素,
最高价氧化物中含D的质量分数为 40%,可推知D的相对原子质量为32,其核内质子数
等于中子数,所以质子数为16,D为S元素,A+是Na+离子,D2-离子是S2-离子,R是由
Na+离子与S2-离子以2:1形成的离子化合物,R是硫化钠。
【详解】
(1)B−离子为Cl−离子,电子排布式为ls22s22p63s23p6或者[Ne]3s23p6;CB 分子为NCl 分子,
3 3
N原子有一对孤对电子,与Cl原子成3个δ键,杂化轨道数为1+3=4,所以为sp3杂化。故
答案为:ls22s22p63s23p6或者[Ne]3s23p6;sp3。
(2)C的氢化物为NH ,N原子采取sp3杂化,N原子有一对孤对电子,所以NH 为三角锥形,
3 3
N原子电负性很强,氨分子间形成氢键,所以氨气比同族其它元素形成的氢化物沸点高。
故答案为:三角锥形;氨分子间形成氢键,所以氨气比同族其它元素形成的氢化物沸点高。
(4)B为Cl元素,D为S元素,同周期,自左而右,电负性增强,所以电负性Cl>S.利用
“在氧化还原反应中,氧化剂氧化性大于氧化产物”原理,一般来说电负性越强,元素的
非金属性越强,对应的单质的氧化性越强,如在Cl+Na S=2NaCl+S↓反应中,Cl2的氧化性
2 2
大于O 的氧化性。故答案为:>;Cl+Na S=2NaCl+S↓;
2 2 2
(5)A+是Na+离子,D2−离子是S2−离子,根据均摊法计算,晶胞含有S2−离子个数8× +6×
=4,含有A+是Na+离子8个,即一个晶胞含有4个硫化钠分子,所以密度为 =g· 。
21.3d104s1 > CuO Cu O < Cu O中Cu的d轨道为全充满状态,较稳定
2 2
O>N [Cu(H O) (NH )]SO 254/(ρa3)
2 2 3 4 4
【详解】
(1)铜原子核电荷数为29,其基态原子的电子排布式为[Ar]3d104s1 ,则价电子排布式为
3d104s1 ,根据能级图可知其核外能级能量的高低3d>4s;
(2)元素A是短周期非金属元素,A的常见氧化物常温下为液态,其熔沸点比同主族其他元
素的氧化物高,可知A为氧元素;
① 甲中氧原子数目为8× +4× +2× +1=4,Cu原子数为4,则甲的化学式为CuO;乙中
氧原子数目为8× +1=2,Cu原子数为4,则乙的化学式为Cu O;
2
② 因 Cu O中Cu+的电子排布式为[Ar]3d10,而CuO中Cu2+的电子排布式为[Ar][Ar]3d9,明
2
显Cu+的d轨道为全充满状态,较稳定,故稳定性CuO<Cu O;
2
(3)两种配体都是10电子的中性分子,且都含氢元素,可知两配体分别为HO和NH ;
2 3
① 两种配体分子中N和O均有孤对电子,可与中心原子间形成配位键,O的非金属性比
N强,即电负性O>N,且NH 的稳定性小于HO,NH 的电子式为 ;
3 2 3
② 由该配合物阳离子的结构可知含有4个NH 和2个HO,则与SO 2-形成的配合物X的
3 2 4
化学式为 [Cu(H O) (NH )]SO ;
2 2 3 4 4
(4)由晶胞结构示意图可知,晶体的堆积模型为面心立方密堆积,晶胞中原子数目为6×
+8× =4,晶胞质量为4×63.5g÷N ,晶胞体积为(a cm)3,则4×63.5g÷N =ρg/cm3×(a cm)3,
A A
故N =254/(ρa3)mol-1。
A
22.分子 配位键 +Br → 或 +Br → 9
2 2
【详解】
本题考查晶体的判断、化学键类型、共面等知识,(1)二茂铁的熔点是173℃(在100℃时
开始升华),沸点是2.19℃,不溶于水,易溶于苯、乙醚等非极性溶剂,这是分子晶体的特
点,因此二茂铁晶体属于分子晶体;碳原子含有孤电子对,铁含有空轨道,所以碳原子和
铁原子之间形成配位键;(2)①环戊二烯中含有碳碳双键,与溴发生加成反应,因此反应方程式为. +Br → 或 +Br → ;②碳碳双键共面,
2 2
碳碳叁键共线以及三点确定一个平面,因此此分子中处于同一平面的原子个数最多有9个。
23.2 3s23p63d10 4 13 N>O>C O SO 或BF
3 3
平面三角形 5 sp3 分子中含有的S原子数越多,相对分子质量就越大,分子间
作用力就越大,物质的熔沸点就越高。 2 MC
8
【详解】
(1)硫是16号元素,根据构造原理,可知基态S原子核外电子排布式是1s22s22p63s23p4,p轨
道有3个,由于原子核外电子总是尽可能的成单排列,而且自旋方向相同,同一轨道最多
容纳2个电子,所以硫的基态原子核外有2个未成对电子。
溴是35号元素,价层电子排布式是4s24p5,则Br原子的基态原子价层电子排布图为
。
(2)Cu是29号元素,原子核外电子排布式是1s22s22p63s23p63d104s1,则基态铜原子的M能层
的电子排布式3s23p63d10。
铝原子核外排布式是1s22s22p63s1,s轨道有1个伸展方向,p轨道有3个伸展方向,所以Al
原子核外电子云有4种不同的伸展方向;Al原子核外13个电子的运动状态各不相同,因此
Al原子核外有13种不同运动状态的电子。
(3)一般情况下同一周期元素的第一电离能呈增大趋势,但第IIA、第VA元素原子处于轨道
的全满、半满的稳定状态,其第一电离能大于相邻元素,因此C、N、O三种元素,第一电
离能由大到小顺序为:N>O>C。
同一周期元素的电负性随原子序数的增大而增强,则C、N、O三种元素电负性大小关系为:
O>N>C,所以电负性最大的是O元素。
(4)与 互为等电子体的分子可以是SO 或BF。
3 3
的中心C原子价层电子对数为3+ =3,没有孤电子对,因此其立体构型为平
面三角形。
(5)共价单键都是σ键,在NH 中2个N原子之间以N-N键结合,每个N原子分别与2个
2 4
H原子形成共价键,故在NH 中含有的σ键数目是1+4=5个;N原子形成3个共价键,每
2 4
个N原子上还有1对孤电子对,因此其中N原子的杂化类型是sp3杂化。
(6)S 、S、S 都是由分子构成的物质,分子之间以分子间作用力结合。物质分子中含有的S
4 6 8
原子数越多,相对分子质量就越大,分子间作用力就越大,物质的熔沸点就越高。
(7)根据石墨结构可知:每个C原子与相邻的3个C原子形成共价键,每个C原子为3个六元环所共用,每个六边形含有6个这种C原子,故其中含有的C原子数为6× =2。
晶胞中M原子处于顶点、面心、内部4个;晶胞中每层石墨烯部分结构中有4条边(8个C
原子)处于晶胞面上,其它C原子处于晶胞内部。晶胞中M原子数目=8× +6× +4=8,C
原子数目=12×4+8×4× =64 ,M、C原子数目之比为1:8,则该插层化合物的化学式是
MC 。
8