文档内容
第2讲 分子结构与性质
[考纲要求]
1.了解共价键的形成、极性、类型(σ键和π键),了解配位键的含义。
2.能用键能、键长、键角等说明简单分子的某些性质。
3.了解杂化轨道理论及简单的杂化轨道类型(sp、sp2、sp3)。
4.能用价层电子对互斥理论或者杂化轨道理论推测简单分子或离子的空间结构。
5.了解范德华力的含义及对物质性质的影响。
6.了解氢键的含义,能列举存在氢键的物质,并能解释氢键对物质性质的影响。
考点一 共价键
1知识梳理
1.共价键的本质与特征
(1)本质:共价键的本质是在原子之间形成__________(电子云的____)。
(2)特征:具有______和______。
2.共价键的分类
分类依据 类型
____键 电子云“______”重叠
形成共价键的原子轨道重叠方式
____键 电子云“______”重叠
____键 共用电子对发生____
形成共价键的电子对是否偏移
____键 共用电子对不发生____
____键 原子间有____共用电子对
原子间共用电子对的数目 ____键 原子间有____共用电子对
____键 原子间有____共用电子对
3.键参数
(1)概念(2)键参数对分子性质的影响
①键能越____,键长越____,分子越稳定。
②
4.等电子原理
(1)等电子体:原子总数相同、______总数相同的粒子互称为等电子体。
(2)等电子原理:等电子体具有相似的化学键特征,它们的许多性质相近,此原理称为
等电子原理,例如CO和N 的____________等都非常相近。
2
[判断] (正确的打“√”,错误的打“×”)
(1)只有非金属原子之间才能形成共价键( )
(2)在所有分子中都存在化学键( )
(3)σ键可以绕键轴旋转,π键不能绕键轴旋转( )
(4)气体单质中一定存在σ键,可能存在π键( )
(5)σ键比π键的电子云重叠程度大,形成的共价键强( )
(6)σ键能单独形成,而π键一定不能单独形成( )
(7)碳碳三键和碳碳双键的键能分别是碳碳单键键能的3倍和2倍( )
(8)键长等于成键两原子的半径之和( )
(9)所有的共价键都有方向性( )
(10)O 分子中仅含非极性键( )
2
(11)CH
与NH+
互为等电子体( )
4 4
[提醒]
(1)只有两原子的电负性相差不大时,才能通过共用电子对形成共价键,当两原子的电负性相差很大(大于1.7)时,不会形成共用电子对,这时形成离子键。
(2)同种元素原子间形成的共价键为非极性键,不同种元素原子间形成的共价键为极性
键。
(3)常见的等电子体:N 与CO,CO 与NO,O
、NO−
与SO
,CO2− 、NO−
与SO
,PO3−
、
2 2 2 3 2 2 3 3 3 4
O2− O−
4 4
S 与Cl , 与BNH(硼氮苯)等。
3 3 6
2对点速练
练点一 共价键类型的判断
1.有以下物质:①HF;②Cl;③HO;④N;⑤CH。
2 2 2 2 4
(1)只含有极性键的是____________________________。
(2)只含有非极性键的是__________________________。
(3)既有极性键又有非极性键的是_____________________________。
(4)只含有σ键的是__________________________。
(5)既有σ键又有π键的是________________________。
2.COCl 分子的结构式为 ,COCl 分子内含有( )
2 2
A.4个σ键 B.2个σ键、2个π键
C.2个σ键、1个π键 D.3个σ键、1个π键
练后归纳
共价键类型的判断
(1)σ键与π键的判断
①由轨道重叠方式判断
“头碰头”重叠为σ键,“肩并肩”重叠为π键。
②由物质的结构式判断通过物质的结构式可以快速有效地判断共价键的种类及数目。共价单键全为σ键,双
键中有一个σ键和一个π键,三键中有一个σ键和两个π键。
③由成键轨道类型判断
s轨道形成的共价键全部是σ键;杂化轨道形成的共价键全部为σ键。
(2)极性键与非极性键的判断
看形成共价键的两原子,不同种元素的原子之间形成的是极性共价键,同种元素的原
子之间形成的是非极性共价键。
练点二 键参数的意义
3.关于键长、键能和键角的说法中不正确的是( )
A.键角是描述分子立体结构的重要参数
B.键长的大小与成键原子的半径和成键数目有关
C.键能越大,键长就越长,共价化合物也就越稳定
D.键角的大小与键长、键能的大小无关
4.Ⅰ.已知H、O、Cl、N 分子中共价键的键能依次为436 kJ·mol-1、497 kJ·mol-
2 2 2 2
1、243 kJ·mol-1、946 kJ·mol-1,
(1)下列叙述正确的是________。
1
A.N—N键键能为 ×946 kJ·mol-1=315.3 kJ·mol-1
3
B.氮分子中共价键的键长比氢分子中共价键的键长短
C.氧分子中氧原子是以共价单键结合的
D.氮分子比氯分子稳定
(2)计算反应3Cl+2NH===N+6HCl的反应热。
2 3 2
(已知:E =391 kJ·mol-1,E =432 kJ·mol-1)
N—H H—Cl
Ⅱ.乙苯催化脱氢制苯乙烯反应:计算上述反应的ΔH________ kJ·mol-1。
练点三 等电子原理的应用
5.下列粒子属于等电子体的是( )
A.CO2−
和SO B.NO和O
3 3 2
C.NO 和O D.HCl和HO
2 3 2
6.根据等电子原理判断,下列说法中错误的是( )
A.BNH 分子中所有原子均在同一平面上
3 3 6
B.BNH 分子中存在双键,可发生加成反应
3 3 6
C.HO+和NH 是等电子体,均为三角锥形
3 3
D.CH
和NH+
是等电子体,均为正四面体形
4 4
7.已知CO 为直线形结构,SO 为平面正三角形结构,NF 为三角锥形结构,试推测
2 3 3
COS、CO2−
、PCl 的空间结构。
3 3
练后归纳
常见等电子体的立体构型
等电子体类型 代表物质 立体构型四原子24电子等电子体 SO 平面三角形
3
四原子26电子等电子体
SO2−
三角锥形
3
五原子32电子等电子体 CCl 正四面体形
4
六原子40电子等电子体 PCl 三角双锥形
5
七原子48电子等电子体 SF 正八面体形
6
考点二 分子的立体构型
1知识梳理
1.价层电子对互斥理论
(1)理论要点
①价层电子对在空间上彼此相距最远时,排斥力____,体系的能量____。
②孤电子对的排斥力较大,孤电子对越多,排斥力越强,键角越小。
(2)价层电子对互斥模型与分子立体构型的关系
电子 成键 孤电子 电子对 分子立
实例 键角
对数 对数 对数 立体构型 体构型
2 2 0 直线形 ______ ____ ____
______
3 0 ____ ____
平面 ______
3
三角形
_____
2 1 ____ ______
_
______
4 0 ____ ____
正四面 ______
4
3 1 体形 ________ ____ ____
2 2 ____ ____ ____
2.杂化轨道理论
(1)杂化轨道概念:在外界条件的影响下,原子内部________的原子轨道重新组合的过
程叫原子轨道的杂化,组合后形成的一组新的原子轨道,叫杂化原子轨道,简称杂化轨道。
(2)杂化轨道的类型与分子立体构型
杂化 杂化轨 杂化轨 立体构型 实例类型
道数目 道间夹角
sp ______ ______ ______ ______
sp2 ______ ______ ______ ______
sp3 ______ ______ ______ ______
3.配位键和配合物
(1)孤电子对
分子或离子中没有跟其他原子共用的电子对称孤电子对。
(2)配位键
①配位键的形成:成键原子一方提供________,另一方提供______形成共价键。
②配位键的表示:常用“______”来表示配位键,箭头指向接受孤电子对的原子,如
H+ H+
4 4
N 可表示为 ,在N 中,虽然有一个N—H键形成过程与其他
3个N—H键形成过程不同,但是一旦形成之后,4个共价键就完全相同。
(3)配合物
如[Cu(NH)]SO
3 4 4
配体有孤电子对,如HO、NH、CO、F-、Cl-、CN-等。
2 3
中心原子有空轨道,如Fe3+、Cu2+、Zn2+、Ag+等。
[思考]N 分子中σ键与π键的数目比n(σ)∶n(π)=________。[Fe(HO)]2+与NO反应生
2 2 6
成的[Fe(NO)(HO)]2+中,NO以N原子与Fe2+形成配位键。请在[Fe(NO)(HO)]2+结构示意图
2 5 2 5
的相应位置补填缺少的配体。
[判断] (正确的打“√”,错误的打“×”)
(1)杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对( )
(2)分子中中心原子若通过sp3杂化轨道成键,则该分子一定为正四面体结构( )
(3)NH 分子为三角锥形,N原子发生sp2杂化( )
3
(4)只要分子构型为平面三角形,中心原子均为sp2杂化( )
(5)中心原子是sp杂化的,其分子构型不一定为直线形( )
(6)杂化轨道间的夹角与分子内的键角不一定相同( )
(7)中心原子杂化类型相同时孤电子对数越多,键角越小( )
(8)杂化轨道与参与杂化的原子轨道数目相同,但能量不同( )
[提醒]
(1)价层电子对互斥模型是价层电子对的立体构型,而分子的立体构型指的是成键电
子对的立体构型,不包括孤电子对。两者是否一致取决于中心原子上有无孤电子对(未用于
形成共价键的电子对),当中心原子上无孤电子对时,两者的构型一致;当中心原子上有孤
电子对时,两者的构型不一致。
(2)价层电子对互斥理论能预测分子的立体构型,但不能解释分子的成键情况,杂化轨
道理论能解释分子的成键情况,但不能预测分子的立体构型。两者相结合,具有一定的互补
性,可达到处理问题简便、迅速、全面的效果。
2对点速练
练点一 “两理论”和“一构型”
1.用价层电子对互斥理论(VSEPR)预测HS和COCl 的立体结构,两个结论都正确的是
2 2
( )
A.直线形;三角锥形 B.V形;三角锥形
C.直线形;平面三角形 D.V形;平面三角形
2.氮的最高价氧化物为无色晶体,它由两种离子构成,已知其阴离子构型为平面三角
形,则其阳离子的构型和阳离子中氮的杂化方式为( )
A.直线形 sp杂化 B.V形 sp2杂化
C.三角锥形 sp3杂化 D.平面三角形 sp2杂化
3.BeCl 是共价分子,可以以单体、二聚体和多聚体形式存在。它们的结构简式如下,
2请写出单体、二聚体和多聚体中Be的杂化轨道类型:
4.(1)石墨烯(图甲)是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分
碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯(图乙)。
①图甲中,1号C与相邻C形成σ键的个数为________。
②图乙中,1 号 C 的杂化方式是________,该 C 与相邻 C 形成的键角________(填
“>”“<”或“=”)图甲中1号C与相邻C形成的键角。
(2)碳元素的单质有多种形式,下图依次是C 、石墨和金刚石的结构图:
60
①金刚石、石墨、C 、碳纳米管等都是碳元素的单质形式,它们互为________。
60
②金刚石、石墨烯(指单层石墨)中碳原子的杂化形式分别为________、________。
5.NH 分子中∠HNH 键角为 107°,而配离子[Zn(NH)]2+中∠HNH 的键角为
3 3 6
109°28′ , 配 离 子 [Zn(NH)]2 + ∠ HNH 键 角 变 大 的 原 因 是
3 6__________________________________。
方法总结
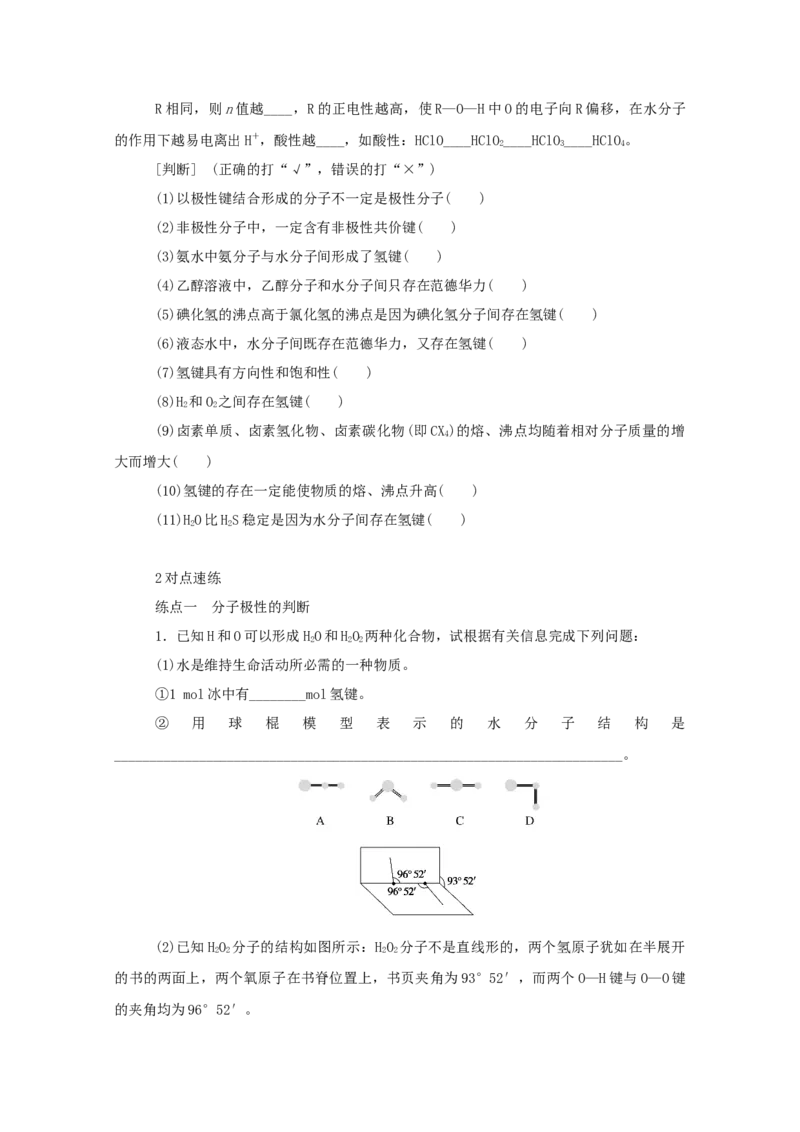
判断分子或离子立体构型“三步曲”
第一步:确定中心原子上的价层电子对数
a为中心原子的价电子数加减离子的电荷数,b为配位原子提供的价电子数,x为非中心原子
的原子个数。
1 1
如NH+
的中心原子为N,a=5-1,b=1,x=4,所以中心原子孤电子对数= (a-xb)=
4 2 2
×(4-4×1)=0。
第二步:确定价层电子对的立体构型
由于价层电子对之间的相互排斥作用,它们趋向于尽可能的相互远离,这样已知价层电子对
的数目,就可以确定它们的立体构型。
第三步:分子立体构型的确定
价层电子对有成键电子对和孤电子对之分,价层电子对的总数减去成键电子对数,得
孤电子对数。根据成键电子对数和孤电子对数,可以确定相应的较稳定的分子立体构型。
练点二 配位键与配合物
6.锂—磷酸氧铜电池正极的活性物质是CuO(PO),可通过下列反应制备:
4 4 2
2NaPO+4CuSO+2NH·HO===CuO(PO)↓+3NaSO+(NH)SO+HO
3 4 4 3 2 4 4 2 2 4 4 2 4 2
请回答下列问题:
(1)上述化学方程式中涉及的N、O、P元素的电负性由小到大的顺序是________。
(2)基态S原子的价电子排布式为________。
(3)(NH)SO 中含有化学键的类型为________。
4 2 4
(4)PO3−
的立体构型是________,其中P原子的杂化方式为________。
4(5)在硫酸铜溶液中加入过量KCN溶液,生成配合物[Cu(CN)]2-,则1 mol CN-中含有
4
的π键数目为____________,1 mol[Cu(CN)]2-中含有的σ键数目为________。
4
7.Ⅰ.铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,五
水硫酸铜可用做杀菌剂。
向CuSO 溶液中加入过量NaOH溶液可生成[Cu(OH)]2-。不考虑空间构型,[Cu(OH)]2-
4 4 4
结构可用示意图表示为____________。
Ⅱ.经研究表明,Fe(SCN) 是配合物,Fe3+与SCN-不仅能以1∶3的个数比配合,还可
3
以其他个数比配合。请按要求填空:
(1)若所得的Fe3+和SCN-的配合物中,主要是Fe3+与SCN-以个数比1∶1配合所得离子
显红色。该离子的离子符号是________。
(2)若Fe3+与SCN-以个数比1∶5配合,则FeCl 与KSCN在水溶液中发生反应的化学方
3
程式可以表示为__________________________________。
考点三 分子间作用力
1知识梳理
1.分子间作用力
(1)概念
物质分子之间普遍存在的相互作用力,称为分子间作用力。
(2)分类
分子间作用力最常见的是________和____。
(3)强弱
范德华力____氢键____化学键。
(4)范德华力
范德华力越强,物质的熔点、沸点越高,硬度越大。一般来说,__________相似的物
质,随着____________的增加,范德华力逐渐____。
(5)氢键
①形成
已经与__________的原子形成共价键的______(该氢原子几乎为裸露的质子)与另一个
分子中__________的原子之间的作用力,称为氢键。
②表示方法
A—H…B③特征
具有一定的____性和____性。
④分类
氢键包括______氢键和______氢键两种。
⑤分子间氢键对物质性质的影响
主要表现为使物质的熔、沸点____,对电离和溶解度等产生影响。
2.分子的性质
(1)分子的极性
类型 非极性分子 极性分子
正电中心和负电中心____的分 正电中心和负电中心______的
形成原因
子 分子
存在的共价键 非极性键或极性键 ______________
分子内原子排列 ____________ ____________
(2)分子的溶解性
①“相似相溶”的规律:非极性溶质一般能溶于______溶剂,极性溶质一般能溶于
____溶剂。若溶剂和溶质分子之间可以形成氢键,则溶质的溶解度____。
②随着溶质分子中憎水基个数的增大,溶质在水中的溶解度减小。如甲醇、乙醇和水
以任意比互溶,而戊醇在水中的溶解度明显减小。
(3)分子的手性
①手性异构:具有完全相同的组成和原子排列的一对分子,如同左手和右手一样互为
____,在三维空间里________的现象。
②手性分子:具有__________的分子。
③手性碳原子:在有机物分子中,连有__________________的碳原子。含有手性碳原
子的分子是手性分子,如
(4)无机含氧酸分子的酸性
无机含氧酸的通式可写成(HO)RO,如果成酸元素
m nR相同,则n值越____,R的正电性越高,使R—O—H中O的电子向R偏移,在水分子
的作用下越易电离出H+,酸性越____,如酸性:HClO____HClO____HClO____HClO。
2 3 4
[判断] (正确的打“√”,错误的打“×”)
(1)以极性键结合形成的分子不一定是极性分子( )
(2)非极性分子中,一定含有非极性共价键( )
(3)氨水中氨分子与水分子间形成了氢键( )
(4)乙醇溶液中,乙醇分子和水分子间只存在范德华力( )
(5)碘化氢的沸点高于氯化氢的沸点是因为碘化氢分子间存在氢键( )
(6)液态水中,水分子间既存在范德华力,又存在氢键( )
(7)氢键具有方向性和饱和性( )
(8)H 和O 之间存在氢键( )
2 2
(9)卤素单质、卤素氢化物、卤素碳化物(即CX)的熔、沸点均随着相对分子质量的增
4
大而增大( )
(10)氢键的存在一定能使物质的熔、沸点升高( )
(11)HO比HS稳定是因为水分子间存在氢键( )
2 2
2对点速练
练点一 分子极性的判断
1.已知H和O可以形成HO和HO 两种化合物,试根据有关信息完成下列问题:
2 2 2
(1)水是维持生命活动所必需的一种物质。
①1 mol冰中有________mol氢键。
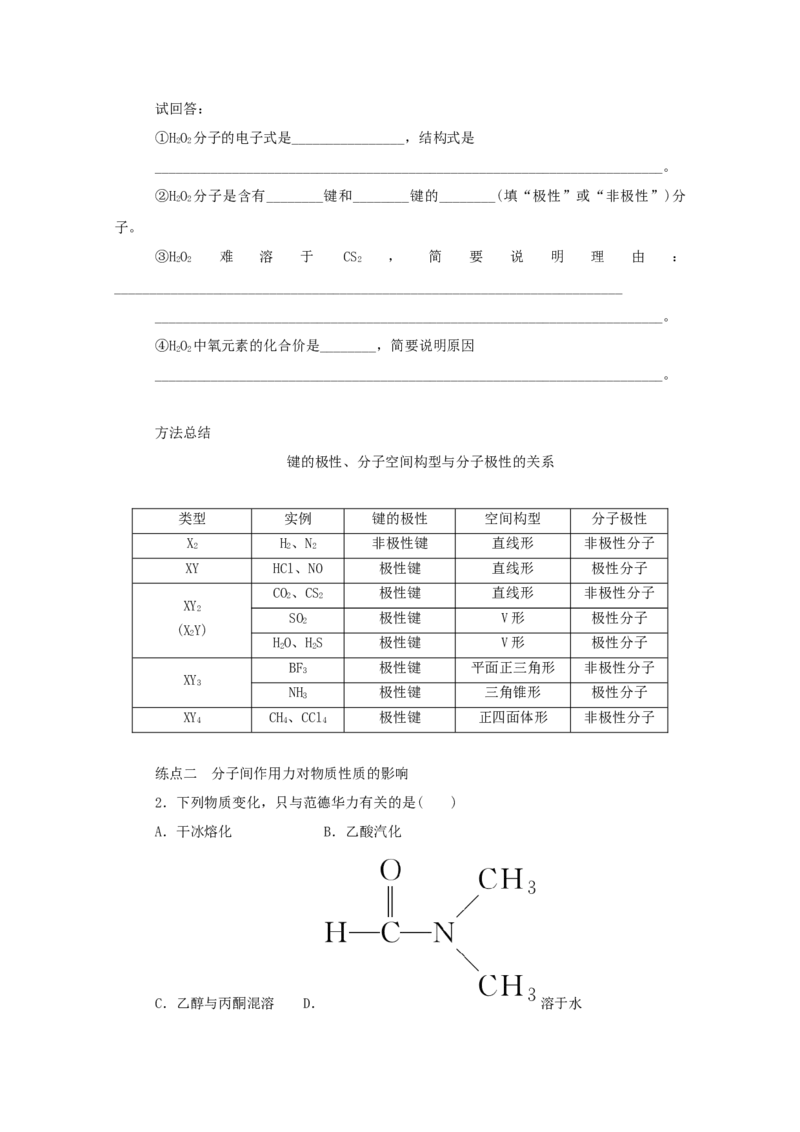
② 用 球 棍 模 型 表 示 的 水 分 子 结 构 是
________________________________________________________________________。
(2)已知HO 分子的结构如图所示:HO 分子不是直线形的,两个氢原子犹如在半展开
2 2 2 2
的书的两面上,两个氧原子在书脊位置上,书页夹角为93°52′,而两个O—H键与O—O键
的夹角均为96°52′。试回答:
①HO 分子的电子式是________________,结构式是
2 2
________________________________________________________________________。
②HO 分子是含有________键和________键的________(填“极性”或“非极性”)分
2 2
子。
③HO 难 溶 于 CS , 简 要 说 明 理 由 :
2 2 2
________________________________________________________________________
________________________________________________________________________。
④HO 中氧元素的化合价是________,简要说明原因
2 2
________________________________________________________________________。
方法总结
键的极性、分子空间构型与分子极性的关系
类型 实例 键的极性 空间构型 分子极性
X H、N 非极性键 直线形 非极性分子
2 2 2
XY HCl、NO 极性键 直线形 极性分子
CO、CS 极性键 直线形 非极性分子
2 2
XY
2
SO 极性键 V形 极性分子
2
(XY)
2
HO、HS 极性键 V形 极性分子
2 2
BF 极性键 平面正三角形 非极性分子
3
XY
3
NH 极性键 三角锥形 极性分子
3
XY CH、CCl 极性键 正四面体形 非极性分子
4 4 4
练点二 分子间作用力对物质性质的影响
2.下列物质变化,只与范德华力有关的是( )
A.干冰熔化 B.乙酸汽化
C.乙醇与丙酮混溶 D. 溶于水E.碘溶于四氯化碳 F.石英熔融
3.按要求回答下列问题:
(1)HCHO分子的立体构型为________形,它加成产物的熔、沸点比CH 的熔、沸点高,
4
其 主 要 原 因 是 ( 须 指 明 加 成 产 物 是 何 物
质)________________________________________________________________________。
(2)S位于周期表中第________族,该族元素氢化物中,HTe比HS沸点高的原因是
2 2
________________________________________________________________________
________________________________________________________________________,
HO 比 HTe 沸 点 高 的 原 因 是
2 2
________________________________________________________________________
________________________________________________________________________。
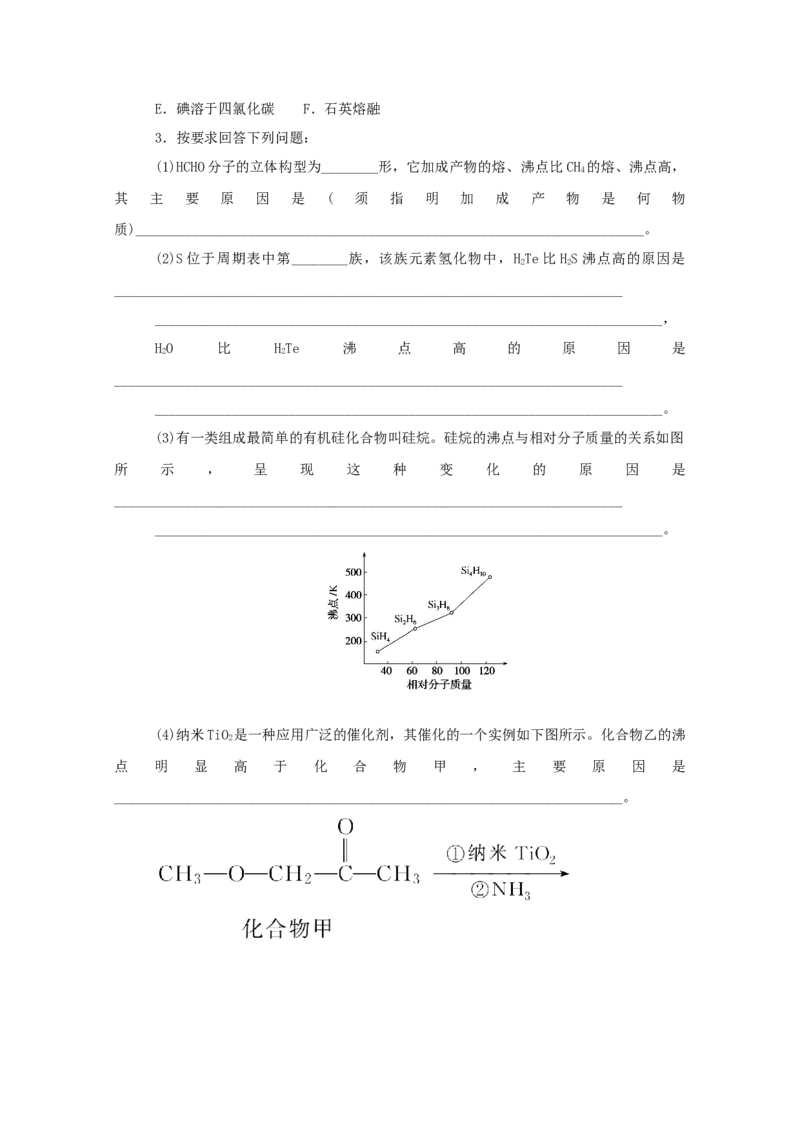
(3)有一类组成最简单的有机硅化合物叫硅烷。硅烷的沸点与相对分子质量的关系如图
所 示 , 呈 现 这 种 变 化 的 原 因 是
________________________________________________________________________
________________________________________________________________________。
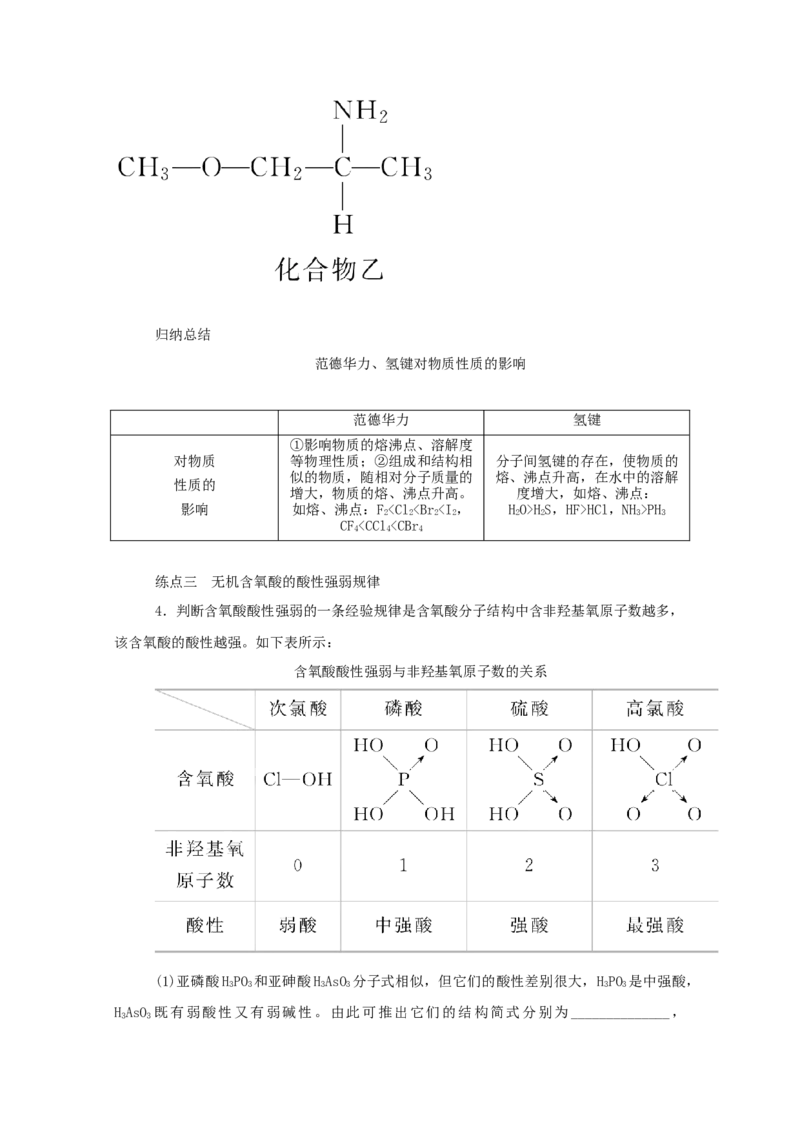
(4)纳米TiO 是一种应用广泛的催化剂,其催化的一个实例如下图所示。化合物乙的沸
2
点 明 显 高 于 化 合 物 甲 , 主 要 原 因 是
________________________________________________________________________。归纳总结
范德华力、氢键对物质性质的影响
范德华力 氢键
①影响物质的熔沸点、溶解度
对物质 等物理性质;②组成和结构相 分子间氢键的存在,使物质的
似的物质,随相对分子质量的 熔、沸点升高,在水中的溶解
性质的
增大,物质的熔、沸点升高。 度增大,如熔、沸点:
影响 如熔、沸点:FHS,HF>HCl,NH>PH
2 2 2 2 2 2 3 3
CFO>C。(3)价电子总数相同,原子总数相同的微粒互为等
电子体,考虑与N元素相邻主族的元素,可知与NH+
互为等电子体的分子是CH 或SiH 。(4)
4 4 4
单键都是σ键,双键中有一个σ键,则1 mol柠檬酸分子中碳原子与氧原子形成7 mol σ
键。
答案:(1)[Ar]3d64s2或1s22s22p63s23p63d64s2 O
(2)sp3 N>O>C (3)CH 或SiH (4)7
4 4
3.解析:(1)Ti 是 22 号元素,所以基态 Ti 原子的核外电子排布式为
1s22s22p63s23p63d24s2。
(2)氟元素非金属性强,TiF 为离子化合物,熔点最高,TiCl 、TiBr 、TiI 为共价化
4 4 4 4
合物,熔点较低,且TiCl 、TiBr 、TiI 结构相似,相对分子质量越大,分子间作用力越强,
4 4 4
熔点越高。
(3)元素的非金属性越强,电负性越大,所以Ca、Ti、O三种元素中,O电负性最大,
Ca的金属性强于Ti,则Ti的电负性强于Ca;阴、阳离子间的作用力为离子键;距离Ca2+最
近的为O2-,共有12个O2-与位于体心处的Ca2+距离相等且最近,故Ca2+的配位数为12。
(4)距离Pb2+最近的是处于面心的I-,Pb2+的配位数为6,图(a)中Ti4+的配位数也为
6,其与图(b)中Pb2+的空间位置相同;CHNH+
中,氮原子形成4个单键,其中有1个是配位
3 3
键,N原子采取sp3杂化;根据均摊法,1个晶胞中含有I-的个数为6×1/2=3,CHNH+
的个
3 3
数为8×1/8=1,Pb2+的个数为1,化学式为PbCHNHI ,摩尔质量为620 g·mol-1,一个晶
3 3 3
620 620
胞的质量为 g,体积为(a×10-7)3 cm3,则晶体密度为 ×1021 g·cm-3。
N a3×N
A A
(5)根据图(c)可知,箭头是由反应物指向生成物,则该过程中Pb和Eu3+反应生成Pb2+
和Eu2+,Eu2+与I 反应生成Eu3+和I-。
2
答案:(1)1s22s22p63s23p63d24s2
(2)TiF 为离子化合物,熔点高,其他三种均为共价化合物,随相对分子质量的增大分
4
子间作用力增大,熔点逐渐升高
(3)O>Ti>Ca 离子键 12620
(4)Ti4+ sp3 ×1021
a3×N
A
(5)2Eu3++Pb===2Eu2++Pb2+ 2Eu2++I===2Eu3++2I-
2
4.解析:(全国卷Ⅰ):(2)乙二胺分子中,氮原子核外孤电子对数为1,σ键数目为
3,则杂化轨道数目为4,故氮原子采取sp3杂化;碳原子核外孤电子对数为0,σ键数目为
4,则杂化轨道数目为4,故碳原子采取sp3杂化。乙二胺的两个N提供孤对电子给Mg2+、Cu2
+等金属离子,以配位键结合成稳定环状离子。
(3)一般来说,晶体熔点:原子晶体>离子晶体>分子晶体。LiO、MgO均为离子晶体,
2
晶格能:LiOLiO;PO 、SO 均为分子晶体,相对分子质量:PO>SO ,
2 2 4 6 2 4 6 2
则分子间作用力:PO>SO,故熔点:PO>SO。
4 6 2 4 6 2
(全国卷Ⅱ):(1)AsH 中As原子价层电子对数为4,其中有一对孤对电子,故AsH 立体
3 3
结构为三角锥形。NH 分子间可以形成氢键,导致NH 沸点高于AsH。
3 3 3
(全国卷Ⅲ):(2)双聚FeCl 分子中两分子FeCl 以配位键形式结合在一起,结构式为
3 3
,Fe的配位数为4。
(4)根据NHHPO 中所含元素在周期表中的位置关系和电负性规律可知,氧元素电负性
4 2 4
最高。NHHPO 中磷原子的价层电子对数为4,故为sp3杂化,P的sp3杂化轨道与O的2p轨道
4 2 4
形成σ键。
答案:(全国卷Ⅰ): (2)sp3 sp3 乙二胺的两个N提供孤对电子给金属离子形成配位
键 Cu2+
(3)LiO、MgO为离子晶体,PO 、SO 为分子晶体。晶格能MgO>LiO,分子间力(分子
2 4 6 2 2
量)PO>SO
4 6 2
(全国卷Ⅱ):(1)三角锥形 低 NH 分子间存在氢键
3(全国卷Ⅲ):(2) 4
(4)O sp3 σ
5.解析:(全国卷Ⅰ):(3)[AlH]-中Al采用sp3杂化,呈正四面体结构。四氢铝锂中
4
存在离子键、配位键和共价键,配位键也是σ键。
(全国卷Ⅱ):(2)价层电子对数包括成键电子对数和孤电子对数,HS中S的成键电子
2
6−1×2 6+1×2
对数为2,孤电子对数为 =2,故价层电子对数为4(或价层电子对数为 =
2 2
6+0×2 6+0×3
4),同理,SO 中S的价层电子对数为 =3,SO 中S的价层电子对数为 =3,
2 2 3 2
HS中S的价层电子对数不同于SO、SO。
2 2 3
(3)S 和SO 均为分子晶体,分子间存在的作用力均为范德华力,S 的相对分子质量大,
8 2 8
分子间范德华力强,故熔点和沸点高。
(4)气态SO 为单分子,分子中S无孤电子对,其分子的立体构型为平面三角形,S和O
3
之间形成双键,故共价键有σ键和π键两种。固态SO 为三聚分子,分子中每个S与4个O
3
成键,S无孤电子对,故原子的杂化轨道类型为sp3。
(全国卷Ⅲ):(3)根据ZnF 晶体的熔点较高可知,ZnF 为离子晶体,含有离子键,而
2 2
ZnCl、ZnBr、ZnI 的化学键以共价键为主、极性较小,故能够溶解在有机溶剂中。
2 2 2
(4)CO2− 中碳原子的价层电子对数为3,中心碳原子采取sp2杂化,故CO2−
的空间构型
3 3
为平面三角形。
答案:(全国卷Ⅰ):(3)正四面体 sp3 AB
(全国卷Ⅱ):(2)HS
2
(3)S 相对分子质量大,分子间范德华力强
8
(4)平面三角 2 sp3杂化
(全国卷Ⅲ):(3)离子键 ZnF 为离子化合物,ZnCl 、ZnBr 、ZnI 的化学键以共价键
2 2 2 2
为主、极性较小
(4)平面三角形 sp2杂化7+2−1
6.解析:(全国卷Ⅰ):(3)I+
离子中价层电子对数为 =4,中心原子为sp3杂
3 2
化,理论构型为四面体形,有2对孤对电子,故离子为V形。
(全国卷Ⅱ):(3)①结合图(b)可知:晶体R中两种阳离子为NH+
和HO+,两种阳离子
4 3
的中心原子均采取sp3杂化;NH+
中成键电子对数为4,HO+中含1个孤电子对和3个成键电
4 3
子对,即中心原子的价层电子对数均为4;两种阳离子中均存在极性键,不存在非极性键。N
H+
和HO+分别为正四面体结构和三角锥形结构,即立体结构不同。②从图(b)可以看出:阴
4 3
离子N− 呈五元环状结构,其含有的σ键总数为5个;N−
中参与形成大π键的电子数为6,
5 5
故可将其中的大π键表示为π6 。③根据图(b)还有的氢键是:(HO+)O—H…N (NH+ )N—H…
5 3 4
N。
(全国卷Ⅲ):(2)根据价层电子对互斥理论,CO 中C原子价层电子对数为2,为sp杂
2
化,而CHOH中C原子的价层电子对数为4,为sp3杂化;
3
(3)影响分子晶体沸点的因素有范德华力和氢键,HO与CHOH均为极性分子,HO中氢
2 3 2
键比甲醇多,故HO的沸点高,CO 与H 均为非极性分子,CO 相对分子质量较大,范德华力
2 2 2 2
大,沸点更高。
(4)Mn(NO)
为离子化合物,Mn2+与NO− 之间是离子键,根据NO−
的结构式,N与O之
3 2 3 3
间存在双键,故除了σ键还存在离子键和π键。
答案:(全国卷Ⅰ):(3)V形 sp3
(全国卷Ⅱ):(3)①ABD C ②5
∏6
5
③(HO+)O—H…N(N−
)
(NH+ )N—H…N(N−
)
3 5 4 5
(全国卷Ⅲ):(2)sp sp3
(3)HO>CHOH>CO>H HO与CHOH均为极性分子,HO中氢键比甲醇多;CO 与H 均为
2 3 2 2 2 3 2 2 2
非极性分子,CO 分子量较大,范德华力较大
2
(4)离子键和π键