文档内容
第 23 讲 氮及其化合物
复习目标 1.了解氮元素单质及其重要化合物的制备方法,掌握其主要性质及应用。2.了
解氮的化合物对环境的影响。
考点一 氮及其氧化物
1.氮的固定
2.氮气
(1)物理性质:无色无味气体,密度比空气略小,难溶于水。
(2)化学性质写出有关化学方程式:
①3Mg+N=====MgN;
2 3 2
②N+3H2NH ;
2 2 3
③N+O========2NO。
2 2
3.氮的氧化物
(1)氮有多种价态的氧化物,氮元素从+1―→+5价都有对应的氧化物,如NO、NO、
2
NO、NO (或NO)、NO,其中属于酸性氧化物的是NO、NO。
2 3 2 2 4 2 5 2 3 2 5
(2)NO和NO 的比较
2
性质 NO NO
2
色、态、味 无色、无味的气体 红棕色、有刺激性气味的气体
溶解性 难溶于水 -
毒性 有毒,大气污染物之一 有毒,大气污染物之一
与水反应 不反应 3NO +HO===2HNO+NO
2 2 3
与氧气反应 2NO+O===2NO 不反应
2 2
提醒 ①NO 与NO 存在下列平衡:2NO NO ,因此实验测得NO 的平均相对分子质
2 2 4 2 2 4 2
量总大于46。②验证某无色气体为NO的方法是向无色气体中通入O(或空气),无色气体变
2
为红棕色。
4.氮氧化物对环境的污染及防治
(1)常见的污染类型
①光化学烟雾:NO 在紫外线作用下,与碳氢化合物发生一系列光化学反应,产生了一种有
x
毒的烟雾。
②酸雨:NO 排入大气中后,与水反应生成HNO 和HNO,随雨雪降到地面。
x 3 2
③破坏臭氧层:NO 可使平流层中的臭氧减少,导致地面紫外线辐射量增加。
2
④NO与血红蛋白结合使人中毒。
(2)常见的NO 尾气处理方法
x
①碱液吸收法
工业尾气中NO 常用碱液吸收处理,NO 、NO的混合气体能被足量烧碱溶液完全吸收的条
x 2
件是n(NO )≥n(NO)。
2
②催化转化法
在催化剂、加热条件下,氨可将氮氧化物转化为无毒气体(N ),或NO 与CO在一定温度下
2 x
催化转化为无毒气体(N 和CO)。一般适用于汽车尾气的处理。
2 2(1)固氮反应一定属于氧化还原反应(√)
(2)N 与O 在放电条件下直接化合成NO (×)
2 2 2
错因:N 与 O 在放电条件下生成 NO 。
2 2
(3)用向上排空气法收集铜粉与稀硝酸反应产生的气体(×)
错因: Cu 与稀硝酸生成 NO , NO 与空气中的 O 反应,不能用排空气法收集。
2
(4)NO 溶于水时,NO 是氧化剂,水是还原剂(×)
2 2
错因:NO 与 H O 反应, NO 既是氧化剂又是还原剂。
2 2 2
(5)可用NO 与水反应制取硝酸,故NO 是酸性氧化物(×)
2 2
错因:NO 与 H O 反应生成 HNO 和 NO ,所以 NO 不是酸性氧化物。
2 2 3 2
1.结合N、NO、NO 的化学性质,用化学方程式解释“雷雨发庄稼”的科学道理。
2 2
答案 ①N+O=====2NO
2 2
②2NO+O===2NO
2 2
③3NO +HO===2HNO+NO
2 2 3
2.NO 和溴蒸气均为红棕色气体,你用哪些实验方法鉴别二者?写出所用试剂和区别的现
2
象。
方案一:试剂________________,现象______________________________________________。
方案二:试剂________________,现象______________________________________________。
方案三:试剂________________,现象______________________________________________。
答案 方案一:AgNO 溶液 NO 中AgNO 溶液无明显变化,溴蒸气中产生浅黄色沉淀
3 2 3
方案二:CCl (或汽油) NO 中CCl (或汽油)仍为无色,溴蒸气中CCl (或汽油)的颜色加深
4 2 4 4
方案三:蒸馏水 NO 中蒸馏水不变色,溴蒸气中水的颜色加深(其他合理的答案均正确)
2
题组一 氮及氧化物的性质和应用
1.(2020·通化高三月考)下列有关氮气的说法正确的是( )
A.氮气是由氮原子构成的双原子分子,所以化学性质不活泼
B.1 mol N 可与3 mol H 完全反应生成2 mol NH
2 2 3
C.电闪雷鸣的雨天,雨水中会含有一定量的硝酸,其中发生的反应之一是 N +
2
2O===2NO
2 2
D.NO、NO 在一定条件下可相互转化,且二者都是引起光化学烟雾的大气污染物
2
答案 D
解析 A项,氮原子最外层有5个电子,氮与氮形成三对共用电子对,达8电子的稳定结构;
B项,氮气与氢气反应生成氨气是可逆反应;C项,氮气与氧气在放电的条件下生成一氧化氮;D项,NO和氧气反应生成NO ;NO 和水反应生成NO。
2 2
2.下列说法中错误的是( )
A.工业上利用合成氨实现人工固氮涉及氧化还原反应
B.通过灼热的铜粉,可以除去N 中的O
2 2
C.除去NO中的NO 气体的方法是将气体依次通入盛有水和浓HSO 的洗气瓶中
2 2 4
D.NO 与HO的反应中氧化剂与还原剂的质量之比为2∶1
2 2
答案 D
解析 NO 与HO的反应中氧化剂与还原剂的质量之比为1∶2。
2 2
3.如图为装有活塞的密闭容器,内盛22.4 mL一氧化氮。若通入11.2 mL氧气(气体体积均
在标准状况下测定),保持温度、压强不变,则容器内物质的密度为( )
A.等于1.369 g·L-1
B.等于2.054 g·L-1
C.在1.369 g·L-1和2.054 g·L-1之间
D.大于2.054 g·L-1
答案 D
解析 一氧化氮与氧气恰好发生反应生成了二氧化氮,
2NO + O === 2NO
2 2
2 1 2
22.4 mL 11.2 mL 22.4 mL
反应后生成了22.4 mL二氧化氮,假设二氧化氮的体积不变,则容器中气体的密度为
ρ(NO )=≈2.054 g·L-1,因存在转化平衡:2NO NO ,则混合气体的体积小于22.4 mL,
2 2 2 4
所以容器中气体的密度应大于2.054 g·L-1。
题组二 氮氧化物对环境的污染及防治
4.(2020·湖南怀化统一考试)化学与生产、生活、环境等社会实际密切相关。下列相关叙述
正确的是( )
A.SO 、CO、NO 都是可形成酸雨的气体
2 2 2
B.75%酒精消毒原理和“84”消毒液(主要成分NaClO)消毒的原理相同
C.纳米铁粉通过物理吸附去除污水中Hg2+、Pb2+等重金属离子
D.汽车尾气中含有的氮氧化物,会加剧酸雨的形成
答案 D
解析 SO 和NO 都是可形成酸雨的气体,CO 不能形成酸雨,但会造成温室效应,A项错
2 2 2
误;75%的酒精消毒的原理是使蛋白质发生变性,“84”消毒液是利用其主要成分NaClO的强氧化性杀菌消毒,原理不相同,B项错误;纳米铁粉能有效地处理污水中的 Hg2+、Pb2
+等重金属离子,与其还原性有关,C项错误。
5.工业上常采用生物硝化法将NH转化为NO来处理氨氮废水,工作流程如图,下列说法
错误的是( )
A.生物硝化法处理废水,会导致水体pH逐渐下降:NH+2O===NO+2H++HO
2 2
B.长期过量使用NH Cl等铵态化肥,易导致土壤酸化,水体富营养化
4
C.检验NH所需的试剂是浓NaOH溶液、湿润的蓝色石蕊试纸
D.微生物保持活性的pH范围为7~9,可以加入石灰石来调节水体的pH
答案 C
解析 NH Cl水解呈酸性,长期过量使用会导致土壤酸化,也会导致水体富营养化,B项正
4
确;检验NH应使用红色石蕊试纸,C项错误;生物硝化法处理废水会使水体呈酸性,可以
加入石灰石与H+反应来调节水体的pH,D项正确。
6.(1)汽车尾气中的CO、NO 在适宜温度下采用催化转化法处理,使它们相互反应生成参
x
与 大 气 循 环 的 无 毒 气 体 。 写 出 NO 被 CO 还 原 的 化 学 方 程 式 :
_____________________________。
(2)用氨可将氮氧化物转化为无毒气体。如4NH +6NO=====5N+6HO。
3 2 2
写出氨气转化NO 的化学方程式:_________________________________________________,
2
该反应中氧化产物与还原产物的质量之比为________。
(3)工业尾气中氮的氧化物常采用碱液吸收法处理。
①NO 被烧碱溶液吸收时,生成两种钠盐,其物质的量之比为 1∶1,写出该反应的化学方
2
程式:________________________________________________________________________。
②NO与NO 按物质的量之比1∶1被足量NaOH溶液完全吸收后只得到一种钠盐,该钠盐
2
的 化 学 式 是
_______________________________________________________________________。
答案 (1)2CO+2NO=====N+2CO
2 2
(2)8NH +6NO =====7N+12HO 4∶3
3 2 2 2
(3)①2NO +2NaOH===NaNO +NaNO +HO
2 3 2 2
②NaNO
2
考点二 典型的氧化性酸——硝酸
1.物理性质硝酸是无色易挥发的液体,有刺激性气味。
2.化学性质
(1)不稳定性
反应:4HNO(浓) =======2HO+4NO ↑+O↑。
3 2 2 2
(2)强氧化性
硝酸无论浓、稀都有强氧化性,而且浓度越大,氧化性越强。
按要求完成下列反应的方程式:
①与金属反应:
稀硝酸与铜反应:
3Cu+8HNO(稀)===3Cu(NO )+2NO↑+4HO;
3 3 2 2
浓硝酸与铜反应:
Cu+4HNO(浓)===Cu(NO )+2NO ↑+2HO。
3 3 2 2 2
②与非金属反应:
浓硝酸与C的反应:
C+4HNO(浓)=====CO↑+4NO ↑+2HO。
3 2 2 2
③与还原性化合物反应:
硝酸可氧化HS、SO 、NaSO 、HI、Fe2+等还原性物质。
2 2 2 3
稀硝酸与FeSO 溶液反应的离子方程式:
4
3Fe2++4H++NO===3Fe3++NO↑+2HO。
2
(3)与有机物反应
①硝化反应(与 反应):
+HNO――→ +HO;
3 2
②颜色反应:含有苯基的蛋白质遇到浓硝酸时变黄色。
(1)实验室也可用锌粒与稀硝酸制取氢气(×)
错因:HNO 有强氧化性,与金属反应时不放出 H 。
3 2
(2)常温下,铁、铝在浓硝酸中的钝化为化学变化(√)
(3)可用稀硝酸与FeS固体反应制取HS(×)
2
错因:HNO 会将- 2 价的硫氧化成单质硫 。
3(4)铜溶于稀硝酸不能体现硝酸的酸性(×)
错因: Cu 与 HNO 反应,生成 Cu(NO ) ,体现 HNO 的酸性。
3 3 2 3
(5)在酸性条件下,NO与I-、Fe2+、SO等离子能大量共存(×)
错因: NO 在酸性条件下有强氧化性,会将 I - 、 Fe 2 + 、 SO 等还原性离子氧化 。
(1)HNO 与金属反应一般不能产生H。
3 2
(2)硝酸的还原产物不只有NO 和NO,很稀的硝酸还原产物也可能为NO、N 或NH NO 。
2 2 2 4 3
(3)硝酸与金属反应时既表现氧化性又表现酸性。
(4)涉及HNO 的离子反应常见的易错问题
3
①忽视NO在酸性条件下的强氧化性。在酸性条件下 NO不能与Fe2+、I-、SO、S2-等还原
性较强的离子大量共存。
②在书写离子方程式时,忽视HNO 的强氧化性,将氧化还原反应简单地写成复分解反应,
3
如易错易混辨析中的(3)。
1.将浓硝酸存放在无色试剂瓶中,一段时间后观察到溶液变黄,用化学方程式解释变黄的
原因,由此得到启示,如何保存浓硝酸?
答案 4HNO(浓) =======2HO+4NO ↑+O↑,浓硝酸应保存在棕色试剂瓶中,并置于
3 2 2 2
阴凉处。
2.用动态观点理解Cu与浓HNO 的反应
3
向一定量的浓硝酸中加入过量的铜片。
①反应开始阶段产生________________色气体,化学方程式为__________________________。
②反应进行一段时间后又产生无色气体,此时的化学方程式为_________________________。
③待反应停止后,再加入少量的稀硫酸,这时 Cu 片上又有气泡产生,原因是
_______________。
答案 ①红棕 Cu+4HNO(浓)===Cu(NO )+2NO ↑+2HO
3 3 2 2 2
②3Cu+8HNO(稀)===3Cu(NO )+2NO↑+4HO
3 3 2 2
③加入稀硫酸后,氢离子与原溶液中硝酸根离子构成强氧化性酸,又能与过量的铜反应
题组一 硝酸的性质及应用
1.(2019·潍坊期末)硝酸是化学实验室中最常用的试剂之一,下列有关硝酸的说法不正确的
是( )
A.浓硝酸和氯水用棕色试剂瓶保存,原理相同
B.将分别蘸有浓硝酸和浓氨水的玻璃棒相互靠近时,有白烟生成
C.常温下铁和铂都不溶于浓硝酸,原理相同D.浓硝酸溅到皮肤上,皮肤会变黄
答案 C
解析 A项,HNO 和氯水中的HClO见光都易分解,都应避光保存,正确;B项,浓HNO
3 3
和浓氨水都具有挥发性,HNO 与NH 化合生成白色固体小颗粒NH NO ,正确;C项,常
3 3 4 3
温下,铁在浓硝酸中钝化,而Pt与浓硝酸不反应,原理不同,错误;D项,浓HNO 能使蛋
3
白质显黄色,正确。
2.将相同质量的铜分别与足量的浓硝酸、稀硝酸反应,下列叙述正确的是( )
A.硝酸浓度越大消耗的硝酸越少,产生的有毒气体也越少
B.反应中转移的电子总数:稀硝酸少于浓硝酸
C.试管内壁上的铜用浓硝酸除去比用稀硝酸好,因为反应速率快
D.两者用排水法收集的气体的体积相同
答案 D
解析 铜完全反应,在进行相关计算时以铜为标准,等质量的铜在反应中失去的电子数相同,
生成的Cu(NO ) 的量相同,浓硝酸被还原为NO ,化合价由+5降到+4,每个氮原子只得
3 2 2
到1个电子,稀HNO 被还原时每个氮原子得到3个电子,故被还原的浓硝酸多、稀硝酸少,
3
生成的NO 也比NO多。用排水法收集气体时,由于会发生反应:3NO +HO===2HNO +
2 2 2 3
NO,故两种情况收集到的气体一样多。
3.某化学兴趣小组进行了有关Cu、硝酸、硫酸化学性质的实验,实验过程如图所示。下列
有关说法正确的是( )
A.①中溶液呈蓝色,试管口有红棕色气体产生,稀硝酸被还原为NO
2
B.③中反应的离子方程式为3Cu+2NO+8H+===3Cu2++2NO↑+4HO
2
C.③中滴加稀硫酸,铜片继续溶解,说明稀硫酸的氧化性比稀硝酸的强
D.由上述实验可知,Cu在常温下既可与稀硝酸反应,又可与稀硫酸反应
答案 B
解析 Cu与稀硝酸发生反应3Cu+8HNO(稀)===3Cu(NO )+2NO↑+4HO,稀硝酸被还原
3 3 2 2
为NO,NO遇空气中的O 生成NO ,故试管口有红棕色气体产生,A错误;③中溶液含有
2 2
NO,滴加稀硫酸后,Cu、NO、H+继续反应生成NO,B正确;③中铜片继续溶解,是因为
稀硫酸提供H+,与NO形成HNO ,继续与Cu反应,C错误;Cu是不活泼金属,在常温下,
3
可与稀硝酸反应,但不能与稀硫酸反应,D错误。
题组二 硝酸反应产物综合实验探究题
4.(2020·桂林高三测试)某校课外活动小组为了探究铜与稀硝酸反应产生的气体主要是 NO而设计了下列实验,装置如图所示(加热装置和固定装置均已略去)。图中K为止水夹(处于
关闭状态),F是一半空的注射器。请回答有关问题:
(1)设计装置A的目的是_______________________________________________________。
(2)在完成(1)中的“操作”后,将装置B中铜丝插入稀硝酸并微热,观察到装置B中的现象
是___________________________________________________________________________;
B中反应的离子方程式为_______________________________________________________。
(3)装置E和F的作用是________________________________________________________;
为实现此作用,其操作方法是___________________________________________________。
(4)装置D的作用是吸收多余的氮氧化物,防止污染空气,兼有____________的功能。
答案 (1)产生CO,赶走装置中的空气,防止因NO与O 反应生成NO 而产生干扰
2 2 2
(2)Cu丝表面产生气泡,稀硝酸液面上方仍为无色,溶液变蓝 3Cu+8H++2NO===3Cu2+
+2NO↑+4HO
2
(3)验证NO的生成 将注射器中的空气推入E中,若气体变为红棕色则说明生成了NO
(4)防止倒吸
考点三 氨 铵盐
1.氨的分子结构和物理性质
电子式 密度 气味 水溶性
比空气小 刺激性气味 极易溶于水(1∶700)
2.氨的化学性质提醒 ①NH 是中学化学中唯一的碱性气体,能使湿润的红色石蕊试纸变蓝,可在推断题
3
中作为解题突破口。
②氨水呈碱性,NH ·H O属于一元弱碱,计算氨水的浓度时,溶质按NH 进行计算。
3 2 3
3.铵盐及NH的检验
(1)铵盐的物理性质
铵盐都是白色固体,均易溶于水。
(2)铵盐的化学性质
(3)NH的检验步骤
未知液――→呈碱性――→使湿润的红色石蕊试纸变蓝色,则证明含NH。
4.氨的实验室制法
(1)加热固态铵盐和碱的混合物
→
↓
→用碱石灰干燥
↓
→用向下排空气法。收集时,一般在管口塞一团棉花球,可减小NH 与空气的对流速率,
3
收集到纯净的NH
3
↓
→①将湿润的红色石蕊试纸置于试管口,试纸变蓝;
②将蘸有浓盐酸的玻璃棒置于试管口,有白烟产生
(2)实验室制取氨的其他方法方法 化学方程式(或原理) 气体发生装置
加热浓氨水 NH ·H O=====NH ↑+HO
3 2 3 2
NaOH溶于水放热,促使氨水分解。
浓氨水+固体NaOH
且OH-浓度的增大有利于NH 的生成
3
CaO与水反应,使溶剂(水)减少;反
应放热,促使氨水分解。化学方程式
浓氨水+固体CaO
为NH ·H O+CaO===NH ↑+
3 2 3
Ca(OH)
2
(3)实验装置的创新
(1)液氨制冷、碘的升华、NH Cl气化都不涉及化学变化(×)
4
错因:NH Cl 气化是 NH Cl 分解生成 NH 与 HC l ,是化学变化 。
4 4 3
(2)能用加热法除去NaCl中的NH Cl的原因是NH Cl为强酸弱碱盐(×)
4 4
错因: 原因是 NH Cl 受热分解生成气体挥发 。
4
(3)现有1 mol·L-1的氨水,则该溶液中NH ·H O的浓度是1 mol·L-1(×)
3 2
错因: 氨水中还含有 NH 、 NH ,故 c (NH ·H O)<1_ mol·L - 1 。
3 3 2
(4)浓氨水可检验氯气管道是否漏气(√)
(1)氨水含有哪些微粒?
答案 HO、NH ·H O、NH 、NH、OH-、H+。
2 3 2 3(2)蘸有浓硝酸的玻璃棒与蘸有浓氨水的玻璃棒靠近,能产生白烟现象吗?简述原因。若将
浓硝酸改为浓硫酸也会出现相同的现象吗?
答案 能,浓硝酸、浓氨水均有挥发性,挥发的 HNO 与NH 相遇生成白色固体小颗粒
3 3
NH NO 。
4 3
不会。
(3)用浓氯化铵溶液处理过的舞台幕布不易着火,其原因是①___________________________;
②____________________________________________。
答案 氯化铵分解吸收热量,降低了温度 氯化铵分解产生的气体隔绝了空气
题组一 氨、铵盐的性质
1.下列说法错误的是( )
A.检验溶液中是否含有NH的实验操作是取少量试液于试管中,加入NaOH溶液并加热,
用湿润的红色石蕊试纸检验产生的气体
B.加热NH Cl和Ca(OH) 混合物,并将产生的气体通入酚酞溶液中,酚酞溶液变成红色
4 2
C.施肥时,草木灰(有效成分为KCO)不能与NH Cl混合使用的原因是KCO 与NH Cl反
2 3 4 2 3 4
应生成氨气会降低肥效
D.因为NH HCO 受热易分解,所以可用作氮肥
4 3
答案 D
解析 NH与NaOH溶液共热生成氨气,氨气是碱性气体,能使湿润的红色石蕊试纸变蓝,
A正确;NH Cl与Ca(OH) 混合加热生成氨气,氨气是碱性气体,通入酚酞溶液中,酚酞溶
4 2
液变成红色,B正确;KCO 溶于水显碱性,与NH Cl反应生成氨气会降低肥效,C正确;
2 3 4
NH HCO 中含有氮元素,可用作氮肥,与受热易分解无关,D错误。
4 3
2.NH 是一种重要的化工原料,可以制备一系列物质(如图所示),下列说法正确的是( )
3
A.NH Cl和NaHCO 都是常用的化肥
4 3
B.NH Cl、HNO 和NaCO 受热时都易分解
4 3 2 3
C.NH 和NO 在一定条件下可发生氧化还原反应
3 2
D.图中所涉及的O 都要用纯氧
2
答案 C
解析 化肥主要是含农作物生长所需的氮、磷、钾营养元素的一些物质,NaHCO 不是常用
3
的化肥,A项不正确;NaCO 受热不易分解,B项不正确;NH 和NO 在一定条件下可以发
2 3 3 2生氧化还原反应,如生成氮气,C项正确;氨的催化氧化用空气就可以,不一定要用纯氧,
D项不正确。
题组二 氨、铵盐的性质实验
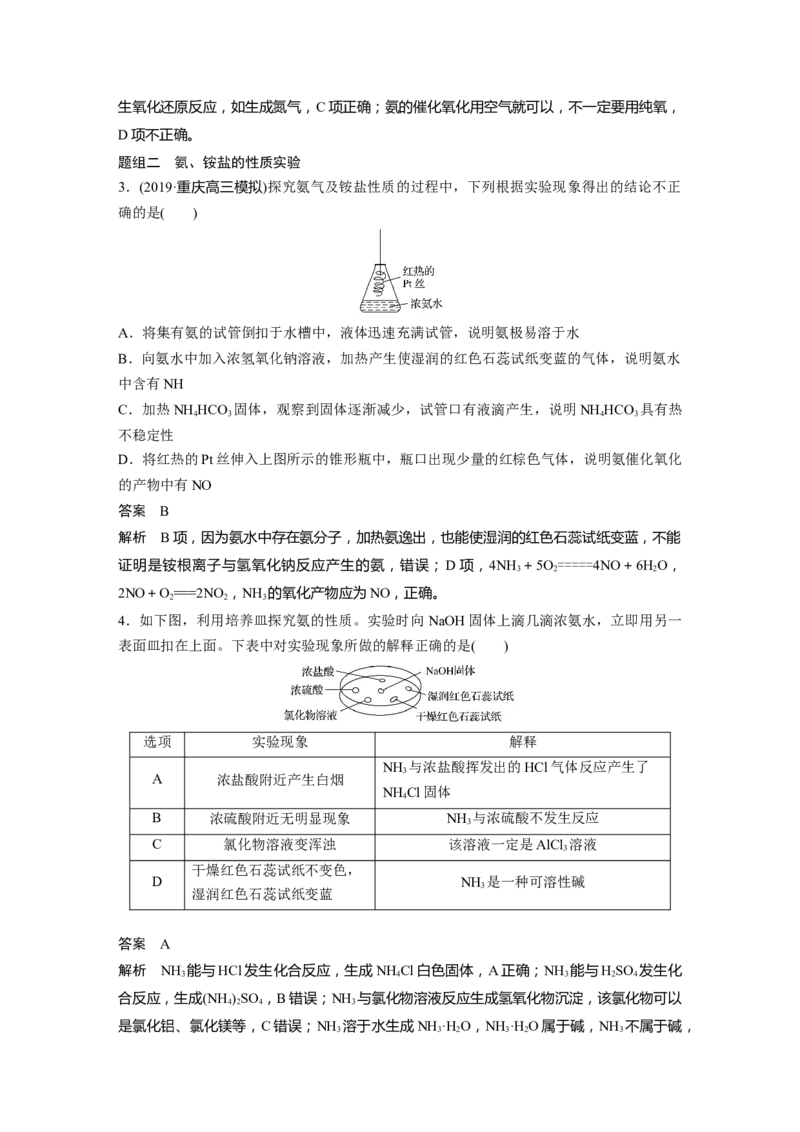
3.(2019·重庆高三模拟)探究氨气及铵盐性质的过程中,下列根据实验现象得出的结论不正
确的是( )
A.将集有氨的试管倒扣于水槽中,液体迅速充满试管,说明氨极易溶于水
B.向氨水中加入浓氢氧化钠溶液,加热产生使湿润的红色石蕊试纸变蓝的气体,说明氨水
中含有NH
C.加热NH HCO 固体,观察到固体逐渐减少,试管口有液滴产生,说明NH HCO 具有热
4 3 4 3
不稳定性
D.将红热的Pt丝伸入上图所示的锥形瓶中,瓶口出现少量的红棕色气体,说明氨催化氧化
的产物中有NO
答案 B
解析 B项,因为氨水中存在氨分子,加热氨逸出,也能使湿润的红色石蕊试纸变蓝,不能
证明是铵根离子与氢氧化钠反应产生的氨,错误;D项,4NH +5O=====4NO+6HO,
3 2 2
2NO+O===2NO ,NH 的氧化产物应为NO,正确。
2 2 3
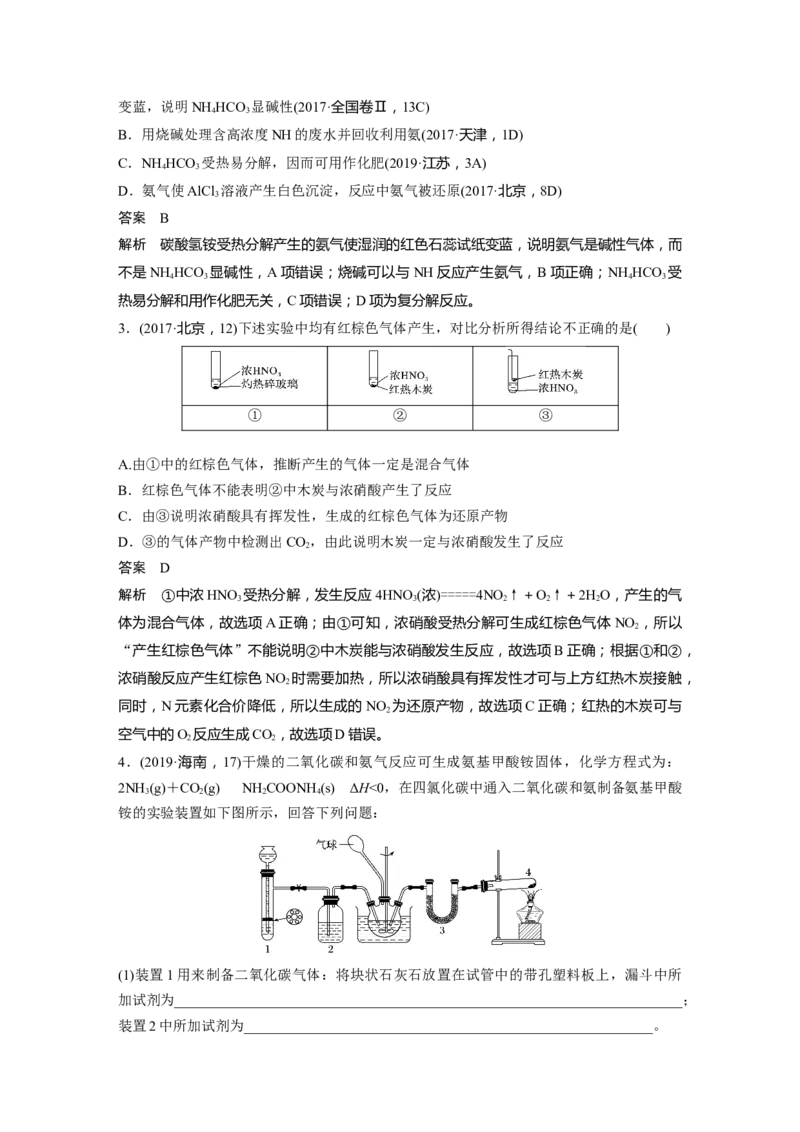
4.如下图,利用培养皿探究氨的性质。实验时向 NaOH固体上滴几滴浓氨水,立即用另一
表面皿扣在上面。下表中对实验现象所做的解释正确的是( )
选项 实验现象 解释
NH 与浓盐酸挥发出的HCl气体反应产生了
3
A 浓盐酸附近产生白烟
NH Cl固体
4
B 浓硫酸附近无明显现象 NH 与浓硫酸不发生反应
3
C 氯化物溶液变浑浊 该溶液一定是AlCl 溶液
3
干燥红色石蕊试纸不变色,
D NH 是一种可溶性碱
3
湿润红色石蕊试纸变蓝
答案 A
解析 NH 能与HCl发生化合反应,生成NH Cl白色固体,A正确;NH 能与HSO 发生化
3 4 3 2 4
合反应,生成(NH )SO ,B错误;NH 与氯化物溶液反应生成氢氧化物沉淀,该氯化物可以
4 2 4 3
是氯化铝、氯化镁等,C错误;NH 溶于水生成NH ·H O,NH ·H O属于碱,NH 不属于碱,
3 3 2 3 2 3D错误。
5.按要求回答问题。
(1)将氨与氯气混合也会产生白烟,用化学方程式解释产生白烟的过程__________________。
(2)在饱和NH Cl溶液中滴加NaAlO ,产生刺激性气味的气体和白色沉淀,用离子方程式解
4 2
释其现象:_________________________________,体现______________________________。
(3)实验室常用饱和氯化铵(NH Cl)与亚硝酸钠(NaNO )加热来制取氮气,写出发生反应的化
4 2
学方程式________________________,体现__________________________________________。
答案 (1)2NH +3Cl===N+6HCl,NH +HCl===NH Cl
3 2 2 3 4
(2)NH+AlO+HO===Al(OH) ↓+NH ↑ NH水解呈酸性
2 3 3
(3)NH Cl+NaNO =====NaCl+N↑+2HO NH的还原性
4 2 2 2
题组三 氨气性质与制备实验综合
6.(2020·西安模拟)氨催化氧化法是工业生产中制取硝酸的主要途径,某同学用该原理在实
验室探究硝酸的制备和性质,设计了如图Ⅰ所示装置。
(1)某同学想用图Ⅱ装置及试剂方便快速地制取少量氨气。
化学试剂:①NH Cl固体、②浓氨水、③NaOH固体。
4
应选择的装置是____________(填字母),选用的试剂是____________(填序号)。选用上述试
剂 制 氨 气 的 理 由 是
_________________________________________________________________。
实验过程中,制气时的实验操作是________________________________________________。
(2)乙装置的作用是______________________;写出受热时丙装置中发生反应的化学方程式:
_____________________________________________________________________________。
(3)当戊中观察到__________________现象,则说明已制得硝酸。某同学按图Ⅰ组装仪器并
检验装置气密性后进行实验,没有观察到此现象,请分析实验失败的可能原因是
___________________________________________________________________________________________
。
如何改进装置:__________________________________________________________________
______________________________________________________________________________。
(4)改进后待反应结束,将丁装置倒立在盛水的水槽中,会观察到的现象是
_________________
_______________________________________________________________________________
。
答案 (1)B ②③ NaOH固体遇水放热,使氨气的溶解度降低,同时可使溶液中c(OH-)增
大,促使NH+OH-NH ·H ONH +HO平衡向右移动,从而使氨气逸出 将浓氨水
3 2 3 2
逐滴滴加到NaOH固体上
(2)干燥氧气和氨的混合气体 4NH +5O=====4NO+6HO
3 2 2
(3)紫色石蕊溶液变红 过量的氨致使戊中溶液不一定呈酸性 在丙和丁之间连接盛有无水
氯化钙的干燥管或盛有浓硫酸的洗气瓶
(4)试管丁内水面慢慢上升,上升到一定高度不再变化,试管内气体颜色由红棕色逐渐变淡
至无色
解析 (1)不加热制取NH 是快速制取少量NH 的措施,具体操作方法是把浓氨水滴到
3 3
NaOH固体上。(2)乙装置可干燥NH 和O;NH 和O 在加热和Cr O 的催化作用下发生催化
3 2 3 2 2 3
氧化反应。(3)HNO 能使紫色石蕊溶液变红;由于NH 过量,可能会与HNO 反应,致使观
3 3 3
察不到溶液变红的现象,故可在丙和丁之间连接一个能除去NH 的装置。
3
1.(2020·天津,6)检验下列物质所选用的试剂正确的是( )
待检验物质 所用试剂
A 海水中的碘元素 淀粉溶液
B SO 气体 澄清石灰水
2
C 溶液中的Cu2+ 氨水
D 溶液中的NH NaOH溶液,湿润的蓝色石蕊试纸
答案 C
解析 淀粉遇碘单质才会变蓝,海水中的碘元素主要是以离子的形式存在,无法检验,A错
误;SO 气体和CO 气体均可使澄清石灰水变浑浊,B错误;铜离子可以和氨水先形成氢氧
2 2
化铜蓝色沉淀,再与氨水结合生成铜氨络合离子[Cu(NH )]2+,可以检验,C正确;氨气可
3 4
使湿润的红色石蕊试纸变蓝,D错误。
2.下列有关说法正确的是( )
A.加热盛有少量NH HCO 固体的试管,并在试管口放置湿润的红色石蕊试纸,石蕊试纸
4 3变蓝,说明NH HCO 显碱性(2017·全国卷Ⅱ,13C)
4 3
B.用烧碱处理含高浓度NH的废水并回收利用氨(2017·天津,1D)
C.NH HCO 受热易分解,因而可用作化肥(2019·江苏,3A)
4 3
D.氨气使AlCl 溶液产生白色沉淀,反应中氨气被还原(2017·北京,8D)
3
答案 B
解析 碳酸氢铵受热分解产生的氨气使湿润的红色石蕊试纸变蓝,说明氨气是碱性气体,而
不是NH HCO 显碱性,A项错误;烧碱可以与NH反应产生氨气,B项正确;NH HCO 受
4 3 4 3
热易分解和用作化肥无关,C项错误;D项为复分解反应。
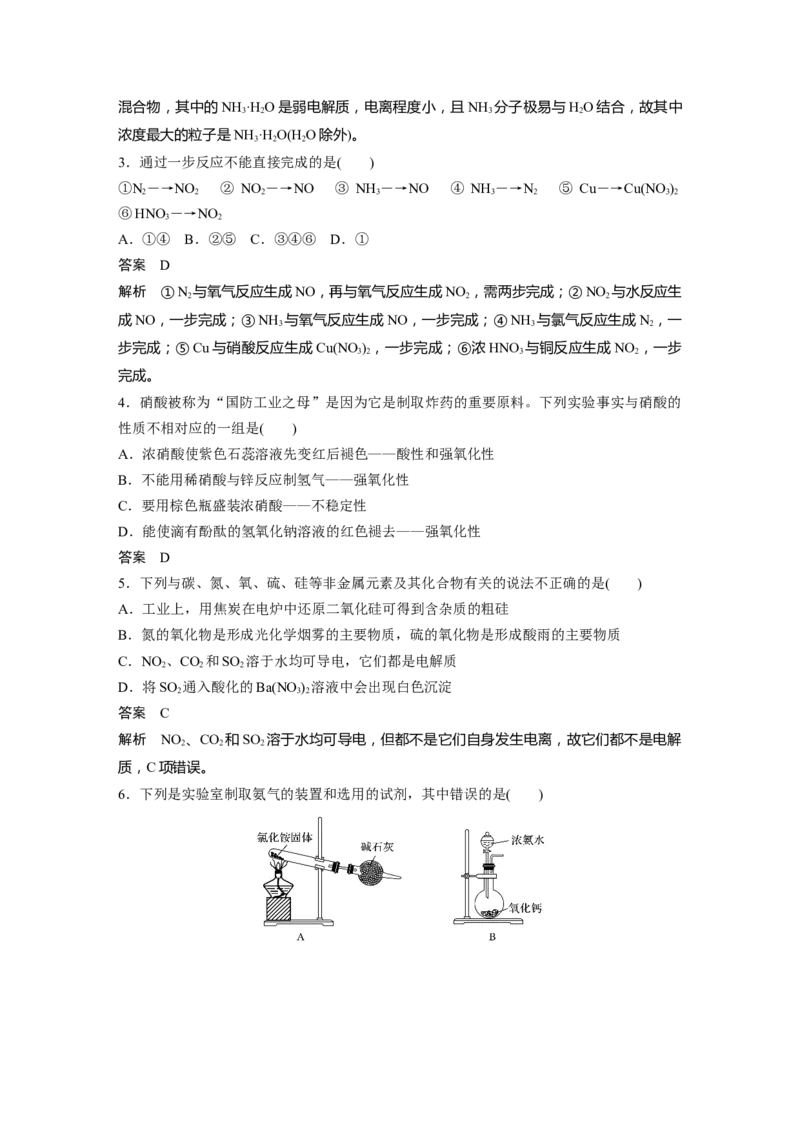
3.(2017·北京,12)下述实验中均有红棕色气体产生,对比分析所得结论不正确的是( )
① ② ③
A.由①中的红棕色气体,推断产生的气体一定是混合气体
B.红棕色气体不能表明②中木炭与浓硝酸产生了反应
C.由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D.③的气体产物中检测出CO,由此说明木炭一定与浓硝酸发生了反应
2
答案 D
解析 ①中浓HNO 受热分解,发生反应4HNO(浓)=====4NO ↑+O↑+2HO,产生的气
3 3 2 2 2
体为混合气体,故选项A正确;由①可知,浓硝酸受热分解可生成红棕色气体NO ,所以
2
“产生红棕色气体”不能说明②中木炭能与浓硝酸发生反应,故选项B正确;根据①和②,
浓硝酸反应产生红棕色NO 时需要加热,所以浓硝酸具有挥发性才可与上方红热木炭接触,
2
同时,N元素化合价降低,所以生成的NO 为还原产物,故选项C正确;红热的木炭可与
2
空气中的O 反应生成CO,故选项D错误。
2 2
4.(2019·海南,17)干燥的二氧化碳和氨气反应可生成氨基甲酸铵固体,化学方程式为:
2NH (g)+CO(g)NH COONH(s) ΔH<0,在四氯化碳中通入二氧化碳和氨制备氨基甲酸
3 2 2 4
铵的实验装置如下图所示,回答下列问题:
(1)装置1用来制备二氧化碳气体:将块状石灰石放置在试管中的带孔塑料板上,漏斗中所
加试剂为________________________________________________________________________;
装置2中所加试剂为__________________________________________________________。(2) 装 置 4 中 试 剂 为 固 体 NH Cl 和 Ca(OH) , 发 生 反 应 的 化 学 方 程 式 为
4 2
_______________________________________________________________________________;
试管口不能向上倾斜的原因是_____________________________________________________
_______________________________________________________________________________
。
装置3中试剂为KOH,其作用为___________________________________________________
_______________________________________________________________________________
。
(3)反应时三颈烧瓶需用冷水浴冷却,其目的是_______________________________________
______________________________________________________________________________。
答案 (1)稀盐酸 浓HSO
2 4
(2)2NH Cl+Ca(OH) =====2NH ↑+2HO+CaCl
4 2 3 2 2
防止冷凝水倒流到试管底部使试管破裂 干燥剂(干燥氨气)
(3)降低温度,使平衡正向移动,提高产量
1.下列有关氮元素的单质及其化合物的说法错误的是( )
①氮气与氧气在放电条件下可直接生成NO
2
②铵盐都不稳定,受热分解都生成氨气
③向Fe(NO ) 溶液中滴加稀盐酸,无明显变化
3 2
④实验室采用加热氯化铵固体,用碱石灰除去氯化氢的方法制备氨气
A.①③④ B.①③
C.①④ D.①②③④
答案 D
解析 在放电条件下,氮气与氧气反应生成的是一氧化氮而不是二氧化氮,一氧化氮不稳定,
易被氧气氧化生成二氧化氮,①错误;硝酸铵加强热时剧烈分解发生爆炸生成氮气、二氧化
氮和水,②错误;向硝酸亚铁溶液中加入稀盐酸,酸性条件下,硝酸根离子具有强氧化性,
能把亚铁离子氧化成铁离子,同时自身被还原成一氧化氮,③错误;氯化铵受热易分解,冷
却时又生成氯化铵,所以得不到氨气,④错误。
2.下列关于氨水的说法中,不正确的是( )
A.氨水和液氨不同,氨水是混合物,液氨是纯净物
B.氨水中物质的量浓度最大的粒子是NH ·H O(水除外)
3 2
C.氨水显弱碱性,是弱电解质
D.在1 mol·L-1氨水中,NH ·H O、NH、NH 的物质的量浓度之和为1 mol·L-1
3 2 3
答案 C
解析 氨极易溶于水,发生如下反应:NH +HONH ·H ONH+OH-;生成的氨水是
3 2 3 2混合物,其中的NH ·H O是弱电解质,电离程度小,且NH 分子极易与HO结合,故其中
3 2 3 2
浓度最大的粒子是NH ·H O(H O除外)。
3 2 2
3.通过一步反应不能直接完成的是( )
①N―→NO ② NO ―→NO ③ NH ―→NO ④ NH ―→N ⑤ Cu―→Cu(NO )
2 2 2 3 3 2 3 2
⑥HNO―→NO
3 2
A.①④ B.②⑤ C.③④⑥ D.①
答案 D
解析 ①N 与氧气反应生成NO,再与氧气反应生成NO ,需两步完成;②NO 与水反应生
2 2 2
成NO,一步完成;③NH 与氧气反应生成NO,一步完成;④NH 与氯气反应生成N ,一
3 3 2
步完成;⑤Cu与硝酸反应生成Cu(NO ) ,一步完成;⑥浓HNO 与铜反应生成NO ,一步
3 2 3 2
完成。
4.硝酸被称为“国防工业之母”是因为它是制取炸药的重要原料。下列实验事实与硝酸的
性质不相对应的一组是( )
A.浓硝酸使紫色石蕊溶液先变红后褪色——酸性和强氧化性
B.不能用稀硝酸与锌反应制氢气——强氧化性
C.要用棕色瓶盛装浓硝酸——不稳定性
D.能使滴有酚酞的氢氧化钠溶液的红色褪去——强氧化性
答案 D
5.下列与碳、氮、氧、硫、硅等非金属元素及其化合物有关的说法不正确的是( )
A.工业上,用焦炭在电炉中还原二氧化硅可得到含杂质的粗硅
B.氮的氧化物是形成光化学烟雾的主要物质,硫的氧化物是形成酸雨的主要物质
C.NO 、CO 和SO 溶于水均可导电,它们都是电解质
2 2 2
D.将SO 通入酸化的Ba(NO ) 溶液中会出现白色沉淀
2 3 2
答案 C
解析 NO 、CO 和SO 溶于水均可导电,但都不是它们自身发生电离,故它们都不是电解
2 2 2
质,C项错误。
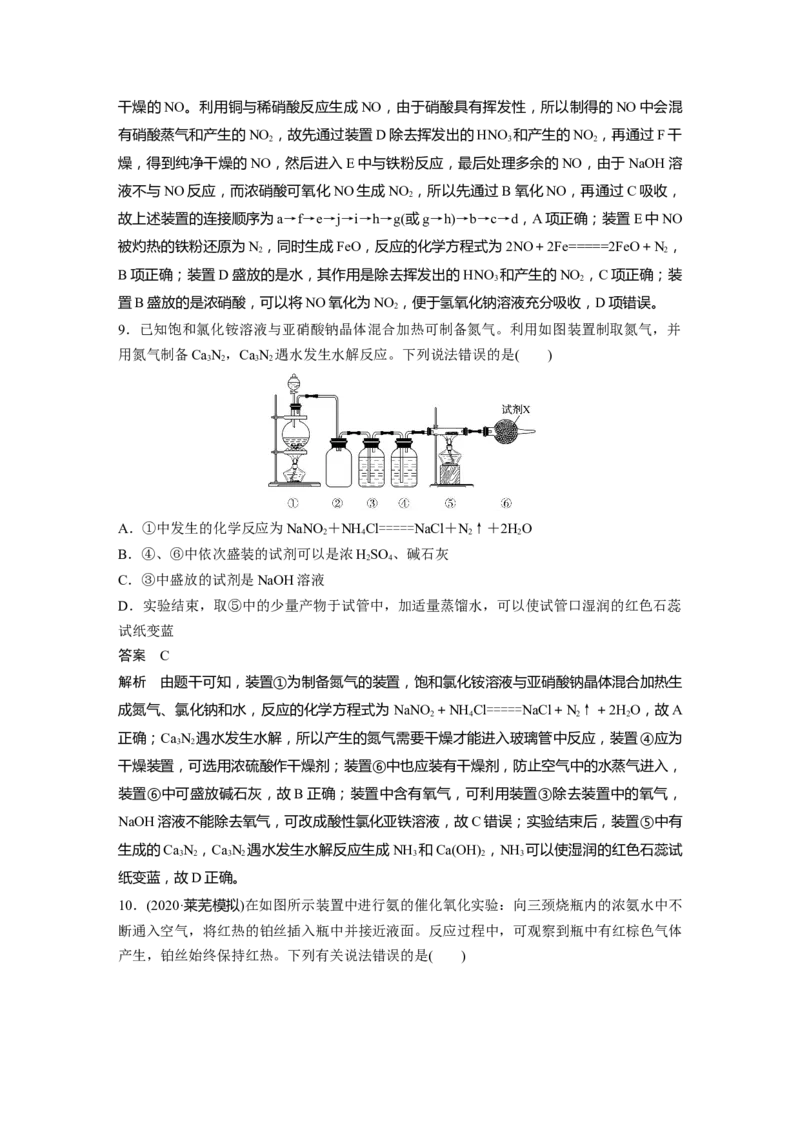
6.下列是实验室制取氨气的装置和选用的试剂,其中错误的是( )答案 A
解析 NH Cl加热生成的NH 和HCl,冷却后又生成NH Cl,不能得到NH 。
4 3 4 3
7.(2020·北京模拟)全氮类物质具有高密度、超高能量及爆炸产物无污染等优点。中国科学
家成功合成全氮阴离子N,N是制备全氮类物质NN的重要中间体,下列说法中不正确的是
( )
A.全氮类物质属于绿色能源
B.每个N中含有35个质子
C.每个N中含有35个电子
D.NN结构中含共价键
答案 C
解析 根据全氮类物质具有高密度、超高能量及爆炸产物无污染等优点可知A正确;N的
质子数为7×5=35,B正确;N含有的电子数为5×7+1=36,C错误;N、N中均含有5
个氮原子,氮原子间以共价键结合,D正确。
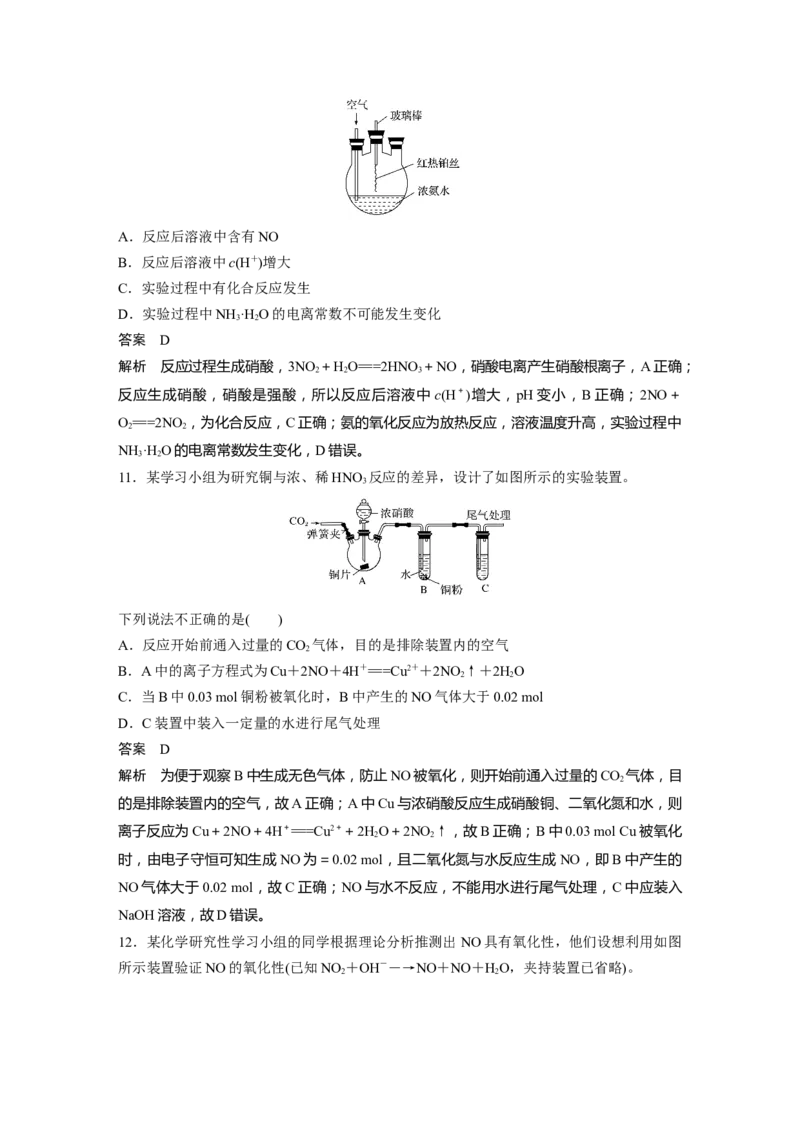
8.(2020·安徽皖江名校联考)某兴趣小组设计用铁粉将NO还原为N(同时生成FeO)。下列
2
说法不正确的是( )
已知:①浓硝酸可氧化NO;②NaOH溶液能吸收NO ,不吸收NO。
2
A.装置的连接顺序为a→f→e→j→i→h→g(或g→h)→b→c→d
B.装置E中发生反应的化学方程式为2NO+2Fe=====2FeO+N
2
C.装置D的作用是吸收挥发出来的硝酸和产生的NO
2
D.装置B的作用是干燥,防止水蒸气进入E中干扰反应
答案 D
解析 根据实验原理“NO被灼热的铁粉还原为N ,同时生成FeO”,所以首先应制备纯净
2干燥的NO。利用铜与稀硝酸反应生成NO,由于硝酸具有挥发性,所以制得的NO中会混
有硝酸蒸气和产生的NO ,故先通过装置D除去挥发出的HNO 和产生的NO ,再通过F干
2 3 2
燥,得到纯净干燥的NO,然后进入E中与铁粉反应,最后处理多余的NO,由于NaOH溶
液不与NO反应,而浓硝酸可氧化NO生成NO ,所以先通过B氧化NO,再通过C吸收,
2
故上述装置的连接顺序为a→f→e→j→i→h→g(或g→h)→b→c→d,A项正确;装置E中NO
被灼热的铁粉还原为N ,同时生成FeO,反应的化学方程式为2NO+2Fe=====2FeO+N ,
2 2
B项正确;装置D盛放的是水,其作用是除去挥发出的HNO 和产生的NO ,C项正确;装
3 2
置B盛放的是浓硝酸,可以将NO氧化为NO ,便于氢氧化钠溶液充分吸收,D项错误。
2
9.已知饱和氯化铵溶液与亚硝酸钠晶体混合加热可制备氮气。利用如图装置制取氮气,并
用氮气制备Ca N,Ca N 遇水发生水解反应。下列说法错误的是( )
3 2 3 2
A.①中发生的化学反应为NaNO +NH Cl=====NaCl+N↑+2HO
2 4 2 2
B.④、⑥中依次盛装的试剂可以是浓HSO 、碱石灰
2 4
C.③中盛放的试剂是NaOH溶液
D.实验结束,取⑤中的少量产物于试管中,加适量蒸馏水,可以使试管口湿润的红色石蕊
试纸变蓝
答案 C
解析 由题干可知,装置①为制备氮气的装置,饱和氯化铵溶液与亚硝酸钠晶体混合加热生
成氮气、氯化钠和水,反应的化学方程式为NaNO +NH Cl=====NaCl+N↑+2HO,故A
2 4 2 2
正确;Ca N 遇水发生水解,所以产生的氮气需要干燥才能进入玻璃管中反应,装置④应为
3 2
干燥装置,可选用浓硫酸作干燥剂;装置⑥中也应装有干燥剂,防止空气中的水蒸气进入,
装置⑥中可盛放碱石灰,故B正确;装置中含有氧气,可利用装置③除去装置中的氧气,
NaOH溶液不能除去氧气,可改成酸性氯化亚铁溶液,故C错误;实验结束后,装置⑤中有
生成的Ca N ,Ca N 遇水发生水解反应生成NH 和Ca(OH) ,NH 可以使湿润的红色石蕊试
3 2 3 2 3 2 3
纸变蓝,故D正确。
10.(2020·莱芜模拟)在如图所示装置中进行氨的催化氧化实验:向三颈烧瓶内的浓氨水中不
断通入空气,将红热的铂丝插入瓶中并接近液面。反应过程中,可观察到瓶中有红棕色气体
产生,铂丝始终保持红热。下列有关说法错误的是( )A.反应后溶液中含有NO
B.反应后溶液中c(H+)增大
C.实验过程中有化合反应发生
D.实验过程中NH ·H O的电离常数不可能发生变化
3 2
答案 D
解析 反应过程生成硝酸,3NO +HO===2HNO+NO,硝酸电离产生硝酸根离子,A正确;
2 2 3
反应生成硝酸,硝酸是强酸,所以反应后溶液中 c(H+)增大,pH变小,B正确;2NO+
O===2NO ,为化合反应,C正确;氨的氧化反应为放热反应,溶液温度升高,实验过程中
2 2
NH ·H O的电离常数发生变化,D错误。
3 2
11.某学习小组为研究铜与浓、稀HNO 反应的差异,设计了如图所示的实验装置。
3
下列说法不正确的是( )
A.反应开始前通入过量的CO 气体,目的是排除装置内的空气
2
B.A中的离子方程式为Cu+2NO+4H+===Cu2++2NO ↑+2HO
2 2
C.当B中0.03 mol铜粉被氧化时,B中产生的NO气体大于0.02 mol
D.C装置中装入一定量的水进行尾气处理
答案 D
解析 为便于观察B中生成无色气体,防止NO被氧化,则开始前通入过量的CO 气体,目
2
的是排除装置内的空气,故A正确;A中Cu与浓硝酸反应生成硝酸铜、二氧化氮和水,则
离子反应为Cu+2NO+4H+===Cu2++2HO+2NO ↑,故B正确;B中0.03 mol Cu被氧化
2 2
时,由电子守恒可知生成NO为=0.02 mol,且二氧化氮与水反应生成NO,即B中产生的
NO气体大于0.02 mol,故C正确;NO与水不反应,不能用水进行尾气处理,C中应装入
NaOH溶液,故D错误。
12.某化学研究性学习小组的同学根据理论分析推测出 NO具有氧化性,他们设想利用如图
所示装置验证NO的氧化性(已知NO +OH-―→NO+NO+HO,夹持装置已省略)。
2 2(1)判断NO有氧化性的理论依据是________________,本套装置气密性检查较简便的操作
是
_______________________________________________________________________________,
装置A中反应的离子方程式为_____________________________________________________
_______________________________________________________________________________
。
(2) 装 置 C 中 试 剂 X 是 ________ , 装 置 B 的 作 用 是
______________________________________
_______________________________________________________________________________
。
(3)本套装置有一个明显的错误,下列分析中正确的是________(填字母)。
A.装置B中导管不应插入液面以下
B.装置E无法吸收NO
C.实验开始后,应不断地向装置E中通入空气
(4)本实验结束时装置D中试管内得到黑色粉末,对黑色粉末的成分,小组的同学提出了不
同的看法:
a.是FeO b.是Fe O c.是FeO与Fe O
3 4 3 4
①甲同学认为仅用磁铁就可以确定黑色粉末的成分到底是哪种情况,他判断的依据与结论是
______________________________________________________________________________。
②若用化学方法分析 a 组和 c 组中的黑色粉末,则需要使用三种试剂,这三种试剂是
____________________________________________________________________________。
答案 (1)NO中氮为+2价,不是氮元素的最低价 关闭分液漏斗活塞,在 E中加水没过导
管微热烧瓶,如果E中出现气泡且停止加热后导管中形成一段液柱,则说明气密性良好
3Cu+8H++2NO===3Cu2++2NO↑+4HO
2
(2)无水CaCl (或其他合理试剂) 吸收装置A中挥发出的HNO(或其他合理答案)
2 3
(3)BC
(4)①若粉末能全部被磁铁吸引,则b对;若完全不能被吸引,则a对;若部分能被吸引,
则c对 ②HCl、KSCN、K[Fe(CN) ](或稀硫酸、酸性KMnO 溶液、KSCN)
3 6 4
解析 (2)装置C是干燥装置,可用无水CaCl 、PO 等试剂干燥NO。硝酸是挥发性酸,对
2 2 5
后续反应会产生干扰,故装置B的作用是用于吸收装置A中挥发出的HNO 。(3)因要吸收
3
HNO(g),故装置B中导管应插入液面下,A项错误;NO是不成盐氧化物,不能与碱反应,
3
B项正确;通入空气后NO被O 氧化为NO ,NO 可被NaOH溶液吸收(或者在O 存在的条
2 2 2 2
件下,NO、O 、OH-反应生成盐),C项正确。(4)①可根据Fe O 能被磁铁吸引,FeO不能
2 3 4被磁铁吸引的性质判断。②用化学方法分析时,先用非氧化性酸将固体溶解,然后用 KSCN
检验有无Fe3+,用K[Fe(CN) ](或酸性KMnO 溶液)检验有无Fe2+,但由于酸性KMnO 溶液
3 6 4 4
能氧化Cl-,故当用盐酸溶解固体时,不能使用KMnO 溶液。
4
13.甲、乙两同学用下图所示装置进行实验,探究硝酸与铁反应的产物(加热装置省略)。
文献记载:ⅰ.在浓硝酸和活泼金属反应过程中,随着硝酸浓度的降低,其生成的产物有+
4、+2、-3价等氮的化合物。
ⅱ.FeSO+NOFe(NO)SO (棕色)(ΔH<0)。
4 4
ⅲ.NO 和NO都能被KMnO 氧化吸收。
2 4
甲的实验操作和现象记录如下:
实验操作 实验现象
打开弹簧夹,通入一段时间
-
CO,关闭弹簧夹
2
打开分液漏斗活塞,将浓硝酸
无明显现象
缓慢滴入烧瓶中,关闭活塞
①A中有红棕色气体产生,一段时间后,气体颜色
加热三颈烧瓶,反应开始后停
逐渐变浅;B中溶液变棕色;C中溶液紫色变浅;
止加热
②反应停止后,A中无固体剩余
请回答下列问题:
(1)滴入浓硝酸加热前没有明显现象的原因是______________________________________。
(2)检验是否生成-3价氮的化合物,应进行的实验操作是___________________________。
(3)甲取少量B中溶液,加热,实验现象是________________________________________。
请用平衡移动原理解释原因:___________________________________________________。
甲依据该现象得出的结论是A中有NO生成。
(4)乙认为甲得出A中有NO生成的证据不足。为获取充足的证据,乙仍采用该装置和操作
进行对照实验,乙作出的改变是________________________________,证明有NO生成的实
验现象是________________________________________________________________________
_____________________________________________________________________________。
答案 (1)常温时,铁遇浓硝酸形成致密氧化膜,阻止反应进一步发生(答“钝化”也可)
(2)取少量反应后A中溶液于试管中,向其中加入足量浓NaOH溶液,加热,用湿润的红色
石蕊试纸接近试管口,若试纸变蓝,则A中生成NH
(3)棕色溶液颜色变浅(或浅绿色),有无色气体逸出,且在空气中变为红棕色 FeSO +
4NOFe(NO)SO (棕色)的正反应为放热反应,加热后,平衡向逆反应方向移动
4
(4)浓硝酸换成稀硝酸 A中没有红棕色气体生成,B中溶液变为棕色
解析 (1)常温下,铁遇浓硝酸发生“钝化”。(2)-3价氮的化合物是NH 或铵盐,而此反
3
应的环境呈酸性,故-3价氮的化合物应是硝酸铵,可利用NH与OH-共热产生NH 的性质
3
检验。(3)B中发生反应FeSO +NOFe(NO)SO (棕色),加热后,上述平衡逆向移动,无
4 4
色气体NO逸出,在空气中变为红棕色,而溶液颜色变浅或变成浅绿色。(4)NO 与水反应生
2
成NO,故可把浓硝酸换成稀硝酸,若A中无红棕色气体生成,但B中溶液变为棕色,可证
明A中有NO生成。