文档内容
专项提能特训 13 多平衡体系的综合分析
1.相同温度下,分别在起始体积均为 1 L 的两个密闭容器中发生反应:X(g)+
2
3Y(g)2XY (g) ΔH=-a kJ·mol-1,实验测得反应的有关数据如下表。
2 3
起始物质的量/mol 达到平衡过
达到平衡所
容器 反应条件 程中的能量
X Y XY 用时间/min
2 2 3
变化
放热0.1a
① 恒容 1 3 0 10
kJ
② 恒压 1 3 0 t 放热b kJ
下列叙述正确的是( )
A.对于上述反应,①②中反应的平衡常数K的数值不同
B.①中:从开始至10 min内的平均反应速率v(X )=0.1 mol·L-1·min-1
2
C.②中:X 的平衡转化率小于10%
2
D.b>0.1a
答案 D
解析 ①②中反应温度相同,平衡常数K的数值相同,A项错误;①中反应放热0.1a kJ,
说明10 min内X 反应了0.1 mol,物质的量浓度改变量为0.1 mol·L-1,所以其平均速率为
2
v(X )=0.01 mol·L-1·min-1,B项错误;据容器①中数据,可算出X 的平衡转化率为10%,
2 2
容器②是恒温恒压,容器①是恒温恒容,容器②相当于在容器①的基础上加压,平衡右移,
所以X 的转化率大于10%,容器②放出的热量比容器①多,C项错误、D项正确。
2
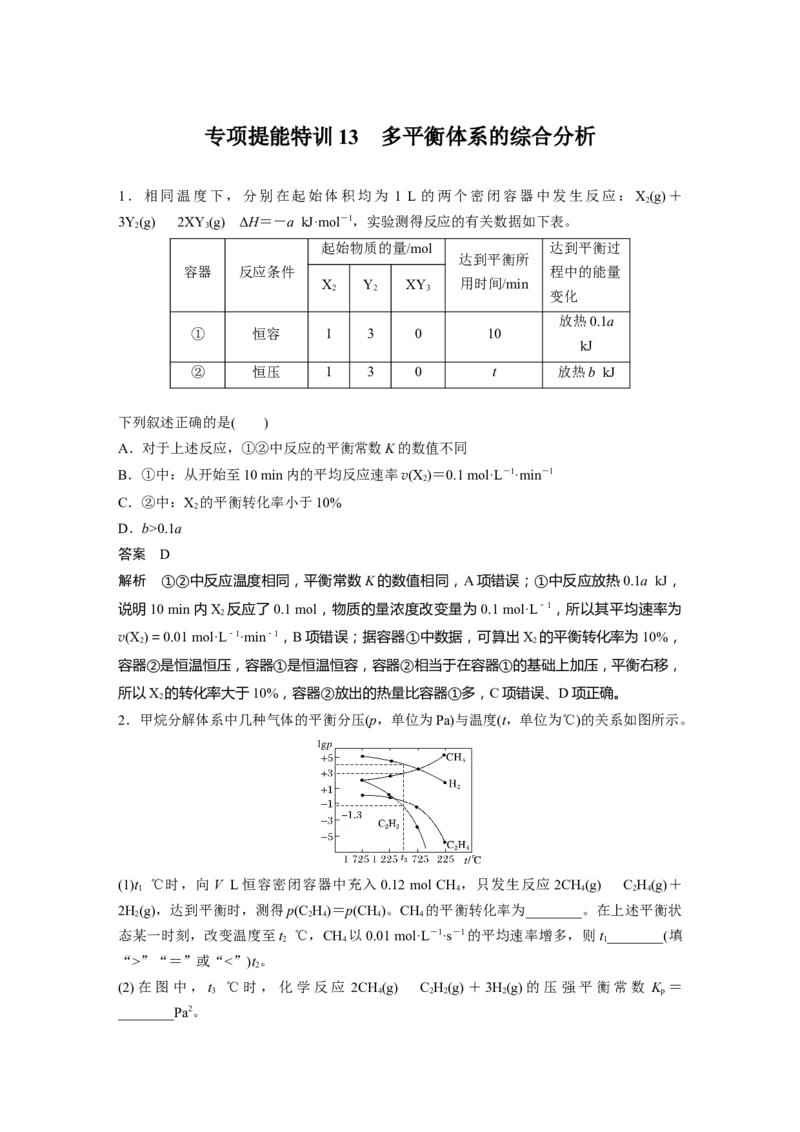
2.甲烷分解体系中几种气体的平衡分压(p,单位为Pa)与温度(t,单位为℃)的关系如图所示。
(1)t ℃时,向V L恒容密闭容器中充入 0.12 mol CH ,只发生反应2CH(g)C H(g)+
1 4 4 2 4
2H(g),达到平衡时,测得p(C H)=p(CH)。CH 的平衡转化率为________。在上述平衡状
2 2 4 4 4
态某一时刻,改变温度至t ℃,CH 以0.01 mol·L-1·s-1的平均速率增多,则t________(填
2 4 1
“>”“=”或“<”)t。
2
(2)在图中,t ℃时,化学反应 2CH(g)C H(g)+3H(g)的压强平衡常数 K =
3 4 2 2 2 p
________Pa2。答案 (1)66.7% > (2)104.7
解析 (1)设平衡时甲烷转化x mol,根据三段式法有:
2CH(g)C H(g)+2H(g)
4 2 4 2
起始量/mol 0.12 0 0
变化量/mol x x
平衡量/mol 0.12-x x
结合题意知0.12-x=,解得x=0.08,故CH 的平衡转化率为×100%≈66.7%。根据题图知
4
2CH(g)C H(g)+2H(g)为吸热反应,改变温度,甲烷的浓度增大,即平衡左移,则温度
4 2 4 2
降低,t>t 。(2)将气体的平衡浓度换为平衡分压,可知t℃时,该反应的压强平衡常数K =
1 2 3 p
= Pa2=104.7 Pa2。
3.有效除去大气中的SO 和氮氧化物,是打赢蓝天保卫战的重中之重。某温度下,NO 气
2 2 5
体在一体积固定的容器中发生如下反应:2NO(g)===4NO (g)+O(g)(慢反应) ΔH<
2 5 2 2
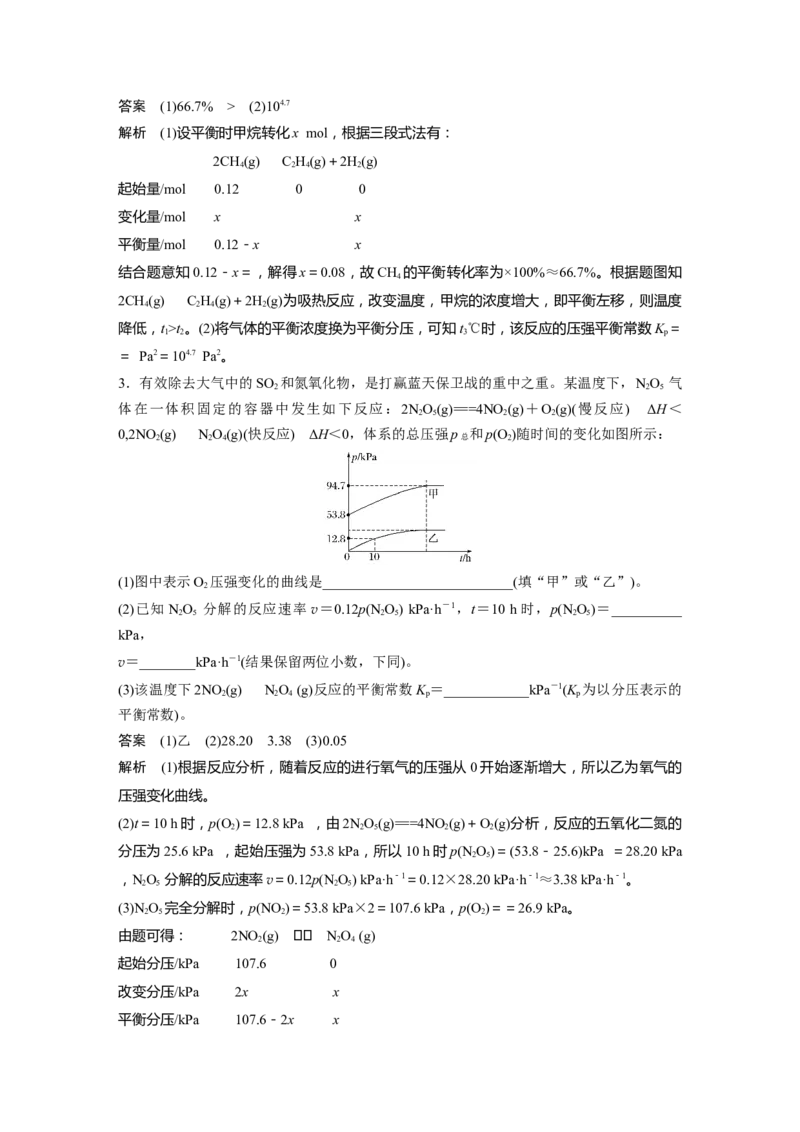
0,2NO(g)NO(g)(快反应) ΔH<0,体系的总压强p 和p(O )随时间的变化如图所示:
2 2 4 总 2
(1)图中表示O 压强变化的曲线是___________________________(填“甲”或“乙”)。
2
(2)已知NO 分解的反应速率 v=0.12p(N O) kPa·h-1,t=10 h时,p(N O)=__________
2 5 2 5 2 5
kPa,
v=________kPa·h-1(结果保留两位小数,下同)。
(3)该温度下2NO (g)NO (g)反应的平衡常数K =____________kPa-1(K 为以分压表示的
2 2 4 p p
平衡常数)。
答案 (1)乙 (2)28.20 3.38 (3)0.05
解析 (1)根据反应分析,随着反应的进行氧气的压强从0开始逐渐增大,所以乙为氧气的
压强变化曲线。
(2)t=10 h时,p(O )=12.8 kPa ,由2NO(g)===4NO (g)+O(g)分析,反应的五氧化二氮的
2 2 5 2 2
分压为25.6 kPa ,起始压强为53.8 kPa,所以10 h时p(N O)=(53.8-25.6)kPa =28.20 kPa
2 5
,NO 分解的反应速率v=0.12p(N O) kPa·h-1=0.12×28.20 kPa·h-1≈3.38 kPa·h-1。
2 5 2 5
(3)N O 完全分解时,p(NO )=53.8 kPa×2=107.6 kPa,p(O )==26.9 kPa。
2 5 2 2
由题可得: 2NO (g) NO (g)
2 2 4
起始分压/kPa 107.6 0
改变分压/kPa 2x x
平衡分压/kPa 107.6-2x x有107.6-2x+x+26.9=94.7 kPa,解得x=39.8 kPa,平衡常数K = kPa-1≈0.05 kPa-1。
p
4.[2019·天津,7(5)]在1 L真空密闭容器中加入a mol PH I固体,t ℃时发生如下反应:
4
PH I(s)PH (g)+HI(g) ①
4 3
4PH (g)P(g)+6H(g) ②
3 4 2
2HI(g)H(g)+I(g) ③
2 2
达平衡时,体系中n(HI)=b mol,n(I)=c mol,n(H )=d mol,则t ℃时反应①的平衡常数
2 2
K值为________(用字母表示)。
答案 (b+)b
解析 反应①生成的n(HI)=体系中n(HI)+2×体系中n(I)=(b+2c) mol,反应②中生成的
2
n(H )=体系中n(H )-反应③中生成的n(H )=(d-c) mol,体系中n(PH )=反应①生成的
2 2 2 3
n(PH )-反应②中转化的n(PH )=[b+2c-(d-c)] mol=(b+) mol,反应①的平衡常数K=
3 3
c(PH )·c(HI)=(b+)b。
3
5.氨催化氧化时会发生如下两个竞争反应Ⅰ、Ⅱ。
4NH (g)+5O(g)4NO(g)+6HO(g) ΔH<0 Ⅰ
3 2 2
4NH (g)+3O(g)2N(g)+6HO(g) ΔH<0 Ⅱ
3 2 2 2
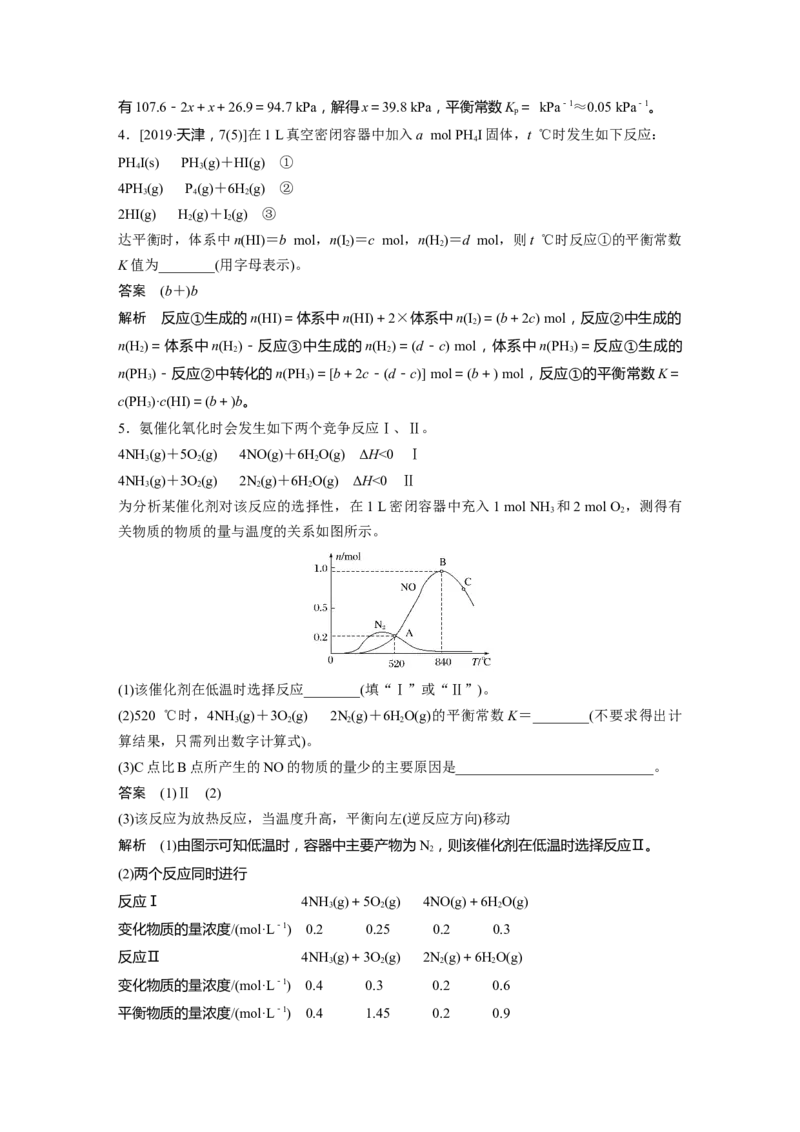
为分析某催化剂对该反应的选择性,在1 L密闭容器中充入1 mol NH 和2 mol O ,测得有
3 2
关物质的物质的量与温度的关系如图所示。
(1)该催化剂在低温时选择反应________(填“Ⅰ”或“Ⅱ”)。
(2)520 ℃时,4NH (g)+3O(g)2N(g)+6HO(g)的平衡常数K=________(不要求得出计
3 2 2 2
算结果,只需列出数字计算式)。
(3)C点比B点所产生的NO的物质的量少的主要原因是____________________________。
答案 (1)Ⅱ (2)
(3)该反应为放热反应,当温度升高,平衡向左(逆反应方向)移动
解析 (1)由图示可知低温时,容器中主要产物为N,则该催化剂在低温时选择反应Ⅱ。
2
(2)两个反应同时进行
反应Ⅰ 4NH (g)+5O(g)4NO(g)+6HO(g)
3 2 2
变化物质的量浓度/(mol·L-1) 0.2 0.25 0.2 0.3
反应Ⅱ 4NH (g)+3O(g)2N(g)+6HO(g)
3 2 2 2
变化物质的量浓度/mol·L-1 0.4 0.3 0.2 0.6
平衡物质的量浓度/mol·L-10.4 1.45 0.2 0.9故520 ℃时4NH (g)+3O(g)2N(g)+6HO(g)的平衡常数K=。
3 2 2 2
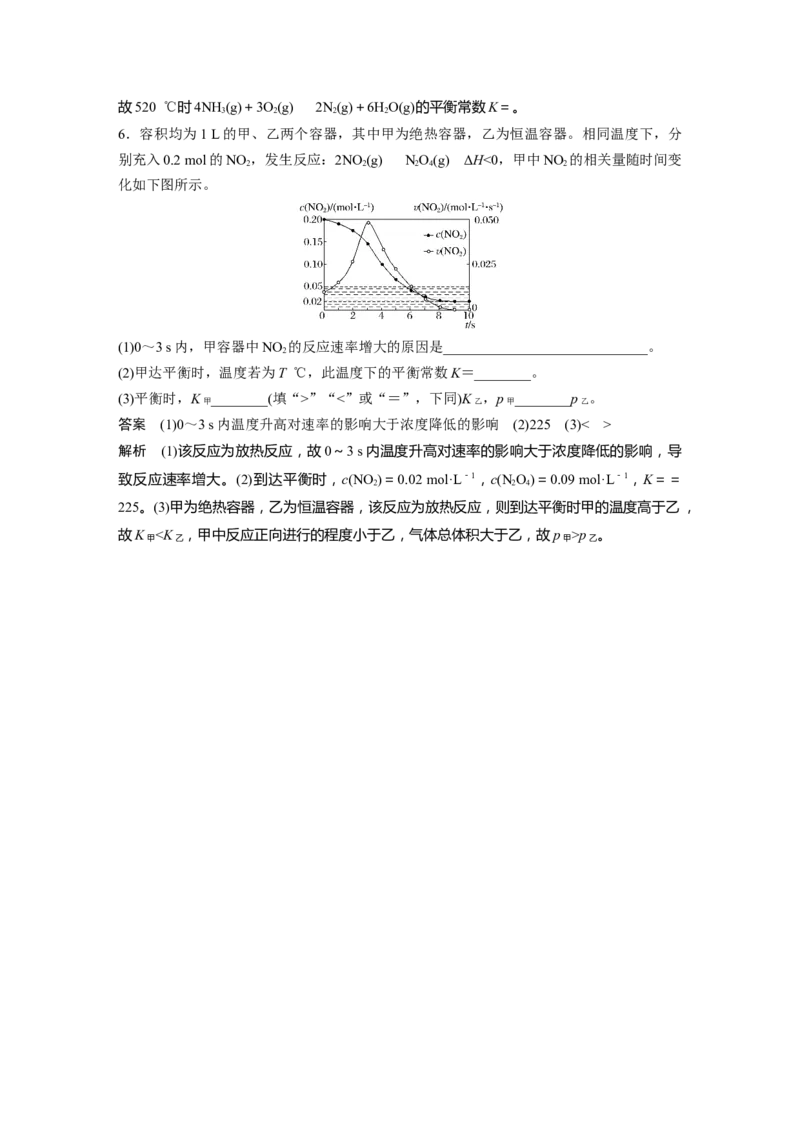
6.容积均为1 L的甲、乙两个容器,其中甲为绝热容器,乙为恒温容器。相同温度下,分
别充入0.2 mol的NO ,发生反应:2NO (g)NO(g) ΔH<0,甲中NO 的相关量随时间变
2 2 2 4 2
化如下图所示。
(1)0~3 s内,甲容器中NO 的反应速率增大的原因是_____________________________。
2
(2)甲达平衡时,温度若为T ℃,此温度下的平衡常数K=________。
(3)平衡时,K ________(填“>”“<”或“=”,下同)K ,p ________p 。
甲 乙 甲 乙
答案 (1)0~3 s内温度升高对速率的影响大于浓度降低的影响 (2)225 (3)< >
解析 (1)该反应为放热反应,故0~3 s内温度升高对速率的影响大于浓度降低的影响,导
致反应速率增大。(2)到达平衡时,c(NO )=0.02 mol·L-1,c(N O)=0.09 mol·L-1,K==
2 2 4
225。(3)甲为绝热容器,乙为恒温容器,该反应为放热反应,则到达平衡时甲的温度高于乙,
故K p 。
甲 乙 甲 乙