文档内容
21 强酸(碱)与弱酸(碱)的比较
弱酸与强酸的根本区别在于弱酸不完全电离,存在电离平衡,常涉及下列几种问题的比较。
1.一元强酸(HCl)与一元弱酸(CHCOOH)的比较
3
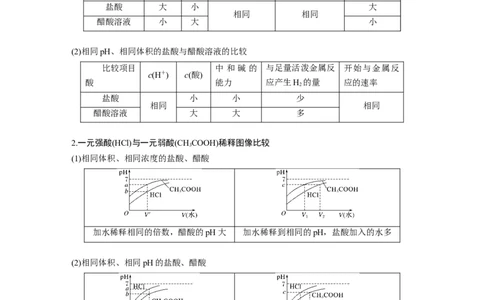
(1)相同物质的量浓度、相同体积的盐酸与醋酸溶液的比较
比较项目 与活泼金属反应 开始与金属
c(H+) pH 中和碱的能力
酸 产生H 的量 反应的速率
2
盐酸 大 小 大
相同 相同
醋酸溶液 小 大 小
(2)相同pH、相同体积的盐酸与醋酸溶液的比较
比较项目 中 和 碱 的 与足量活泼金属反 开始与金属反
c(H+) c(酸)
酸 能力 应产生H 的量 应的速率
2
盐酸 小 小 少
相同 相同
醋酸溶液 大 大 多
2.一元强酸(HCl)与一元弱酸(CHCOOH)稀释图像比较
3
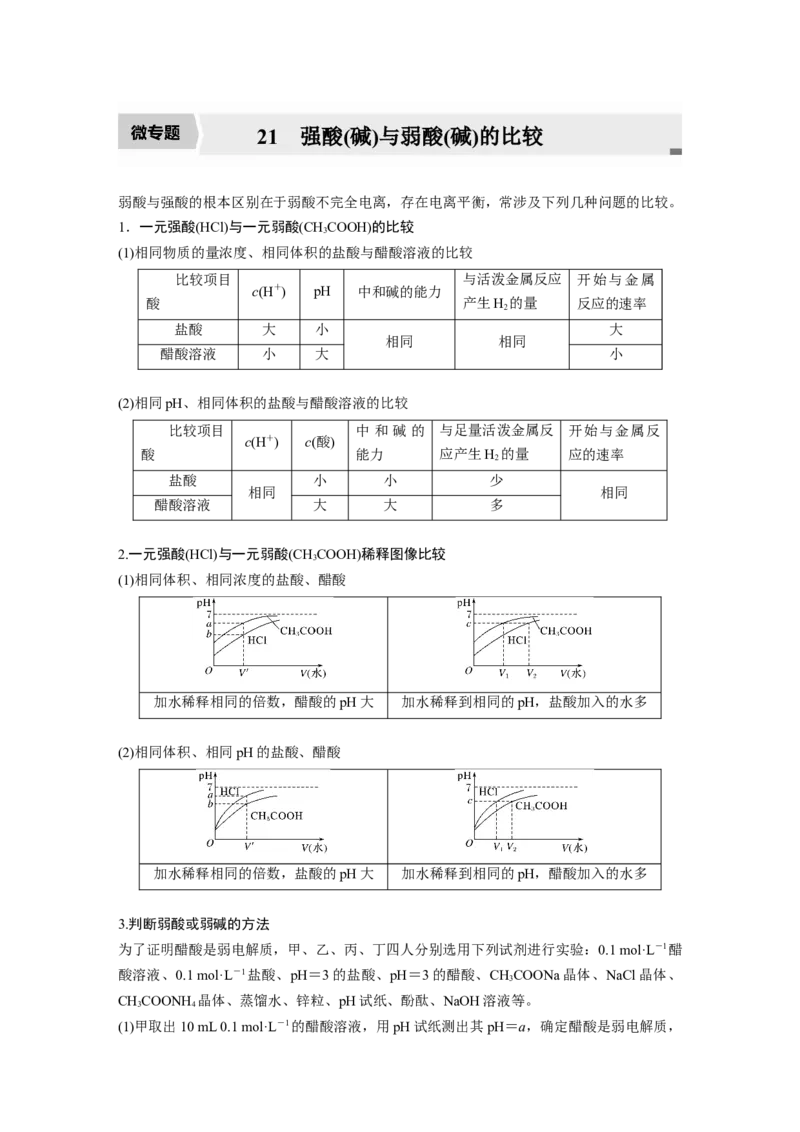
(1)相同体积、相同浓度的盐酸、醋酸
加水稀释相同的倍数,醋酸的pH大 加水稀释到相同的pH,盐酸加入的水多
(2)相同体积、相同pH的盐酸、醋酸
加水稀释相同的倍数,盐酸的pH大 加水稀释到相同的pH,醋酸加入的水多
3.判断弱酸或弱碱的方法
为了证明醋酸是弱电解质,甲、乙、丙、丁四人分别选用下列试剂进行实验:0.1 mol·L-1醋
酸溶液、0.1 mol·L-1盐酸、pH=3的盐酸、pH=3的醋酸、CHCOONa晶体、NaCl晶体、
3
CHCOONH 晶体、蒸馏水、锌粒、pH试纸、酚酞、NaOH溶液等。
3 4
(1)甲取出10 mL 0.1 mol·L-1的醋酸溶液,用pH试纸测出其pH=a,确定醋酸是弱电解质,则a应该满足的关系是 ,理由是 。
(2)乙分别取pH=3的醋酸和盐酸各1 mL,分别用蒸馏水稀释到100 mL,然后用pH试纸分
别测定两溶液的pH,则可认定醋酸是弱电解质,判断的依据是
。
(3)丙分别取pH=3的盐酸和醋酸各10 mL,然后加入质量相同的锌粒,醋酸放出H 的平均
2
速率快,则认定醋酸是弱电解质,你认为这一方法正确吗? ,请说明理由:
。
(4)丁用CHCOONa晶体、NaCl晶体、蒸馏水和酚酞做实验,也论证了醋酸是弱酸的事实,
3
该同学的实验操作和现象是
。
答案 (1)a>1 醋酸是弱酸,不能完全电离 (2)盐酸的pH=5,醋酸的pH<5 (3)正确 由
于醋酸是弱酸,随着反应的进行,醋酸不断电离,c(H+)变化小,产生H 的平均速率醋酸比
2
盐酸快 (4)将CHCOONa晶体、NaCl晶体分别溶于适量水配成溶液,再分别滴入酚酞溶液,
3
CHCOONa溶液变浅红色,NaCl溶液不变色
3
判断弱电解质的三个思维角度
角度一:弱电解质的定义,即弱电解质不能完全电离。
(1)测定一定浓度的HA溶液的pH。
(2)与同浓度盐酸比较导电性。
(3)与同浓度的盐酸比较和锌反应的快慢。
角度二:弱电解质溶液中存在电离平衡,条件改变,平衡移动。
(1)从一定pH的HA溶液稀释前后pH的变化判断。
(2)从升高温度后pH的变化判断。
(3)从等体积、等pH的HA溶液、盐酸分别与过量的锌反应生成H 的量判断。
2
角度三:弱电解质形成的盐类能水解,如判断CHCOOH为弱酸可用下面两个现象:
3
(1)配制某浓度的醋酸钠溶液,向其中加入几滴酚酞溶液。现象:溶液变为浅红色。
(2)用玻璃棒蘸取一定浓度的醋酸钠溶液滴在pH试纸上,测其pH。现象:pH>7。
题组一 判断弱酸或弱碱的方法
1.下列事实中不能证明CHCOOH是弱电解质的是( )
3
A.常温下某CHCOONa溶液的pH=8
3
B.常温下0.1 mol·L-1CHCOOH溶液的pH=2.8
3
C.向CHCOOH溶液中加入少量CHCOONa固体,溶解后溶液的pH变大
3 3
D.0.1 mol·L-1的乙酸溶液与同体积0.1 mol·L-1的氢氧化钠溶液恰好反应
答案 D解析 常温下,醋酸钠溶液的pH=8,说明醋酸钠为强碱弱酸盐,水解呈碱性,可证明醋酸
为弱酸,故A错误;测得0.1 mol·L-1CHCOOH溶液的pH=2.8,说明醋酸未完全电离,可
3
证明醋酸为弱酸,故B错误;向CHCOOH溶液中加入少量CHCOONa固体,溶解后溶液
3 3
的pH变大,说明CHCOOH存在电离平衡,则CHCOOH为弱酸,故C错误;酸与氢氧化
3 3
钠溶液反应,与酸的强弱没有关系,则 0.1 mol·L-1的乙酸溶液与同体积0.1 mol·L-1的氢氧
化钠溶液恰好反应,不能说明乙酸是弱电解质,故D正确。
2.下列事实中,能说明MOH是弱碱的是( )
A.0.1 mol·L-1MOH溶液可以使酚酞溶液变红
B.常温下,0.1 mol·L-1MOH溶液中c(OH-)<0.1 mol·L-1
C.MOH溶液的导电能力比NaOH溶液弱
D.等体积的0.1 mol·L-1MOH溶液与0.1 mol·L-1盐酸恰好完全反应
答案 B
解析 0.1 mol·L-1MOH溶液可以使酚酞溶液变红,说明MOH能电离出氢氧根离子,但不
能说明MOH的电离程度,所以不能说明MOH是弱电解质,A错误;常温下,0.1 mol·L-
1MOH溶液中,c(OH-)<0.1 mol·L-1,说明MOH没有完全电离,则MOH为弱碱,B正确;
等体积的0.1 mol·L-1MOH溶液与0.1 mol·L-1盐酸混合,无论MOH是强碱还是弱碱,都恰
好完全反应,D错误。
题组二 强酸(碱)与弱酸(碱)的比较
3.在相同条件下将0.24 g Mg分别与0.2 mol·L-1 80 mL的盐酸、0.2 mol·L-1 100 mL的醋
酸反应,下列说法错误的是( )
A.两个反应开始时的反应速率:v(HCl)大于v(CHCOOH)
3
B.反应进行完全产生的气体的物质的量:n(HCl)等于n(CHCOOH)
3
C.在上述盐酸中加入少量的醋酸钠固体,不改变产生气体的物质的量,但能使该反应的化
学反应速率降低
D.上述盐酸和醋酸的pH,前者小于后者
答案 B
4.相同体积、相同pH的某一元强酸溶液①和某一元中强酸溶液②分别与足量的锌粉发生
反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是( )答案 C
解析 强酸完全电离,中强酸部分电离,随着反应的进行,中强酸会继续电离出 H+,所以
溶液②产生氢气的体积多,在相同时间内,②的反应速率比①快。
5.(2020·烟台联考)两种一元碱MOH和ROH的溶液分别加水稀释,溶液pH的变化如图所示,
下列叙述不正确的是( )
A.MOH是一种弱碱
B.在x点,c(M+)=c(R+)
C.稀释前,c(ROH)=10c(MOH)
D.稀释前MOH溶液和ROH溶液中由水电离出的c(OH-)前者是后者的10倍
答案 C
解析 A项,由图像可知稀释相同倍数,MOH的pH变化程度小,故MOH为弱碱;B项,
在x点,c(OH-)=c(M+)+c(H+)=c(R+)+c(H+),x点时MOH和ROH溶液中c(H+)均为
10-11 mol·L-1,c(OH-)均为10-3 mol·L-1,故c(M+)=c(R+);C项,MOH为弱碱,若ROH
为强碱,则稀释前c(ROH)<10c(MOH);D项,稀释前MOH溶液中由水电离出的c(OH-)=
10-12 mol·L-1;ROH溶液中由水电离出的c(OH-)=10-13 mol·L-1,故前者是后者的10倍。
6.在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸:
(1)当三种酸的物质的量浓度相同时,c(H+)由大到小的顺序是 (用字母表示,下
同)。
(2)同体积、同物质的量浓度的三种酸,中和 NaOH 的能力由大到小的顺序是
。
(3)若三者c(H+)相同时,物质的量浓度由大到小的顺序是 。
(4)当三者c(H+)相同且体积也相同时,分别放入足量的锌,相同状况下产生气体的体积由大
到小的顺序是 。
(5)当三者c(H+)相同且体积也相同时,同时加入形状、密度、质量完全相同的锌,若产生相
同体积的H(相同状况),则开始时反应速率的大小关系为 ,
2
反应所需时间的长短关系是 。
(6)将c(H+)相同的三种酸均加水稀释至原来的100倍后,c(H+)由大到小的顺序是 。(7)将c(H+)相同且体积也相同的三种酸,分别与等浓度的 NaOH稀溶液反应至pH=7,则消
耗NaOH溶液的体积大小关系为 。
答案 (1)b>a>c (2)b>a=c (3)c>a>b (4)c>a=b
(5)a=b=c a=b>c (6)c>a=b
(7)c>a=b
解析 解答本题要注意以下三点:① HCl、HSO 都是强酸,但 HSO 是二元酸;
2 4 2 4
②CHCOOH是弱酸,在水溶液中不能完全电离;③醋酸溶液中存在CHCOOHCHCOO
3 3 3
-+H+的电离平衡。