文档内容
单元检测十四 物质结构与性质
一、选择题(本题包括15小题,每小题3分,共45分。在每小题给出的四个选项中,只有
一项是符合题目要求的)
1.下列各项叙述正确的是( )
A.N、P、As的电负性随原子序数的增大而增大
B.价电子排布为4s24p3的元素位于第四周期第ⅤA族,是p区元素
C.2p和3p轨道形状均为哑铃形,能量也相等
D.氮原子的最外层电子排布图:
2.下列各组表述中,两个微粒一定不属于同种元素原子的是( )
A.3p能级有一个空轨道的基态原子和核外电子排布为1s22s22p63s23p2的原子
B.M层全充满而N层为4s2的原子和核外电子排布为1s22s22p63s23p63d64s2的原子
C.最外层电子数是核外电子总数的的原子和价电子排布为4s24p5的原子
D.2p能级有一个未成对电子的基态原子和价电子排布为2s22p5的原子
3.下列关于元素第一电离能的说法不正确的是( )
A.钾元素的第一电离能小于钠元素的第一电离能,故钾的活泼性强于钠
B.因同周期元素的原子半径从左到右逐渐减小,故第一电离能必依次增大
C.最外层电子排布为ns2np6(若只有K层时为1s2)的原子,第一电离能较大
D.对于同一元素而言,原子的电离能I<I<I<…
1 2 3
4.对于短周期元素形成的各分子,下表所述的对应关系错误的是( )
选项 A B C D
分子式 CH NH CO SCl
4 3 2 2
VSEPR模型名称 正四面体形 四面体形 直线形 四面体形
分子的空间结构名称 正四面体形 平面三角形 直线形 V形
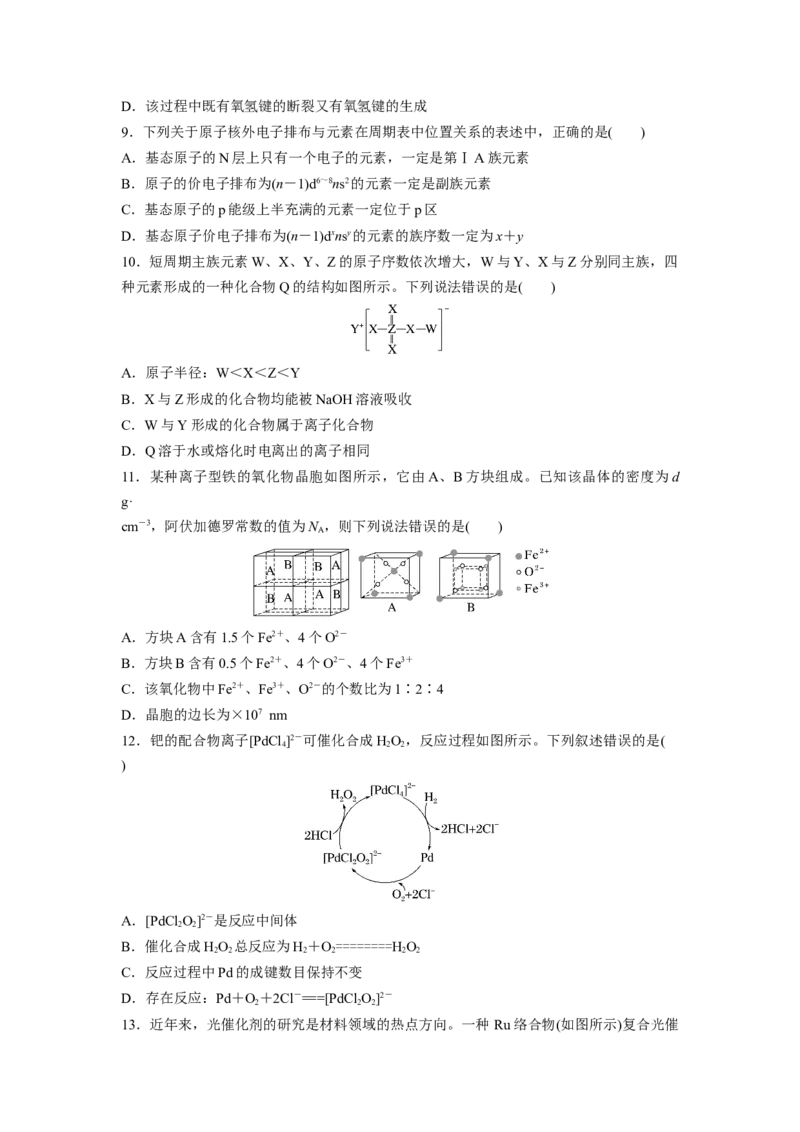
5.已知各种硝基苯酚的性质如下表:
25 ℃,水
名称 结构式 熔点/℃ 沸点/℃
中溶解度/g
邻硝基苯酚 0.2 45 100间硝基苯酚 1.4 96 194
对硝基苯酚 1.7 114 295
下列关于各种硝基苯酚的叙述不正确的是( )
A.邻硝基苯酚分子内形成氢键,使其熔、沸点低于另两种硝基苯酚
B.间硝基苯酚不仅分子间能形成氢键,也能与水分子形成氢键
C.对硝基苯酚分子间能形成氢键,使其熔、沸点较高
D.三种硝基苯酚都不能与水分子形成氢键,所以在水中溶解度小
6.下列有关原子晶体的叙述不正确的是( )
A.金刚石和二氧化硅晶体的最小结构单元都是正四面体
B.1 mol金刚石中的C—C数目是2N ,1 mol SiO 晶体中的Si—O数目是4N
A 2 A
C.水晶和干冰在熔化时,晶体中的共价键都会断裂
D.SiO 晶体是原子晶体,所以晶体中不存在分子,SiO 不是它的分子式
2 2
7.元素周期表是安置元素的一座“大厦”,已知原子的下列结构或性质,能确定其在周期
表中的“单元号和房间号”即位置的是( )
A.某元素原子的第二电子层电子排布图为
B.某元素在某种化合物中的化合价为+4
C.某元素的原子最外层电子数为6
D.某元素的原子价电子排布式为5s25p1
8.硫酸盐(含SO、HSO)气溶胶是雾霾的成分之一。科学家发现通过“水分子桥”,处于
纳米液滴中的SO可以将电子快速转移给周围的气相 NO 分子,雾霾中硫酸盐生成的主要
2
过程示意图如图。
下列说法错误的是( )
A.“水分子桥”主要靠氢键形成
B.过程①②中硫元素均被氧化
C.NO 是生成硫酸盐的催化剂
2D.该过程中既有氧氢键的断裂又有氧氢键的生成
9.下列关于原子核外电子排布与元素在周期表中位置关系的表述中,正确的是( )
A.基态原子的N层上只有一个电子的元素,一定是第ⅠA族元素
B.原子的价电子排布为(n-1)d6~8ns2的元素一定是副族元素
C.基态原子的p能级上半充满的元素一定位于p区
D.基态原子价电子排布为(n-1)dxnsy的元素的族序数一定为x+y
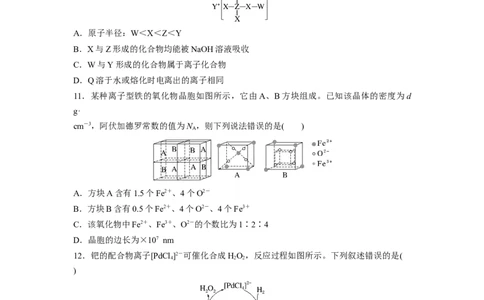
10.短周期主族元素W、X、Y、Z的原子序数依次增大,W与Y、X与Z分别同主族,四
种元素形成的一种化合物Q的结构如图所示。下列说法错误的是( )
A.原子半径:W<X<Z<Y
B.X与Z形成的化合物均能被NaOH溶液吸收
C.W与Y形成的化合物属于离子化合物
D.Q溶于水或熔化时电离出的离子相同
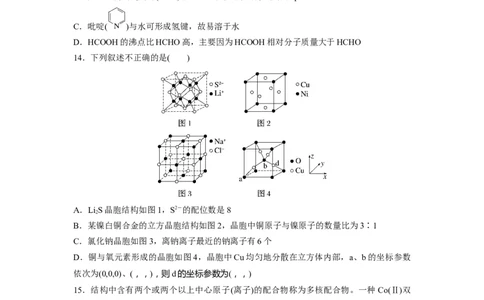
11.某种离子型铁的氧化物晶胞如图所示,它由A、B方块组成。已知该晶体的密度为d
g·
cm-3,阿伏加德罗常数的值为N ,则下列说法错误的是( )
A
A.方块A含有1.5个Fe2+、4个O2-
B.方块B含有0.5个Fe2+、4个O2-、4个Fe3+
C.该氧化物中Fe2+、Fe3+、O2-的个数比为1∶2∶4
D.晶胞的边长为×107 nm
12.钯的配合物离子[PdCl ]2-可催化合成HO ,反应过程如图所示。下列叙述错误的是(
4 2 2
)
A.[PdCl O]2-是反应中间体
2 2
B.催化合成HO 总反应为H+O========HO
2 2 2 2 2 2
C.反应过程中Pd的成键数目保持不变
D.存在反应:Pd+O+2Cl-===[PdCl O]2-
2 2 2
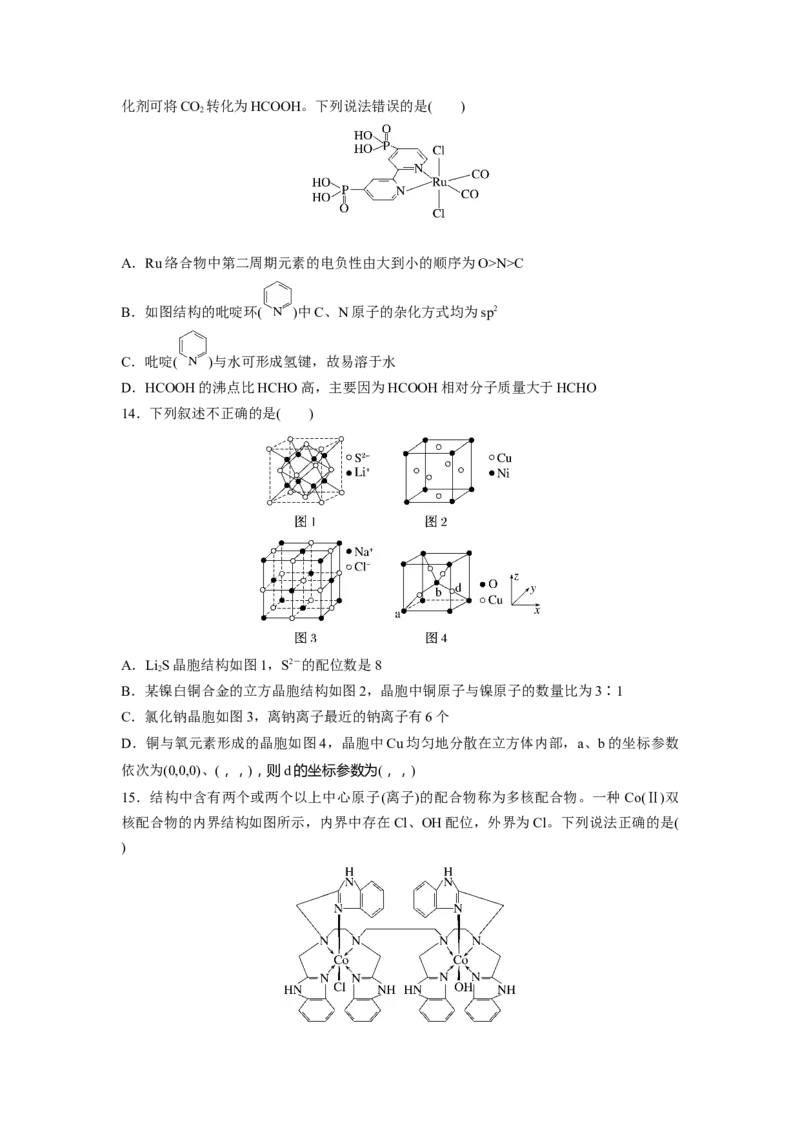
13.近年来,光催化剂的研究是材料领域的热点方向。一种 Ru络合物(如图所示)复合光催化剂可将CO 转化为HCOOH。下列说法错误的是( )
2
A.Ru络合物中第二周期元素的电负性由大到小的顺序为O>N>C
B.如图结构的吡啶环( )中C、N原子的杂化方式均为sp2
C.吡啶( )与水可形成氢键,故易溶于水
D.HCOOH的沸点比HCHO高,主要因为HCOOH相对分子质量大于HCHO
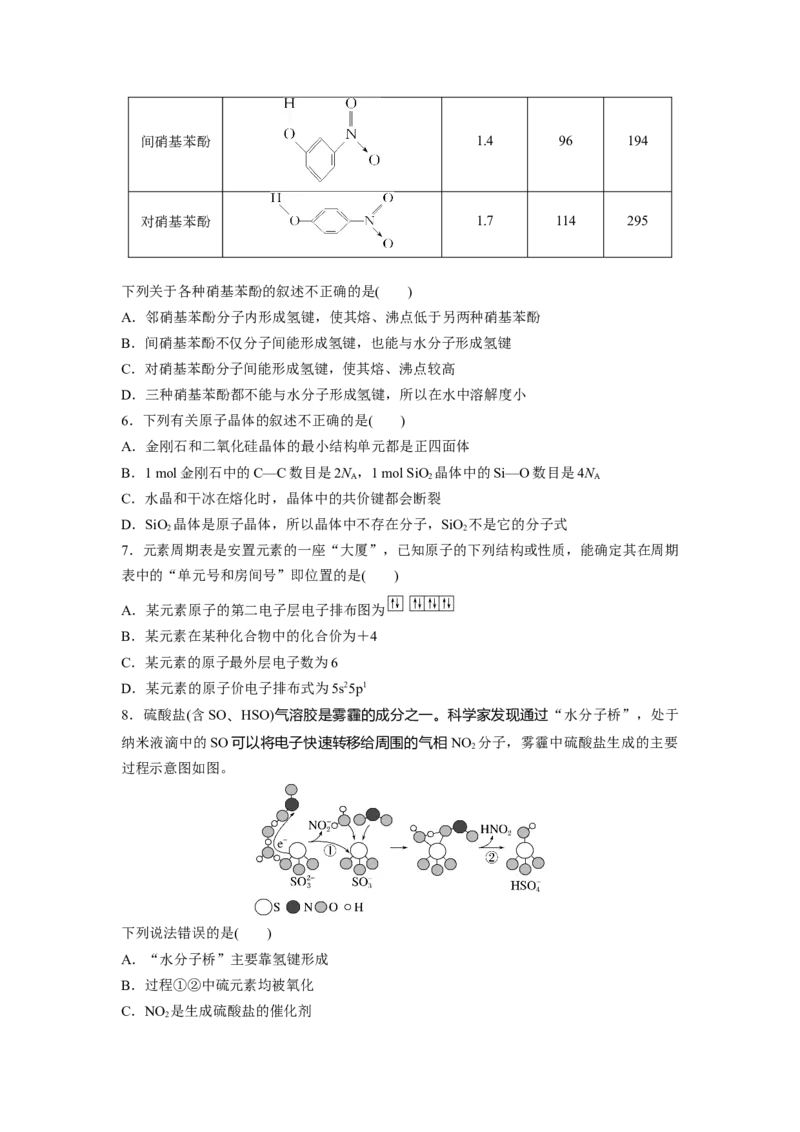
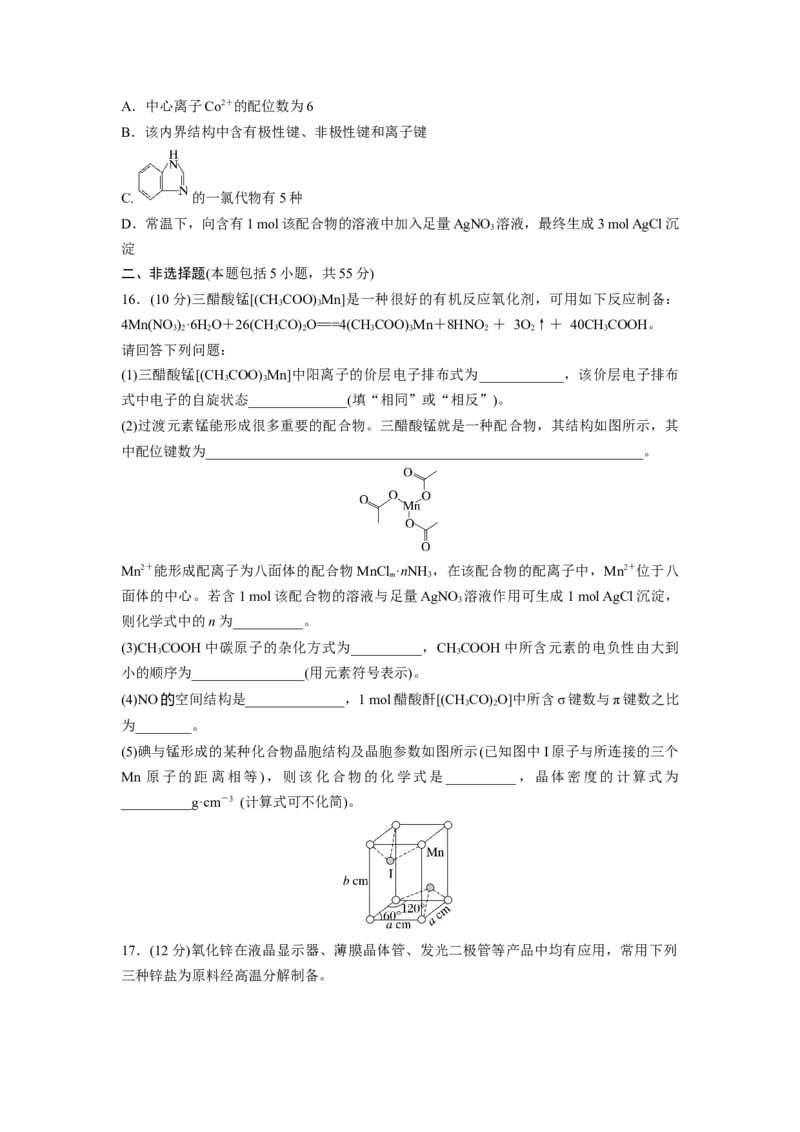
14.下列叙述不正确的是( )
A.LiS晶胞结构如图1,S2-的配位数是8
2
B.某镍白铜合金的立方晶胞结构如图2,晶胞中铜原子与镍原子的数量比为3∶1
C.氯化钠晶胞如图3,离钠离子最近的钠离子有6个
D.铜与氧元素形成的晶胞如图4,晶胞中Cu均匀地分散在立方体内部,a、b的坐标参数
依次为(0,0,0)、(,,),则d的坐标参数为(,,)
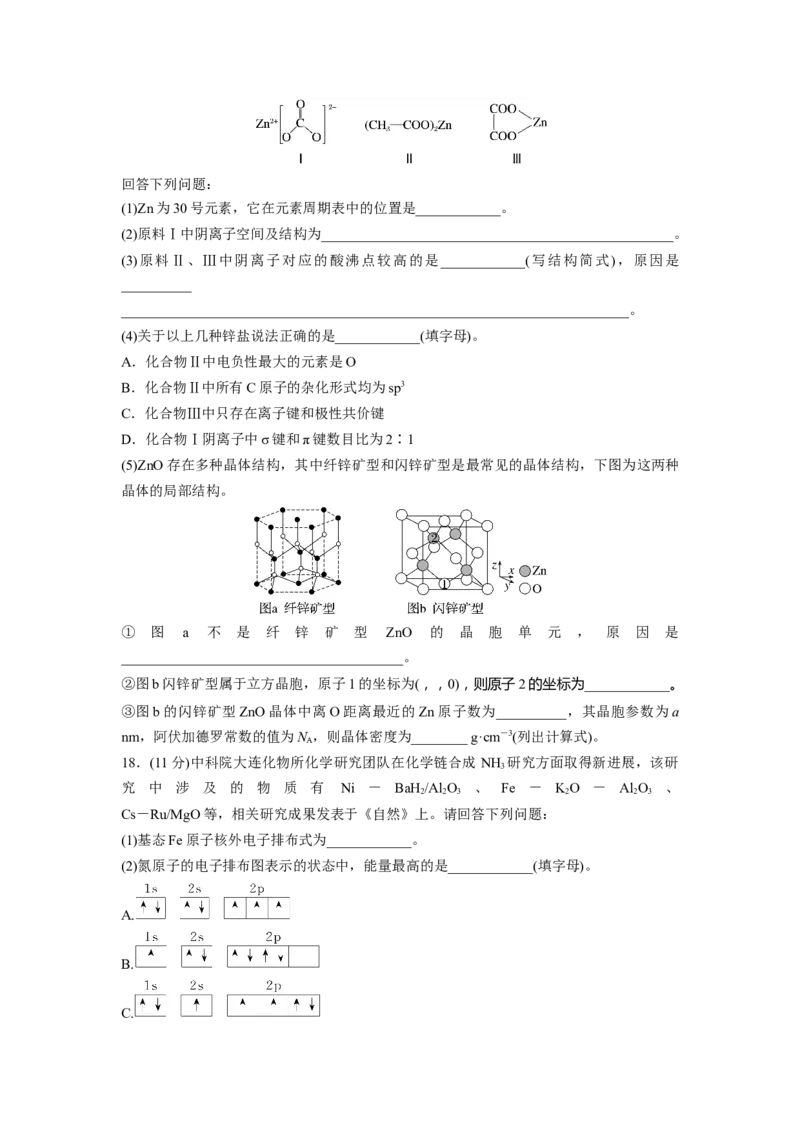
15.结构中含有两个或两个以上中心原子(离子)的配合物称为多核配合物。一种Co(Ⅱ)双
核配合物的内界结构如图所示,内界中存在Cl、OH配位,外界为Cl。下列说法正确的是(
)A.中心离子Co2+的配位数为6
B.该内界结构中含有极性键、非极性键和离子键
C. 的一氯代物有5种
D.常温下,向含有1 mol该配合物的溶液中加入足量AgNO 溶液,最终生成3 mol AgCl沉
3
淀
二、非选择题(本题包括5小题,共55分)
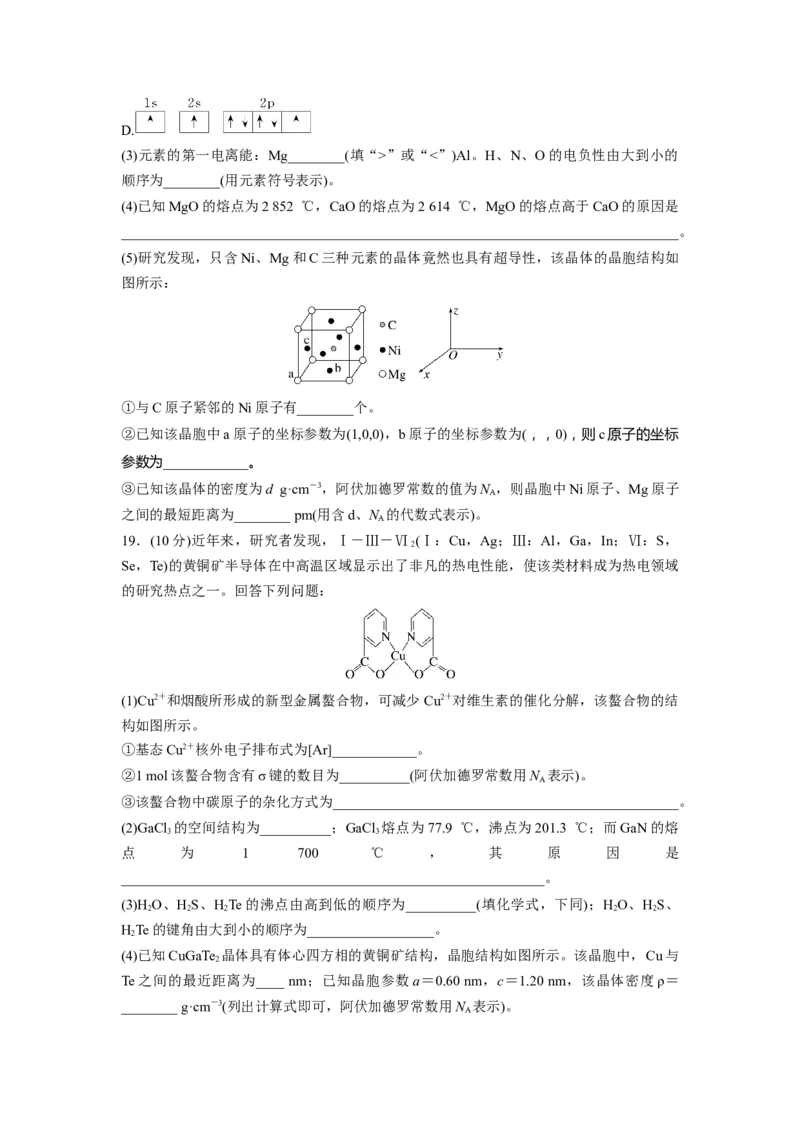
16.(10分)三醋酸锰[(CH COO) Mn]是一种很好的有机反应氧化剂,可用如下反应制备:
3 3
4Mn(NO)·6H O+26(CHCO) O===4(CHCOO) Mn+8HNO + 3O↑+ 40CHCOOH。
3 2 2 3 2 3 3 2 2 3
请回答下列问题:
(1)三醋酸锰[(CH COO) Mn]中阳离子的价层电子排布式为____________,该价层电子排布
3 3
式中电子的自旋状态______________(填“相同”或“相反”)。
(2)过渡元素锰能形成很多重要的配合物。三醋酸锰就是一种配合物,其结构如图所示,其
中配位键数为______________________________________________________________。
Mn2+能形成配离子为八面体的配合物MnCl ·nNH ,在该配合物的配离子中,Mn2+位于八
m 3
面体的中心。若含1 mol该配合物的溶液与足量AgNO 溶液作用可生成1 mol AgCl沉淀,
3
则化学式中的n为__________。
(3)CH COOH中碳原子的杂化方式为__________,CHCOOH中所含元素的电负性由大到
3 3
小的顺序为________________(用元素符号表示)。
(4)NO的空间结构是______________,1 mol醋酸酐[(CH CO) O]中所含σ键数与π键数之比
3 2
为________。
(5)碘与锰形成的某种化合物晶胞结构及晶胞参数如图所示(已知图中I原子与所连接的三个
Mn 原子的距离相等),则该化合物的化学式是__________,晶体密度的计算式为
__________g·cm-3 (计算式可不化简)。
17.(12分)氧化锌在液晶显示器、薄膜晶体管、发光二极管等产品中均有应用,常用下列
三种锌盐为原料经高温分解制备。回答下列问题:
(1)Zn为30号元素,它在元素周期表中的位置是____________。
(2)原料Ⅰ中阴离子空间及结构为__________________________________________________。
(3)原料Ⅱ、Ⅲ中阴离子对应的酸沸点较高的是____________(写结构简式),原因是
__________
________________________________________________________________________。
(4)关于以上几种锌盐说法正确的是____________(填字母)。
A.化合物Ⅱ中电负性最大的元素是O
B.化合物Ⅱ中所有C原子的杂化形式均为sp3
C.化合物Ⅲ中只存在离子键和极性共价键
D.化合物Ⅰ阴离子中σ键和π键数目比为2∶1
(5)ZnO存在多种晶体结构,其中纤锌矿型和闪锌矿型是最常见的晶体结构,下图为这两种
晶体的局部结构。
① 图 a 不 是 纤 锌 矿 型 ZnO 的 晶 胞 单 元 , 原 因 是
________________________________________。
②图b闪锌矿型属于立方晶胞,原子1的坐标为(,,0),则原子2的坐标为____________。
③图b的闪锌矿型ZnO晶体中离O距离最近的Zn原子数为__________,其晶胞参数为a
nm,阿伏加德罗常数的值为N ,则晶体密度为________ g·cm-3(列出计算式)。
A
18.(11分)中科院大连化物所化学研究团队在化学链合成 NH 研究方面取得新进展,该研
3
究 中 涉 及 的 物 质 有 Ni - BaH/Al O 、 Fe - KO - Al O 、
2 2 3 2 2 3
Cs-Ru/MgO等,相关研究成果发表于《自然》上。请回答下列问题:
(1)基态Fe原子核外电子排布式为____________。
(2)氮原子的电子排布图表示的状态中,能量最高的是____________(填字母)。
A.
B.
C.D.
(3)元素的第一电离能:Mg________(填“>”或“<”)Al。H、N、O的电负性由大到小的
顺序为________(用元素符号表示)。
(4)已知MgO的熔点为2 852 ℃,CaO的熔点为2 614 ℃,MgO的熔点高于CaO的原因是
_______________________________________________________________________________。
(5)研究发现,只含Ni、Mg和C三种元素的晶体竟然也具有超导性,该晶体的晶胞结构如
图所示:
①与C原子紧邻的Ni原子有________个。
②已知该晶胞中a原子的坐标参数为(1,0,0),b原子的坐标参数为(,,0),则c原子的坐标
参数为____________。
③已知该晶体的密度为d g·cm-3,阿伏加德罗常数的值为N ,则晶胞中Ni原子、Mg原子
A
之间的最短距离为________ pm(用含d、N 的代数式表示)。
A
19.(10分)近年来,研究者发现,Ⅰ-Ⅲ-Ⅵ (Ⅰ:Cu,Ag;Ⅲ:Al,Ga,In;Ⅵ:S,
2
Se,Te)的黄铜矿半导体在中高温区域显示出了非凡的热电性能,使该类材料成为热电领域
的研究热点之一。回答下列问题:
(1)Cu2+和烟酸所形成的新型金属螯合物,可减少Cu2+对维生素的催化分解,该螯合物的结
构如图所示。
①基态Cu2+核外电子排布式为[Ar]____________。
②1 mol该螯合物含有σ键的数目为__________(阿伏加德罗常数用N 表示)。
A
③该螯合物中碳原子的杂化方式为_________________________________________________。
(2)GaCl 的空间结构为__________;GaCl 熔点为77.9 ℃,沸点为201.3 ℃;而GaN的熔
3 3
点 为 1 700 ℃ , 其 原 因 是
____________________________________________________________。
(3)H O、HS、HTe的沸点由高到低的顺序为__________(填化学式,下同);HO、HS、
2 2 2 2 2
HTe的键角由大到小的顺序为__________________。
2
(4)已知CuGaTe 晶体具有体心四方相的黄铜矿结构,晶胞结构如图所示。该晶胞中,Cu与
2
Te之间的最近距离为____ nm;已知晶胞参数a=0.60 nm,c=1.20 nm,该晶体密度ρ=
________ g·cm-3(列出计算式即可,阿伏加德罗常数用N 表示)。
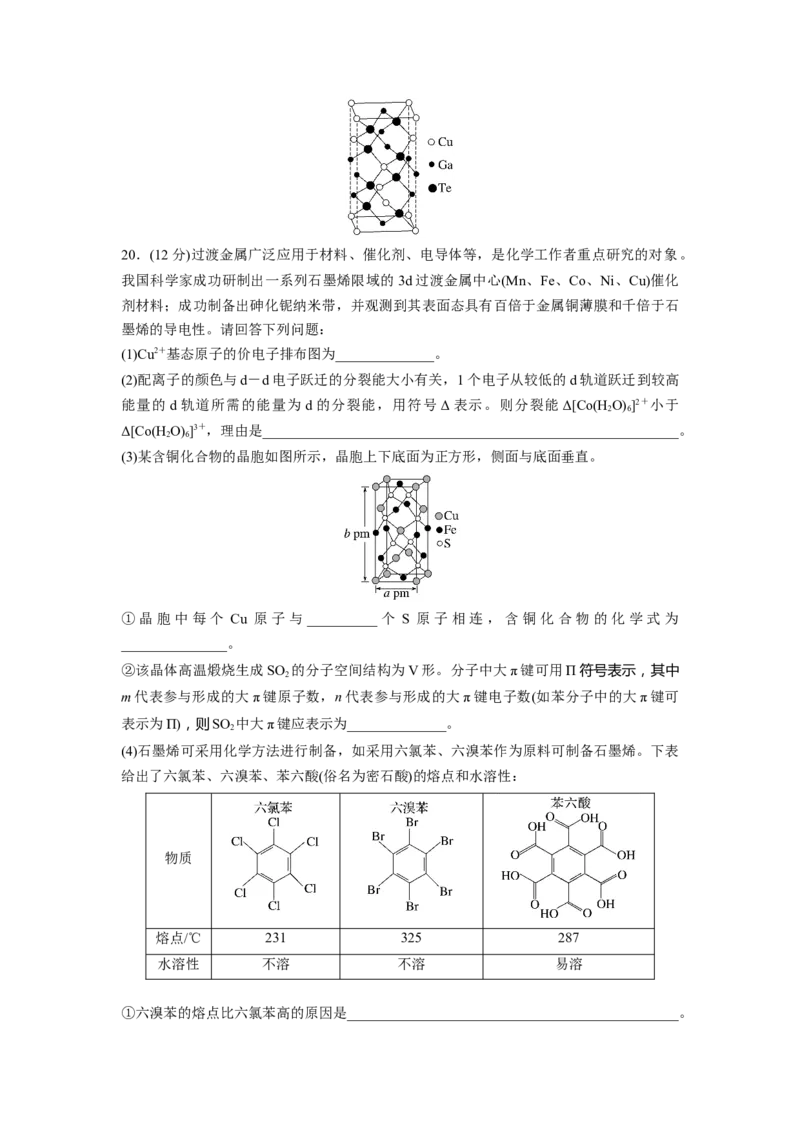
A20.(12分)过渡金属广泛应用于材料、催化剂、电导体等,是化学工作者重点研究的对象。
我国科学家成功研制出一系列石墨烯限域的3d过渡金属中心(Mn、Fe、Co、Ni、Cu)催化
剂材料;成功制备出砷化铌纳米带,并观测到其表面态具有百倍于金属铜薄膜和千倍于石
墨烯的导电性。请回答下列问题:
(1)Cu2+基态原子的价电子排布图为______________。
(2)配离子的颜色与d-d电子跃迁的分裂能大小有关,1个电子从较低的d轨道跃迁到较高
能量的d轨道所需的能量为 d的分裂能,用符号 Δ表示。则分裂能 Δ[Co(H O) ]2+小于
2 6
Δ[Co(H O) ]3+,理由是___________________________________________________________。
2 6
(3)某含铜化合物的晶胞如图所示,晶胞上下底面为正方形,侧面与底面垂直。
①晶胞中每个 Cu 原子与__________个 S 原子相连,含铜化合物的化学式为
_______________。
②该晶体高温煅烧生成SO 的分子空间结构为V形。分子中大π键可用Π符号表示,其中
2
m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可
表示为Π),则SO 中大π键应表示为______________。
2
(4)石墨烯可采用化学方法进行制备,如采用六氯苯、六溴苯作为原料可制备石墨烯。下表
给出了六氯苯、六溴苯、苯六酸(俗名为密石酸)的熔点和水溶性:
物质
熔点/℃ 231 325 287
水溶性 不溶 不溶 易溶
①六溴苯的熔点比六氯苯高的原因是_______________________________________________。② 苯 六 酸 与 六 溴 苯 、 六 氯 苯 的 水 溶 性 存 在 明 显 的 差 异 , 原 因 是
___________________________。
③ 苯 六 酸 分 子 中 C 的 杂 化 方 式 是
___________________________________________________。
(5)铌元素(Nb)为一种金属元素,其基态原子的核外电子排布式为[Kr]4d45s1。下列不同Nb
微粒的核外电子排布式中,失去最外层1个电子所需能量最小的是________(填字母)。
a.[Kr]4d35s2
b.[Kr]4d25s15p2
c.[Kr]4d4
d.[Kr]4d3
(6)β-MnSe的结构中Se为面心立方最密堆积,晶胞结构如图所示。若该晶体的晶胞参数为a
pm,阿伏加德罗常数的值为N 。则距离最近的两个锰原子之间的距离为________ pm。
A
单元检测十四 物质结构与性质答案解析
1.
答案 B
解析 同主族元素从上到下,电负性逐渐减小,则N、P、As的电负性随原子序数的增大
而减小,故A错误;价电子排布为4s24p3的元素有4个电子层,最外层电子数为5,位于第
四周期第ⅤA族,是p区元素,故B正确;p轨道均为哑铃形,离原子核越远,能量越高,
2p 轨道的能量低于 3p 轨道,故 C 错误;由洪特规则可知最外层电子排布图应为
,故D错误。
2.
答案 B
解析 3p能级有一个空轨道,说明3p上填2个电子,则3s上肯定已填满,价电子排布为
3s23p2,A选项不符合题意;M层全充满而N层为4s2,价电子排布为3d104s2,是锌元素,
价电子排布为3d64s2是铁元素,B选项符合题意;价电子排布为4s24p5,则核外电子排布为
1s22s22p63s23p63d104s24p5;最外层电子数是核外电子总数的原子,可按下述方法讨论:若最
外层电子数为1,核外电子总数为5,不合理,最外层电子数为2,核外电子总数为10,不
合理,同理,可知只有最外层电子数为7,核外电子总数为35时合理,其电子排布式也是1s22s22p63s23p63d104s24p5,二者是同种元素的原子,C选项不符合题意;2p能级有一个未成
对电子,可以是2p1,也可以是2p5,因此二者不一定属于同种元素的原子,D选项不符合
题意。
3.
答案 B
解析 A项,同一主族,从上到下元素的第一电离能越来越小,金属性越来越强;B项,
同周期的第ⅡA与第ⅢA族,第ⅤA与第ⅥA族,第一电离能出现了反常;C项,ns2np6
的原子为稀有气体元素的原子, 第一电离能较大;D项,同一元素的原子,I<I<I。
1 2 3
4.答案 B
解析 C原子形成了4个σ键,孤电子对数为0,VSEPR模型及分子的空间结构均是正四
面体形,A项正确;N原子有1对孤电子对且形成了3个σ键,VSEPR模型为四面体形,
分子的空间结构为三角锥形,B项错误;C原子的价层电子对数为2+×(4-2×2)=2,
VSEPR模型为直线形,分子的空间结构也为直线形,C项正确;S原子有2对孤电子对且
形成了2个σ键,VSEPR模型为四面体形,分子的空间结构为V形,D项正确。
5.
答案 D
解析 当分子形成分子内氢键时,就难再形成分子间氢键,故其熔、沸点低,A正确;间
硝基苯酚中与N原子相连的O原子易与水分子中的H原子形成氢键,B正确、D错误;形
成分子间氢键后,物质的熔、沸点升高,C正确。
6.
答案 C
解析 金刚石和二氧化硅晶体的基本结构单元都是正四面体,A正确;金刚石中,1个C
原子与另外4个C原子形成C—C,这个C原子对每个单键的贡献只有,所以1 mol C原子
形成的C—C为4×=2 mol,而二氧化硅晶体中1个Si原子与4个O原子形成4个Si—O,
则1 mol SiO 晶体中Si—O为4 mol,B正确;水晶是原子晶体,在熔化时,共价键断裂形
2
成自由移动的Si、O原子,而分子晶体干冰熔化时,分子间作用力被大大削弱,形成自由
移动的CO 分子,C==O不会断裂,C错误。
2
7.
答案 D
解析 从Ne开始元素原子的第二电子层电子排布图均为 ,故只知道第二电子
层电子排布图无法确定元素的位置,A不符合题意;某元素在某种化合物中的化合价为+4
无法确定其位置,如CO 中C为+4价,C位于第二周期第ⅣA族,NO 中N为+4价,N
2 2 4
位于第二周期第ⅤA族,B不符合题意;某元素的原子最外层电子数为 6无法确定其周期,
如O位于第二周期第ⅥA族,S位于第三周期第ⅥA族,即第ⅥA族元素的原子最外层电子数均为6,C不符合题意;原子价电子排布式为5s25p1的元素位于第五周期第ⅢA族,能
确定其位置,D符合题意。
8.
答案 C
解析 水分子中氧原子的电负性较大,水分子之间主要形成氢键,“水分子桥”中SO中
的氧原子和水分子中的氢原子、NO 中的氧原子和水分子中的氢原子之间,主要靠氢键形
2
成,故A不符合题意;过程①表示SO转化为SO,硫元素的化合价从+4升高为+5,过程
②表示SO转化为HSO,硫元素的化合价从+5升高到+6,均被氧化,故B不符合题意;
根据图中的转化关系,NO 转化为HNO ,氮元素的化合价从+4降低到+3,被还原,作
2 2
氧化剂,故C符合题意;根据图示,SO加入一个水分子转化为HSO的过程,有水分子中
氢氧键的断裂,NO 加入一个水分子转化为HNO 的过程中有氢氧键的形成,故D不符合
2 2
题意。
9.
答案 C
解析 基态原子的N层上只有一个电子的元素,可能为K、Cr或Cu,K为主族元素,Cr、
Cu为副族元素,故A错误;副族元素的d能级电子数为10或1~5,原子的价电子排布为
(n-1)d6~8ns2的元素为第Ⅷ族元素,故B错误;基态原子p能级上半充满的元素,电子最
后填充p能级,属于p区,故C正确;第ⅢB~ⅦB族及第Ⅷ族元素,其族序数为外围电
子中d、s能级含有的电子数目之和,即x+y,但第ⅠB族、第ⅡB族元素,族序数等于外
围电子排布中s能级中的电子数y,故D错误。
10.
答案 D
解析 由题给信息分析知,W、X、Y、Z分别为H、O、Na、S,Q为NaHSO 。同一周期
4
表从左到右原子半径逐渐减小,同一主族元素从上到下原子半径逐渐增大,原子半径:H
<O<S<Na,A项正确;SO 和SO 均属于酸性氧化物,均能被NaOH溶液吸收,B项正
2 3
确;H和Na形成的化合物为NaH,NaH属于离子化合物,C项正确;NaHSO 溶于水电离
4
出Na+、H+、SO,熔化时电离出Na+和HSO,D项错误。
11.
答案 D
解析 根据均摊法计算A含有1+4×=1.5个亚铁离子、4个氧离子,故A正确;根据均
摊法计算B含有4×=0.5个亚铁离子、4个氧离子、4个铁离子,故B正确;Fe2+处于晶胞
的顶点、面心以及A方块的体心,O2-位于A、B方块的内部,Fe3+处于B方块内部,晶胞
中Fe2+数目为4+8×+6×=8,Fe3+数目为4×4=16,O2-数目为4×8=32,故Fe2+、Fe3
+、O2-的个数比为8∶16∶32=1∶2∶4,故C正确;晶胞中含有Fe2+、Fe3+、O2-的个数分别是8、16、32,它们的相对原子质量之和是 8×232,根据m=ρV可得 g=d g·cm-
3×a3,a=×107nm,故D错误。
12.
答案 C
解析 由图可知,钯的配合物离子[PdCl ]2-先与氢气反应生成Pd,Pd继续与O 和Cl-反应
4 2
生成[PdCl O]2-,[PdCl O]2-再与HCl反应生成HO ,所以[PdCl O]2-是反应中间体,故
2 2 2 2 2 2 2 2
A正确;由图可知发生的总反应为H+O========HO,故B正确;[PdCl O]2-中Pd形成
2 2 2 2 2 2
6个键,可以看出 Pd 的成键数目发生改变,故 C 错误;在流程中存在 Pd+O +2Cl-
2
===[PdCl O]2-,故D正确。
2 2
13.
答案 D
解析 第二周期元素除 Ne 电负性从左往右逐渐增强,故电负性由大到小的顺序为
O>N>C,A正确;如图结构的吡啶环( )中C、N原子的价层电子对数均为3,故杂化方
式均为sp2,B正确;吡啶( )含电负性强的N元素,氮原子能与水形成氢键,C正确;
HCOOH存在分子间作用力和氢键,且HCOOH分子间氢键作用较强,D错误。
14.
答案 C
解析 Li+与S2-的个数比为2∶1,则Li+与S2-的配位数之比为1∶2,由LiS的晶胞结构
2
可知,Li+的配位数为4,则S2-的配位数是8,A正确;晶胞中Ni原子的个数为8×=1,
Cu原子的个数为6×=3,则晶胞中铜原子与镍原子的数量比为3∶1,B正确;以1个顶点
Na+为研究对象,在图示晶胞中离其最近的Na+为位于面心上的3个Na+,由于顶点Na+为
8个晶胞共有,面心Na+为2个晶胞共有,则氯化钠晶胞中离钠离子最近的钠离子有=12
个,C错误;晶胞中Cu均匀地分散在立方体内部,位于体对角线上,与体心O的距离为体
对角线的,a、b的坐标参数依次为(0,0,0)、(,,),则d的坐标参数为(,,),D正确。
15.
答案 A
解析 中心离子Co2+与5个N原子、1个Cl-或5个N原子、1个OH-形成配位键,则配
位数为6,故A正确;含有C—H、C—N极性键、C—C非极性键,不含有离子键,故B
错误; 的一氯代物有6种,故C错误;中心离子为Co2+,则1 mol该配合物外界
有2 mol Cl-,加入足量AgNO 溶液,最终生成2 mol AgCl沉淀,故D错误。
3
16.答案 (1)3d4 相同 (2)3 5 (3)sp2、sp3 O>C>H (4)V形 6∶1
(5)MnI (或)
2
解析 (1)Mn为25号元素,根据构造原理知,Mn的基态原子核外电子排布为[Ar]3d54s2,
故 Mn3+核外电子排布式为[Ar]3d4,价层电子排布式为 3d4,该价层电子排布图为
,电子的自旋状态相同。
(2)由三醋酸锰的结构可知,配位键数为3;由1 mol该配合物与足量AgNO 作用生成1 mol
3
AgCl沉淀,知1 mol配合物电离出1 mol Cl-,即配离子显+1价,又因为外界有1个Cl
-,且Mn显+2价,所以[MnCl ·nNH ]+中有1个氯原子,即p=1,又因为该配合物为八
p 3
面体的配合物,Mn2+位于八面体的中心,如图 所示,其中数字处的小圆
圈表示 NH 分子或 Cl-,该配合物配位数为 6,所以 n=6-1=5,该配合物为
3
MnCl ·5NH 。
2 3
(3)CH COOH中甲基上C原子价层电子对数是4、羧基上C原子价层电子对数是3,根据价
3
层电子对互斥模型判断碳原子的杂化方式前者为sp3、后者是sp2;元素的非金属性越强,
其电负性越大,在CHCOOH中所含元素的非金属性:O>C>H,则电负性:O>C>H。
3
(4)NO中N原子价层电子对数为2+=2+1=3,含一对孤电子对,根据价层电子对互斥模
型判断该离子空间结构为V形;单键全是 σ键,双键含一个 σ键和一个π键,醋酸酐
[(CH CO) O]的结构简式可表示为 ,1 mol 醋酸酐中含12 mol σ键与2
3 2
mol π键,则σ键数与π键数之比为6∶1。
(5)由晶胞图知,I在内部,有2个,Mn在顶点,数目为×8=1,即化合物的化学式为
MnI ;ρ=== g·cm-3= g·cm-3。
2
17.
答案 (1)第四周期第ⅡB族
(2)平面三角形
(3)HOOC—COOH 草酸的相对分子质量高于醋酸,同时草酸存在两个羧基结构,可以分
别与其他分子形成分子间氢键
(4)A
(5)①晶胞单元是晶体的最小重复结构单元,该结构中包含了三个更小的重复结构单元
②(,,) ③4
解析 (2)Ⅰ中阴离子为CO,据图可知C原子形成碳氧双键,采取sp2杂化,空间结构为平面三角形。(3)Ⅱ、Ⅲ中阴离子对应的酸分别为CHCOOH(醋酸)、HOOC—COOH(草酸),
3
草酸的相对分子质量高于醋酸,同时草酸存在两个羧基结构,可以分别与其他分子形成分
子间氢键,所以HOOCCOOH的沸点较高。(4)化合物Ⅱ中O元素的非金属性最强,电负性
最大,
A正确;化合物Ⅱ中甲基上的碳原子为饱和碳原子,为sp3杂化,而羧基中的碳原子为sp2
杂化,B错误;化合物Ⅲ中两个C原子之间为非极性共价键,C错误;单键均为σ键,双
键中有一个σ键、一个π键,所以化合物Ⅰ阴离子中σ键和π键数目比为3∶1,D错误。
(5)②根据原子1的坐标可知底面左上角O原子为原点,晶胞棱长为单位1,原子2位于体
对角线上,坐标为(,,)。③以顶面面心的O原子为例,该晶胞中有2个Zn原子距离其最
近且相等,该晶胞的上方晶胞中还有两个,所以离O距离最近的Zn原子数为4;根据晶胞
结构可知一个晶胞中有4个Zn原子,化学式为ZnO,所以一个晶胞O原子的个数也为4,
则晶胞的质量为 g,晶胞参数为a nm,则体积为a3 nm3=a3×10-21 cm3,所以密度为
g·cm-3。
18.
答案 (1)[Ar]3d64s2 (2)D (3)> O>N>H (4)Mg2+的半径小于Ca2+,MgO的离子键强
于CaO的离子键 (5)①6 ②(,0,) ③××1010
解析 (1)Fe是26号元素,核外电子排布式为 1s22s22p63s23p63d64s2,简化电子排布式为
[Ar]3d64s2。(2)基态氮原子具有的能量最低,激发态氮原子具有的能量较高,且较高能级轨
道排布的电子越多原子具有的能量越高,D选项中1s和2s轨道中各有一个电子跃迁到2p
能级,能量最高。(3)Mg元素原子3s能级为全充满的稳定状态,第一电离能高于同周期相
邻元素的,故第一电离能:Mg>Al;元素的非金属性越强,电负性越大,故电负性:O>N
>H。(4)MgO、CaO均属于离子晶体,离子所带电荷数相同,Mg2+的半径小于Ca2+的半径,
MgO的离子键强于CaO的离子键,故MgO的熔点高于CaO的。(5)①C原子处于体心,与
其紧邻的Ni原子处于面心,与C原子紧邻的Ni原子有6个。②c原子处于晶胞左侧面面
心,a原子的坐标参数为(1,0,0),b原子的坐标参数为(,,0),故c原子的坐标参数为(,
0,)。③Ni、Mg原子之间的最大距离等于晶胞边长的倍,晶胞中C原子数目为1,Mg原
子数目为8×=1,Ni原子数目为6×=3,故晶胞质量为 g,设晶胞边长为a pm,则 g=
d g·cm-3×(a×10-10 cm)3,解得a=×1010,晶胞中Ni原子、Mg原子之间的最短距离为
××1010 pm。
19.
答案 (1)①3d9 ②30N ③sp2 (2)平面三角形 GaCl 为分子晶体,GaN为共价晶体
A 3
(3)H O>HTe>HS HO>HS>HTe (4)
2 2 2 2 2 2
解析 (1)①Cu元素位于第四周期第ⅠB族,原子序数为29,价电子排布式为3d104s1,因
此Cu2+的核外电子排布式为[Ar]3d9。②单键之间有一个σ键,双键之间有一个σ键、一个π 键,因此 1 mol 该螯合物中含有σ键的数目为30N 。③根据螯合物的结构简式,有
A
、 、 三种碳原子,C的杂化方式为sp2。(2)Ga与Al同主族,
GaCl 中有
3
3个σ键,孤电子对数为=0,价层电子对数为 3,即GaCl 的空间结构为平面三角形;
3
GaCl 熔点为77.9 ℃,沸点为201.3 ℃,熔、沸点低,这是分子晶体的特点,推出GaCl
3 3
为分子晶体,GaN的熔点为1 700 ℃,熔点高,是共价晶体的特点,推出GaN为共价晶体。
(3)H O、HTe、HS都属于分子晶体,HO分子间存在氢键,HS和HTe分子间不存在氢
2 2 2 2 2 2
键,HO的沸点最高,HTe的相对分子质量比HS大,因此HTe的沸点高于HS,从而推
2 2 2 2 2
出沸点高低顺序是HO>HTe>HS;O、S、Te同族,电负性:O>S>Te,电负性越小,
2 2 2
对氢原子的吸引力越弱,2个H—X(X为O、S、Te)的成键电子对之间的排斥力越弱,即键
角的大小顺序是HO>HS>HTe。(4)取晶胞的 ,如图 ,△ABC为等腰三角形,
2 2 2
B向AC作垂线得BD,BD的距离应是a的,即BD= nm,AD的距离是 nm,因此AB的
距离为 nm= nm;Cu原子位于顶点、面上、体内,该晶胞所含Cu的个数为8×+4×+1
=4,即该晶胞的质量为 g,晶胞的体积为(0.60×10-7)2×(1.20×10-7) cm3,该晶胞的密度
为 g·cm-3。
20.
答案 (1)
(2)前者带2个正电荷,后者带 3个正电荷,后者对电子的吸引力较大 (3)①4 CuFeS
2
②Π (4)①六溴苯的相对分子质量大于六氯苯,所以六溴苯的范德华力比六氯苯的强
②苯六酸含多个羧基,与水形成分子间氢键,易溶于水 ③sp2 (5)b (6)a
解析 (3)①从晶胞结构看,每个Cu原子与4个S原子相连;晶胞中硫原子位于晶胞内部,
数目为8,铁原子数目为6×+4×=4,铜原子数目为4×+1+8×=4,含铜化合物的化
学式为 CuFeS 。② SO 中大 π 键是由 3 个原子提供 4 个电子构成的,应表示为 Π。
2 2
(4)①六溴苯和六氯苯都为共价化合物,结构相似,因为六溴苯的相对分子质量大于六氯苯,
所以六溴苯的范德华力比六氯苯的强,所以六溴苯的熔点比六氯苯高。②苯六酸含多个羧
基,与水形成分子间氢键,易溶于水,所以苯六酸与六溴苯、六氯苯的水溶性存在明显的
差异。③苯六酸分子苯环上的碳和羧基上的碳都为sp2杂化。(5)选项中各微粒失去一个电
子,前两个为激发态的第一电离能,c为第二电离能,d为第三电离能,第一、二、三电离
能依次增大,基态的电离能大于激发态的,且5p能级的能量高于4d能级,所以失去最外
层1个电子所需能量最小的是b。 (6)距离最近的两个锰原子之间的距离为面对角线的一半,即a pm。