文档内容
2023届高考化学一轮复习过关训练题:化学反应速率与化学平衡
一、选择题(本大题共16小题)
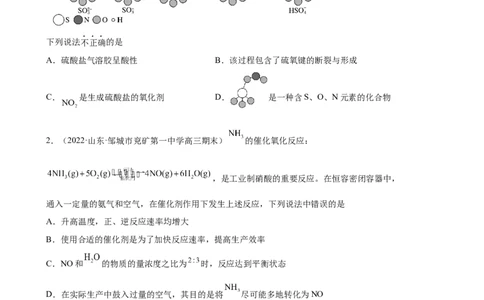
1.(2022·北京·和平街第一中学三模)硫酸盐(含 、 )气溶胶是 的成分之一。近
期科研人员提出了雾霾微颗粒中硫酸盐生成的转化机理,其主要过程示意图如下:
下列说法不正确的是
A.硫酸盐气溶胶呈酸性 B.该过程包含了硫氧键的断裂与形成
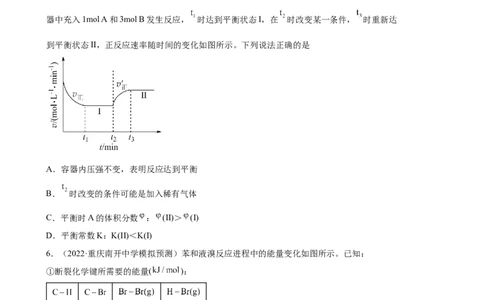
C. 是生成硫酸盐的氧化剂 D. 是一种含S、O、N元素的化合物
2.(2022·山东·邹城市兖矿第一中学高三期末) 的催化氧化反应:
,是工业制硝酸的重要反应。在恒容密闭容器中,
通入一定量的氨气和空气,在催化剂作用下发生上述反应,下列说法中错误的是
A.升高温度,正、逆反应速率均增大
B.使用合适的催化剂是为了加快反应速率,提高生产效率
C.NO和 的物质的量浓度之比为 时,反应达到平衡状态
D.在实际生产中鼓入过量的空气,其目的是将 尽可能多地转化为NO
3.(2022·江苏徐州·高三阶段练习)关于反应CO(g)+CH (g)=2CO(g)+2H(g);ΔH=247kJ·mol-1
2 4 2 1
说法正确的是
A.该反应在任何温度下都可自发进行
B.反应CO(s)+CH(g)=2CO(g)+2H(g);ΔH<247kJ·mol-1
2 4 2 2
C.反应中每生成1molH ,转移电子的数目为3×6.02×1023
2
D.在过渡元素区域内选择高效催化剂可以降低反应的焓变,提高化学反应速率
4.(2022·广东·执信中学高三阶段练习)在一定温度下的恒容密闭容器中,能说明反应已达到平衡的是
A.容器内的总压强不随时间变化
B.容器中气体的平均相对分子质量不随时间变化
C. 键断裂,同时有 键断裂
D. 和 的消耗速率相等
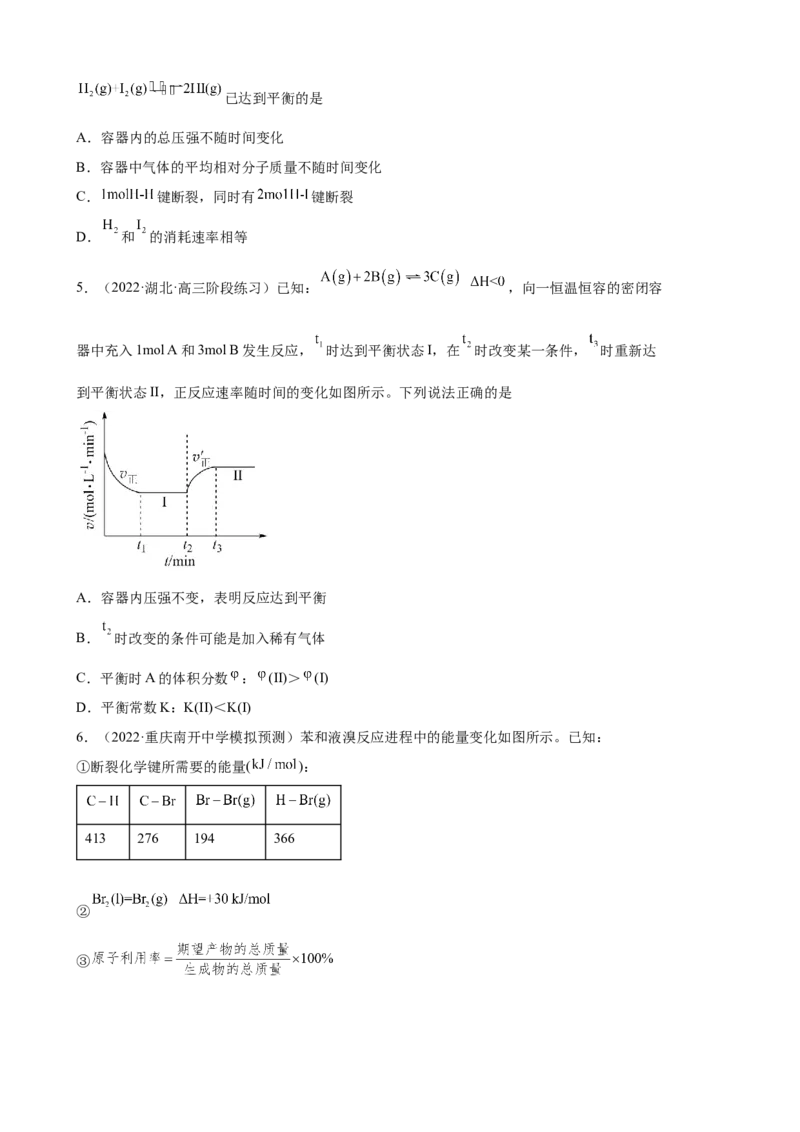
5.(2022·湖北·高三阶段练习)已知: ,向一恒温恒容的密闭容
器中充入1mol A和3mol B发生反应, 时达到平衡状态I,在 时改变某一条件, 时重新达
到平衡状态II,正反应速率随时间的变化如图所示。下列说法正确的是
A.容器内压强不变,表明反应达到平衡
B. 时改变的条件可能是加入稀有气体
C.平衡时A的体积分数 : (II)> (I)
D.平衡常数K:K(II)<K(I)
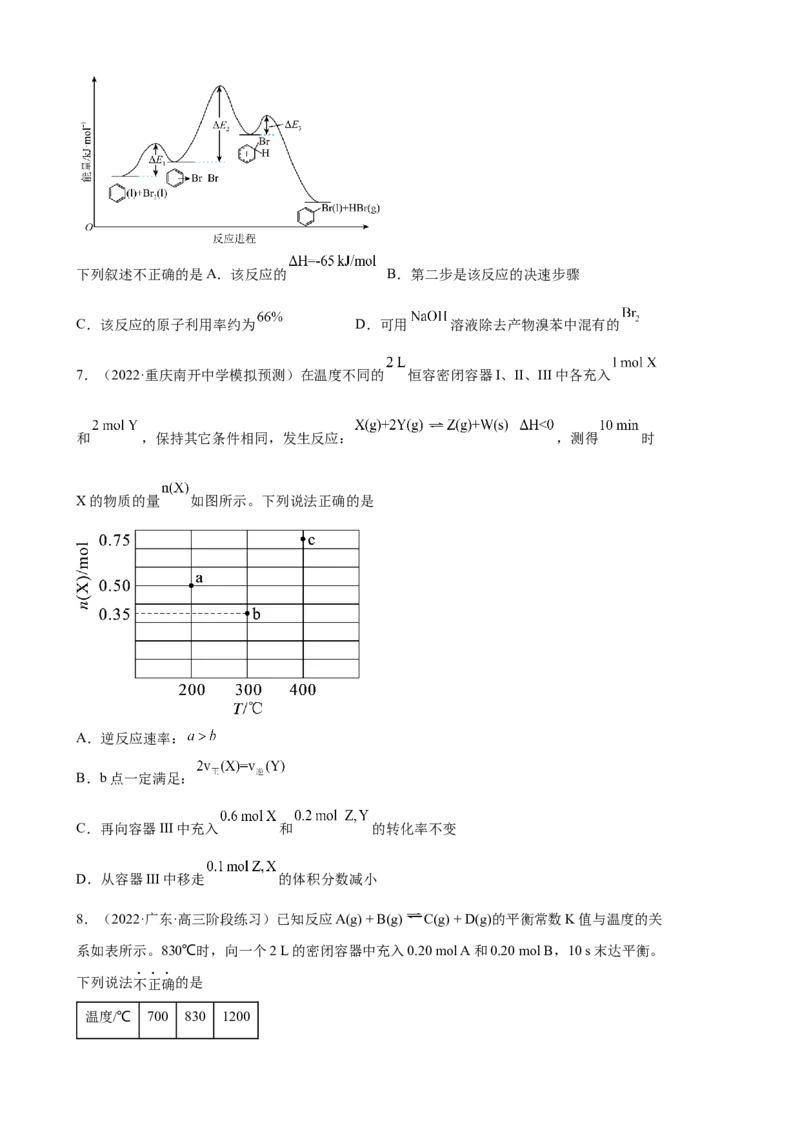
6.(2022·重庆南开中学模拟预测)苯和液溴反应进程中的能量变化如图所示。已知:
①断裂化学键所需要的能量( ):
413 276 194 366
②
③下列叙述不正确的是A.该反应的 B.第二步是该反应的决速步骤
C.该反应的原子利用率约为 D.可用 溶液除去产物溴苯中混有的
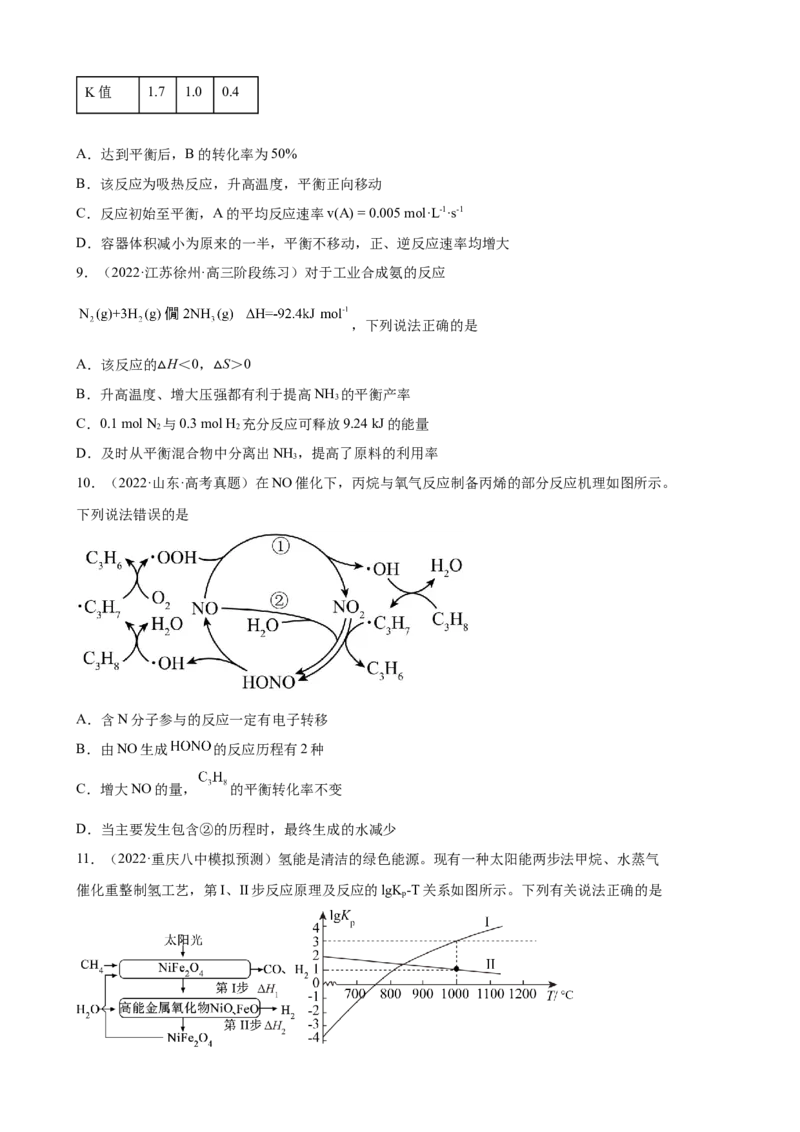
7.(2022·重庆南开中学模拟预测)在温度不同的 恒容密闭容器I、II、III中各充入
和 ,保持其它条件相同,发生反应: ,测得 时
X的物质的量 如图所示。下列说法正确的是
A.逆反应速率:
B.b点一定满足:
C.再向容器III中充入 和 的转化率不变
D.从容器III中移走 的体积分数减小
8.(2022·广东·高三阶段练习)已知反应A(g) + B(g) C(g) + D(g)的平衡常数K值与温度的关
系如表所示。830℃时,向一个2 L的密闭容器中充入0.20 mol A和0.20 mol B,10 s末达平衡。
下列说法不正确的是
温度/℃ 700 830 1200K值 1.7 1.0 0.4
A.达到平衡后,B的转化率为50%
B.该反应为吸热反应,升高温度,平衡正向移动
C.反应初始至平衡,A的平均反应速率v(A) = 0.005 mol·L-1·s-1
D.容器体积减小为原来的一半,平衡不移动,正、逆反应速率均增大
9.(2022·江苏徐州·高三阶段练习)对于工业合成氨的反应
,下列说法正确的是
A.该反应的 H<0, S>0
B.升高温度、△增大压△强都有利于提高NH
3
的平衡产率
C.0.1 mol N 与0.3 mol H 充分反应可释放9.24 kJ的能量
2 2
D.及时从平衡混合物中分离出NH ,提高了原料的利用率
3
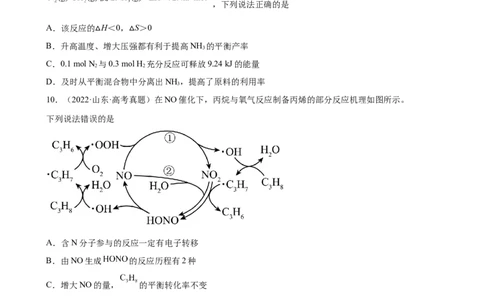
10.(2022·山东·高考真题)在NO催化下,丙烷与氧气反应制备丙烯的部分反应机理如图所示。
下列说法错误的是
A.含N分子参与的反应一定有电子转移
B.由NO生成 的反应历程有2种
C.增大NO的量, 的平衡转化率不变
D.当主要发生包含②的历程时,最终生成的水减少
11.(2022·重庆八中模拟预测)氢能是清洁的绿色能源。现有一种太阳能两步法甲烷、水蒸气
催化重整制氢工艺,第I、II步反应原理及反应的lgK -T关系如图所示。下列有关说法正确的是
pA.CH(g)+HO(g) CO(g)+3H(g) H<0
4 2 2
B.NiFe
2
O
4
改变反⇌应历程,降低了反△应活化能,提升了反应物的平衡转化率
C.1000℃时,反应CH(g)+HO(g) CO(g)+3H(g)平衡常数K=4
4 2 2 p
D.某温度下,向反应体系中通入等⇌体积的CH
4
(g)和H
2
O(g),达到平衡时CH
4
的转化率为
60%、则此时混合气体中H 的体积分数为56.25%
2
12.(2022·重庆八中模拟预测)采用BASF高压法钴碘催化制备醋酸循环过程如图所示。下列
说法错误的是
A.HCo(CO) 为该反应的催化剂
4
B.步骤②中只有极性键的断裂和形成
C.HO、CHI均为该反应的中间产物
2 3
D.总反应方程式为CHOH+CO CHCOOH
3 3
13.(2022·北京·北师大实验中学三模)在一定条件下,利用CO 合成CHOH的反应如下:
2 3
CO(g) + 3H(g) CHOH(g) + H O(g) △H,研究发现,反应过程中会有副反应:CO(g) +
2 2 3 2 1 2
H(g) CO(g)+ H O(g) △H,温度对CHOH、CO的平衡产率影响如图所示。下列说法中,
2 2 2 3
不正确的是A.△H<0,△H>0
1 2
B.增大压强有利于加快合成反应的速率
C.实际生产过程中,升高温度一定降低CHOH的产率
3
D.实际生产过程中,可以通过使用合适的催化剂提高CHOH的选择性
3
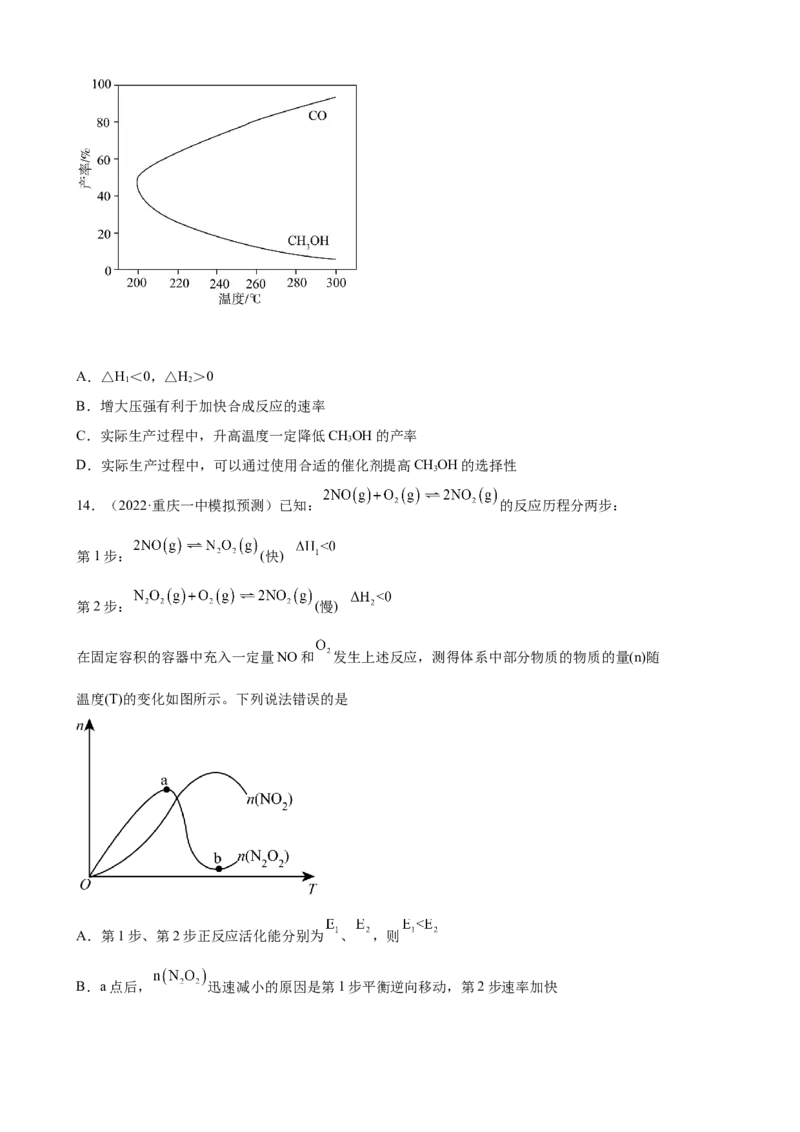
14.(2022·重庆一中模拟预测)已知: 的反应历程分两步:
第1步: (快)
第2步: (慢)
在固定容积的容器中充入一定量NO和 发生上述反应,测得体系中部分物质的物质的量(n)随
温度(T)的变化如图所示。下列说法错误的是
A.第1步、第2步正反应活化能分别为 、 ,则
B.a点后, 迅速减小的原因是第1步平衡逆向移动,第2步速率加快C.b点后, 增加的原因是第2步平衡逆向移动的程度比第1步的大
D.若其他条件不变,仅将容器变为恒压状态,则体系建立平衡的时间不变
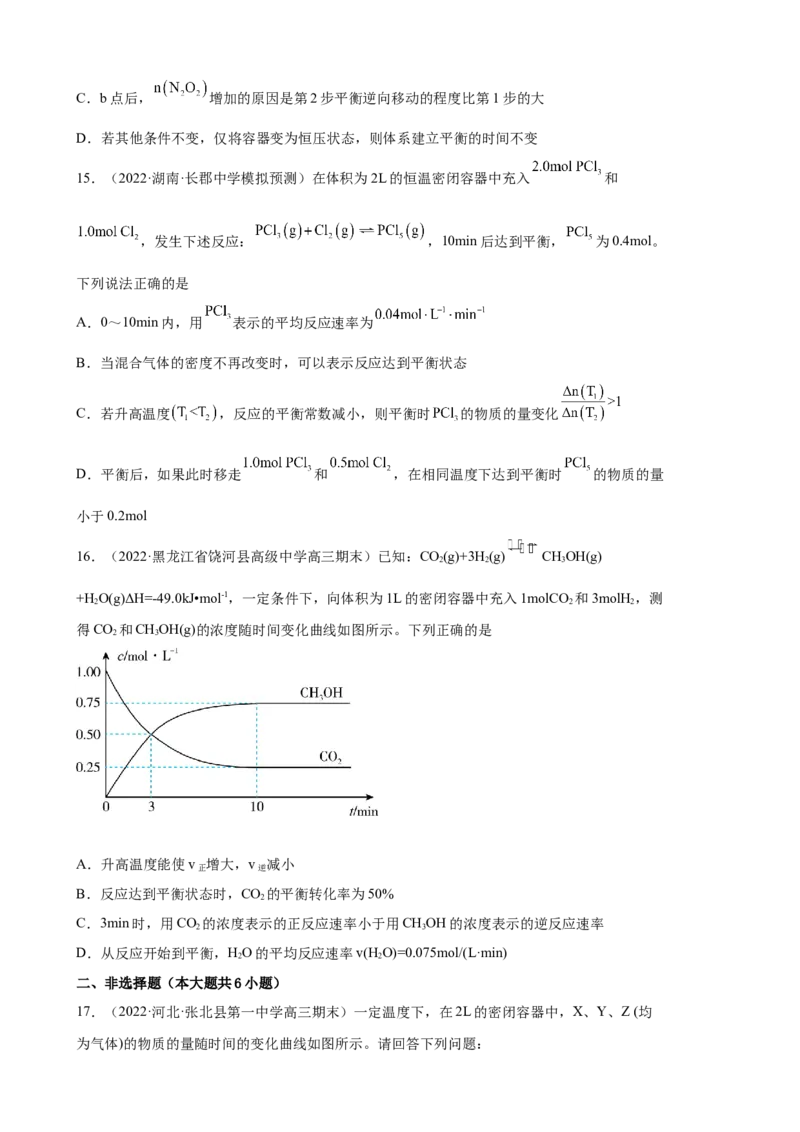
15.(2022·湖南·长郡中学模拟预测)在体积为2L的恒温密闭容器中充入 和
,发生下述反应: ,10min后达到平衡, 为0.4mol。
下列说法正确的是
A.0~10min内,用 表示的平均反应速率为
B.当混合气体的密度不再改变时,可以表示反应达到平衡状态
C.若升高温度 ,反应的平衡常数减小,则平衡时 的物质的量变化
D.平衡后,如果此时移走 和 ,在相同温度下达到平衡时 的物质的量
小于0.2mol
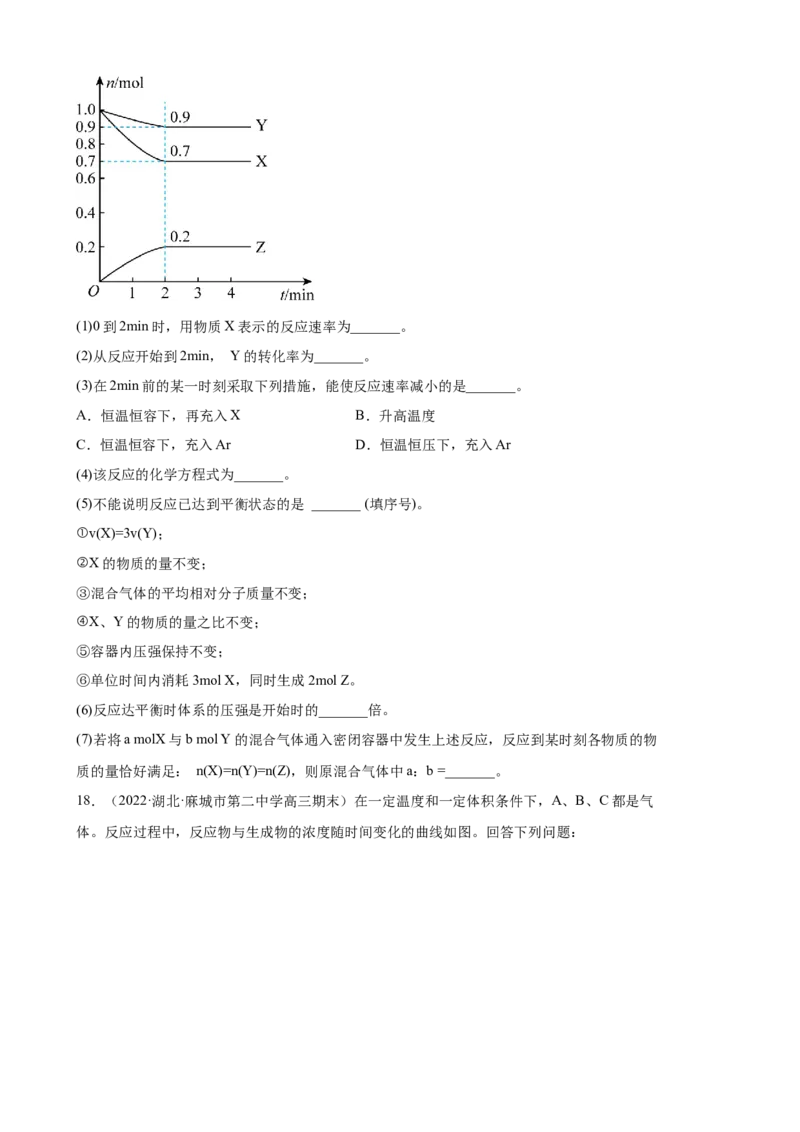
16.(2022·黑龙江省饶河县高级中学高三期末)已知:CO(g)+3H(g) CHOH(g)
2 2 3
+H O(g)ΔH=-49.0kJ•mol-1,一定条件下,向体积为1L的密闭容器中充入1molCO 和3molH ,测
2 2 2
得CO 和CHOH(g)的浓度随时间变化曲线如图所示。下列正确的是
2 3
A.升高温度能使v 增大,v 减小
正 逆
B.反应达到平衡状态时,CO 的平衡转化率为50%
2
C.3min时,用CO 的浓度表示的正反应速率小于用CHOH的浓度表示的逆反应速率
2 3
D.从反应开始到平衡,HO的平均反应速率v(H O)=0.075mol/(L·min)
2 2
二、非选择题(本大题共6小题)
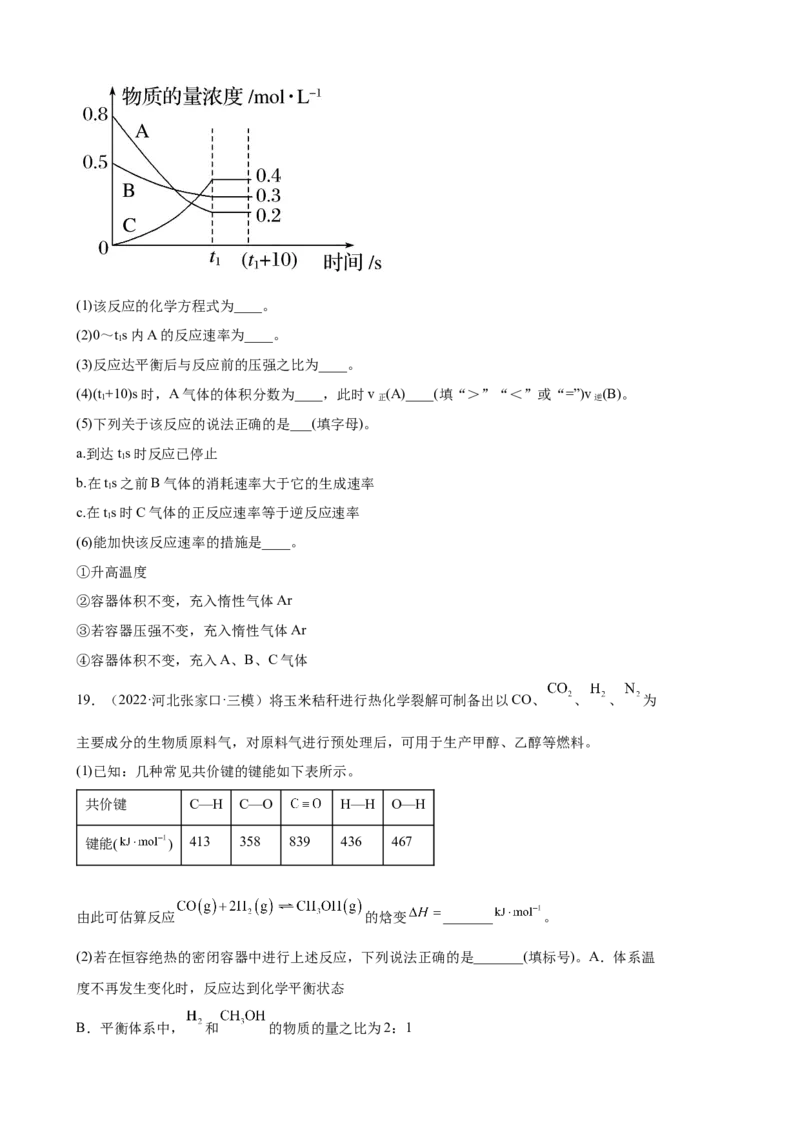
17.(2022·河北·张北县第一中学高三期末)一定温度下,在2L的密闭容器中,X、Y、Z (均
为气体)的物质的量随时间的变化曲线如图所示。请回答下列问题:(1)0到2min时,用物质X表示的反应速率为_______。
(2)从反应开始到2min, Y的转化率为_______。
(3)在2min前的某一时刻采取下列措施,能使反应速率减小的是_______。
A.恒温恒容下,再充入X B.升高温度
C.恒温恒容下,充入Ar D.恒温恒压下,充入Ar
(4)该反应的化学方程式为_______。
(5)不能说明反应已达到平衡状态的是 _______ (填序号)。
①v(X)=3v(Y);
②X的物质的量不变;
③混合气体的平均相对分子质量不变;
④X、Y的物质的量之比不变;
⑤容器内压强保持不变;
⑥单位时间内消耗3mol X,同时生成2mol Z。
(6)反应达平衡时体系的压强是开始时的_______倍。
(7)若将a molX与b mol Y的混合气体通入密闭容器中发生上述反应,反应到某时刻各物质的物
质的量恰好满足: n(X)=n(Y)=n(Z),则原混合气体中a:b =_______。
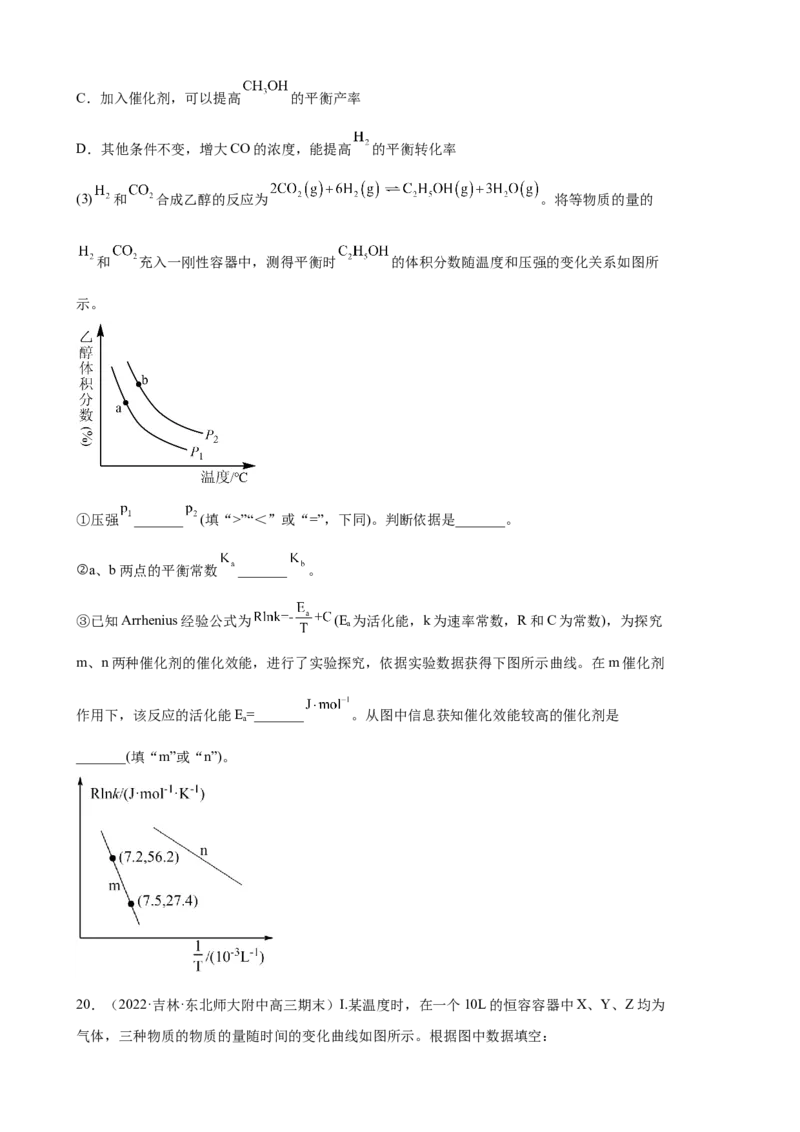
18.(2022·湖北·麻城市第二中学高三期末)在一定温度和一定体积条件下,A、B、C都是气
体。反应过程中,反应物与生成物的浓度随时间变化的曲线如图。回答下列问题:(1)该反应的化学方程式为____。
(2)0~ts内A的反应速率为____。
1
(3)反应达平衡后与反应前的压强之比为____。
(4)(t +10)s时,A气体的体积分数为____,此时v (A)____(填“>”“<”或“=”)v (B)。
1 正 逆
(5)下列关于该反应的说法正确的是___(填字母)。
a.到达ts时反应已停止
1
b.在ts之前B气体的消耗速率大于它的生成速率
1
c.在ts时C气体的正反应速率等于逆反应速率
1
(6)能加快该反应速率的措施是____。
①升高温度
②容器体积不变,充入惰性气体Ar
③若容器压强不变,充入惰性气体Ar
④容器体积不变,充入A、B、C气体
19.(2022·河北张家口·三模)将玉米秸秆进行热化学裂解可制备出以CO、 、 、 为
主要成分的生物质原料气,对原料气进行预处理后,可用于生产甲醇、乙醇等燃料。
(1)已知:几种常见共价键的键能如下表所示。
共价键 C—H C—O H—H O—H
键能( ) 413 358 839 436 467
由此可估算反应 的焓变 _______ 。
(2)若在恒容绝热的密闭容器中进行上述反应,下列说法正确的是_______(填标号)。A.体系温
度不再发生变化时,反应达到化学平衡状态
B.平衡体系中, 和 的物质的量之比为2:1C.加入催化剂,可以提高 的平衡产率
D.其他条件不变,增大CO的浓度,能提高 的平衡转化率
(3) 和 合成乙醇的反应为 。将等物质的量的
和 充入一刚性容器中,测得平衡时 的体积分数随温度和压强的变化关系如图所
示。
①压强 _______ (填“>”“<”或“=”,下同)。判断依据是_______。
②a、b两点的平衡常数 _______ 。
③已知Arrhenius经验公式为 (E 为活化能,k为速率常数,R和C为常数),为探究
a
m、n两种催化剂的催化效能,进行了实验探究,依据实验数据获得下图所示曲线。在m催化剂
作用下,该反应的活化能E=_______ 。从图中信息获知催化效能较高的催化剂是
a
_______(填“m”或“n”)。
20.(2022·吉林·东北师大附中高三期末)I.某温度时,在一个10L的恒容容器中X、Y、Z均为
气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:(1)该反应的化学方程式为_______;
(2)反应开始至2min,以气体X表示的平均反应速率为_______;
(3)平衡时混合气体的平均相对分子质量M_______(填“大于”,“小于”或“等于”下同)起始
2
时的平均相对分子质量M;
1
(4)将amolX与bmolY的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:
,则气体X和气体Y的转化率之比为_______。
II.已知硫代硫酸钠溶液与稀硫酸反应的化学方程式为
,某学习小组探究一定条件下影响化学反应速率
的因素,如下表所示:
(5)对比实验I、III的目的为:_______。若实验III、IV为证明浓度对速率的影响,则
X=_______,Y=_______。
溶液 稀
实验序号 温度
I 25 5 0.1 10 0.1 5
II 25 5 0.2 5 0.2 10
III 35 5 0.1 10 0.1 5
IV 35 5 0.2 X 0.2 Y
21.(2022·黑龙江·高三期末)回答下列问题:
(1)I.如表是该小组研究影响过氧化氢HO 分解速率的因素时采集的一组数据:用10mLH O 制取
2 2 2 2
150mLO 所需的时间(秒)。
230%H O 15%H O 10%H O 5%H O
2 2 2 2 2 2 2 2
无催化剂、不加热 几乎不反应 几乎不反应 几乎不反应 几乎不反应
无催化剂、加热 360s 480s 540s 720s
MnO 催化剂、加热 10s 25s 60s 120s
2
该研究小组在设计方案时。考虑了浓度、____、____等因素对过氧化氢分解速率的影响。
(2)II.100mL1mol·L-1稀硫酸与过量锌粒反应,一定温度下,为了减缓反应速率,又不影响生成氢
气的总量,可采取的措施是____。
A.加入少量碳酸钠粉末 B.加入少量硫酸铜溶液 C.加入适量NaSO 溶液 D.加
2 4
热 E.加水
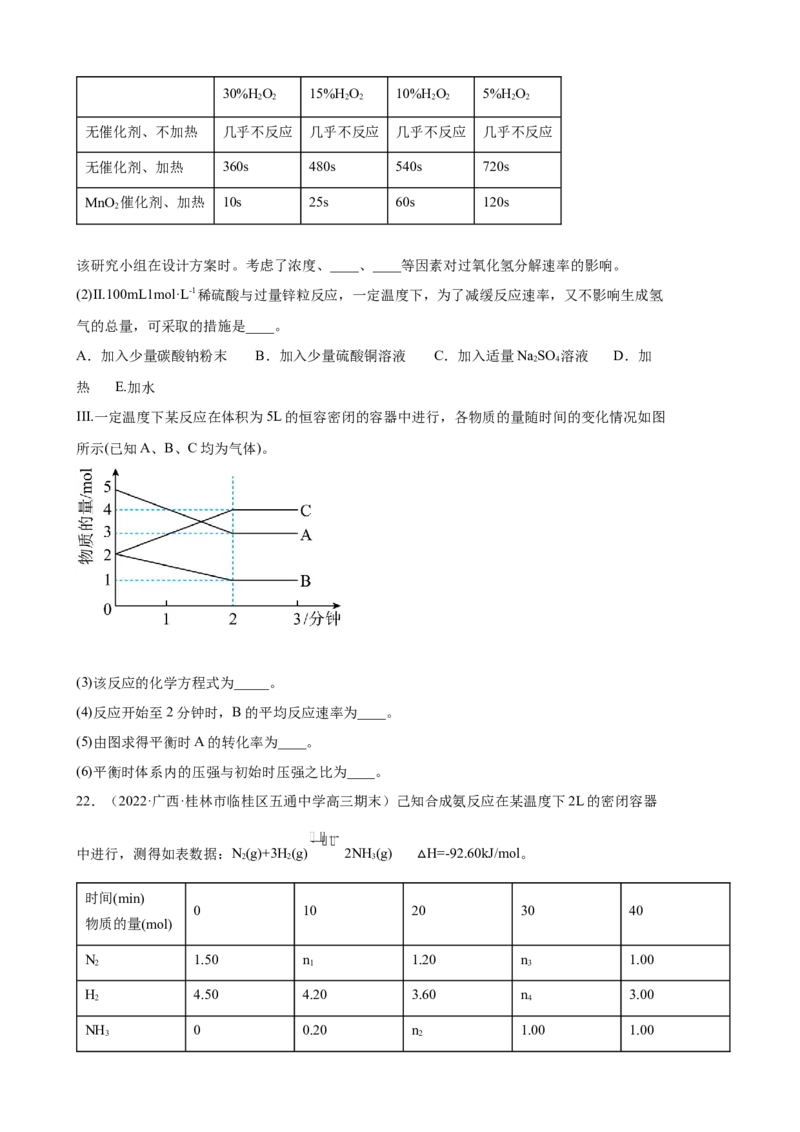
III.一定温度下某反应在体积为5L的恒容密闭的容器中进行,各物质的量随时间的变化情况如图
所示(已知A、B、C均为气体)。
(3)该反应的化学方程式为_____。
(4)反应开始至2分钟时,B的平均反应速率为____。
(5)由图求得平衡时A的转化率为____。
(6)平衡时体系内的压强与初始时压强之比为____。
22.(2022·广西·桂林市临桂区五通中学高三期末)己知合成氨反应在某温度下2L的密闭容器
中进行,测得如表数据:N(g)+3H(g) 2NH (g) H=-92.60kJ/mol。
2 2 3
△
时间(min)
0 10 20 30 40
物质的量(mol)
N 1.50 n 1.20 n 1.00
2 1 3
H 4.50 4.20 3.60 n 3.00
2 4
NH 0 0.20 n 1.00 1.00
3 2根据表中数据回答:
(1)反应进行到20min时放出的热量为____kJ。
(2)0-10min内的平均反应速率v(N )为____mol/(L·min)。
2
(3)此温度下该逆反应的化学平衡常数K(逆)=____(保留两位小数) 。
(4)反应达到平衡后,若往平衡体系中再加入N、H 和NH 各1.00mol,化学平衡将____(填“正
2 2 3
向移动”或“逆向移动”或“不移动”)。参考答案:
1.D
2.C
3.C
4.C
5.C
6.A
7.C
8.B
9.D
10.D
11.D
12.B
13.C
14.D
15.CD
16.D
17.(1)0.075 mol/(L·min)
(2)10%
(3)D
(4)3X(g)+Y(g) 2Z(g)
(5)① ⑥
(6)0.9
(7)5:3
18.(1)3A+B 2C
(2) mol·L-1·s-1
(3)9∶13
(4) 22.2% >
(5)bc
(6)①④19.(1)-353
(2)AD
(3) < 该反应为气体分子数减小的反应,温度相同时,压强越大,平衡体系中
乙醇的体积分数越大 > n
20.(1)3X+Y 2Z
(2)0.015 mol/(L•min)
(3)大于
(4)
(5) 探究温度对反应速率的影响 5 10
21.(1) 温度 催化剂
(2)CE
(3)2A(g)+B(g) 2C(g)
(4)0.1mol·L-1·min-1
(5)40%
(6)8:9
22.(1)27.78
(2)0.005
(3)6.75
(4)正向移动