文档内容
热点强化 18 水解常数(K )与电离常数的关系及应用
h
1.水解常数的概念
(1)含义:盐类水解的平衡常数,称为水解常数,用K 表示。
h
(2)表达式:
①对于A-+HOHA+OH-,K =________________________;
2 h
②对于B++HOBOH+H+,K =________________________。
2 h
(3)意义和影响因素
①K 越大,表示相应盐的水解程度________;
h
②K 只受温度的影响,升高温度,K ___________________________________________。
h h
答案 (2)① ②
(3)①越大 ②增大
2.水解常数(K )与电离常数的定量关系(以CHCOONa为例)
h 3
CHCOONa溶液中存在如下水解平衡:
3
CHCOO-+HOCHCOOH+OH-
3 2 3
K =
h
=
==
因而K(或K )与K 的定量关系:
a h w
(1)K·K =K 或K ·K =K
a h w b h w
(2)Na CO 的水解常数K =
2 3 h
(3)NaHCO 的水解常数K =
3 h
拓展 可以用电离平衡常数与水解常数的大小关系判断弱酸的酸式盐溶液的酸碱性,以
HCO为例,已知K =:
a1
电离方程式:HCOH++CO
K =
a2
水解方程式:HCO+HOHCO+OH-
2 2 3
K ==,只需比较K 和K =的大小即可判断弱酸的酸式盐溶液的酸碱性。
h a2 h
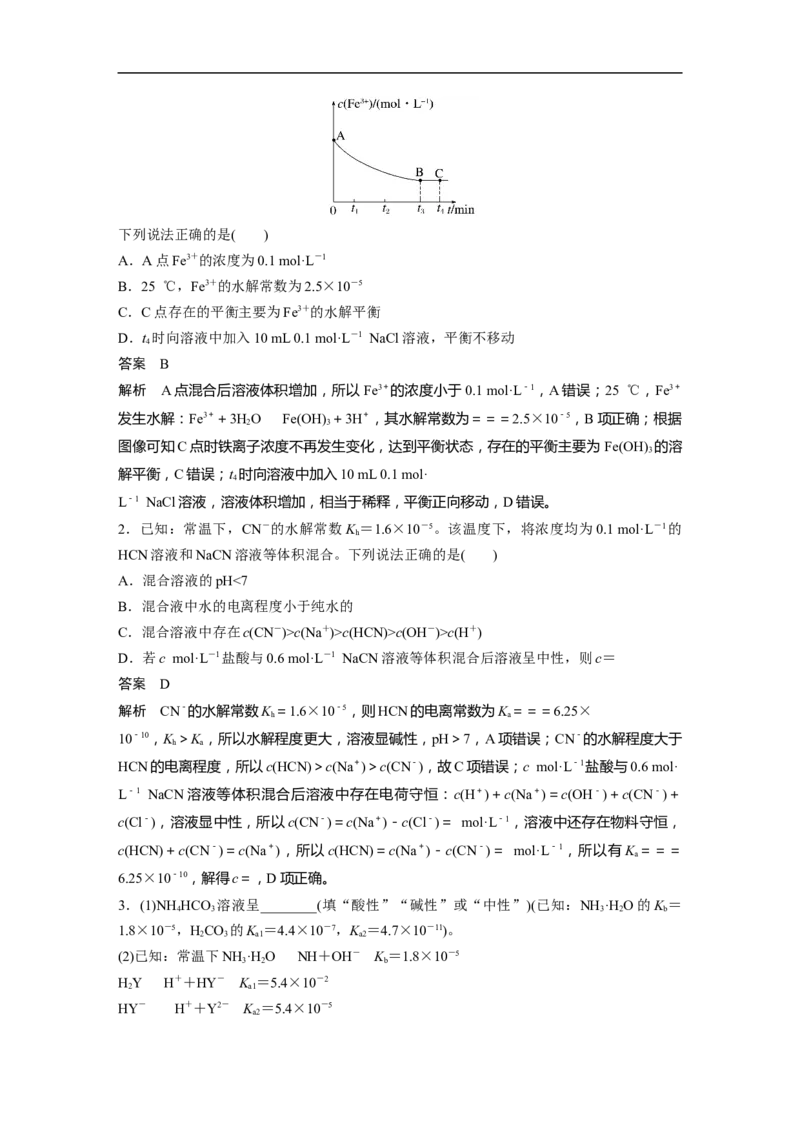
1.(2022·高州长坡中学模拟)25 ℃,K [Fe(OH) ]=4.0×10-38,向 10 mL 0.1 mol·L-1的
sp 3
FeCl 溶液中加入30 mL 0.1 mol·L-1的NaOH溶液发生反应,混合溶液中c(Fe3+)与时间(t)的
3
变化如图所示。下列说法正确的是( )
A.A点Fe3+的浓度为0.1 mol·L-1
B.25 ℃,Fe3+的水解常数为2.5×10-5
C.C点存在的平衡主要为Fe3+的水解平衡
D.t 时向溶液中加入10 mL 0.1 mol·L-1 NaCl溶液,平衡不移动
4
答案 B
解析 A点混合后溶液体积增加,所以Fe3+的浓度小于0.1 mol·L-1,A错误;25 ℃,Fe3+
发生水解:Fe3++3HOFe(OH) +3H+,其水解常数为===2.5×10-5,B项正确;根据
2 3
图像可知C点时铁离子浓度不再发生变化,达到平衡状态,存在的平衡主要为Fe(OH) 的溶
3
解平衡,C错误;t 时向溶液中加入10 mL 0.1 mol·
4
L-1 NaCl溶液,溶液体积增加,相当于稀释,平衡正向移动,D错误。
2.已知:常温下,CN-的水解常数K =1.6×10-5。该温度下,将浓度均为0.1 mol·L-1的
h
HCN溶液和NaCN溶液等体积混合。下列说法正确的是( )
A.混合溶液的pH<7
B.混合液中水的电离程度小于纯水的
C.混合溶液中存在c(CN-)>c(Na+)>c(HCN)>c(OH-)>c(H+)
D.若c mol·L-1盐酸与0.6 mol·L-1 NaCN溶液等体积混合后溶液呈中性,则c=
答案 D
解析 CN-的水解常数K =1.6×10-5,则HCN的电离常数为K===6.25×
h a
10-10,K >K,所以水解程度更大,溶液显碱性,pH>7,A项错误;CN-的水解程度大于
h a
HCN的电离程度,所以c(HCN)>c(Na+)>c(CN-),故C项错误;c mol·L-1盐酸与0.6 mol·
L-1 NaCN溶液等体积混合后溶液中存在电荷守恒:c(H+)+c(Na+)=c(OH-)+c(CN-)+
c(Cl-),溶液显中性,所以c(CN-)=c(Na+)-c(Cl-)= mol·L-1,溶液中还存在物料守恒,
c(HCN)+c(CN-)=c(Na+),所以c(HCN)=c(Na+)-c(CN-)= mol·L-1,所以有K ===
a
6.25×10-10,解得c=,D项正确。
3.(1)NH HCO 溶液呈________(填“酸性”“碱性”或“中性”)(已知:NH ·H O的K =
4 3 3 2 b
1.8×10-5,HCO 的K =4.4×10-7,K =4.7×10-11)。
2 3 a1 a2
(2)已知:常温下NH ·H ONH+OH- K =1.8×10-5
3 2 b
HYH++HY- K =5.4×10-2
2 a1
HY-H++Y2- K =5.4×10-5
a2则(NH )Y溶液的pH________7(填“>”“<”或“=”)。
4 2
(3)NO 尾气常用NaOH溶液吸收,生成NaNO 和NaNO 。已知NO的水解常数K =2×
2 3 2 h
10-11,常温下,某NaNO 和HNO 混合溶液的pH为5,则混合溶液中c(NO)和c(HNO)的比
2 2 2
值为__________________。
答案 (1)碱性 (2)< (3)50
解析 (1)NH水解溶液显酸性,其水解常数为K (NH)==≈5.6×10-10,HCO水解溶液显碱
h
性,其水解常数为K (HCO)==≈2.3×10-8,所以HCO的水解程度大于NH的水解程度,
h
溶液显碱性。
(2)K (NH)==≈5.6×10-10,K (Y2-)==≈1.9×10-10,水解程度:NH>Y2-,则(NH )Y溶
h h 4 2
液呈酸性,溶液的pH<7。
(3)常温下,某NaNO 和HNO 混合溶液的pH为5,该溶液中c(OH-)= mol·L-1=
2 2
10-9 mol·L-1,结合K (NO)=,可知c(NO)∶c(HNO)=c(OH-)∶K (NO)=10-9∶(2×10-11)
h 2 h
=50。
4.(2022·安徽桐城中学模拟)(1)已知某温度时,K =1.0×10-12,NaCO 溶液的水解常数K
w 2 3 h
=2.0×10-3,则当溶液中c(HCO)∶c(CO)=2∶1时,试求该溶液的pH=__________。
(2)已知25 ℃时,NH ·H O的电离常数K =1.8×10-5,该温度下1 mol·L-1的NH Cl溶液中
3 2 b 4
c(H+)=________ mol·L-1(已知:≈2.36)。
(3)25 ℃时,HSO HSO+H+的电离常数K=1×10-2,则该温度下NaHSO 水解反应的
2 3 a 3
平衡常数 K =________________,若向 NaHSO 溶液中加入少量的 I ,则溶液中将
h 3 2
________(填“增大”“减小”或“不变”)。
答案 (1)9 (2)2.36×10-5 (3)1×10-12 增大
解 析 (1)K = = 2.0×10 - 3 , 又 c(HCO)∶c(CO) = 2∶1 , 则 c(OH - ) =
h
10-3 mol·L-1,结合K =1.0×10-12,可得c(H+)=10-9 mol·L-1。
w
(2)K ==,c(H+)≈c(NH ·H O),而c(NH)≈1 mol·L-1,所以c(H+)≈= mol·L-1≈2.36×10
h 3 2
-5 mol·L-1。
(3)25 ℃时,HSO的水解方程式为HSO+HOHSO +OH-,则NaHSO 的水解常数K =
2 2 3 3 h
====1×10-12,当加入少量I 时,发生反应HSO+I +HO===3H++SO+2I-,溶液酸
2 2 2
性增强,c(H+)增大,c(OH-)减小,但是温度不变,K 不变,则=增大。
h
5.磷酸是三元弱酸,常温下三步电离常数分别是 K =7.1×10-3,K =6.2×10-8,K =
a1 a2 a3
4.5×
10-13,解答下列问题:
(1)常温下同浓度① NaPO 、② NaHPO 、③ NaH PO 的 pH 由小到大的顺序是
3 4 2 4 2 4
______________(填序号)。
(2)常温下,NaH PO 的水溶液pH________(填“>”“<”或“=”)7。
2 4
(3)常温下,NaHPO 的水溶液呈________(填“酸”“碱”或“中”)性,用K 与K 的相对
2 4 a h大小,说明判断理由:_______________________________________________________。
答案 (1)③<②<① (2)< (3)碱 NaHPO 的水解常数K ===≈1.61×10-7,K >
2 4 h h
K ,即HPO的水解程度大于其电离程度,因而NaHPO 溶液显碱性
a3 2 4
解析 (2)NaH PO 的水解常数
2 4
K ===
h
≈1.4×10-12,K >K ,即HPO的电离程度大于其水解程度,因而pH<7。
a2 h 2
比较酸式盐电离与水解的大小:
酸式盐电离常数大于10-7,电离大于水解,盐溶液呈酸性;
酸式盐电离常数小于10-7,水解大于电离,盐溶液呈碱性。
酸碱性 举例 解释
pH>7 NaHCO 、KHS、NaHPO 水解大于电离
3 2 4
pH<7 NaHSO、KHC O、NaH PO 电离大于水解
3 2 4 2 4