文档内容
第 52 讲 无机化工流程题的解题策略
复习目标 1.培养从试题提供的新信息中准确地提取实质性内容,并与已有知识块整合重
组为新知识块的能力。2.培养将实际问题分解,通过运用相关知识,采用分析、综合的方法,
解决简单化学问题的能力。3.培养将分析和解决问题的过程及成果用正确的化学术语及文字、
图表、模型、图形等表达并做出解释的能力。
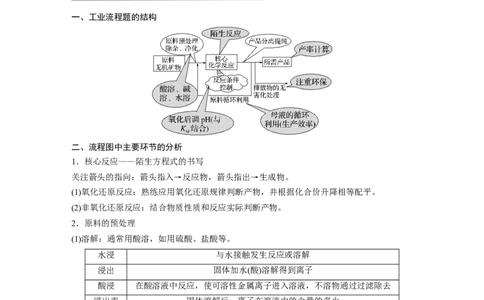
一、工业流程题的结构
二、流程图中主要环节的分析
1.核心反应——陌生方程式的书写
关注箭头的指向:箭头指入→反应物,箭头指出→生成物。
(1)氧化还原反应:熟练应用氧化还原规律判断产物,并根据化合价升降相等配平。
(2)非氧化还原反应:结合物质性质和反应实际判断产物。
2.原料的预处理
(1)溶解:通常用酸溶,如用硫酸、盐酸等。
水浸 与水接触发生反应或溶解
浸出 固体加水(酸)溶解得到离子
酸浸 在酸溶液中反应,使可溶性金属离子进入溶液,不溶物通过过滤除去
浸出率 固体溶解后,离子在溶液中的含量的多少
(2)灼烧、焙烧、煅烧:改变结构,使一些物质能溶解,并使一些杂质在高温下氧化、分解。
(3)审题时要“瞻前顾后”,注意物质性质及反应原理的前后联系。
3.常用的控制反应条件的方法
(1)调节溶液的pH。常用于使某些金属离子形成氢氧化物沉淀。调节 pH所需的物质一般应
满足两点:
①能与H+反应,使溶液pH增大;
②不引入新杂质。例如:若要除去Cu2+中混有的Fe3+,可加入CuO、CuCO 、Cu(OH) 、Cu (OH) CO 等物质
3 2 2 2 3
来调节溶液的pH,不可加入NaOH溶液、氨水等。
(2)控制温度。根据需要升温或降温,改变反应速率或使平衡向需要的方向移动。
(3)趁热过滤。防止某物质降温时析出。
(4)冰水洗涤。洗去晶体表面的杂质离子,并减少晶体在洗涤过程中的溶解损耗。
4.常用的提纯方法
(1)水溶法:除去可溶性杂质。
(2)酸溶法:除去碱性杂质。
(3)碱溶法:除去酸性杂质。
(4)氧化剂或还原剂法:除去还原性或氧化性杂质。
(5)加热灼烧法:除去受热易分解或易挥发的杂质。
(6)调节溶液的pH法:如除去酸性溶液中的Fe3+等。
5.常用的分离方法
(1)过滤:分离难溶物和易溶物,根据特殊需要采用趁热过滤或者抽滤等方法。
(2)萃取和分液:利用溶质在互不相溶的溶剂里的溶解度不同提取分离物质,如用 CCl 或苯
4
萃取溴水中的溴。
(3)蒸发结晶:提取溶解度随温度变化不大的溶质,如从溶液中提取NaCl。
(4)冷却结晶:提取溶解度随温度变化较大的溶质、易水解的溶质或结晶水合物,如KNO 、
3
FeCl 、CuCl 、CuSO ·5H O、FeSO ·7H O等。
3 2 4 2 4 2
(5)蒸馏或分馏:分离沸点不同且互溶的液体混合物,如分离乙醇和甘油。
(6)冷却法:利用气体液化的特点分离气体,如合成氨工业采用冷却法分离平衡混合气体中
的氨气。
类型一 物质制备类化工流程题
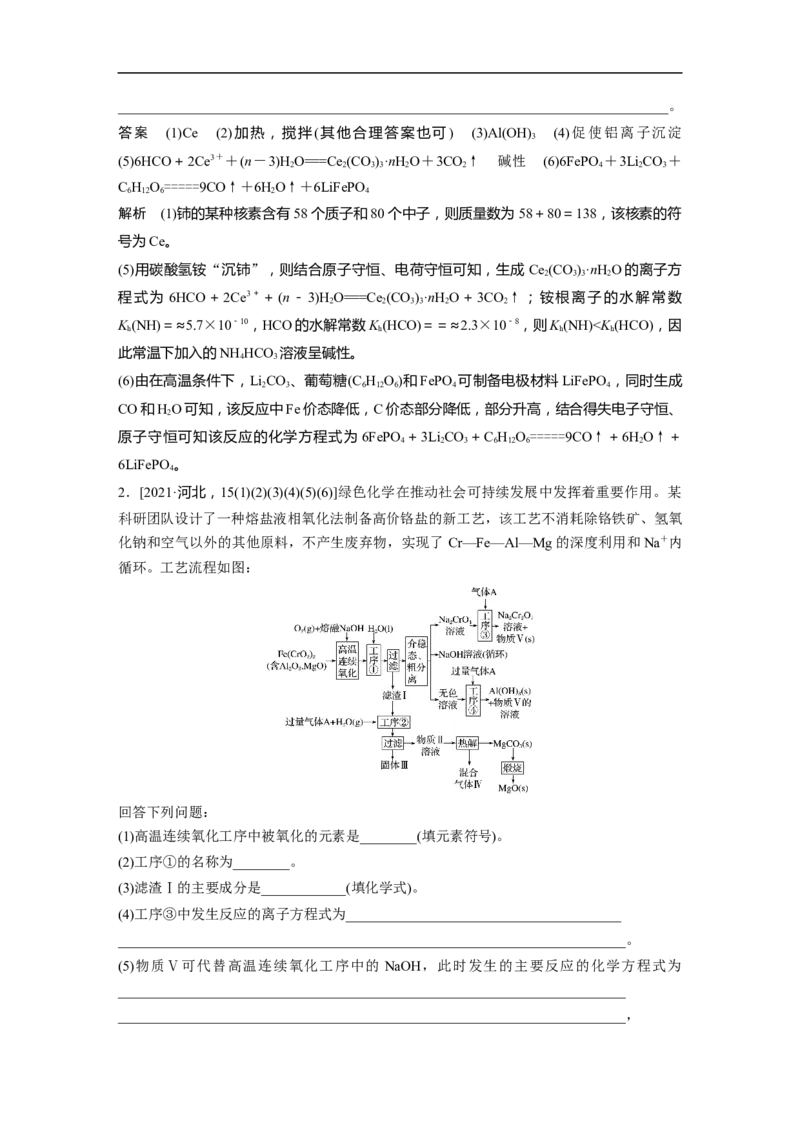
1.[2021·山东,17(1)(2)(3)]工业上以铬铁矿(FeCrO ,含Al、Si氧化物等杂质)为主要原料
2 4
制备红矾钠(Na Cr O·2H O)的工艺流程如图。回答下列问题:
2 2 7 2
(1)焙烧的目的是将FeCr O 转化为NaCrO 并将Al、Si氧化物转化为可溶性钠盐,焙烧时气
2 4 2 4
体与矿料逆流而行,目的是______________________。
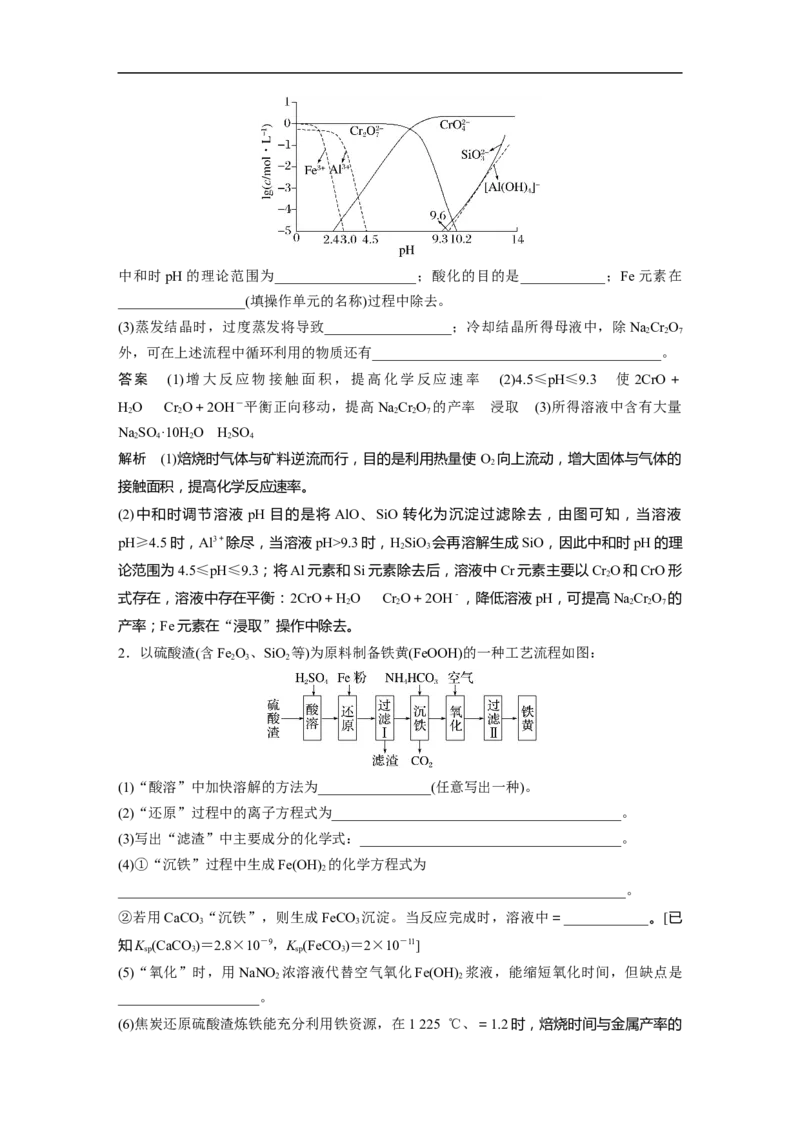
(2)矿物中相关元素可溶性组分物质的量浓度c与pH的关系如图所示。当溶液中可溶性组分
浓度c≤1.0×10-5 mol·L-1时,可认为已除尽。中和时pH的理论范围为____________________;酸化的目的是____________;Fe元素在
__________________(填操作单元的名称)过程中除去。
(3)蒸发结晶时,过度蒸发将导致__________________;冷却结晶所得母液中,除NaCr O
2 2 7
外,可在上述流程中循环利用的物质还有_________________________________________。
答案 (1)增大反应物接触面积,提高化学反应速率 (2)4.5≤pH≤9.3 使 2CrO+
HOCr O+2OH-平衡正向移动,提高NaCr O 的产率 浸取 (3)所得溶液中含有大量
2 2 2 2 7
NaSO ·10H O HSO
2 4 2 2 4
解析 (1)焙烧时气体与矿料逆流而行,目的是利用热量使 O 向上流动,增大固体与气体的
2
接触面积,提高化学反应速率。
(2)中和时调节溶液 pH 目的是将 AlO、SiO 转化为沉淀过滤除去,由图可知,当溶液
pH≥4.5时,Al3+除尽,当溶液pH>9.3时,HSiO 会再溶解生成SiO,因此中和时pH的理
2 3
论范围为4.5≤pH≤9.3;将Al元素和Si元素除去后,溶液中Cr元素主要以Cr O和CrO形
2
式存在,溶液中存在平衡:2CrO+HOCr O+2OH-,降低溶液pH,可提高NaCr O 的
2 2 2 2 7
产率;Fe元素在“浸取”操作中除去。
2.以硫酸渣(含Fe O、SiO 等)为原料制备铁黄(FeOOH)的一种工艺流程如图:
2 3 2
(1)“酸溶”中加快溶解的方法为________________(任意写出一种)。
(2)“还原”过程中的离子方程式为_________________________________________。
(3)写出“滤渣”中主要成分的化学式:_____________________________________。
(4)①“沉铁”过程中生成Fe(OH) 的化学方程式为
2
________________________________________________________________________。
②若用CaCO “沉铁”,则生成FeCO 沉淀。当反应完成时,溶液中=____________。[已
3 3
知K (CaCO)=2.8×10-9,K (FeCO)=2×10-11]
sp 3 sp 3
(5)“氧化”时,用NaNO 浓溶液代替空气氧化Fe(OH) 浆液,能缩短氧化时间,但缺点是
2 2
____________________。
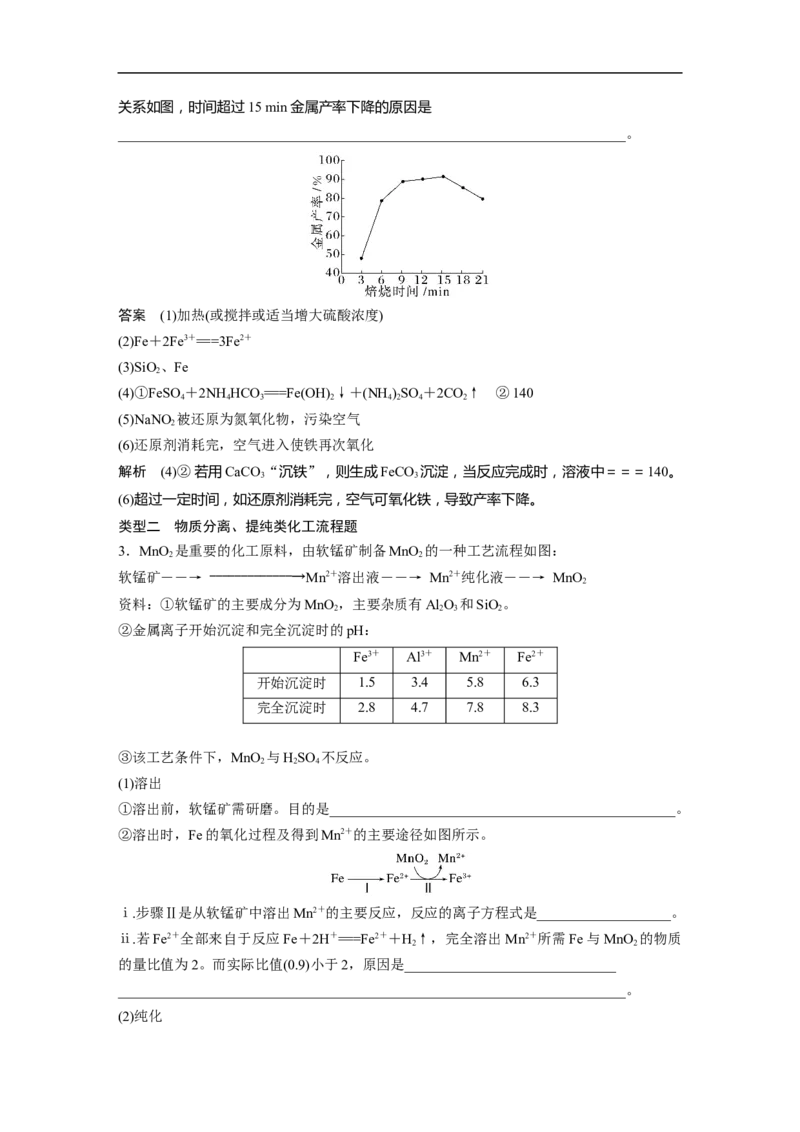
(6)焦炭还原硫酸渣炼铁能充分利用铁资源,在1 225 ℃、=1.2时,焙烧时间与金属产率的关系如图,时间超过15 min金属产率下降的原因是
________________________________________________________________________。
答案 (1)加热(或搅拌或适当增大硫酸浓度)
(2)Fe+2Fe3+===3Fe2+
(3)SiO、Fe
2
(4)①FeSO +2NH HCO ===Fe(OH) ↓+(NH )SO +2CO↑ ②140
4 4 3 2 4 2 4 2
(5)NaNO 被还原为氮氧化物,污染空气
2
(6)还原剂消耗完,空气进入使铁再次氧化
解析 (4)②若用CaCO “沉铁”,则生成FeCO 沉淀,当反应完成时,溶液中===140。
3 3
(6)超过一定时间,如还原剂消耗完,空气可氧化铁,导致产率下降。
类型二 物质分离、提纯类化工流程题
3.MnO 是重要的化工原料,由软锰矿制备MnO 的一种工艺流程如图:
2 2
软锰矿――→ ―――――――――――――→Mn2+溶出液――→ Mn2+纯化液――→ MnO
2
资料:①软锰矿的主要成分为MnO ,主要杂质有Al O 和SiO。
2 2 3 2
②金属离子开始沉淀和完全沉淀时的pH:
Fe3+ Al3+ Mn2+ Fe2+
开始沉淀时 1.5 3.4 5.8 6.3
完全沉淀时 2.8 4.7 7.8 8.3
③该工艺条件下,MnO 与HSO 不反应。
2 2 4
(1)溶出
①溶出前,软锰矿需研磨。目的是_________________________________________________。
②溶出时,Fe的氧化过程及得到Mn2+的主要途径如图所示。
ⅰ.步骤Ⅱ是从软锰矿中溶出Mn2+的主要反应,反应的离子方程式是___________________。
ⅱ.若Fe2+全部来自于反应Fe+2H+===Fe2++H↑,完全溶出Mn2+所需Fe与MnO 的物质
2 2
的量比值为2。而实际比值(0.9)小于2,原因是______________________________
________________________________________________________________________。
(2)纯化已知:MnO 的氧化性与溶液pH有关。纯化时先加入MnO ,后加入NH ·H O,调溶液
2 2 3 2
pH≈5,说明试剂加入顺序及调节pH的原因:______________________________________
________________________________________________________________________。
(3)电解
Mn2+纯化液经电解得MnO 。生成MnO 的电极反应式是_____________________。
2 2
(4)产品纯度测定
向a g产品中依次加入足量b g Na C O 和足量稀HSO ,加热至充分反应,再用c mol·L-1
2 2 4 2 4
KMnO 溶液滴定剩余NaC O 至终点,消耗KMnO 溶液的体积为d L(已知:MnO 及MnO
4 2 2 4 4 2
均被还原为Mn2+。相对分子质量:MnO :86.94、NaC O:134.0)。
2 2 2 4
产品纯度为________(用质量分数表示)。
答案 (1)①增大反应速率,提高浸出率
②ⅰ.MnO +4H++2Fe2+===Mn2++2Fe3++2HO ⅱ.二氧化锰能够氧化单质铁为Fe2+
2 2
(2)MnO 的氧化性随酸性的减弱逐渐减弱;除去溶液中的 Fe3+、Al3+ (3)Mn2+-2e-+
2
2HO===MnO ↓+4H+ (4)×100%
2 2
解析 (1)②i.根据反应途径可知,二氧化锰与亚铁离子反应生成二价锰离子和铁离子,则反
应的离子方程式为MnO +4H++2Fe2+===Mn2++2Fe3++2HO。
2 2
ii.根据反应方程式可知,Fe2+与MnO 的物质的量比值为2,实际反应时,二氧化锰能够氧
2
化单质铁为Fe2+,故实际比值(0.9)小于2。
(2)MnO 的氧化性与溶液pH有关,且随酸性的减弱,氧化性逐渐减弱,溶液显酸性时,二
2
氧化锰的氧化性较强,故纯化时先加入MnO ,后加入NH ·H O,调溶液pH≈5,除去溶液
2 3 2
中的Al3+、Fe3+。
(3)电解时,溶液呈酸性,Mn2+失电子,与水反应生成二氧化锰和氢离子,则电极反应式为
Mn2+-2e-+2HO===MnO ↓+4H+。
2 2
(4)根据题意可知,部分草酸钠与二氧化锰发生氧化还原反应,剩余部分再与高锰酸钾反应:
5NaC O +2KMnO +8HSO ===KSO +2MnSO +10CO↑+8HO+5NaSO ,则与二氧化
2 2 4 4 2 4 2 4 4 2 2 2 4
锰反应的草酸钠的物质的量为-×5;根据反应:MnO +NaC O +2HSO ===NaSO +
2 2 2 4 2 4 2 4
MnSO +2CO↑+2HO,则n(MnO )=n(Na C O),产品纯度为
4 2 2 2 2 2 4
×100%=×100%。
化学工艺流程题的分析方法
主线分析“原料→中间转化物质→目标产物”
(1)反应与物质的转化:分析每一步操作的目的及所发生的化学反应,跟踪物质转化的形式。
尤其要注意原料中的杂质在流程中是如何被除去的。滤渣、滤液成分的确定:反应过程中哪
些物质(离子)发生了变化?产生了哪些新离子?这些离子间是否能发生化学反应?所加试剂是否过量?
(2)循环物质的确定
(3)副产品的判断
1.(2021·湖南,17)Ce (CO) 可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)
2 3 3
主要以CePO 形式存在,还含有SiO 、Al O 、Fe O 、CaF 等物质。以独居石为原料制备
4 2 2 3 2 3 2
Ce (CO)·nHO的工艺流程如下:
2 3 3 2
回答下列问题:
(1)铈的某种核素含有58个质子和80个中子,该核素的符号为____________。
(2)为提高“水浸”效率,可采取的措施有________________________________________(至
少写两条)。
(3)滤渣Ⅲ的主要成分是____________________________________________(填化学式)。
(4)加入絮凝剂的目的是__________________。
(5)“沉铈”过程中,生成Ce (CO)·nHO的离子方程式为____________________________,
2 3 3 2
常温下加入的NH HCO 溶液呈________(填“酸性”“碱性”或“中性”)(已知:NH ·H O
4 3 3 2
的K =1.75×10-5,HCO 的K =4.4×10-7,K =4.7×10-11)。
b 2 3 al a2
(6)滤渣Ⅱ的主要成分为FePO ,在高温条件下,LiCO 、葡萄糖(C H O)和FePO 可制备电
4 2 3 6 12 6 4
极材料LiFePO ,同时生成CO和HO,该反应的化学方程式为______________________
4 2______________________________________________________________________________。
答案 (1)Ce (2)加热,搅拌(其他合理答案也可) (3)Al(OH) (4)促使铝离子沉淀
3
(5)6HCO+2Ce3++(n-3)H O===Ce (CO)·nHO+3CO↑ 碱性 (6)6FePO +3LiCO +
2 2 3 3 2 2 4 2 3
C H O=====9CO↑+6HO↑+6LiFePO
6 12 6 2 4
解析 (1)铈的某种核素含有58个质子和80个中子,则质量数为58+80=138,该核素的符
号为Ce。
(5)用碳酸氢铵“沉铈”,则结合原子守恒、电荷守恒可知,生成 Ce (CO)·nHO的离子方
2 3 3 2
程式为 6HCO+2Ce3++(n-3)H O===Ce (CO)·nHO+3CO↑;铵根离子的水解常数
2 2 3 3 2 2
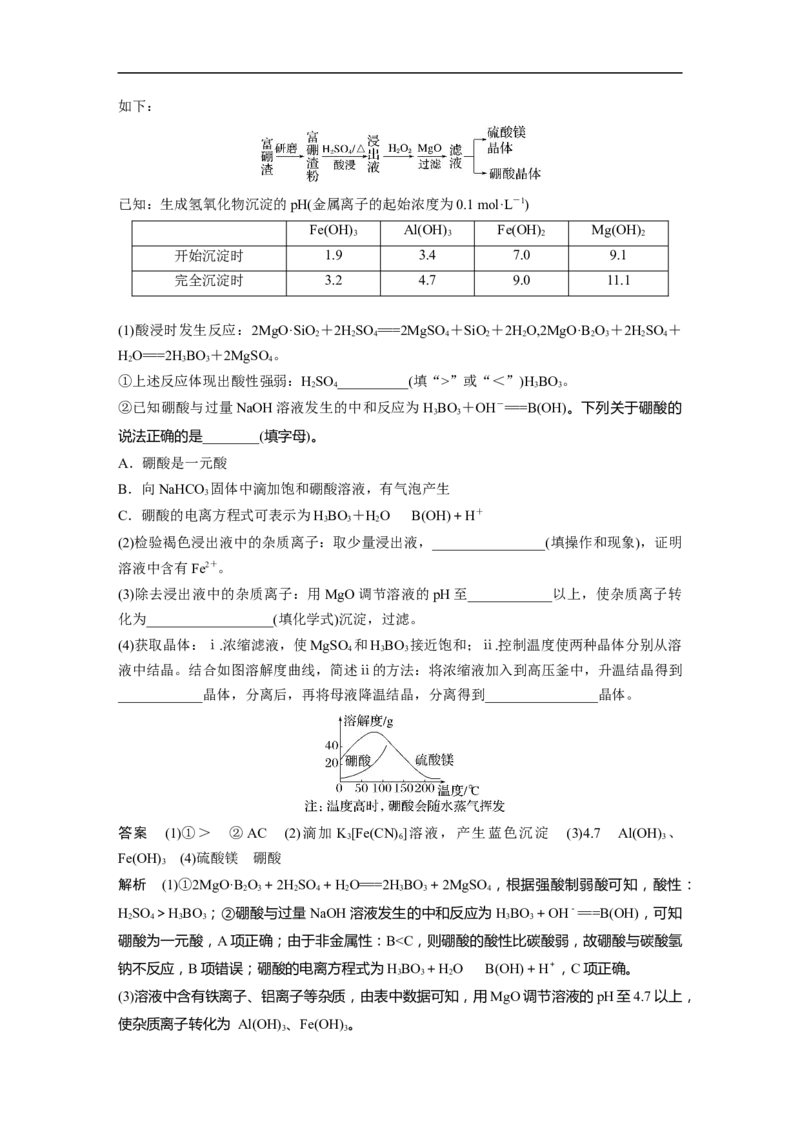
K (NH)=≈5.7×10-10,HCO的水解常数K (HCO)==≈2.3×10-8,则K (NH)”或“<”)H BO。
2 4 3 3
②已知硼酸与过量NaOH溶液发生的中和反应为HBO +OH-===B(OH)。下列关于硼酸的
3 3
说法正确的是________(填字母)。
A.硼酸是一元酸
B.向NaHCO 固体中滴加饱和硼酸溶液,有气泡产生
3
C.硼酸的电离方程式可表示为HBO+HOB(OH)+H+
3 3 2
(2)检验褐色浸出液中的杂质离子:取少量浸出液,________________(填操作和现象),证明
溶液中含有Fe2+。
(3)除去浸出液中的杂质离子:用MgO调节溶液的pH至____________以上,使杂质离子转
化为__________________(填化学式)沉淀,过滤。
(4)获取晶体:ⅰ.浓缩滤液,使MgSO 和HBO 接近饱和;ⅱ.控制温度使两种晶体分别从溶
4 3 3
液中结晶。结合如图溶解度曲线,简述ⅱ的方法:将浓缩液加入到高压釜中,升温结晶得到
____________晶体,分离后,再将母液降温结晶,分离得到________________晶体。
答案 (1)①> ② AC (2)滴加 K[Fe(CN) ]溶液,产生蓝色沉淀 (3)4.7 Al(OH) 、
3 6 3
Fe(OH) (4)硫酸镁 硼酸
3
解析 (1)①2MgO·B O +2HSO +HO===2HBO +2MgSO ,根据强酸制弱酸可知,酸性:
2 3 2 4 2 3 3 4
HSO >HBO ;②硼酸与过量NaOH溶液发生的中和反应为HBO +OH-===B(OH),可知
2 4 3 3 3 3
硼酸为一元酸,A项正确;由于非金属性:B