文档内容
衡水泰华决胜二三高考化学暑假必刷密卷新高考版
A.C N 中C的化合价为-4
衡水泰华中学决胜高考化学暑假必刷密卷 第 20套 3 4
组编人:张莹莹
B.反应的两个阶段均为吸热过程
做题时间:2022 年__月___日,__:__—__:__ 校对人: 李庆霞 C.阶段Ⅱ中,H O 既是氧化剂,又是还原剂
2 2
审核人:王立明
D.通过该反应,实现了化学能向太阳能的转化
实际得分:____家长签字(严禁代签):______
励志格言:人生的旅途,前途很远,也很暗。然而不要怕,不怕的人的面前才有路。
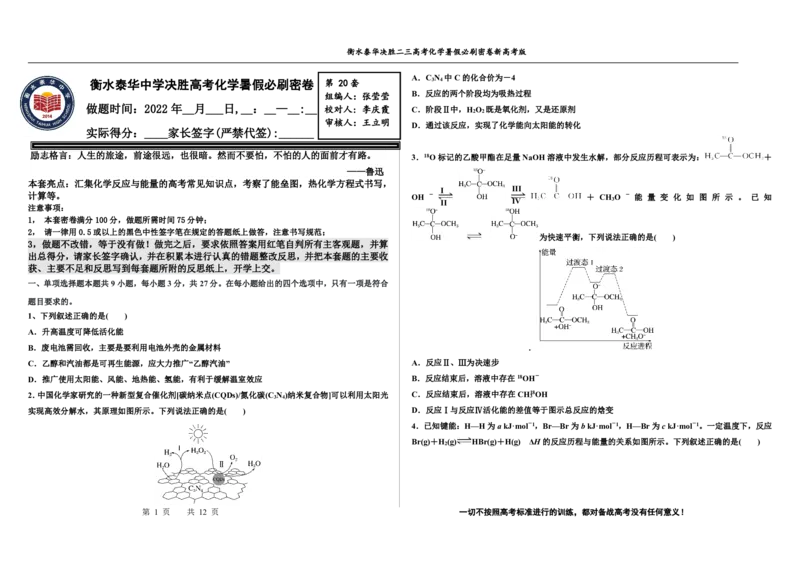
3.18O标记的乙酸甲酯在足量NaOH溶液中发生水解,部分反应历程可表示为: +
——鲁迅
本套亮点:汇集化学反应与能量的高考常见知识点,考察了能垒图,热化学方程式书写,
I III
计算等。 OH - + CH O - 能 量 变 化 如 图 所 示 。 已 知
II IV 3
注意事项:
1, 本套密卷满分100分,做题所需时间75分钟;
2, 请一律用0.5或以上的黑色中性签字笔在规定的答题纸上做答,注意书写规范;
为快速平衡,下列说法正确的是( )
3,做题不改错,等于没有做!做完之后,要求依照答案用红笔自判所有主客观题,并算
出总得分,请家长签字确认,并在积累本进行认真的错题整改反思,并把本套题的主要收
获、主要不足和反思写到每套题所附的反思纸上,开学上交。
一、单项选择题本题共9小题,每小题3分,共27分。在每小题给出的四个选项中,只有一项是符合
题目要求的。
1、下列叙述正确的是( )
A.升高温度可降低活化能
B.废电池需回收,主要是要利用电池外壳的金属材料 .
C.乙醇和汽油都是可再生能源,应大力推广“乙醇汽油” A.反应Ⅱ、Ⅲ为决速步
D.推广使用太阳能、风能、地热能、氢能,有利于缓解温室效应 B.反应结束后,溶液中存在18OH-
2.中国化学家研究的一种新型复合催化剂[碳纳米点(CQDs)/氮化碳(C 3 N 4 )纳米复合物]可以利用太阳光 C.反应结束后,溶液中存在CH1 3 8OH
实现高效分解水,其原理如图所示。下列说法正确的是( ) D.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓变
4.已知键能:H—H为akJ·mol-1,Br—Br为bkJ·mol-1,H—Br为ckJ·mol-1。一定温度下,反应
Br(g)+H (g) HBr(g)+H(g) ΔH的反应历程与能量的关系如图所示。下列叙述正确的是( )
2
第 1 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
A.该反应的正反应是放热反应 A.无论是否鼓入空气,负极的电极反应式均为Fe-2e- ===Fe2+
B.ΔH=E 1 -E 2 ,加入催化剂时,E 1 、E 2 及ΔH均减小 B.不鼓入空气时,正极的电极反应式为H+ + e- ===H
C.已知a>c,若反应H
2
(g)+Br
2
(g) 2HBr(g) ΔH<0,则b>a C.鼓入空气时,每生成1mol·OH有2mol电子发生转移
D.升高温度,正、逆反应速率均加快,且正反应速率加快的程度较大 D.处理含有草酸(H C O )的污水时,上端开口应打开并鼓入空气
2 2 4
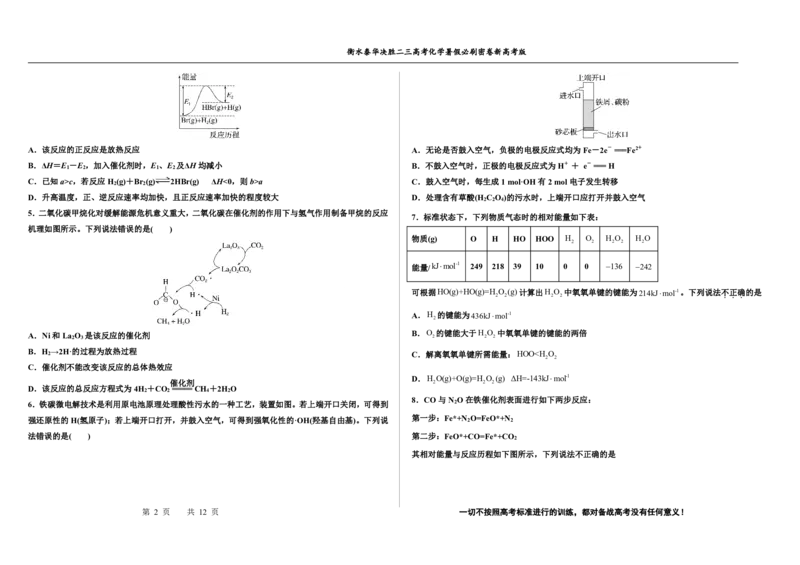
5.二氧化碳甲烷化对缓解能源危机意义重大,二氧化碳在催化剂的作用下与氢气作用制备甲烷的反应
7.标准状态下,下列物质气态时的相对能量如下表:
机理如图所示。下列说法错误的是( )
物质(g) O H HO HOO H O H O H O
2 2 2 2 2
能量/kJmol-1 249 218 39 10 0 0 136 242
可根据HO(g)+HO(g)=H
2
O
2
(g)计算出H
2
O
2
中氧氧单键的键能为214kJmol-1。下列说法不
.
正
.
确
.
的是
A.H 的键能为436kJmol-1
2
A.Ni和La 2 O 3 是该反应的催化剂 B.O 2 的键能大于H 2 O 2 中氧氧单键的键能的两倍
B.H
2
→2H·的过程为放热过程
C.解离氧氧单键所需能量:HOOⅠ
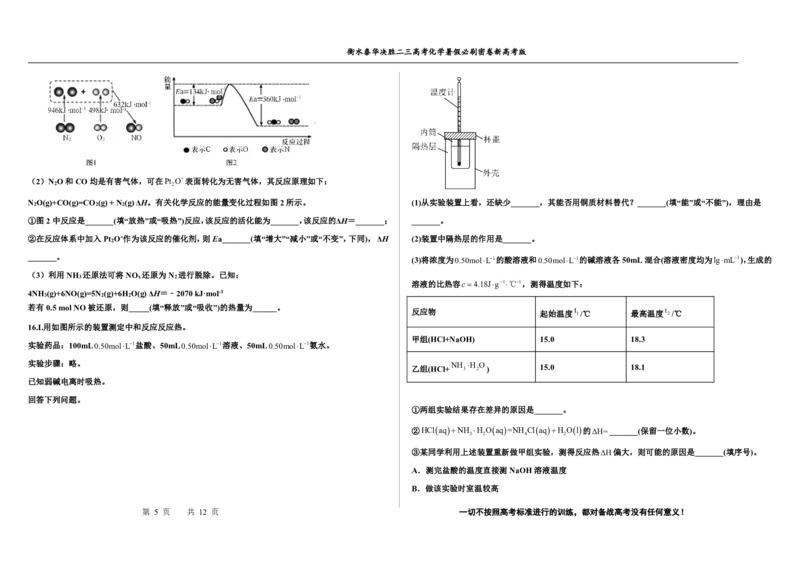
二、不定项选择题:本题共4小题,每小题4分,共16分。在每小题给出的四个选项中,有一项或两 C.生成P的速率:Ⅲ>Ⅱ D.进程Ⅳ中,Z没有催化作用
项符合题目要求。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项,
只选一个且正确得2分,选两个且都正确的得4分,但只要选错一个,该小题得0分。
12.(2022·山东日照·一模)下列说法正确的是
10.我国科学家实现了在铜催化剂条件下将DMF[(CH
3
)
2
NCHO]转化为三甲胺[N(CH
3
)
3
]。计算机 A.蛋白质溶液中加入饱和CuSO
4
溶液可发生盐析
模拟单个DMF分子在铜催化剂表面的反应历程如图所示,下列说法正确的是( )
B.由反应CH (g)+2O (g)=CO (g)+2H O(g) ΔH=-805kJmol-1可知,甲烷的燃烧热为805kJmol1
4 2 2 2
第 3 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
C.铅蓄电池放电时的正极反应式为PbO +2e-+4H++SO2-=PbSO +2H O
2 4 4 2
C(石墨,s)+O (g)=CO (g) ΔH=-393.5kJmol-1 C(金刚石,s)+O (g)=CO (g) ΔH=-395kJmol-1
D. 2 2 , 2 2 ,结
1
论:相同条件下金刚石比石墨稳定 (2)已知CH 3 OH(l)的燃烧热ΔH=-726.5kJ·mol-1,CH 3 OH(l)+ O 2 (g)===CO 2 (g)+2H 2 (g)
2
ΔH=-akJ·mol-1,则a______(填“>”“<”或“=”)726.5。
13.HBr被O 氧化依次由如下Ⅰ、Ⅱ、Ⅲ三步反应组成:
2 (3)将Cl 和H O(g)通过灼热的炭层,生成HCl和CO,当有1molCl 参与反应时释放出145.0kJ热量,
2 2 2 2
Ⅰ.HBr(g)+O (g)===HOOBr(g)
2 写出该反应的热化学方程式:_____________________________________________。
Ⅱ.HOOBr(g)+HBr(g)===2HOBr(g)
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所
Ⅲ.HOBr(g)+HBr(g)===H O(g)+Br (g)
2 2 得物质可作耐高温材料:4Al(s)+3TiO (s)+3C(s)===2Al O (s)+3TiC(s) ΔH=
2 2 3
1molHBr(g)被氧化为Br
2
(g)放出12.67kJ热量,其能量与反应进程的关系如图所示:
-1176.0kJ·mol-1,则反应过程中,每转移1mol电子放出的热量为__________。
(5)已知:①C(s)+O (g)===CO (g) ΔH =-393.5kJ·mol-1
2 2 1
②2CO(g)+O (g)===2CO (g)
2 2
ΔH =-566kJ·mol-1
2
③TiO (s)+2Cl (g)===TiCl (s)+O (g)
2 2 4 2
ΔH =+141kJ·mol-1
3
下列说法正确的是( )
则TiO (s)+2Cl (g)+2C(s)===TiCl (s)+2CO(g)的ΔH=__________。
2 2 4
A.反应Ⅰ、Ⅱ、Ⅲ均为放热反应
(6)已知拆开1molH—H,1molN—H,1molN≡N分别需要的能量是436kJ、391kJ、946kJ,则N (g)
2
B.Ⅰ的反应速率最慢
与H (g)反应生成NH (g)的热化学方程式为___________________________________。
2 3
C.HOOBr(g)比HBr(g)和O (g)稳定
2
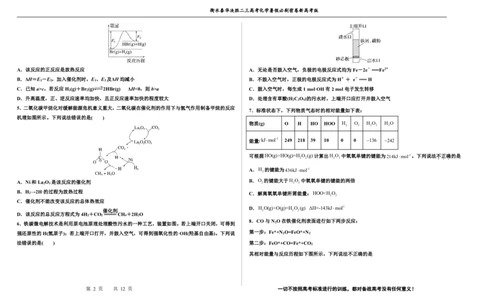
15. 汽车尾气中的主要污染物是NO 和CO,它们是现代化城市中的重要大气污染物。
x
D.热化学方程式为4HBr(g)+O (g)===2H O(g)+2Br (g) ΔH=-12.67kJ·mol-1
2 2 2
(1)汽车发动机工作时会引发N 和O 反应生成NO,其能量变化如图1所示,则图1中三种分子最
2 2
稳定的是_______,图1中对应反应的热化学方程式为________________。
三、非选择题:共57分,每个试题考生都必须作答。
14. 碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活中主要的能源物质。
请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下,ΔH=+88.6kJ·mol-1,则M、N相比,较
稳定的是________。
第 4 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
(2)N O和CO均是有害气体,可在Pt O+表面转化为无害气体,其反应原理如下:
2 2
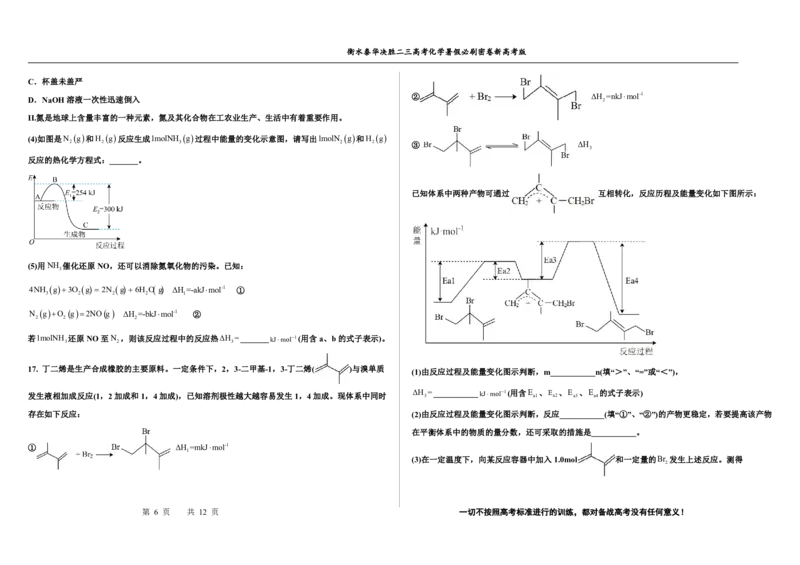
N O(g)+CO(g)=CO (g)+N (g)ΔH。有关化学反应的能量变化过程如图2所示。 (1)从实验装置上看,还缺少_______,其能否用铜质材料替代?_______(填“能”或“不能”),理由是
2 2 2
①图2中反应是_______(填“放热”或“吸热”)反应,该反应的活化能为_______,该反应的ΔH=_______; _______。
②在反应体系中加入Pt O+作为该反应的催化剂,则Ea_______(填“增大”“减小”或“不变”,下同),ΔH (2)装置中隔热层的作用是_______。
2
_______。
(3)将浓度为0.50molL1的酸溶液和0.50molL1的碱溶液各50mL混合(溶液密度均为lgmL1),生成的
(3)利用NH 还原法可将NO 还原为N 进行脱除。已知:
3 x 2
溶液的比热容c4.18Jg1℃1,测得温度如下:
4NH (g)+6NO(g)=5N (g)+6H O(g)ΔH=﹣2070kJ·mol-1
3 2 2
若有0.5molNO被还原,则_____(填“释放”或“吸收”)的热量为______。
反应物 起始温度 t 1/℃ 最高温度t 2/℃
16.I.用如图所示的装置测定中和反应反应热。
甲组(HCl+NaOH) 15.0 18.3
实验药品:100mL0.50molL1盐酸、50mL0.50molL1溶液、50mL0.50molL1氨水。
实验步骤:略。 乙组(HCl+ NH 3 H 2 O ) 15.0 18.1
已知弱碱电离时吸热。
回答下列问题。
①两组实验结果存在差异的原因是_______。
②HClaqNH H Oaq=NH ClaqH Ol的ΔH=_______(保留一位小数)。
3 2 4 2
③某同学利用上述装置重新做甲组实验,测得反应热ΔH偏大,则可能的原因是_______(填序号)。
A.测完盐酸的温度直接测NaOH溶液温度
B.做该实验时室温较高
第 5 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
C.杯盖未盖严
D.NaOH溶液一次性迅速倒入 ② ΔH 2 =nkJmol-1
II.氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
(4)如图是N g和H g反应生成1molNH g过程中能量的变化示意图,请写出1molN g和H g
2 2 3 2 2 ③ ΔH
3
反应的热化学方程式:_______。
已知体系中两种产物可通过 互相转化,反应历程及能量变化如下图所示:
(5)用NH 催化还原NO,还可以消除氮氧化物的污染。已知:
3
4NH g3O g 2N g 6H O g ΔH =-akJmol-1 ①
3 2 2 2 1
N gO g2NOg ΔH =-bkJmol-1 ②
2 2 2
若1molNH 还原NO至N ,则该反应过程中的反应热ΔH =_______kJmol1(用含a、b的式子表示)。
3 2 3
17. 丁二烯是生产合成橡胶的主要原料。一定条件下,2,3-二甲基-1,3-丁二烯( )与溴单质 (1)由反应过程及能量变化图示判断,m___________n(填“>”、“=”或“<”),
发生液相加成反应(1,2加成和1,4加成),已知溶剂极性越大越容易发生1,4加成。现体系中同时
ΔH
3
=___________kJmol1(用含E
a1
、E
a2
、E
a3
、E
a4
的式子表示)
存在如下反应: (2)由反应过程及能量变化图示判断,反应___________(填“①”、“②”)的产物更稳定,若要提高该产物
在平衡体系中的物质的量分数,还可采取的措施是___________。
① ΔH =mkJmol-1
1
(3)在一定温度下,向某反应容器中加入1.0mol 和一定量的Br 发生上述反应。测得
2
第 6 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
假期作业第二十套答题纸
的平衡转化率为a,平衡时Br 为bmol,若以物质的量分数表示的平衡常数K ,反应③的
2 x
14.
(1)____________________________。
平衡常数K =4,则产物 的选择性百分比为___________(选择性是指目标产物在
x3
(2)________________。
最终产物中的比率),开始加入的Br 的物质的量为___________mol,反应①的平衡常数
2 (3)_____________________________________________________________________________________。
K
x1
=___________。
(4)___________________________________。
(5)___________________________________。
(6)_____________________________________________________________________________________。
15.
(1)______________________,________________________________________________________。
(2)
①_________________,_____________________,_____________________________________;
②______________________, ΔH______________________。
(3)____________________(填“释放”或“吸收”)的热量为__________________________。
16.
(1)__________________,___________(填“能”或“不能”),理由是________________________________。
(2)________________________________________________________。
(3)
①_____________________________________________________________________________________。
第 7 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
衡水泰华中学决胜高考化学暑假必刷密卷第二十套化学参考答案
一,1.答案 D
②________________________________(保留一位小数)。
解析 对于同一分子的活化能是定值,升高温度活化能不改变,选项A错误;主要回收废电池的铁壳
③______________________(填序号)。 和其中的“黑”原料,并进行二次产品的开发制造,选项B错误;汽油是不可再生能源,选项C错误;
太阳能、风能、地热能、氢能是清洁能源,推广使用能减少二氧化碳的排放,选项D正确。
(4)_____________________________________________________________________________________。
2.答案 C
(5)___________________________kJmol1(用含a、b的式子表示)。 解析 依据化合物中化合价代数和为0,因C
3
N
4
中N的化合价为-3,所以C的化合价为+4,A项错
误;阶段Ⅱ过氧化氢分解生成氧气和水为放热反应,B项错误;阶段Ⅱ中,H O 发生歧化反应,既是
2 2
17.
氧化剂,又是还原剂,C项正确;利用太阳光实现高效分解水的反应,实现了太阳能向化学能的转化,
(1)____________________,ΔH
3
=___________kJmol1(用含E
a1
、E
a2
、E
a3
、E
a4
的式子表示) D项错误。
3.答案 B
(2)_____________________,_______________________________________________________。
解析 一般来说,反应的活化能越高,反应速率越慢,由图可知,反应Ⅰ和反应Ⅳ的活化能较高,因
(3)________________,_____________________,____________________________________。
此反应的决速步为反应Ⅰ、Ⅳ,故A错误;反应Ⅰ为加成反应,而 为
快速平衡,反应Ⅱ的成键和断键方式为 或 ,后者能生成18OH-,因此
反应结束后,溶液中存在 18OH-,故 B 正确;反应Ⅲ的成键和断键方式为 或
,因此反应结束后溶液中不会存在CH18OH,故C错误;该总反应对应反应物的总能
3
量高于生成物的总能量,总反应为放热反应,因此 和CH O-的总能量与
3
和OH-的总能量之差等于图示总反应的焓变,故D错误。
第 8 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
4.答案 D
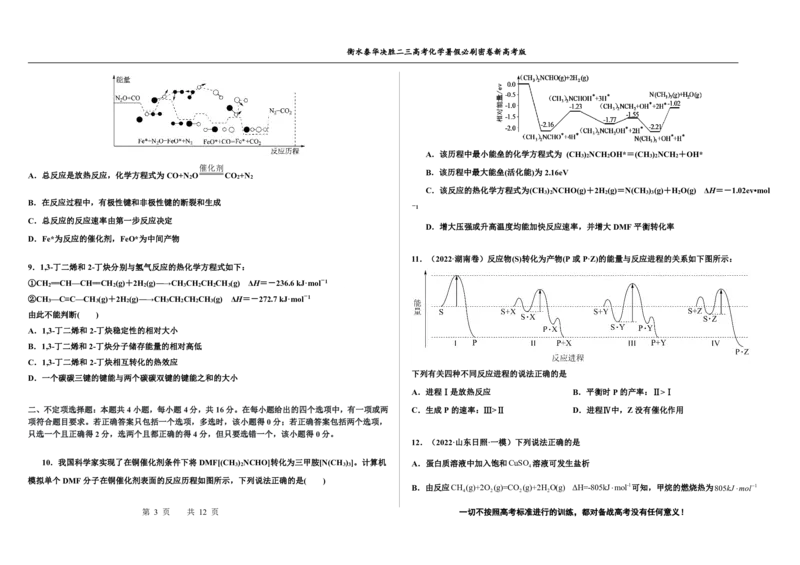
B.由题干反应历程图可知,在反应过程中,反应物中CO和N O中的C-O、N-O极性键断裂,CO
2 2
解析 由图可知,E 为正反应活化能,E 为逆反应活化能,E >E ,ΔH=E -E >0,为吸热反应,A
1 2 1 2 1 2 中有C-O极性键形成,即整个过程中没有非极性键的断裂和生成,B错误;
错误;加入催化剂时,E 、E 减小,但ΔH不变,B错误;由于H—H的键能大于H—Br的键能,若
1 2
C.总由题干反应历程图可知,第一步反应的活化能大于第二步反应,即第一步反应为慢反应,则整
反应H (g)+Br (g) 2HBr(g) ΔH<0,则Br—Br的键能应小于H—Br的键能,即c>b,又a>c,则
2 2
个反应的反应速率由第一步反应决定,C正确;
a>b,C错误;该反应为吸热反应,升高温度,正、逆反应速率均加快,正反应速率加快的程度大于逆
反应速率加快的程度,使平衡向正反应方向移动,D正确。
D.由题干反应历程图可知,Fe*反应过程中参与反应,但反应前后不变,即Fe*为反应的催化剂,FeO*
5.答案 B 为中间产物,D正确;
解析 由图可知该循环中Ni和La O 是该反应的催化剂,故A正确;H →2H·为断键的过程,该过程 9.答案 D
2 3 2
为吸热过程,故B错误;催化剂可以降低反应的活化能,但不能改变该反应的总体热效应,故C正确; 解析 根据盖斯定律可知,①-②即得到CH 2 ==CH—CH==CH 2 (g)―→CH 3 —C≡C—CH 3 (g) ΔH=+
催化剂
36.1kJ·mol-1,这说明1,3-丁二烯转化为2-丁炔是吸热反应,因此在物质的量相等的条件下,1,3-丁二
根据图中信息得到该反应的总反应方程式为4H +CO =====CH +2H O,故D正确。
2 2 4 2
烯的总能量低于2-丁炔的总能量,则1,3-丁二烯比2-丁炔的稳定性强,因此A、B、C三项均正确;反
6.答案 C
应热等于断开化学键吸收的能量与形成化学键所放出的能量的差值,但由于不能确定碳碳单键的键能,
解析 在原电池中,铁作负极,电极反应式是 Fe-2e-===Fe2+,故A正确;不鼓入空气时,正极发
因此根据热化学方程式不能确定一个碳碳三键的键能与两个碳碳双键的键能之和的大小,D项错误。
生还原反应为H++ e- === H,故 B 正确;鼓入空气时,氧气在正极发生的电极反应为O +4e-+
2
2H O===4·OH,每生成1mol·OH有1mol电子发生转移,故C错误。
2
二、不定项选择题(每个小题有1-2个正确选项,共5小题,每题4分,部分分2分,共20分)
7.答案 C
10.【答案】A
【解析】A.根据表格中的数据可知,H 的键能为218×2=436kJmol-1,A正确;
2
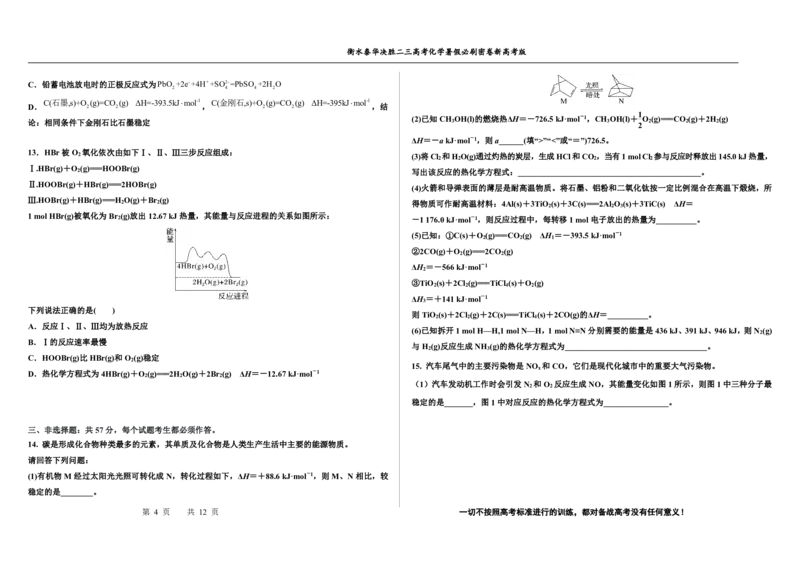
【解析】从图中可以看出,在正向进行的三个反应中,其能垒分别为:-1.23-(-2.16)=0.93、
B.由表格中的数据可知O 的键能为:249×2=498kJmol-1,由题中信息可知H O 中氧氧单键的键能
2 2 2
-1.55-(-1.77)=0.22、-1.02-(-2.21)=1.19。A项,从以上分析知,该历程中最小能垒为0.22,是由
为214kJmol-1,则O 的键能大于H O 中氧氧单键的键能的两倍,B正确;
2 2 2
(CH ) NCH OH*转化为(CH ) NCH 的反应,化学方程式为 (CH ) NCH OH*=(CH ) NCH +OH*,
C.由表格中的数据可知HOO=HO+O,解离其中氧氧单键需要的能量为249+39-10=278kJmol-1,H O 3 2 2 3 2 2 3 2 2 3 2 2
2 2
A正确;B项,该历程中最大能垒(活化能)为1.19eV,B不正确;C项,该反应的总反应是由(CH ) NCHO(g)
中氧氧单键的键能为214kJmol-1,C错误; 3 2
转化为N(CH ) (g),但1.02ev•为单个(CH ) NCHO(g)反应时放出的热量,所以热化学方程式为
D.由表中的数据可知H O(g)+O(g)=H O (g)的ΔH=-136-249-(-242)=-143kJmol-1,D正确; 3 3 3 2
2 2 2
(CH ) NCHO(g)+2H (g)=N(CH ) (g)+H O(g) ΔH=-1.02N ev•mol-1,C不正确;D项,增大压强
8.【答案】B 3 2 2 3 3 2 A
或升高温度均能加快反应速率,但升高温度平衡逆向移动,不能增大DMF平衡转化率,D不正确;
催化剂
【解析】A.由题干反应历程图可知,该反应的总反应化学方程式为CO+N O CO +N ,反应物
2 2 2 故选A。
11.【答案】AD
的总能量高于生成物的总能量,则是放热反应,A正确;
第 9 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
【解析】A.由图中信息可知,进程Ⅰ中S的总能量大于产物P的总能量,因此进程I是放热反应,A 三、非选择题(共50分,共5道大题)
14. 【答案】 (1)M (2)<
说法正确;
(3)2Cl (g)+2H O(g)+C(s)===4HCl(g)+CO (g) ΔH=-290.0kJ·mol-1
B.进程Ⅱ中使用了催化剂X,但是催化剂不能改变平衡产率,因此在两个进程中平衡时P的产率相 2 2 2
(4)98.0kJ (5)-80kJ·mol-1
同,B说法不正确;
(6)N (g)+3H (g) 2NH (g) ΔH=-92.0kJ·mol-1
2 2 3
C.进程Ⅲ中由S•Y转化为P•Y的活化能高于进程Ⅱ中由S•X转化为P•X的活化能,由于这两步反应
解析 (1)有机物M经过太阳光光照转化为N的过程吸收能量,则N能量高,比M活泼,较稳定的化
分别是两个进程的决速步骤,因此生成P的速率为Ⅲ<Ⅱ,C说法不正确;
合物为M。
D.由图中信息可知,进程Ⅳ中S吸附到Z表面生成S•Z,然后S•Z转化为产物P•Z,由于P•Z没有 (2)甲醇燃烧生成CO (g)和H (g)属于不完全燃烧,放出的热量少,所以a<726.5。
2 2
转化为P+Z,因此,Z没有表现出催化作用,D说法正确; (3)有1molCl 2 参与反应时释放出145.0kJ热量,2mol 氯气反应放热290.0kJ,反应的热化学方程式:
2Cl (g)+2H O(g)+C(s)===4HCl(g)+CO (g) ΔH=-290.0kJ·mol-1。
综上所述,本题选AD。 2 2 2
(4)4Al(s)+3TiO (s)+3C(s)===2Al O (s)+3TiC(s) ΔH=-1176.0kJ·mol-1,转移12mol电子放热1
2 2 3
12.【答案】C
1176.0
176.0kJ,则反应过程中,每转移1mol电子放出的热量为 kJ=98.0kJ。
【详解】
12
(5)根据盖斯定律,由①×2-②+③得:TiO (s)+2Cl (g)+2C(s)===TiCl (s)+2CO(g),其焓变ΔH=
A.CuSO 是重金属盐,蛋白质溶液中加入饱和CuSO 溶液可发生变性,而不是盐析,A错误; 2 2 4
4 4
ΔH ×2-ΔH +ΔH =-80kJ·mol-1。
1 2 3
B.生成物中H O(g)是水蒸气,不是液态水H O(l),燃烧热指的是生成稳定氧化物,而氧的稳定氧化
2 2 (6)在反应N +3H 2NH 中,断裂3molH—H、1molN≡N共吸收的能量:3×436kJ+946kJ=2254
2 2 3
物为液态水,故甲烷燃烧热不是805kJmol1,B错误;
kJ,生成2molNH ,共形成6molN—H,放出的能量为6×391kJ=2346kJ,吸收的热量少,放出
3
C.铅蓄电池放电时的正极得电子发生还原反应,反应式为:PbO +2e-+4H++SO2-=PbSO +2H O,C 的热量多,该反应为放热反应,放出的热量为2346kJ-2254kJ=92kJ,则N 2 (g)与H 2 (g)反应生成
2 4 4 2
NH (g)的热化学方程式为N (g)+3H (g) 2NH (g) ΔH=-92.0kJ·
3 2 2 3
正确;
mol-1。
D.将D项两式子相减得:C(石墨,s)=C(金刚石,s) ΔH=+1.5KJ·mol-1,石墨变成金刚石要吸热,说
15.
明石墨比等量的金刚石能量低,物质能量越低越稳定,所以相同条件下石墨比金刚石稳定,D错误;
(1) N N (g)+O (g)=2NO(g) ΔH=+180kJ·mol-1
2 2 2
故答案选C。
(2) 放热 134kJ·mol-1 -226kJ·mol-1 减小 不变
13. 【答案】B
解析 第一步反应的反应物总能量低于生成物总能量,所以为吸热反应,故A错误;第一步反应需要 (3) 释放 172.5kJ
的活化能最大,即反应Ⅰ的反应速率最慢,故B正确;HOOBr(g)的能量比HBr(g)和O (g)的总能量高, 【解析】
2
能量越高,物质越不稳定,故C错误;根据题意,1molHBr(g)被氧化为Br
2
(g)放出12.67kJ热量,
(1)
则热化学方程式为4HBr(g)+O (g)===2H O(g)+2Br (g) ΔH=-50.68kJ·mol-1,故D错误。
2 2 2
第 10 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
键能越大越稳定,图1中三种分子最稳定的是N ,该反应中的反应热=反应物的键能和-生成物的键能
2
和=(946+498)kJ/mol-2×632kJ/mol=+180kJ/mol,热化学方程式为:N (g)+O (g)=2NO(g)△H=+180
2 2
kJ•mol-1;
(2)
①由图可知,N O(g)和CO(g)具有的总能量大于CO (g)和N (g)具有的总能量,则反应放热;该反应的
2 2 2
活化能为134kJ·mol-1;该反应的ΔH=正反应的活化能-逆反应的活化能
=134kJ/mol-360kJ/mol=-226kJ/mol;
②催化剂能改变反应途径,降低反应的活化能,则没有Pt O+参与该转化过程,则E 将变大,但不能
2 a
改变反应始态和终态,不能改变焓变;
(3)
当有6molNO被还原,放出2070kJ能量,若有0.5molNO被还原,则释放172.5kJ。
16.(1) 环形玻璃搅拌棒 不能 金属材质易散热,使实验误差增大
第( )套化学暑假必刷密卷专用反思表
(2)减少实验过程中的热量损失
填表时间:2022 年__月___日,__:__;反思人:___________家长签字:_____________
(3) NH •H O为弱碱,电离时要吸热,导致放热较少 -51.8kJ/mol AC
3 2
本套暴露的主要问题
(4)N (g)+3H (g) 2NH (g)△H=-92kJ/mol
2 2 3
板块 该板块失分 对每一分失分的原因反思
a-3b
(5)-
4
17.(1) > E -E +E -E
a1 a2 a3 a4 单项选 总分27 分
(2) ② 在极性大的溶剂中进行反应 择题 丢了( )分
0.2a(1b) 双选题 总分16 分
(3) 80% (b+a)
(1a)b
丢了( )分
主观题 总分57 分
丢了( )分
本套题的主要收获
第 11 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
知识上
的收获
技巧上
的收获
本套题的综合反思
做题状
态
做题结
果
自我提
醒
第 12 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!