文档内容
衡水泰华决胜二三高考化学暑假必刷密卷新高考版
衡水泰华中学决胜高考化学暑假必刷密卷 第 2 套
组编人:王艳娜
做题时间:2022 年__月___日,__:__—__:__ 校对人: 李庆霞
发生装置
审核人:王立明
实际得分:____家长签字(严禁代签):______
励志格言:胜利的时候不要忘却从前;失败的时候不要忘记还有将来。
本套亮点:汇集非金属元素各地最新模拟题,有基础考查题,也有新颖且有思维量的题目,
充分利用,定能查漏补缺,收获满满。 A.A B.B C.C D.D
注意事项:
3.2022年2月4日北京冬奥会开幕了,精彩的冬奥会离不开“化学元素”,下列叙述错误的是
1, 本套密卷满分100分,做题所需时间75分钟;
2, 请一律用0.5或以上的黑色中性签字笔在规定的答题纸上做答,注意书写规范;
选
3,做题不改错,等于没有做!做完之后,要求依照答案用红笔自判所有主客观题,并算 冬奥会的“化学元素” 叙述
出总得分,请家长签字确认,并在积累本进行认真的错题整改反思,并把本套题的主要收 项
获、主要不足和反思写到每套题所附的反思纸上,开学上交。
二氧化碳为无毒气体,符合绿
一、单项选择题本题共9小题,每小题3分,共27分。在每小题给出的四个选项中,只有一项是符合
A 二氧化碳直冷制冰技术打造世界“最快冰面”
题目要求的。
色冬奥理念
1.明朝李时珍名著《本草纲目》中记载:“以铅打成钱,穿成串,瓦盆盛生醋,以串横盆中,离醋三
石墨烯主要目的是增加制服硬
寸,仍以瓦盆覆之,置阴处,候生霜刷下,仍合住。”(注:霜即醋酸铅,又称为铅糖)。下列有关说法
B 用石墨烯制作冬奧会赛时制服“山河映朝霞”系列
度
不正确的是
A.瓦盆也叫泥盆,用泥做成,瓦盆和建筑材料水泥、砖都属于硅酸盐产品 氮气熔点很低,可以达到“极
C “极速”液氮速冻机,-35℃下保证食品品质与安全
B.“离醋三寸,……置阴处,候生霜刷下”,说明醋酸具有挥发性 速”冷冻效果
C.“铅打成钱,穿成串”的目的是增大接触面积,从而加快反应速率
智能穿戴式体温计“腋下创可贴”是防疫利器,精准实时自动报 微型原电池为“腋下创可贴”温
D.该过程中涉及的铅、醋、醋酸铅三种物质均属于电解质 D
温,充电1小时可使用10天 度计提供电能
2.制备下列气体所需的反应物和发生装置均可行的是
选项 A B C D
A.A B.B C.C D.D
气体 一氧化氮 氯气 硫化氢 氨气
反应物 铜丝、稀硝酸 浓盐酸、高锰酸钾溶液 硫化钠固体、浓硫酸 铵盐、熟石灰
第 1 页 共 15 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
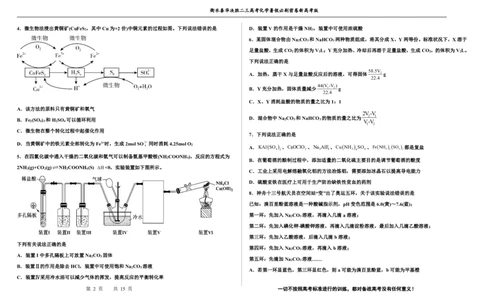
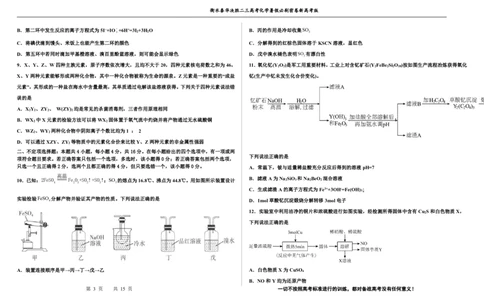
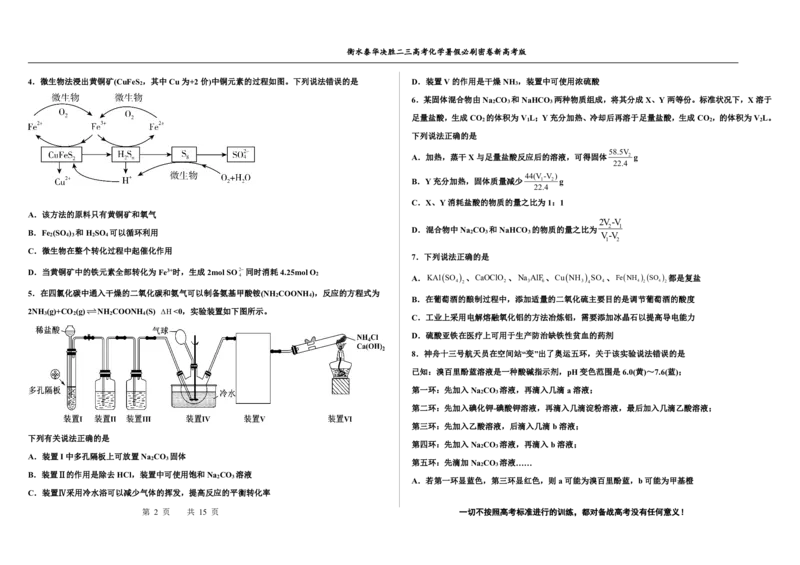
4.微生物法浸出黄铜矿(CuFeS ,其中Cu为+2价)中铜元素的过程如图。下列说法错误的是 D.装置V的作用是干燥NH ,装置中可使用浓硫酸
2 3
6.某固体混合物由Na CO 和NaHCO 两种物质组成,将其分成X、Y两等份。标准状况下,X溶于
2 3 3
足量盐酸,生成CO 的体积为V L;Y充分加热、冷却后再溶于足量盐酸,生成CO ,的体积为V L。
2 1 2 2
下列说法正确的是
58.5V
A.加热,蒸干X与足量盐酸反应后的溶液,可得固体 2 g
22.4
44(V-V )
B.Y充分加热,固体质量减少 1 2 g
22.4
C.X、Y消耗盐酸的物质的量之比为1:1
A.该方法的原料只有黄铜矿和氧气
2V-V
B.Fe 2 (SO 4 ) 3 和H 2 SO 4 可以循环利用 D.混合物中Na 2 CO 3 和NaHCO 3 的物质的量之比为 V 2 -V 1
1 2
C.微生物在整个转化过程中起催化作用
7.下列说法正确的是
D.当黄铜矿中的铁元素全部转化为Fe3+时,生成2molSO2同时消耗4.25molO
4 2 A.KAlSO 、CaOClO 、Na AlF 、CuNH SO 、FeNH SO 都是复盐
4 2 2 3 6 3 4 4 4 2 4 2
5.在四氯化碳中通入干燥的二氧化碳和氨气可以制备氨基甲酸铵(NH COONH ),反应的方程式为
2 4 B.在葡萄酒的酿制过程中,添加适量的二氧化硫主要目的是调节葡萄酒的酸度
2NH
3
(g)+CO
2
(g)NH
2
COONH
4
(S) ΔH<0,实验装置如下图所示。
C.工业上采用电解熔融氧化铝的方法冶炼铝,需要添加冰晶石以提高导电能力
D.硫酸亚铁在医疗上可用于生产防治缺铁性贫血的药剂
8.神舟十三号航天员在空间站“变”出了奥运五环,关于该实验说法错误的是
已知:溴百里酚蓝溶液是一种酸碱指示剂,pH变色范围是6.0(黄)~7.6(蓝);
第一环:先加入Na CO 溶液,再滴入几滴a溶液;
2 3
第二环:先加入碘化钾-碘酸钾溶液,再滴入几滴淀粉溶液,最后加入几滴乙酸溶液;
第三环:先加入乙酸溶液,后滴入几滴b溶液;
下列有关说法正确的是
第四环:先加入Na CO 溶液,再滴入b溶液;
2 3
A.装置I中多孔隔板上可放置Na CO 固体
2 3 第五环:先滴加Na CO 溶液……
2 3
B.装置Ⅱ的作用是除去HCl,装置中可使用饱和Na CO 溶液
2 3 A.若第一环显蓝色,第三环显红色,则a可能为溴百里酚蓝,b可能为甲基橙
C.装置Ⅳ采用冷水浴可以减少气体的挥发,提高反应的平衡转化率
第 2 页 共 15 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
B.第二环中发生反应的离子方程式为5I−+IO+6H+=3I +3H O B.丙的作用是冷却收集SO
3 2 2 3
C.将碘伏滴到馒头、米饭上也能产生第二环的颜色 C.分解得到的红棕色固体溶于KSCN溶液,显红色
D.第五环中若同时滴加甲基橙溶液、溴百里酚蓝溶液,则可能会显示绿色 D.戊中溴水褪色表明SO 有漂白性
2
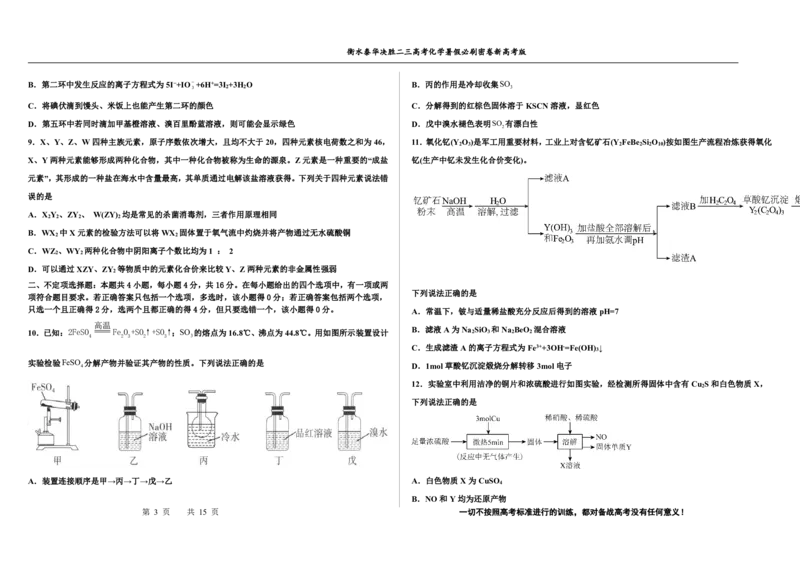
9.X、Y、Z、W四种主族元素,原子序数依次增大,且均不大于20,四种元素核电荷数之和为46, 11.氧化钇(Y O )是军工用重要材料,工业上对含钇矿石(Y FeBe Si O )按如图生产流程冶炼获得氧化
2 3 2 2 2 10
X、Y两种元素能够形成两种化合物,其中一种化合物被称为生命的源泉。Z元素是一种重要的“成盐 钇(生产中钇未发生化合价变化)。
元素”,其形成的一种盐在海水中含量最高,其单质通过电解该盐溶液获得。下列关于四种元素说法错
误的是
A.X Y 、ZY 、 W(ZY) 均是常见的杀菌消毒剂,三者作用原理相同
2 2 2 2
B.WX 中X元素的检验方法可以将WX 固体置于氧气流中灼烧并将产物通过无水硫酸铜
2 2
C.WZ 、WY 两种化合物中阴阳离子个数比均为1 : 2
2 2
D.可以通过XZY、ZY 等物质中的元素化合价来比较Y、Z两种元素的非金属性强弱
2
二、不定项选择题:本题共4小题,每小题4分,共16分。在每小题给出的四个选项中,有一项或两
下列说法正确的是
项符合题目要求。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项,
只选一个且正确得2分,选两个且都正确的得4分,但只要选错一个,该小题得0分。 A.常温下,铍与适量稀盐酸充分反应后得到的溶液pH=7
高温
10.已知:2FeSO Fe O +SO↑+SO↑;SO 的熔点为16.8℃、沸点为44.8℃。用如图所示装置设计 B.滤液A为Na 2 SiO 3 和Na 2 BeO 2 混合溶液
4 2 3 2 3 3
C.生成滤渣A的离子方程式为Fe3++3OH-=Fe(OH) ↓
3
实验检验FeSO 分解产物并验证其产物的性质。下列说法正确的是
4 D.1mol草酸钇沉淀煅烧分解转移3mol电子
12.实验室中利用洁净的铜片和浓硫酸进行如图实验,经检测所得固体中含有Cu S和白色物质X,
2
下列说法正确的是
A.装置连接顺序是甲→丙→丁→戊→乙 A.白色物质X为CuSO
4
B.NO和Y均为还原产物
第 3 页 共 15 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
C.参加反应的浓硫酸中,表现氧化性的占25%
D.NO与Y的物质的量之和可能为2mol
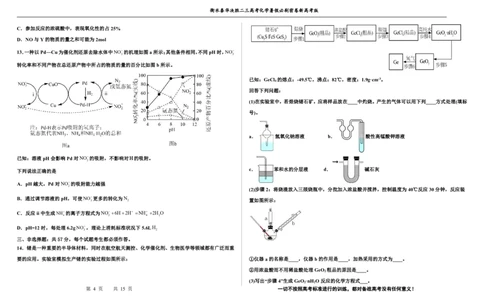
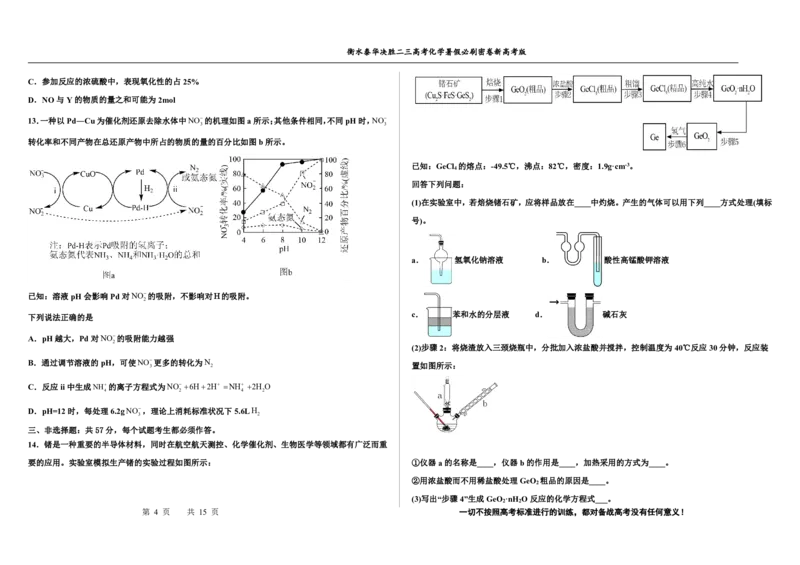
13.一种以Pd―Cu为催化剂还原去除水体中NO的机理如图a所示;其他条件相同,不同pH时,NO
3 3
转化率和不同产物在总还原产物中所占的物质的量的百分比如图b所示。
已知:GeCl 的熔点:-49.5℃,沸点:82℃,密度:1.9g·cm-3。
4
回答下列问题:
(1)在实验室中,若焙烧锗石矿,应将样品放在____中灼烧。产生的气体可以用下列____方式处理(填标
号)。
a. 氢氧化钠溶液 b. 酸性高锰酸钾溶液
已知:溶液pH会影响Pd对NO的吸附,不影响对H的吸附。
2
下列说法正确的是
c. 苯和水的分层液 d. 碱石灰
A.pH越大,Pd对NO的吸附能力越强
2
(2)步骤2:将烧渣放入三颈烧瓶中,分批加入浓盐酸并搅拌,控制温度为40℃反应30分钟,反应装
B.通过调节溶液的pH,可使NO
3
更多的转化为N
2 置如图所示:
C.反应ii中生成NH的离子方程式为NO6H2H NH 2H O
4 2 4 2
D.pH=12时,每处理6.2gNO,理论上消耗标准状况下5.6LH
3 2
三、非选择题:共57分,每个试题考生都必须作答。
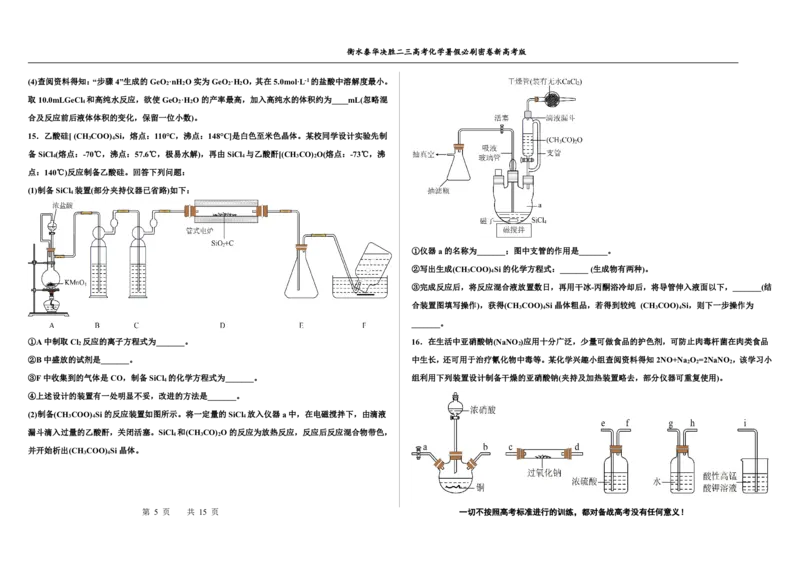
14.锗是一种重要的半导体材料,同时在航空航天测控、化学催化剂、生物医学等领域都有广泛而重
要的应用。实验室模拟生产锗的实验过程如图所示: ①仪器a的名称是____,仪器b的作用是____,加热采用的方式为____。
②用浓盐酸而不用稀盐酸处理GeO 粗品的原因是____。
2
(3)写出“步骤4”生成GeO ·nH O反应的化学方程式___。
2 2
第 4 页 共 15 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
(4)查阅资料得知:“步骤4”生成的GeO ·nH O实为GeO ·H O,其在5.0mol·L-1的盐酸中溶解度最小。
2 2 2 2
取10.0mLGeCl 和高纯水反应,欲使GeO ·H O的产率最高,加入高纯水的体积约为____mL(忽略混
4 2 2
合及反应前后液体体积的变化,保留一位小数)。
15.乙酸硅[(CH COO) Si,熔点:110°C,沸点:148°C]是白色至米色晶体。某校同学设计实验先制
3 4
备SiCl (熔点:-70℃,沸点:57.6℃,极易水解),再由SiCl 与乙酸酐[(CH CO) O(熔点:-73℃,沸
4 4 3 2
点:140℃)反应制备乙酸硅。回答下列问题:
(1)制备SiCl 装置(部分夹持仪器已省路)如下:
4
①仪器a的名称为_______;图中支管的作用是_______。
②写出生成(CH COO) Si的化学方程式:_______(生成物有两种)。
3 4
③完成反应后,将反应混合液放置数日,再用干冰-丙酮浴冷却后,将导管伸入液面以下,_______(结
合装置图填写操作),获得(CH COO) Si晶体粗品,若得到较纯 (CH COO) Si,则下一步操作为
3 4 3 4
_______。
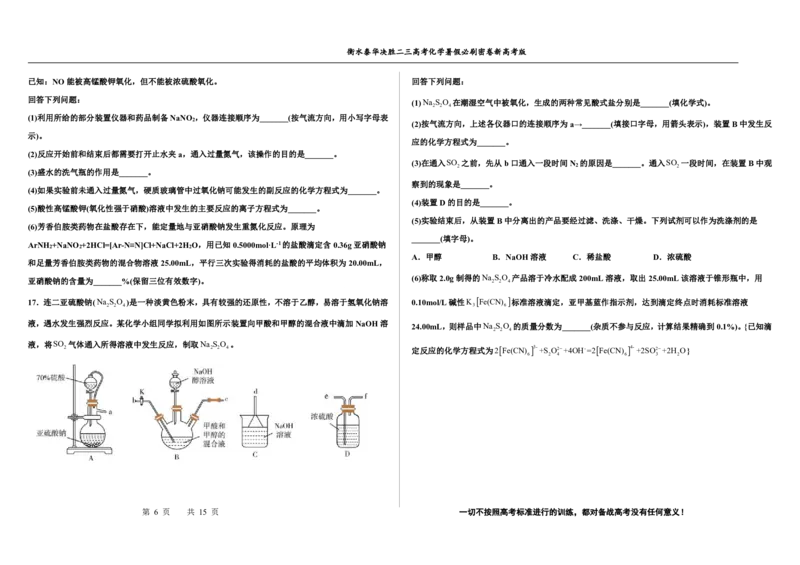
①A中制取Cl 反应的离子方程式为_______。 16.在生活中亚硝酸钠(NaNO )应用十分广泛,少量可做食品的护色剂,可防止肉毒杆菌在肉类食品
2 2
②B中盛放的试剂是_______。 中生长,还可用于治疗氰化物中毒等。某化学兴趣小组查阅资料得知2NO+Na O =2NaNO ,该学习小
2 2 2
③F中收集到的气体是CO,制备SiCl 的化学方程式为_______。 组利用下列装置设计制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)。
4
④上述设计的装置有一处明显不妥,改进的方法是_______。
(2)制备(CH COO) Si的反应装置如图所示。将一定量的SiCl 放入仪器a中,在电磁搅拌下,由滴液
3 4 4
漏斗滴入过量的乙酸酐,关闭活塞。SiCl 和(CH CO) O的反应为放热反应,反应后反应混合物带色,
4 3 2
并开始析出(CH COO) Si晶体。
3 4
第 5 页 共 15 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
已知:NO能被高锰酸钾氧化,但不能被浓硫酸氧化。 回答下列问题:
回答下列问题:
(1)Na S O 在潮湿空气中被氧化,生成的两种常见酸式盐分别是_______(填化学式)。
2 2 4
(1)利用所给的部分装置仪器和药品制备NaNO ,仪器连接顺序为_______(按气流方向,用小写字母表
2 (2)按气流方向,上述各仪器口的连接顺序为a→_______(填接口字母,用箭头表示),装置B中发生反
示)。
应的化学方程式为_______。
(2)反应开始前和结束后都需要打开止水夹a,通入过量氮气,该操作的目的是_______。
(3)在通入SO 之前,先从b口通入一段时间N 的原因是_______。通入SO 一段时间,在装置B中观
2 2 2
(3)盛水的洗气瓶的作用是_______。
察到的现象是_______。
(4)如果实验前未通入过量氮气,硬质玻璃管中过氧化钠可能发生的副反应的化学方程式为_______。
(4)装置D的目的是_______。
(5)酸性高锰酸钾(氧化性强于硝酸)溶液中发生的主要反应的离子方程式为_______。
(5)实验结束后,从装置B中分离出的产品要经过滤、洗涤、干燥。下列试剂可以作为洗涤剂的是
(6)芳香伯胺类药物在盐酸存在下,能定量地与亚硝酸钠发生重氮化反应。原理为
_______(填字母)。
ArNH +NaNO +2HCl=[Ar-N≡N]Cl+NaCl+2H O,用已知0.5000mol·L-1的盐酸滴定含0.36g亚硝酸钠
2 2 2
A.甲醇 B.NaOH溶液 C.稀盐酸 D.浓硫酸
和足量芳香伯胺类药物的混合物溶液25.00mL,平行三次实验得消耗的盐酸的平均体积为20.00mL,
亚硝酸钠的含量为_______%(保留三位有效数字)。
(6)称取2.0g制得的Na
2
S
2
O
4
产品溶于冷水配成200mL溶液,取出25.00mL该溶液于锥形瓶中,用
17.连二亚硫酸钠(Na S O )是一种淡黄色粉末,具有较强的还原性,不溶于乙醇,易溶于氢氧化钠溶 0.10mol/L碱性K Fe(CN) 标准溶液滴定,亚甲基蓝作指示剂,达到滴定终点时消耗标准溶液
2 2 4 3 6
液,遇水发生强烈反应。某化学小组同学拟利用如图所示装置向甲酸和甲醇的混合液中滴加NaOH溶
24.00mL,则样品中Na S O 的质量分数为_______(杂质不参与反应,计算结果精确到0.1%)。{已知滴
2 2 4
液,将SO 气体通入所得溶液中发生反应,制取Na S O 。
2 2 2 4 定反应的化学方程式为2Fe(CN) 3- +S O2+4OH-=2Fe(CN) 4- +2SO2+2H O}
6 2 4 6 3 2
第 6 页 共 15 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
衡水泰华中学决胜高考化学暑假必刷密卷第二套化学答题纸 (2) 。
14.(除标注外每空2分) (3)
(1) (每空1分) (4)
(2)① , , 。 (5)
② 。 (6) _______
(3) 。 17.(每空2分)
(4)____。 (1)
15.(除标注外每空2分) (2) , 。
① 。 (3) 。 。
② 。 (4) 。
③ 。 (5)_______。
④ 。 (6)_______
(2)
① ; (1分) 。(1分)
② (1分)
③
16(每空2分)
(1)
第 7 页 共 15 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
衡水泰华中学决胜高考化学暑假必刷密卷第二套化学参考答案 B.用石墨烯制作冬奧会赛时制服“山河映朝霞”系列,使用石墨烯的主要目的是石墨烯具有超强的导
热性、升温快速,B项错误;
1【答案】D
C.“极速”液氮速冻机主要利用N 的熔点很低,能迅速降温的特点,可使食品快速结晶,-35℃下保证
【解析】 2
食品品质与安全,C项正确;
【详解】
D.智能穿戴式体温计“腋下创可贴”是防疫利器,精准实时自动报温,充电1小时可使用10天,微型
A.瓦盆也叫泥盆,用泥做成,瓦盆和水泥、砖都属于硅酸盐材料,A正确;
原电池能将化学能转化成电能,为“腋下创可贴”温度计提供电能,D项正确;
B.“离醋三寸,……置阴处,候生霜刷下”,铅和醋有段距离,能生成醋酸铅,说明醋酸具有挥发性,
答案选B。
B正确;
4【答案】A
C.“铅打成钱,穿成串”的目的是增大接触面积,加快反应速率,C正确;
【解析】
D.铅是单质,醋是混合物,二者既不是电解质,也不是非电解质;醋酸铅是(弱)电解质,D错误;
【分析】
故选D。
由微生物法浸出黄铜矿中铜元素的过程示意图可知,黄铜矿与氢离子、铁离子反应生成铜离子、亚铁
2【答案】A
离子和H S ,亚铁离子在微生物作用下与氧气反应生成铁离子;铁离子与H S 反应生成亚铁离子、
【解析】 2 n 2 n
氢离子和S ,亚铁离子在微生物作用下与氧气反应生成铁离子;S 与氧气和水反应生成硫酸根离子和
【详解】 8 8
氢离子,则微生物是浸出过程的催化剂,总反应的方程式为
A.Cu与稀硝酸反应生成NO,抽动铜丝可使反应停止,图中装置可制备NO,A正确;
B.高锰酸钾溶液与浓盐酸直接反应制备氯气,不需要加热,所以不需要酒精灯,B错误; 4CuFeS 2 +17O 2 +2H 2 SO 4 微生物 4CuSO 4 +2Fe 2 (SO 4 ) 3 +2H 2 O,浸出过程中硫酸和硫酸铁可循环使用。
C.硫化钠固体与浓硫酸发生氧化还原反应不生成硫化氢,应选稀硫酸,C错误; 【详解】
D.铵盐固体、熟石灰为固固加热制备氨气,不能用固液反应产生气体的装置,D错误; A.由分析可知,该方法的原料为黄铜矿、硫酸和氧气,故A错误;
故选A。 B.由分析可知,出过程中硫酸和硫酸铁可循环使用,故B正确;
3【答案】B C.由分析可知,微生物是浸出过程的催化剂,故C正确;
【解析】 D.由分析可知,当黄铜矿中的铁元素全部转化为铁离子时,生成2mol硫酸根时,反应消耗氧气的物
【详解】 1
质的量为17mol× =4.25,故D正确;
4
A.通常情况下二氧化碳是一种无色无味的气体,是空气的组成成分之一,无毒,二氧化碳直冷制冰
故选A。
符合绿色冬奥理念,A项正确; 5【答案】C
第 8 页 共 15 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
【解析】 关系不确定,A错误;
【详解】 B.碳酸氢钠受热分解,质量减少为水和二氧化碳的质量,B错误;
A.多孔隔板上应该放置是难溶性固体,而Na CO 易溶于水,所以多孔隔板上应该放置CaCO 固体,
C.两个过程最后都得到氯化钠,根据原子守恒分析,X、Y消耗盐酸的物质的量之比为1:1,C正
2 3 3
确;
与稀盐酸制备CO ,A错误;
2
V x V 2V -V
D.x+y= 1 , +y= 2 ,解 y= 2 1 ,则碳酸钠和碳酸氢钠的物质的量比例为:
B.装置II的作用是除去CO 中的HCl杂质,可使用的是饱和的NaHCO 溶液,饱和Na CO 溶液仍 22.4 2 22.4 22.4
2 3 2 3
2V -V
然会与CO 反应而损耗CO ,B错误; 2 1 ,D错误;
2 2 2V-2V
1 2
C.氨气是易挥发的气体,冷水浴确实可以减少NH 的挥发,且反应
故选C。
3
7【答案】D
2NH(g)+CO(g) NH COONH(s) ΔΗ<0为放热反应,利用冷水浴降低温度,可促使平衡向正反
3 2 2 4
【解析】
应方程移动,从而提高反应的平衡转化率,C正确;
【详解】
D.浓硫酸与NH 可反应,所以不能用浓硫酸干燥NH ,要用碱石灰干燥NH ,故装置IV为装有碱石
3 3 3 A.复盐是由两种金属离子(或铵根离子)和一种酸根离子构成的盐,CuNH SO 不符合复盐定义,A
3 4 4
灰的球形干燥管,D错误;
项错误;
故合理选项为C。
B.葡萄酒酿造中适量添加二氧化硫,可防止葡萄酒在陈酿和储藏过程中被氧化,B项错误;
6【答案】C
C.工业上采用电解熔融氧化铝的方法冶炼铝,添加冰晶石降低氧化铝熔点,C项错误;
【解析】
D.硫酸亚铁能治疗缺铁性贫血,可用于生产防治缺铁性贫血的药剂,D项正确;
【详解】
答案选D。
8【答案】B
反应涉及的方程式为: ,NaHCO +HCl=NaCl+H O+CO ,
3 2 2
【解析】
【详解】
Na CO +2HCl=2NaCl+H O+CO 假设每份中碳酸氢钠的物质的量为xmol,碳酸钠的物质的量为
2 3 2 2
A.碳酸钠溶液显碱性,pH>7.6,加入溴百里酚蓝显蓝色,乙酸溶液显酸性,加入甲基橙会变红,A
V x V
ymol,则有x+y= 1 , +y= 2 正确;
22.4 2 22.4
A.X与盐酸反应后的溶液蒸干后得到氯化钠,根据以上方程式分析,氯化钠和二氧化碳的物质的量 B.酸性环境中碘离子和碘酸根发生归中反应,但乙酸为弱酸,不能拆,正确离子方程式为
第 9 页 共 15 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
5I−+IO+6CH COOH=3I +3H O+6CH COO-,B错误; 性质装置,根据已知中SO 熔点为16.8℃、沸点为44.8℃,则丙可以将SO 冷却下来,既证明有SO 存
3 3 2 2 3 3 3 3
C.第二环中因生成碘单质而变蓝,馒头、米饭中富含淀粉,遇碘也会变蓝,C正确;
在,又实现了SO 和SO 的分离,然后检验SO ,验证SO 的性质,因此装置的连接顺序为甲→丙→丁
2 3 2 2
D.碳酸钠溶液显碱性,加入溴百里酚蓝显蓝色,加入甲基橙会变黄,黄、蓝混合会使溶液显绿色,D
→戊→乙,故A选项正确;
正确;
B.根据已知中SO 熔点为16.8℃、沸点为44.8℃,则丙可以将SO 冷却下来,所以丙的作用是冷却收
3 3
综上所述答案为B。
9【答案】C
集SO
3
,故B选项正确;
【解析】 C.氧化铁不溶于KSCN溶液,应先将红棕色固体溶于盐酸,再加KSCN溶液,C项错误;
【分析】
D.戊中溴水褪色,表明SO 有还原性,发生的反应为:SO Br 2H O=2HBrH SO,故D选项
2 2 2 2 2 4
X、Y两种元素能够形成两种化合物,其中一种化合物被称为生命的源泉。则X、Y分别为H、O。Z
错误。
形成的一种盐在海水中含量最高,Z为Cl。四种元素核电荷数之和为46,则W为20号元素Ca。
故选AB选项。
【详解】
11【答案】BD
A.三种物质分别为H O 、ClO 、Ca(ClO) ,三者均具有较强的氧化性,可利用氧化性进行消毒杀菌,
2 2 2 2 【解析】
A项正确;
【分析】
B.CaH 与O 反应变为H O遇CuSO 溶液变蓝,说明X为H元素,B项正确;
2 2 2 4 Y FeBe Si O 可以写成Y O ·FeO·2BeO·2SiO ,与NaOH高温反应以及加水溶解后,根据流程Y元
2 2 2 10 2 3 2
C.WZ 、WY 分别为CaCl 和CaO ,前者是由Ca2+和2个Cl-组成阴阳离子之比为1:2,而后者是由
2 2 2 2 素转化成Y(OH) ,FeO为碱性氧化物,不与NaOH反应,但+2价Fe被氧化成+3价,即得到Fe O ,
3 2 3
Ca2+和O2
2
-阴阳离子之比为1:1,C项错误;
SiO 2 为酸性氧化物,与NaOH反应生成Na 2 SiO 3 ,Be与Al处于对角线,性质类似与Al及其化合物的
D.XZY、ZY 为HClO和ClO 中Cl均呈现出了正价而O均呈现出负价,说明O的电子能力强于 性质,BeO与NaOH反应生成Na BeO ,滤液A为Na SiO 、Na BeO ,沉淀中加入盐酸并调节pH,
2 2 2 2 2 3 2 2
Cl,所以O的非金属性强于Cl,D项正确; Fe3+转化成氢氧化铁沉淀,Y(OH) 与盐酸反应生成YCl ,据此分析;
3 3
故选C。 【详解】
10【答案】AB A.根据对角线原则,铍与铝化学性质相似,AlCl 溶液因Al3+水解显酸性,因此BeCl 溶液由于Be2+
3 2
【解析】 水解显酸性,故A错误;
【详解】 B.由题中工业流程可判断,钇元素与铁元素都存在于滤渣中,矿石中的铍元素和硅元素都应在滤液A
A.甲为FeSO 高温分解装置,乙为气体吸收装置,丙为冷却装置,丁为SO 检验装置,戊为验证SO 中,硅元素与NaOH反应后以Na 2 SiO 3 形式存在,铍元素与铝元素化学性质相似,与NaOH反应后以
4 2 2
第 10 页 共 15 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
Na
2
BeO
2
形式存在,故B正确; 3CuS16H4NO 6Cu23S4NO8HO得到0.8molNO与0.6molS,NO与S物质的量之
2 3 2
C.滤渣A由FeCl 与氨水反应得到,一水合氨为弱电解质,不可拆,离子方程式应为
3 和为1.4mol,D不正确;
Fe3++3NH 3 ·H 2 O=Fe(OH) 3 ↓+3NH 4 ,故C错误; 答案选AC。
高温 13【答案】BC
D.草酸钇沉淀煅烧分解的化学方程式为Y (C O ) Y O +3CO↑+3CO ↑,草酸根中+2价碳发生歧
2 2 4 3 2 3 2
【解析】
化反应,1mol草酸钇分解转移3mol电子,故D正确; 【详解】
答案为BD。 A.由图b可知,随着pH减小,n(N )增大,n(铵态氮)变化不大,则还原产物中n(N ):n(铵态氮)比
2 2
12【答案】AC 值增大,Pd表面吸附的NO和个数比变大,而溶液pH会影响Pd对NO的吸附,不影响对H的吸附,
2 2
【解析】
即pH越小,Pd对NO的吸附能力越强,A错误;
2
【分析】
B.由图b信息可知,pH值不同还原产物也不同,pH为4时主要还原产物为N2、pH为12时,还原
由图知,铜与足量浓硫酸反应生成Cu S和白色物质X,无气体生成,生成Cu S时铜元素从0价升高
2 2
到+1价、硫元素从+6价降低到-2价,则按得失电子数守恒、必定存在其他产物(所含元素化合价升高)、
产物几乎全是NO
2
,故通过调节溶液的pH,可使NO
3
更多的转化为N
2
,B正确;
按元素质量守恒只能为CuSO 4 ,则白色物质X为CuSO 4 ,配平得到该反应方程式为: C.由图a可知,反应ii即NO和H反应生成NH,根据氧化还原反应配平可得,反应ii中生成NH
2 4 4
5Cu4H 2 SO 4 (浓)=3CuSO 4 Cu 2 S4H 2 O ,据此回答。 的离子方程式为NO6H2H NH 2H O ,C正确;
2 4 2
【详解】
A. 据分析,白色物质X为CuSO 4 ,A正确; D.由图b可知,pH=12时,还原产物几乎全是NO 2 ,则每处理6.2g即 =0.1mol NO 3 ,根
B.Cu S和白色物质CuSO 加稀硫酸和稀硝酸时溶解,存在反应:
2 4 0.1mol
据电子守恒可知,理论上消耗标准状况下 ×22.4L/mol=1.12LH ,D错误;
2
2
3CuS16H4NO 6Cu23S4NO8HO,Y为S单质,则NO为还原产物、Y为氧化产物,
2 3 2
故答案为:BC。
B不正确;
14【答案】(1) 坩埚 abd
C.由 5Cu4H SO (浓)=3CuSO Cu S4H O 可知,硫元素从+6价降低到-2价时表现氧化性,则参 (2) 恒压滴液漏斗 冷凝回流反应物,提高反应物的转化率或利用率 水浴加热 加快反应速
2 4 4 2 2
加反应的浓硫酸中,表现氧化性的占25%,C正确; 率,同时抑制生成的GeCl 水解
4
D.由 5Cu4H SO (浓)= 3CuSO Cu S4H O 知,3molCu生成0.6molCu 2 S,0.6molCu 2 S发生反应 (3)GeCl 4 +(n+2)H 2 O=GeO 2 •nH 2 O+4HCl
2 4 4 2 2
第 11 页 共 15 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
(4)60.7 (3)
【解析】 由分析可知,“步骤4”生成GeO ·nH O反应即GeCl 和高纯水反应生成GeO ·nH O和HCl,该反应
2 2 4 2 2
【分析】 的化学方程式为:GeCl +(n+2)H O=GeO •nH O+4HCl,故答案为:
4 2 2 2
本题为工艺流程题,是用锗石矿来制备Ge,先进行步骤1焙烧,原理为: GeCl +(n+2)H O=GeO •nH O+4HCl;
4 2 2 2
焙烧
4[Cu S·FeS·GeS ]+27O 8CuO+2Fe O +4GeO +16SO ,然后再GeO 粗品中加入浓盐酸,主要反 (4)
2 2 2 2 3 2 2 2
查阅资料得知:“步骤4”生成的GeO ·nH O实为GeO ·H O,其在5.0mol·L-1的盐酸中溶解度最小,
应为:GeO +4HCl=GeCl +2H O,已知GeCl 的熔点:-49.5℃,沸点:82℃,密度:1.9g·cm-3,则通 2 2 2 2
2 4 2 4
取10.0mLGeCl 和高纯水反应,欲使GeO ·H O的产率最高,则根据反应方程式:
过步骤3粗馏得到GeCl 精品,步骤4中精品GeCl 与高纯水反应得到GeO ·nH O,反应原理为: 4 2 2
4 4 2 2
GeCl +(n+2)H O=GeO •nH O+4HCl,步骤5为加热使GeO ·nH O失去结晶水变为高纯GeO ,最后
4 2 2 2 2 2 2
用H 还原GeO 可得高纯Ge,据此分析解题。
2 2
(1)
在实验室中,若焙烧锗石矿,焙烧固体应将样品放在坩埚中灼烧,由分析可知,产生的气体为SO
2
,
可知,n=0.3535mol,
0.3535
×103 =70.7mL,则加入高纯水的体积约为70.7-10.0=60.7mL,故答案为:
5
据此分析解题:
60.7。
a.SO 能够被NaOH溶液完全吸收,干燥管能够防止倒吸,a符合题意;
2 15【答案】(1) 2MnO+16H++10Cl=2Mn2++5Cl +8H O 饱和食盐
4 2 2
b.SO 能够被酸性高锰酸钾溶液完全吸收,双球管能够防止倒吸,b符合题意;
2 水 SiCl 极易水解,故装置E、F之间需连接盛有浓硫酸的集气
4
c.虽然苯能够防止倒吸,但SO 不能被水完全吸收,c不合题意;
2 瓶装置
d.SO 能够被碱石灰完全吸收,d符合题意;
2 (2) 三颈烧瓶 平衡压强,使液体能够顺利滴落
故答案为:坩埚;abd;
SiCl +4CH CO OCH COO Si+4CH COCl 打开活塞,抽真空,以除去烧瓶中多余的液
4 3 2 3 4 3
(2)
体 重结晶
①由题干实验装置图可知,仪器a的名称是恒压滴液漏斗,仪器b即球形冷凝管的作用是冷凝回流反
【解析】
应物,提高反应物的转化率或利用率,本实验需控制温度为40℃,故加热采用的方式为水浴加热,故
【分析】
答案为:恒压滴液漏斗;冷凝回流反应物,提高反应物的转化率或利用率;
装置A中,高锰酸钾和浓盐酸反应,制取氯气;装置A中所制备的氯气中含有水蒸气和氯化氢,故需
②用浓盐酸而不用稀盐酸处理GeO 粗品的原因是浓度越大反应速率越快,同时增大溶液酸性,抑制
2
先除去氯化氢,后除去水蒸气,则装置B用于除去氯化氢,即B中盛放饱和食盐水,C中盛放浓硫酸;
GeCl 水解,故答案为:加快反应速率,同时抑制生成的GeCl 水解;
4 4
第 12 页 共 15 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
装置D中氯气、二氧化硅和C反应,生成SiCl 和CO;装置E,用于收集SiCl ;装置F,用于收集 16【答案】(1)bghefcd(dc)efi或bghefed(dc)i
4 4
CO,进行尾气处理。 (2)反应前为排尽装置内的空气,防止过氧化钠或NO与其反应;反应后为排尽装置内NO,防止拆卸
(1) 装置时污染环境
①装置A中,高锰酸钾和浓盐酸反应,制取氯气,离子方程式为: (3)除去挥发的HNO 并将生成的NO 转化为NO
3 2
2MnO+16H++10Cl=2Mn2++5Cl +8H O ,故答案为:2MnO+16H++10Cl=2Mn2++5Cl +8H O ; (4)2NO 2 +Na 2 O 2 =2NaNO 3
4 2 2 4 2 2
②装置A中所制备的氯气中含有水蒸气和氯化氢,故需先除去氯化氢,后除去水蒸气,则装置B用于 (5)3MnO- 4 +5NO+4H+=3Mn2++5NO 3 -+2H 2 O
除去氯化氢,即B中盛放饱和食盐水,故答案为:饱和食盐水; (6)95.8%
③由题意可知,装置D中氯气、二氧化硅和C反应,生成SiCl 和CO,化学方程式为 【解析】
4
【分析】
,故答案为 :;
本实验先用稀硝酸与Cu反应制取NO,反应方程式为:3Cu+8HNO (稀)=3Cu(NO ) +2NO↑+4H O,
④由于SiCl 极易水解,故装置E、F之间需连接盛有浓硫酸的集气瓶装置,防止装置F中的水蒸气进 3 3 2 2
4
结合提示2NO+Na O ═2NaNO ,2NO +Na O ═2NaNO 可知,为保证产品纯度,应避免二氧化氮产生,
入装置E中,降低SiCl 产率,故答案为:SiCl 极易水解,故装置E、F之间需连接盛有浓硫酸的集 2 2 2 2 2 2 3
4 4
故反应开始前打开止水夹K,通入氮气排除装置内的空气,用盛水的洗气瓶为进一步保障除去二氧化
气瓶装置;
氮,盛有浓硫酸的洗气瓶的作用为干燥NO,防止水蒸气与过氧化钠反应产生氧气进而影响产品纯度,
(2)
最后盛放酸性高锰酸钾用于除去过量的NO防止污染环境,据此分析答题。
①仪器a的名称为三颈烧瓶;恒压漏斗中的支管作用为平衡压强,使液体能够顺利滴落,故答案为:
(1)
三颈烧瓶;平衡压强,使液体能够顺利滴落;
本实验利用反应2NO+Na O =2NaNO 制备亚硝酸钠,首先利用铜与浓硝酸反应制备NO ,用水除去
②SiCl 和(CH CO) O 反应,生成(CH COO) Si和CH COCl,化学方程式为: 2 2 2 2
4 3 2 3 4 3
挥发的HNO 并将生成的NO 转化为NO,用浓硫酸干燥NO,反应后用酸性高锰酸钾吸收未反应的
3 2
SiCl +4CH CO OCH COO Si+4CH COCl,故答案为:
4 3 2 3 4 3
NO气体,防止污染空气,连接顺序为bghefed(dc)efi或bghefcd(dc)i,故答案为:bghefed(dc)efi或
SiCl +4CH CO OCH COO Si+4CH COCl;
4 3 2 3 4 3 bghefcd(dc)i;
③由题意中SiCl 和(CH CO) O的反应为放热反应,反应后反应混合物带色,并开始析出(CH COO) Si, (2)
4 3 2 3 4
则完成反应后,将反应混合液放置数日,再用干冰-丙酮浴冷却后,此时(CH COO) Si析出,将导管伸 反应前为排尽装置内的空气,防止过氧化钠或NO与其反应;反应后为排尽装置内NO,防止拆卸装
3 4
入液面以下,打开活塞,抽真空,以除去烧瓶中多余的液体;若得到较纯的(CH COO) Si,下一步的 置时污染环境,故答案为:反应前为排尽装置内的空气,防止过氧化钠或NO与其反应;反应后为排
3 4
操作为重结晶,故答案为:打开活塞,抽真空,以除去烧瓶中多余的液体;重结晶。 尽装置内NO,防止拆卸装置时污染环境;
第 13 页 共 15 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
(3) 【解析】
水的作用是除去挥发的HNO 并将生成的NO 转化为NO,故答案为:除去挥发的HNO 并将生成的 【分析】
3 2 3
NO 2 转化为NO; A中亚硫酸钠和70%硫酸反应制备二氧化硫气体,为防止Na S O 遇水发生强烈反应,前后都通过浓
2 2 4
(4)
硫酸干燥二氧化硫气体,然后通入B中生成Na S O ,最后通入C中尾气吸收。
2 2 4
未通入过量氮气,NO会与空气中的氧气反应,生成NO 气体,硬质玻璃管中发生的副反应为
2
(1)
2NO +Na O =2NaNO ,故答案为:2NO +Na O =2NaNO ;
2 2 2 3 2 2 2 3
Na S O 中S为+3价,故在空气中被氧化生成两种常见酸式盐为NaHSO 和NaHSO 。
(5) 2 2 4 3 4
酸性高锰酸钾溶液可氧化NO气体,反应的离子方程式为3MnO-+5NO+4H+=3Mn2++5NO-+2H O,故 (2)
4 3 2
根据分析可知,按气流方向,上述各仪器口的连接顺序为a→bcef d(或
答案为:3MnO-+5NO+4H+=3Mn2++5NO-+2H O;
4 3 2
ef bcef d )。装置B中二氧化硫、甲酸和氢氧化钠反应的化学方程式
(6)
根据反应ArNH
2
十NaNO
2
十2HCl=[Ar-N≡N]Cl+NaCl+2H
2
O,可知NaNO
2
~2HCl,设NaNO
2
的浓度
为HCOOH+NaOH=HCOONa+H O, (或
2
1 2
为c,可得 ,得c=0.2000mol/L,亚硝酸钠的含量
25.00mLc 0.5000molL20.00mL HCOOH+2SO +2NaOH=Na S O +CO +2H O )。
2 2 2 4 2 2
0.2000mol/L0.025L69g/mol
= 100%≈95.8%,故答案为:95.8%。
0.36g (3)
17【答案】(1)NaHSO 和NaHSO 因Na S O 具有较强的还原性,为防止Na S O 被氧化,先从b口通入一段时间N ,排尽装置中的空
3 4 2 2 4 2 2 4 2
(2) bcef d(或ef bcef d ) 气。通入SO 一段时间,发生上述反应,产生不溶于乙醇的淡黄色固体Na S O 和产生大量气泡。
2 2 2 4
HCOOH+NaOH=HCOONa+H O, (或 (4)
2
因Na S O 遇水发生强烈反应,装置D中浓硫酸的作用为阻止装置C中水蒸气进入装置B中,避免生
HCOOH+2SO +2NaOH=Na S O +CO +2H O ) 2 2 4
2 2 2 4 2 2
成的Na S O 与水反应。
(3) 排尽装置中的空气,防止连二亚硫酸钠被氧化 有黄色晶体析出,并产生大量气泡 2 2 4
(4)阻止装置C中水蒸气进入装置B中,避免生成的Na S O 与水反应 (5)
2 2 4
因Na S O 具有较强的还原性,不溶于乙醇,易溶于氢氧化钠溶液,遇水发生强烈反应,故选甲醇为
(5)A 2 2 4
(6)83.5% 洗涤剂。
第 14 页 共 15 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
(6)
25.00mL溶液消耗K Fe(CN) 的物质的量为0.10mol/L×0.024mL=0.0024mol,则200mL溶液消耗
3 6
K Fe(CN) 的物质的量为0.0192mol,根据2Fe(CN) 3- +S O2+4OH-=2Fe(CN) 4- +2SO2+2H O可
3 6 6 2 4 6 3 2
第( )套化学暑假必刷密卷专用反思表
得Na S O 的物质的量为0.0096mol,则样品中Na S O 的质量分数为
2 2 4 2 2 4
填表时间:2022 年__月___日,__:__;反思人:___________家长签字:_____________
0.0096mol174g/mol
100%83.5% 。 本套暴露的主要问题
2.0g
板块 该板块失分 对每一分失分的原因反思
单项选 总分27 分
择题 丢了( )分
双选题 总分16 分
丢了( )分
主观题 总分57 分
丢了( )分
本套题的主要收获
知识上
的收获
技巧上
的收获
本套题的综合反思
做题状
态
做题结
果
自我提
醒
第 15 页 共 15 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!