文档内容
审慎 、规范、速度 扎实备考每一天,铸就高考新辉煌! 衡水泰华决胜二三高考化学暑假必刷密卷新高考版
衡水泰华中学决胜高考化学暑假必刷密卷 第6套 D.氢氧化铁胶体中滴加少量稀硫酸:Fe(OH) +H+=Fe3++3H O
3 2
组编人:张莹莹
做题时间:2022年 月 日, : —— :
校对人:张云暖
3.(2022·上海宝山·二模)下列离子在溶液中因发生氧化还原反应而不能大量共存的是
审核人:王立明
A.H O+、NO-、Fe2+、Na+ B.Ag+、NO-、Cl-、K+
实际得分: 家长签字(严禁代签): 3 3 3
C.K+、Ba2+、OH-、SO2- D.Cu2+、NH+、Br-、OH-
4 4
励志格言:
4.(2022·天津·模拟预测)常温下,下列各组离子在指定溶液中可能大量共存的是
既然我已经踏上这条道路,那么,任何东西都不应妨碍我沿着这条路走下去
--康德 A.麦芽糖溶液中:MnO、K+、H+、SO2
4 4
本套亮点:汇集非金属元素各地最新模拟题,考察了离子共存,方程式书写,离子浓
度计算等高考常见知识点。 B.含有大量Fe3+的溶液中:Al3+、CO2、NH、Br-
3 4
注意事项:
1, 本套密卷满分100分,做题所需时间75分钟; C.pH=0的溶液中:K+、Na+、SO2、S O2
4 2 3
2, 请一律用0.5或以上的黑色中性签字笔在规定的答题纸上做答,注意书写规范;
3,做题不改错,等于没有做!做完之后,要求依照答案用红笔自判所有主客观题,并 D.水电离出来的c(H+)=10-13mo/L的溶液:K+、CO2、Br-、AlO
3 2
算出总得分,请家长签字确认,并在积累本进行认真的错题整改反思,并把本套题的
主要收获、主要不足和反思写到每套题所附的反思纸上,开学上交。
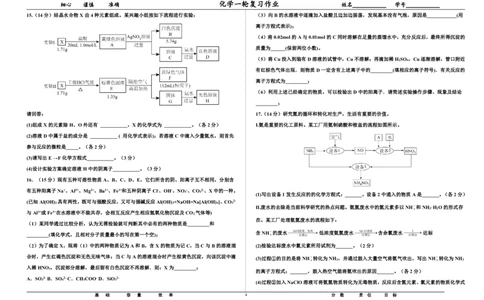
5.(2022·湖南·模拟预测)某盐M由两种阳离子和一种阴离子构成,为了确定M的组成,进行
一、单项选择题本题共9小题,每小题3分,共27分。在每小题给出的四个选项中,只有一项是 如图实验:
符合题目要求的。
1.(2022·湖南·涟源市第一中学三模)常温下,下列各组离子在指定溶液中一定能大量共存的是
A.水电离的c(H+)=1×10−13mol·L−1的溶液中:K+、Na+、AlO、CO2
2 3
B.0.1mol·L−1KI溶液中:Na+、NH+、ClO−、OH−
4
下列说法正确的是
c
H
Δ
C.
c OH
11012的溶液中:K+、Na+、CO
3
2、NO
3
A.加入NaOH溶液的离子反应为NH
4
+OH- NH
3
↑+H
2
O
B.上述白色沉淀是BaSO
4
D.能使酚酞变红的溶液中:Na+、NH+、SO2、HCO
4 4 3
C.加入氯水发生的离子反应为Fe2++Cl =2Cl-+Fe3+
2
2.(2022·福建·模拟预测)下列关于离子反应的说法正确的是
D.M可能是NH Fe(SO )
4 4 2
A.水电离的c(H+)=10-2mol·L-1的溶液中:Na+、Mg2+、Cl-、HCO可以大量共存
3
B.1mol·L-1的纯碱溶液中:K+、Fe2+、Cl-、NO可以大量共存
3
C.小苏打溶液中通入氨气:HCO+NH ·H O=NH+CO2+H O
3 3 2 4 3 2
可能用到的相对原子质量:C-12 H-1 O-16 N-14 S-32 P-31 Cl-35.5 Si-28 F-19 Br-80 I-127 Na-23 Mg-24 Al-27 K-39 Ca-40 Cu-64 Fe-56 Ba-137 Ag-108 第1讲,第2套,第1页化学一轮复习作业
细心 谨慎 准确 姓名 学号
6.(2022·天津·模拟预测)某溶液可能含有Cl-、SO2-、CO2-、NH+、Fe3+、Al3+和K+。取该溶液100mL, 二、不定项选择题:本题共4小题,每小题4分,共16分。在每小题给出的四个选项中,有一项
4 3 4
加入过量NaOH溶液加热,得到0.02mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得1.6g 或两项符合题目要求。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两
个选项,只选一个且正确得2分,选两个且都正确的得4分,但只要选错一个,该小题得0分。
固体;向上述滤液中加足量BaCl 溶液,得到4.66g不溶于盐酸的沉淀。有关原溶液中说法不正确
2
的是
10.(2021·浙江·模拟预测)固体M由Fe
2
SO
4
3
、Fe、KBr、K
2
SO
3
、AgNO
3
和BaCl
2
中的几种
A.至少存在4种离子 B.Cl-一定存在,且c(Cl-)≥0.4mol / L 或全部物质组成。①取少量M加足量稀H SO 产生气体X、溶液Y和白色固体Z。向溶液Y中加
2 4
C.SO2-、NH+、Fe3+一定存在,Al3+、K+、Cl-可能存在
4 4
少量稀AgNO 溶液,产生白色沉淀(Ag SO 是微溶物,浓度较小时不会沉淀);②另取少量Y,加
3 2 4
D.SO2-、NH+、Fe3+、Cl-一定存在,CO2-一定不存在
4 4 3
入足量NaOH溶液产生白色沉淀,一段时间后颜色变深。下列说法正确的是
7.(2022·上海嘉定·一模)实验室需配制一种仅含四种离子(不包括水电离出的离子并忽略水解)
A.气体X一定是SO 或H B.M中一定含有Fe SO
2 2 2 4 3
的混合溶液,且在混合液中四种离子的物质的量浓度均为0.5mol•L-1,下面四个选项中能达到此目
的是
C.M中一定不含KBr,一定有BaCl
2
D.Z一定是BaSO
4
A.Fe2+、Na+、NO-、Cl- B.Mg2+、NH+、SO2-、NO-
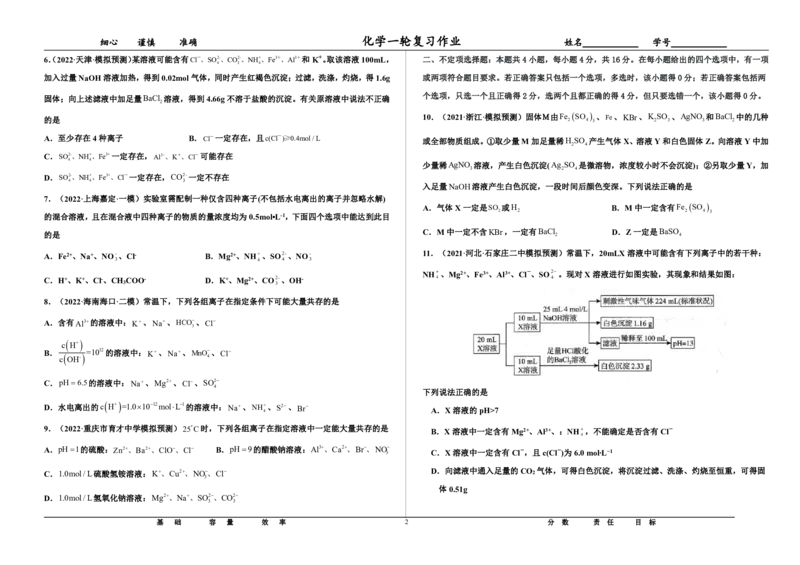
11.(2021·河北·石家庄二中模拟预测)常温下,20mLX溶液中可能含有下列离子中的若干种:
3 4 4 3
NH、Mg2+、Fe3+、Al3+、Cl-、SO2。现对X溶液进行如图实验,其现象和结果如图:
C.H+、K+、Cl-、CH COO- D.K+、Mg2+、CO2-、OH- 4 4
3 3
8.(2022·海南海口·二模)常温下,下列各组离子在指定条件下可能大量共存的是
A.含有Al3的溶液中:K、Na、HCO、Cl
3
c
H+
B.
c OH-
=1012的溶液中:K、Na、MnO
4
、Cl
C.pH6.5的溶液中:Na、Mg2、Cl、SO2
4
下列说法正确的是
D.水电离出的c H+ =1.01012molL1的溶液中:Na、NH
4
、S2、Br
A.X溶液的pH>7
9.(2022·重庆市育才中学模拟预测)25C时,下列各组离子在指定溶液中一定能大量共存的是 B.X溶液中一定含有Mg2+、Al3+、:NH,不能确定是否含有Cl-
4
A.pH1的硫酸:Zn2、Ba2、ClO、Cl B.pH9的醋酸钠溶液:Al3、Ca2、Br、NO
3
C.X溶液中一定含有Cl-,且c(Cl-)为6.0mol∙L−1
C.1.0mol/L硫酸氢铵溶液:K、Cu2、NO、Cl D.向滤液中通入足量的CO 2 气体,可得白色沉淀,将沉淀过滤、洗涤、灼烧至恒重,可得固
3
体0.51g
D.1.0mol/L氢氧化钠溶液:Mg2、Na、SO2、CO2
3 3
基 础 容 量 效 率 2 分 数 责 任 目 标化学一轮复习作业
细心 谨慎 准确 姓名 学号
12.(2020·山东青岛二模)化学上常用标准电极电势数据φθ(氧化型/还原型)比较物质氧化能力。φθ值
三、非选择题:共57分,第14~16题为必考题,每个试题考生都必须作答。第17~18题为选考题,
越高,氧化型的氧化能力越强。利用表格所给数据分析,以下说法的错误的是( )
考生根据要求作答。
氧化型
φθ(Co3+/Co2+) φθ(HClO/Cl-)
14.(14分)现有四种溶液m,n,p、q,分别含阴阳离子NH、Na、Ba2、Al3、 OH 、SO2、
/还原型 4 4
酸性介质 1.84V 1.49V HCO、NO中的各一种,为了确定组成,进行了以下实验:将四种溶液两两混合,发现m、n能
3 3
氧化型 φθ[Co(OH)
3 φθ(ClO-/Cl-) 剧烈反应,产生白色沉淀和无色气体,p、q能产生无色有刺激性气味的气体,p与m,n均有沉
/还原型 /Co(OH)
2
]
淀产生,且在m中逐滴滴入p时,沉淀增多,后减少但没有完全消失。回答下列问题。
碱性介质 0.17V x
(1)p是________,q是_________(均填化学式)。(各1分)
A. 推测:x<1.49V (2)写出在m中逐滴滴入p,沉淀减少时发生反应的离子方程式__________。(2分)
B.Co O 与浓盐酸发生反应:
3 4 (3)实验室检验q中阳离子需要的试剂和试纸是___________。(2分)
Co O +8H+===Co2++2Co3++4H O
3 4 2
(4)经分析,SO2存在于_________(填m、n、p、q)溶液中,实验室常用重量法检验该溶液中SO2
C. 碱性条件下可发生反应: 4 4
2Co(OH) +NaClO+H O===2Co(OH) +NaCl 离子的浓度,步骤如下:Ⅰ用量筒取该溶液8.0mL并转移至小烧杯中;Ⅱ加入盐酸酸化,然后加
2 2 3
D. 与元素Co同周期同族元素中,第三电离能I 最小的是Fe
3 入足量的BaCl 溶液(沉淀反应在接近沸腾的温度下进行);Ⅲ过滤所得沉淀;洗涤,烘干后得到ag
2
13.(2022·湖南·模拟预测)宏观辨识与微观探析是化学学科核心素养之一。下列实验对应的离子
固体。(1分)
方程式正确的是
①所用量筒的规格为___________。(2分)
A.用食醋和淀粉碘化钾溶液检验加碘盐中含KIO 3 :5IIO 3 6H 3I 2 3H 2 O A.10mL B.50mL C.100mL D.500mL
B.用酸性KMnO 溶液除去CO 中的SO :5SO 2H O2MnO5SO22Mn 24H ②过滤时,沉淀物颗粒的大小会影响过滤速度,从利于过滤的角度分析,沉淀反应需要在接近沸
4 2 2 2 2 4 4
腾的温度下进行的原因可能是__________。(2分)
C.用足量Na CO 溶液吸收尾气Cl :Cl CO2 ClClOCO
2 3 2 2 3 2
③检验沉淀洗涤干净的方法是___________。(2分)
电解
D.用Al作电极电解NaCl溶液:2Cl2H O 2OHH Cl ④计算,硫酸根的浓度为___________mol/L(用含a的式子表示)。(1分)
2 2 2
基 础 容 量 效 率 3 分 数 责 任 目 标化学一轮复习作业
细心 谨慎 准确 姓名 学号
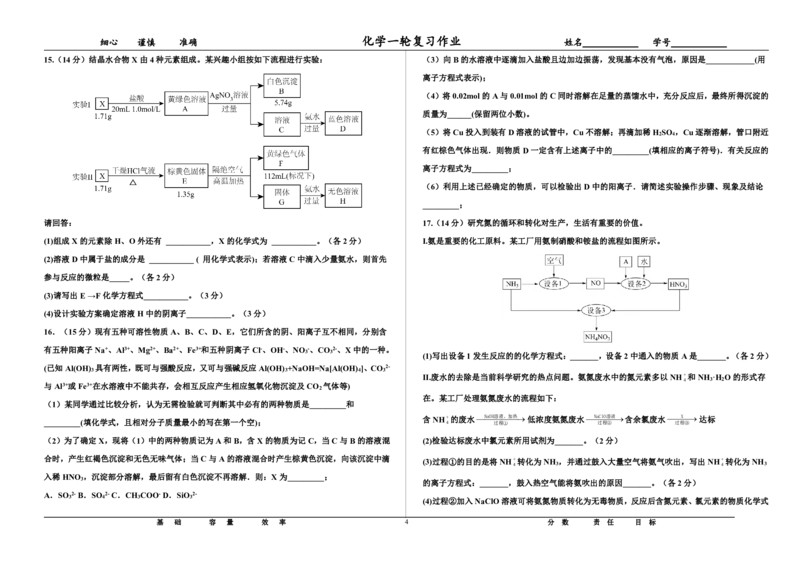
15.(14分)结晶水合物X由4种元素组成。某兴趣小组按如下流程进行实验: (3)向B的水溶液中逐滴加入盐酸且边加边振荡,发现基本没有气泡,原因是____________(用
离子方程式表示);
(4)将0.02mol的A与0.01mol的C同时溶解在足量的蒸馏水中,充分反应后,最终所得沉淀的
质量为______(保留两位小数)。
(5)将Cu投入到装有D溶液的试管中,Cu不溶解;再滴加稀H SO ,Cu逐渐溶解,管口附近
2 4
有红棕色气体出现.则物质D一定含有上述离子中的_________(填相应的离子符号).有关反应的
离子方程式为_________;
(6)利用上述已经确定的物质,可以检验出D中的阳离子.请简述实验操作步骤、现象及结论
_________;
请回答: 17.(14分)研究氮的循环和转化对生产,生活有重要的价值。
(1)组成X的元素除H、O外还有 ___________,X的化学式为 ___________。(各2分) I.氨是重要的化工原料。某工厂用氨制硝酸和铵盐的流程如图所示。
(2)溶液D中属于盐的成分是 ___________( 用化学式表示);若溶液C中滴入少量氨水,则首先
参与反应的微粒是_____。(各2分)
(3)请写出E→F化学方程式___________。(3分)
(4)设计实验方案确定溶液H中的阴离子___________。(3分)
16.(15分)现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含
有五种阳离子Na+、Al3+、Mg2+、Ba2+、Fe3+和五种阴离子Cl-、OH-、NO -、CO 2-、X中的一种。
3 3 (1)写出设备1发生反应的的化学方程式:_______,设备2中通入的物质A是_______。(各2分)
(已知Al(OH) 具有两性,既可与强酸反应,又可与强碱反应Al(OH) +NaOH=Na[Al(OH) ]、CO 2-
3 3 4 3
II.废水的去除是当前科学研究的热点问题。氨氮废水中的氮元素多以NH和NH ·H O的形式存
4 3 2
与Al3+或Fe3+在水溶液中不能共存,会相互反应产生相应氢氧化物沉淀及CO 气体等)
2
在。某工厂处理氨氮废水的流程如下:
(1)某同学通过比较分析,认为无需检验就可判断其中必有的两种物质是_________和
_________(填化学式,且相对分子质量最小的写在第一个空);
含NH
4
的废水NaOH
过
溶
程
液
①
、加热 低浓度氨氮废水Na
过
Cl
程
O溶
②
液含余氯废水
过
程
X
③
达标
(2)为了确定X,现将(1)中的两种物质记为A和B,含X的物质为记C,当C与B的溶液混 (2)检验达标废水中氯元素所用试剂为_______。(2分)
合时,产生红褐色沉淀和无色无味气体;当C与A的溶液混合时产生棕黄色沉淀,向该沉淀中滴 (3)过程①的目的是将NH转化为NH ,并通过鼓入大量空气将氨气吹出,写出NH转化为NH
4 3 4 3
入稀HNO ,沉淀部分溶解,最后留有白色沉淀不再溶解.则:X为_________;
3 的离子方程式:_______,鼓入热空气能将氨吹出的原因_______。(各2分)
A.SO 2-B.SO 2-C.CH COO-D.SiO 2-
3 4 3 3 (4)过程②加入NaClO溶液可将氨氮物质转化为无毒物质,反应后含氮元素、氯元素的物质化学式
基 础 容 量 效 率 4 分 数 责 任 目 标化学一轮复习作业
细心 谨慎 准确 姓名 学号
分别为_______、_______。(各1分)
(2)____________________________________________( 用化学式表示);____________________
(5)含余氯废水的主要成分是NaClO及HClO,X可选用以下_______溶液以达到去除余氯的目的(填
(3)____________________________________________________________。(3分)
字母)。(1分)
(4)____________________________________________________________。(3分)
a.KOH b.Na SO c.KMnO d.NaCl
2 3 4
写出该物质除去HClO的离子方程式:_______。(1分)
16.(15分,除标注外,各2分)
(1)_________________________________和______________________________;(各1分)
(2)_______________________________________;
(3)______________________________________________________________(用离子方程式表示);
(4)_______________________________(保留两位小数)。
假期作业第六套答题纸
(5)________________________(填相应的离子符号)__________________________________;
(6)_________________________________________________________________________;(3分)
14.(14分,除标注外,各2分)
17.(14分,除标注外,各2分)
(1)p是____________________________,q是________________________(均填化学式)。(各1分)
(1)___________________________________,__________________________________________。
(2)离子方程式_____________________________________________________________________。
(2)__________________________________________。
(3)______________________________________。(4)__________________(填m、n、p、q)(1分)
(3)__________________________________________,___________________________________。
①_________________。
(4)______________________________________、_____________________________。(各1分)
②_________________________________________________________________________________。
(5)__________________________________________(填字母)。(1分)
③________________________________________________________________________________。
___________________________________________________________________________。(1分)
④_________________________mol/L(用含a的式子表示)。(1分)
15.(14分,除标注外,各2分)
(1)_______________________________________, _______________________________________。
基 础 容 量 效 率 5 分 数 责 任 目 标化学一轮复习作业
细心 谨慎 准确 姓名 学号
【解析】A.麦芽糖具有还原性,会和酸性高锰酸钾反应,不能大量共存,A错误;B.铁离子、
衡水泰华中学决胜高考化学暑假必刷密卷第六套化学参考答案 铝离子会和碳酸根离子发生双水解反应,不能共存,B错误;C.pH=0的溶液为强酸性,S O2会
2 3
1.【答案】C 和氢离子反应生成硫单质和硫酸根离子,不能共存,C错误;D.水电离出来的c(H+)=10-13mo/L
【解析】A.水电离的c(H+)=1×10−13mol·L−1的溶液中水的电离受到抑制,可能是强酸性也可能是 的溶液,可能为碱性溶液,在碱性溶液中,该四种离子均能存在且相互不反应,可能共存,D正
强碱性,酸性溶液中AlO、CO2不能大量存在,A不符合题意;B.ClO−具有强氧化性,会将 确;故选D。
2 3
5.【答案】B
c
H
I-氧化,且NH+和OH−不能大量共存,B不符合题意;C. 11012的溶液显碱性,四种 【解析】由题干实验图示信息可知,实验1中加入KSCN溶液,无明显现象,加入氯水后,溶液
4 c OH
变红色,说明原溶液中含有Fe2+,实验2中加入浓NaOH溶液加热后产生能使湿润的红色石蕊试
离子相互之间不反应,也不与OH−反应,可以大量共存,C符合题意;D.能使酚酞变红的溶液显 纸变蓝的气体,说明原溶液中含有NH+
4,实验3先加入足量的稀盐酸,无明显现象,在足量的BaCl
2
碱性,NH+、HCO不能在强碱性溶液中大量存在,D不符合题意;综上所述答案为C。
4 3 SO2-
溶液产生白色沉淀,说明原溶液中含有 4 ,由此分析可知,某盐M的组成为(NH 4 ) 2 Fe(SO 4 ) 2 ,
2.【答案】C
据此分析解题。A.由分析可知,原溶液中含有Fe2+和NH+
4,故加入NaOH溶液的离子反应为
【解析】A.水电离的c(H+)=10-2mol·L-1的溶液为盐水解使溶液显较强酸性的溶液或较强碱性溶液,
Δ
Fe2++NH+3OH- NH ↑+H O+Fe(OH) ↓,A错误;B.由分析可知,上述白色沉淀是BaSO ,
HCO在强酸性的溶液或较强碱性溶液中均不能大量共存,A项错误;B.1mol·L-1的纯碱溶液中, 4 3 2 2 4
3
B正确;C.加入氯水发生的离子反应为2Fe2++Cl =2Cl-+2Fe3+,原离子方程式电荷不守恒,C错
2
Fe2+与CO2生成FeCO 沉淀不能大量共存,B项错误;C.小苏打溶液中通入氨气,生成正盐和
3 3
误;D.由分析可知,原溶液中含有Fe2+、不含Fe3+,则M不可能是NH Fe(SO ) ,M的组成为:
4 4 2
水,离子方程式为HCO 3 +NH 3 ·H 2 O=NH 4 +CO 3 2+H 2 O,C项正确;D.胶体粒子带电荷,加 (NH 4 ) 2 Fe(SO 4 ) 2 ,D错误;故答案为:B。
入电解质时会发生聚沉,氢氧化铁胶体中滴加少量稀硫酸(电解质)时,先发生聚沉,生成Fe(OH) 6.【答案】C
3
沉淀,继续加入稀硫酸,才会发生Fe(OH)
3
与H+的反应,生成Fe3+和H
2
O,D项错误;故选C。
【解析】由于加入过量NaOH溶液,加热得到0.02mol气体,说明一定有NH+,且物质的量为
4
3.【答案】A
0.02mol;同时产生红褐色沉淀,说明一定有Fe3+,1.6g固体为氧化铁,物质的量为0.01mol,故
【解析】A.存在水合氢离子,则酸性环境下Fe2+被NO氧化为Fe3+不共存,A选;
3 有0.02molFe3+,一定没有CO2-;4.66g不溶于盐酸的沉淀为硫酸钡,一定有SO2-,物质的量为
3 4
B. Ag+与Cl-生成氯化银沉淀不共存,不是氧化还原反应,B不选;C. Ba2+与SO2 4 生成硫酸 0.02mol;根据电荷守恒,一定有Cl-,至少0.02mol×3+0.02-0.02mol×2=0.04mol,物质的量浓度
钡沉淀不共存,不是氧化还原反应,C不选;D. Cu2+、NH能分别与OH-生成氢氧化铜沉淀和 至少0.04mol÷0.1L=0.4mol/L。A. 由上述分析可知,至少存在Cl-、SO2
4
-、NH+
4
、Fe3+,故A正确;
4
B. 由电荷守恒可知,Cl-一定存在,且c(Cl-)≥0.4mol / L,故B正确;C. Cl-一定存在,故C错
NH ·H O不共存,不是氧化还原反应,D不选;答案:A。
3 2
4.【答案】D 误;D. 由上述分析可知,SO2 4 -、NH+ 4 、Fe3+、Cl-一定存在, CO 3 2-一定不存在,故D正确;故选:
基 础 容 量 效 率 6 分 数 责 任 目 标化学一轮复习作业
细心 谨慎 准确 姓名 学号
C。 溶液Y中一定含有Fe2+,不含Fe3+,原固体M中可能含有Fe,与稀硫酸反应生成Fe2+和H ,也
2
7.【答案】B 可能含有Fe (SO ) ,被亚硫酸根还原为Fe2+;原固体中可能含有AgNO ,酸性条件下的硝酸根具
2 4 3 3
【解析】A.该组离子之间不反应,可大量共存,但物质的量浓度均为0.5mol•L-1,不遵循电荷守 有氧化性,被Fe或亚硫酸根全部还原成NO,银离子则转化成氯化银沉淀,部分可能会转化成硫
恒,故A不选;B.该组离子之间不反应,可大量共存,且物质的量浓度均为0.5mol•L-1,遵循电 酸银沉淀。综上可知固体M中一定有BaCl ,Fe和Fe (SO ) 二者至少含有一种,可能有AgNO
2 2 4 3 3
荷守恒,故B选;C.H+、CH COO-不能大量共存,故C不选;D.Mg2+分别与CO2-、OH-反应, 和K 2 SO 3 ,一定没有KBr;气体X可能是H 2 ,可能是SO 2 ,可能是H 2 和SO 2 混合,可能是H 2
3 3
和NO混合,可能是SO 和NO混合,可能是H 、SO 和NO混合;白色固体Z可能是BaSO ,
不能大量共存,故D不选;故选:B。 2 2 2 4
可能是BaSO 和AgCl,还可能是BaSO 、AgCl和AgSO 。A.气体X可能是H ,可能是SO ,
8.【答案】C 4 4 4 2 2
可能是H 和SO 混合,可能是H 和NO混合,可能是SO 和NO混合,可能是H 、SO 和NO
c
H 2 2 2 2 2 2
【解析】A.Al3与HCO
3
能发生双水解反应,二者不能共存,A不符合题意;B.
c OH
1012的
混合,A项错误;B.M中一定有Fe和Fe 2 (SO 4 ) 3 二者至少含有一种,B项错误;C.根据分析M
中一定有BaCl ,一定没有KBr,C项正确;D.白色固体Z可能是BaSO ,可能是BaSO 和AgCl,
溶液呈酸性,酸性条件下,MnO能氧化Cl,二者不能共存,B不符合题意;C.常温下,pH6.5 2 4 4
4
还可能是BaSO 、AgCl和AgSO ,D项错误。
4 4
的溶液呈弱酸性,Na、Mg2、Cl、SO2可以大量共存,C符合题意;D.常温下,水电离出
4
答案为C。
的c H 1.01012molL1的溶液既可以为酸性溶液又可以为碱性溶液;酸性溶液中,S2-不能大
11.【答案】CD
量存在,碱性溶液中,NH+不能大量存在,D不符合题意;故选C。
【解析】10mLX溶液中加入足量盐酸酸化的氯化钡溶液得到硫酸钡沉淀2.33g,物质的量为0.01mol
4
硫酸钡即硫酸根物质的量为0.01mol,10mLX溶液中加入0.1mol氢氧化钠溶液得到0.01mol氨气
9.【答案】C
即0.01mol铵根离子,生成1.16g氢氧化镁沉淀即物质的量为0.02mol,还剩余氢氧化钠物质的量
【解析】A. pH1的硫酸:酸性条件下次氯酸跟与氯离子反应生成氯气,不能共存,A错误;B.
为0.01mol,根据氢氧根物质的量关系说明还有0.04mol氢氧根与铝离子反应生成偏铝酸根,则铝
pH9的醋酸钠溶液:碱性条件下铝离子会生成氢氧化铝沉淀,B错误;C. 1.0mol/L硫酸氢铵溶
离子物质的量为0.01mol,根据电荷守恒,说明还含有氯离子。A.X溶液中铝离子水解,说明溶
液:K、Cu2、NO、Cl相互之间均不反应,可共存,C正确;D. 1.0mol/L氢氧化钠溶液:镁
3
液显酸性,故A错误;B.X溶液中一定含有Mg2+、Al3+、NH、SO2,根据电荷守恒,还含有
4 4
离子和碳酸根、亚硫酸根会生成碳酸镁、亚硫酸镁沉淀,镁离子与氢氧根也会生成氢氧化镁沉淀,
Cl-,故B错误;C.根据电荷守恒,说明X溶液中一定含有Cl-,n(Cl-)=0.01mol×1+0.02mol×2
D错误; 故选C。
+0.01mol×3-0.01mol×2=0.06mol,则c(Cl-)为6.0mol∙L−1,故C正确;D.滤液中含有偏铝酸
钠溶液,向滤液中通入足量的CO 气体,可得白色沉淀,将沉淀过滤、洗涤、灼烧至恒重,根据
二、不定项选择题(每个小题有1-2个正确选项,共5小题,每题4分,部分分2分,共20分) 2
铝元素守恒可得氧化铝物质的量为0.01mol即0.51g固体,故D正确。
10.【答案】C
综上所述,答案为CD。
【解析】溶液Y中加入少量AgNO 生成白色沉淀,则该沉淀为AgCl,则原固体M中一定含有
3
12. B 解析 因为氧化性:HClO>ClO-,所以电极电势φθ(HClO/Cl-)>φθ(ClO-/Cl-),推
BaCl ,一定不含KBr;溶液Y中加入NaOH溶液,产生白色沉淀,且一段时间后颜色变深,则
2
基 础 容 量 效 率 7 分 数 责 任 目 标化学一轮复习作业
细心 谨慎 准确 姓名 学号
测:x<1.49V,A正确;酸性介质中φθ(Co3+/Co2+)=1.84V>φθ(HClO/Cl-),Co3+要氧化氯离
(1)根据上述分析,p为BaOH ,q为NH NO ,故答案依次为BaOH ,NH NO 。
2 4 3 2 4 3
子,B错误;题中提供信息无法判断x是否大于0.17V,只能根据经验,ClO-/在碱性环境下
(2)m为Al (SO ) ,p为BaOH ,沉淀为氢氧化铝,沉淀减少时的离子方程式为
也具有很强的氧化性判断,C 正确;26 号元素 Fe 基态原子核外电子排布式为 2 4 3 2
1s22s22p63s23p63d64s2,失去 3 个电子变为铁离子时,三价铁离子的电子排布式为 AlOH OH AlO2H O,故答案为AlOH OH AlO2H O。
3 2 2 3 2 2
1s22s22p63s23p63d5,因为三价铁离子处于半满的稳定状态,所以与元素Co同周期同族元素中,
(3)q为NH NO ,则检验NH的方法为:取待测液于试管中,加入浓氢氧化钠溶液,加热,用湿润
4 3 4
第三电离能I 最小的是Fe,D正确。
3
的红色石蕊试纸检验逸出的气体,若试纸变蓝,则原待测液中含NH,故需要的试剂或试纸为氢
13. B 4
三、非选择题(共50分,共5道大题) 氧化钠溶液和红色石蕊试纸,故答案为NaOH溶液,红色石蕊试纸。
14.【答案】(1)BaOH 2 (1分) NH 4 NO 3 (1分) (4)m为Al 2 (SO 4 ) 3 ,故SO2 4 存在于m溶液中;故答案为:m。
(2) AlOH OH AlO2H O (2分)
①量筒量取液体时,所选规格遵循“近而大”的原则,故选规格为10mL的量筒;故答案选A。
3 2 2
②过滤时,沉淀物颗粒的大小会影响过滤速度,颗粒较大,有利于液体顺利滤出,故沉淀过程在
(3)NaOH溶液(1分) 红色石蕊试纸 (1分)
接近沸腾的温度下进行,是为了尽量使沉淀凝聚,即有利于产生颗粒较大的沉淀,或有利于晶体
(4)m(1分) ①A (1分)
生长。
②沸腾时,有利于产生颗粒较大的沉淀或有利于晶体生长(2分)
③检验沉淀是否洗涤干净,本质就是沉淀表面是否仍有可溶性离子残留,即是否有Cl-残留,故方
③用小试管取最后-次洗涤液少许,向其中加入少量的AgNO 溶液,如没有浑浊,说明沉淀洗涤干
3
法是,取最后一次洗涤液少许于试管中,向其中加入少量的AgNO 溶液,如没有浑浊,说明沉淀
3
净,反之,说明沉淀没有洗涤干净(2分)
洗涤干净,反之,说明沉淀没有洗涤干净,故答案为:用小试管取最后-次洗涤液少许,向其中加
125a
④ (2分)
233
入少量的AgNO 溶液,如没有浑浊,说明沉淀洗涤干净,反之,说明沉淀没有洗涤干净。
3
【解析】由m中逐滴滴入p时,沉淀增多,后减少但没有完全消失,可知在现有离子中,能满足
a
④烘干后的固体成分仍为BaSO ,硫元素守恒,故8.0mL溶液,n(SO2)=n(BaSO )= mol,则
先沉淀后部分溶解现象的,一定是向铝盐溶液中逐滴滴入强碱溶液,故m为可溶性铝盐,p为强 4 4 4 233
n 125a 125a
碱,再结合碱过量,沉淀未溶解完全,说明强碱与铝盐混合,除了有氢氧化铝生成,还有其他沉 c(SO2)= = mol/L;故答案为 。
4 V 233 233
淀生成,则可判断出m为Al 2 (SO 4 ) 3 ,p为BaOH 2 ,则p、q能产生无色有刺激性气味的气体,q 15.【答案】(1)Cu、Cl(2分) CuCl 2 ∙2H 2 O(2分)
(2)NH NO 、Ag(NH ) NO 、Cu(NH ) (NO ) (2分) H+(2分)
含NH,m、n能剧烈反应,产生白色沉淀和无色气体,符合铝离子与HCO双水解生成氢氧化铝 4 3 3 2 3 3 4 3 2
4 3
隔绝空气
和二氧化碳的现象,则n含HCO,由于所剩离子仅为Na和NO,溶液呈电中性,故q为NH NO , (3)2CuCl 2 Cl 2 ↑+2CuCl(2分)
3 3 4 3 高温
n为NaHCO 。
3 (4)取少量H溶液,滴加酚酞,若变红,则含有OH-;另取少量H溶液,加入硝酸酸化,再加硝酸
基 础 容 量 效 率 8 分 数 责 任 目 标化学一轮复习作业
细心 谨慎 准确 姓名 学号
银溶液,若有白色沉淀生成,则含有Cl-(2分) 16.16.【答案】Na CO Ba(OH) B CO 2-+H+=HCO -
2 3 2 3 3
【解析】由实验Ⅰ可知,溶液C中加入过量氨水,生成蓝色沉淀D,则D中含有[Cu(NH ) ]2+,X 6.09g NO - 3Cu+8H++2NO -=3Cu2++2NO↑+4H O 往D的溶液中逐渐加入Ba(OH) 溶液
3 4 3 3 2 2
中含有铜元素;白色沉淀B为AgCl,n(AgCl)=
5.74g
0.04mol,20mL1.0mol/L盐酸中所含
直至过量,若先出现白色沉淀后又逐渐溶解,则D中含有Al3+,E中含有Mg2+.(或往D的溶液
143.5g/mol
中加入适量Na CO 溶液若产生了白色沉淀和无色无味的气体,则D中含有Al3+,E中含有Mg2+)
Cl-的物质的量为0.02mol,则X中所含Cl-的物质的量为0.04mol-0.02mol=0.02mol,从而得出X 2 3
【解析】
中含有CuCl ,其物质的量为0.01mol。
2
(1)因阳离子中Al3+、Mg2+、Ba2+、Fe3+均不能与CO 2-共存,所以CO 2-只能与Na+结合成Na CO
0.36g 3 3 2 3
由实验Ⅱ可知,结晶水的质量为1.71g-1.35g=0.36g,物质的量为 0.02mol,CuCl 的物质
2
18g/mol
存在,又因Al3+、Mg2+、Fe3+均不能与OH-共存,所以OH-只能与Ba2+结合成Ba(OH) 存在,则
2
0.112L
的量为0.01mol,生成Cl
2
的物质的量为 0.005mol,则固体G为CuCl。综合实验Ⅰ、
必有Na CO 、Ba(OH) ;(2)当C与B的溶液混合时,产生红褐色沉淀和无色无味气体,很明
22.4L/mol 2 3 2
Ⅱ,X的化学式为CuCl ∙2H O。 显是Fe3+与CO 2-发生双水解的现象,不难得出B为Na CO ,A为Ba(OH) ,C中有Fe3+,又因
2 2 3 2 3 2
(1)由以上分析可知,组成X的元素除H、O外还有Cu、Cl,X的化学式为CuCl ∙2H O。答案为: C与A反应产生的白色沉淀不溶于稀HNO ,则C为Fe (SO ) ,故答案为B;(3)B为碳酸钠溶
2 2 3 2 4 3
Cu、Cl;CuCl ∙2H O; 液,滴加稀盐酸生成了NaHCO ,因此无气泡,离子反应为CO 2-+H+=HCO -;(4)0.02mol的
2 2 3 3 3
(2)由分析可知,溶液C中含有过量的AgNO 、Cu(NO ) 、HNO 等,加入过量氨水,AgNO 最终 Ba(OH) 与0.01mol的Fe (SO ) 反应,即0.02molBa2+、0.04molOH-、0.02molFe3+、0.03molSO 2-,
3 3 2 3 3 2 2 4 3 4
生成Ag(NH ) NO ,Cu(NO ) 最终生成Cu(NH ) (NO ) ,另外还有NH NO 生成,则溶液D中属 故生成0.02molBaSO 和0.04/3molFe(OH) 沉淀,计算得沉淀质量约为
3 2 3 3 2 3 4 3 2 4 3 4 3
于盐的成分是NH NO 、Ag(NH ) NO 、Cu(NH ) (NO ) ;若溶液C中滴入少量氨水,则首先与 0.02mol×233g/mol+0.04/3mol×107g/mol=6.09g;(5)将Cu投入到装有D溶液的试管中,Cu不溶
4 3 3 2 3 3 4 3 2
HNO 反应,所以首先参与反应的微粒是H+。答案为:NH NO 、Ag(NH ) NO 、Cu(NH ) (NO ) ; 解;再滴加稀H SO ,Cu逐渐溶解,管口附近有红棕色气体出现,说明D中含有的阴离子应具有
3 4 3 3 2 3 3 4 3 2 2 4
H+; 强氧化性,应为NO -,反应的离子方程式为3Cu+8H++2NO -=3Cu2++2NO↑+4H O;(6)D,E中
3 3 2
隔绝空气 的阳离子为Al3+、Mg2+,检验Al3+,可逐渐加入Ba(OH) 溶液直至过量,若先出现白色沉淀后又
2
(3)由分析知,E为CuCl 、F为Cl ,则E→F化学方程式为2CuCl Cl ↑+2CuCl。答案
2 2 2 2
高温 逐渐溶解,因Al3+易水解,也可加入Na CO 溶液,若产生了白色沉淀和无色无味的气体;往D
2 3
隔绝空气 的溶液中逐渐加入Ba(OH) 溶液直至过量,若先出现白色沉淀后又逐渐溶解,则D中含有Al3+,
2
为:2CuCl Cl ↑+2CuCl;
2 2
高温 E中含有Mg2+.(或往D的溶液中加入适量Na CO 溶液若产生了白色沉淀和无色无味的气体,则
2 3
(4)固体G为CuCl,加入过量氨水,则溶液H中所含阴离子可能为Cl-、OH-,确定溶液H中的阴 D中含有Al3+,E中含有Mg2+)。
离子的方法是:取少量H溶液,滴加酚酞,若变红,则含有OH-;另取少量H溶液,加入硝酸酸 催化剂
17.(1) 4NH +5O 4NO+6H O 空气或O
3 2 2 2
化,再加硝酸银溶液,若有白色沉淀生成,则含有Cl-。答案为:取少量H溶液,滴加酚酞,若变
红,则含有OH-;另取少量H溶液,加入硝酸酸化,再加硝酸银溶液,若有白色沉淀生成,则含 (2)硝酸和硝酸银
有Cl-。 (3) NH+OH- NH ↑+H O 利用热空气能够降低NH 的溶解度,以便于NH 挥发逸出
4 3 2 3 3
基 础 容 量 效 率 9 分 数 责 任 目 标化学一轮复习作业
细心 谨慎 准确 姓名 学号
(4) N Cl-
2
(5) b SO2+HClO Cl-+SO2+H+
3 4
第( )套化学暑假必刷密卷专用反思表
填表时间:2022 年__月___日,__:__;反思人:___________家长签字:_____________
本套暴露的主要问题
板块 该板块失分 对每一分失分的原因反思
单项选 总分27 分
择题 丢了( )分
双选题 总分16 分
丢了( )分
主观题 总分57 分
丢了( )分
本套题的主要收获
知识上
的收获
技巧上
的收获
本套题的综合反思
做题状
态
做题结
果
自我提
基 础 容 量 效 率 10 分 数 责 任 目 标化学一轮复习作业
细心 谨慎 准确 姓名 学号
醒
基 础 容 量 效 率 11 分 数 责 任 目 标