文档内容
衡水泰华决胜二三高考化学暑假必刷密卷新高考版
衡水泰华中学决胜高考化学暑假必刷密卷 第8 套 3.双氧水(H O )与下列溶液反应,不能体现H O 氧化性的是
2 2 2 2
组编人:张云暖
做题时间:2022 年__月___日,__:__—__:__ 校对人: 贾美菁 A.酸性KMnO 溶液 B.淀粉KI溶液
4
审核人:王立明
实际得分:____家长签字(严禁代签):______ C.溶有SO 的BaCl 溶液 D.盐酸酸化的FeCl 溶液
2 2 2
励志格言:幸福不会从天而降,梦想不会自动成真。实现我们的奋斗目标,开创我们 4.古医典富载化学知识,下述之物见其氧化性者为
的美好未来,必须紧紧依靠人民、始终为了人民 A.金(Au):“虽被火亦未熟"
本套亮点:汇集氧化还原反应和陌生方程式书写各地最新模拟题,有基础考查题,也有新
B.石灰(CaO):“以水沃之,即热蒸而解”
颖且有思维量的题目,充分利用,定能查漏补缺,收获满满。
注意事项: C.石硫黄(S):“能化……银、铜、铁,奇物”
1, 本套密卷满分100分,做题所需时间75分钟;
2, 请一律用0.5或以上的黑色中性签字笔在规定的答题纸上做答,注意书写规范; D.石钟乳(CaCO ):“色黄,以苦酒(醋)洗刷则白”
3
3,做题不改错,等于没有做!做完之后,要求依照答案用红笔自判所有主客观题,并算
5.高铜酸钾是一种难溶于水的黑色粉末状固体,与高铁酸钾性质相似。可以由四羟基合铜酸钾和次溴
出总得分,请家长签字确认,并在积累本进行认真的错题整改反思,并把本套题的主要收
获、主要不足和反思写到每套题所附的反思纸上,开学上交。
酸在冰水浴中合成:①K
2
CuOH
4
HBrOKCuO
2
KBrKBrOH
2
O(未配平)。高铜酸钾在酸
一、单项选择题本题共9小题,每小题3分,共27分。在每小题给出的四个选项中,只有一项是符合
题目要求的。 性条件下不稳定:②KCuO H SO O CuSO H OK SO (未配平)。下列说法不正确的是
2 2 4 2 4 2 2 4
△
1. 反应MnO 4HCl 浓 MnCl +Cl 2H O中,还原剂是 A.①中氧化剂和还原剂的物质的量之比为1:2
2 2 2 2
B.②若有标况下5.6LO 生成,转移电子0.2N
2 A
A.MnO B.HCl C.MnCl D.Cl
2 2 2
C.②中KCuO 既表现氧化性,又表现还原性
2.下列实验中的颜色变化与氧化还原反应无关的是 2
D.由①②可知氧化性强弱顺序为:HBrOKCuO O
A B C D 2 2
实 向FeCl 溶液中加入 铜丝加热后,伸入无 向酸性KMnO 溶液 向FeSO 溶液中加入
6.实验室制备KMnO
4
过程为:①高温下在熔融强碱性介质中用KClO
3
氧化MnO
2
制备K
2
MnO
4
;②水
3 4 4
验 KSCN溶液 水乙醇中 中加入乙醇 NaOH溶液
溶后冷却,调溶液pH至弱碱性,K MnO 歧化生成KMnO 和MnO ;③减压过滤,将滤液蒸发浓缩、
2 4 4 2
现 铜丝先变黑,后又重 先产生白色沉淀,最终 冷却结晶,再减压过滤得KMnO 。下列说法正确的是
溶液变为血红色 溶液紫色褪去 4
象 新变为红色 变为红褐色
A.①中用瓷坩埚作反应器
A.A B.B C.C D.D B.①中用NaOH作强碱性介质
第 1 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
二.不定项选择题:本题共4小题,每小题4分,共16分。在每小题给出的四个选项中,有一项或两
C.②中K MnO 只体现氧化性
2 4
项符合题目要求。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项,
D.MnO 转化为KMnO 的理论转化率约为66.7%
2 4
只选一个且正确得2分,选两个且都正确的得4分,但只要选错一个,该小题得0分。
7.宏观辨识与微观探析是化学学科核心素养之一。 下列对应离子方程式书写正确的是
10. 中华文化源远流长,在浩瀚的历史文明中有许多关于化学的记载。下列说法错误的是
A.在CuCl 和FeCl 混合溶液中加入少量的Fe:Fe+Cu2+=Fe2++Cu
2 3 A.《淮南万毕术》中“曾青得铁则化为铜”,矿石“曾青”的主要成分为CuO
B.向Na 2 S 2 O 3 溶液中通入足量氯气:S 2 O 3 2-+4Cl 2 +5H 2 O=2SO2 4 - +8Cl-+10H+ B.《梦溪笔谈》中“石穴中水,所滴者皆为钟乳”,该现象涉及化合反应
C.向NH Al(SO ) 溶液中加入Ba(OH) 溶液至SO2-恰好沉淀完全:Al3++2SO2-+2Ba2+
C.《吕氏春秋》中“金(即铜)柔锡柔,合两柔则刚”,体现了合金硬度方面的特性
4 4 2 2 4 4
D.《天工开物》中“凡火药,硫为纯阳,硝为纯阴”,其中硫体现了还原性
+4OH-=AlO- +2BaSO ↓+2H O
2 4 2
11.下列有关结论正确的是
D.用铜电极电解硫酸铜溶液:2Cu2++2H 2 O 通电 Cu+O 2 ↑+4H+ A.常温常压下,向冷的浓硫酸中放入纯铜片,没有明显现象,说明铜与浓硫酸发生了钝化
8.NaClO /尿素复合吸收剂是一种良好的NO吸收剂,吸收原理为: B.将少量H S通入某NaClO溶液中,有SO2生成,说明该条件下氧化性:ClO SO2
2 2 4 4
①3NaClO 4NO2H O4HNO 3NaCl;②6NO2CONH 5N 2CO 4H O。 C.加热NaCl与浓H SO 的混合物可制得HCl,说明H SO 的酸性比HCl的酸性强
2 2 3 2 2 2 2 2 2 4 2 4
下列推断正确的是
D.浓HNO 和稀HNO 与Cu反应的还原产物分别为NO 和NO,不能说明稀HNO 的氧化性更强
3 3 2 3
A.物质的氧化性:HNO NaClO NO
3 2 12.利用锌灰(主要成分为ZnO,含有CuO、PbO、SiO 、FeO、Fe O 等杂质)制备高纯ZnO的工艺
2 2 3
B.复合吸收剂中NaClO
2
与尿素会发生氧化还原反应
流程如下,下列说法错误的是:
C.反应②中碳元素被NO氧化
D.反应②中若14molNO被完全吸收,则此过程转移电子为28mol
9.溴化钾(KBr)可作为分析试剂、感光剂、神经镇静剂等,工业上制取溴化钾的方法之一为:先将尿
素(H NCONH )加到K CO 溶液中,然后在不断搅拌下缓慢注入液溴,随即发生反应:
2 2 2 3
3K 2 CO 3 +H 2 NCONH 2 +3Br 2 =6KBr+4CO 2 ↑+N 2 ↑+2H 2 O。下列有关此反应的说法正确的是 A.滤渣1的主要成分为SiO 、PbSO
2 4
A.尿素作还原剂,CO 、N 是氧化产物 B.若制取1molKBr,转移电子数目为2N
2 2 A
B.步骤1中发生反应的离子方程式为:MnO+3Fe2++7H O3FeOH +MnO +5H
4 2 3 2
C.此方法成本低,且制得的KBr纯净 D. 实验室中KBr密封保存在无色广口瓶中
C.加入的试剂a为Zn,目的是除去Cu2
第 2 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
D.取步骤3后的干燥滤饼11.2g煅烧,可得产品8.1g,则x=2 子方程式是___。
13.实验室以含锌废液(主要成分为ZnSO ,含少量的Fe2+、Mn2+)为原料制备ZnCO ·2Zn(OH) 的实 (6)PbO 与浓盐酸共热生成黄绿色气体,反应的离子方程式为__。
4 3 2 2
验流程如下: (7)一氯胺(NH Cl)是一种重要的水消毒剂,写出产生消毒物质的化学方程式:___。
2
(8)MnO(OH) +I-+H+→Mn2++I +H O(未配平),其化学计量数依次为___。
2 2 2
(9)O 将Mn2+氧化成MnO(OH) 的离子方程式:_______。
2 2
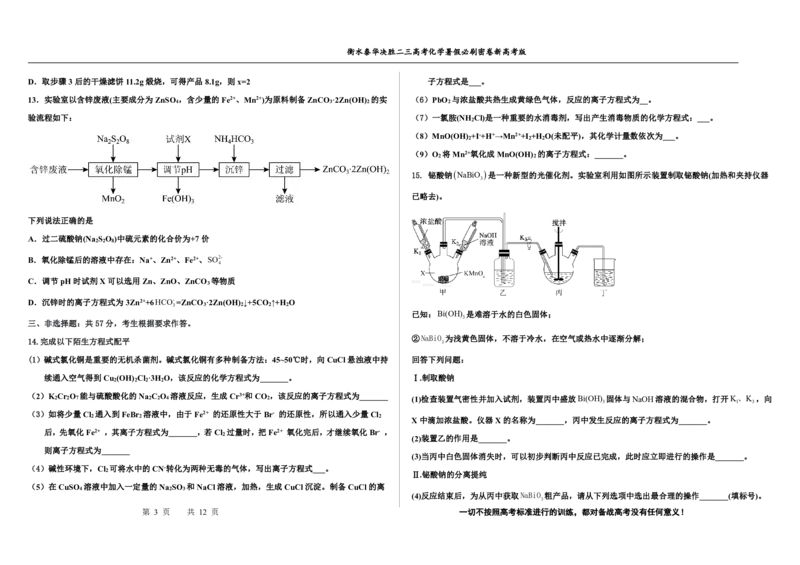
15. 铋酸钠NaBiO 是一种新型的光催化剂。实验室利用如图所示装置制取铋酸钠(加热和夹持仪器
3
已略去)。
下列说法正确的是
A.过二硫酸钠(Na S O )中硫元素的化合价为+7价
2 2 8
B.氧化除锰后的溶液中存在:Na+、Zn2+、Fe2+、SO2-
4
C.调节pH时试剂X可以选用Zn、ZnO、ZnCO 等物质
3
D.沉锌时的离子方程式为3Zn2++6HCO-=ZnCO ·2Zn(OH) ↓+5CO ↑+H O
3 3 2 2 2
已知:Bi(OH) 是难溶于水的白色固体;
3
三、非选择题:共57分,考生根据要求作答。
②NaBiO 为浅黄色固体,不溶于冷水,在空气或热水中逐渐分解;
14.完成以下陌生方程式配平 3
(1)碱式氯化铜是重要的无机杀菌剂。碱式氯化铜有多种制备方法:45~50℃时,向CuCl悬浊液中持 回答下列问题:
续通入空气得到Cu (OH) Cl ·3H O,该反应的化学方程式为_______。 Ⅰ.制取酸钠
2 2 2 2
(2)K 2 Cr 2 O 7 能与硫酸酸化的Na 2 C 2 O 4 溶液反应,生成Cr3+和CO 2 ,该反应的离子方程式为_______ (1)检查装置气密性并加入试剂,装置丙中盛放Bi(OH) 固体与NaOH溶液的混合物,打开K、K ,向
3 1 3
(3)如将少量Cl 通入到FeBr 溶液中,由于Fe2+ 的还原性大于Br- 的还原性,所以通入少量Cl
2 2 2 X中滴加浓盐酸。仪器X的名称为_______,丙中发生反应的离子方程式为_______。
后,先氧化Fe2+ ,其离子方程式为_______,若Cl 过量时,把Fe2+ 氧化完后,才继续氧化Br- ,
2 (2)装置乙的作用是_______。
则离子方程式为_______
(3)当丙中白色固体消失时,可以初步判断丙中反应已完成,此时应立即进行的操作是_______。
(4)碱性环境下,Cl 可将水中的CN-转化为两种无毒的气体,写出离子方程式___。
2 Ⅱ.铋酸钠的分离提纯
(5)在CuSO 溶液中加入一定量的Na SO 和NaCl溶液,加热,生成CuCl沉淀。制备CuCl的离
4 2 3
(4)反应结束后,为从丙中获取NaBiO 粗产品,请从下列选项中选出最合理的操作_______(填标号)。
3
第 3 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
a.在冰水中冷却;b.用普通漏斗过滤;c.用布氏漏斗抽滤;d.冷水洗涤;e.热水洗涤;f.自然晾干;g.在 (1)下面是消除NO 排放的三个案例:
x
干燥器中干燥 ①利用纯碱溶液可以吸收硝酸厂废气中的NO和NO [n(NO):n(NO )=1:1],该过程中发生反应的化学
2 2
Ⅲ.铋酸钠的应用——检验Mn2+ 方程式为___________。
(5)往待检液中加入铋酸钠晶体,加硫酸酸化,生成Bi3+,且溶液变为紫红色,证明待检液中存在Mn2+。 ②三元催化可以将汽车尾气中的CO和NO
x
进行净化处理,该过程中发生反应的化学方程式为
产生紫红色现象的离子方程式为_______。 ___________。
Ⅳ.酸钠纯度的测定 ③利用尿素消除NO 污染的转化反应为Ⅰ.NO+O NO ,Ⅱ.NO +CONH 无污染气体。
x 2 2 2 2 2
(6)取上述制得的NaBiO
3
(M=209)粗产品mg,加入足量的稀硫酸和MnSO
4
稀溶液使其完全反应,再
尿素中C元素的化合价___________,反应Ⅱ的化学方程式为___________。
用nmolL-1的H
2
C
2
O
4
标准溶液滴定,滴定终点时消耗H
2
C
2
O
4
溶液VmL。该产品的纯度是_______(用含 (2)为测定热电厂排放气中SO
2
的含量,进行了如下实验:标准状况下,将排放气匀速通入
n、m、V的代数式表示)。
100mL0.5mol/L酸性KMnO 溶液中。若排放气的流速为aLmin-1,经过bmin溶液恰好褪色,则该排
4
16. 化学工业为疫情防控提供了强有力的物质支撑。氯的许多化合物既是重要化工原料,又是高效、
放气中SO 的含量为___________g/L。
2
广谱的灭菌消毒剂。回答下列问题:
(3)通过如下流程可实现SO 和NO综合处理并获得保险粉(Na S O )和硝铵。
2 2 2 4
(1)Cl O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl 反应来制备,该反应为歧化反应(氧
2 2
化剂和还原剂为同一种物质的反应)。上述制备Cl O的化学方程式为
2
_______________________________。
(2)ClO 常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO 、NaHSO 、
2 2 4
NaHCO 的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO 溶液。上述过程中,生成
3 2
ClO 2 的反应属于歧化反应,每生成1molClO 2 消耗NaClO 2 的量为____________mol;产生“气泡”的 ①装置Ⅲ中生成Ce4+与S 2 O 4 2的物质的量之比为___________。
化学方程式为__________________。 ②装置Ⅳ中溶液含有amolL1NO和bmolL1NO,欲将cL该溶液完全转化为硝铵,需要通入O 与
2 3 2
(3)“84消毒液”的有效成分为NaClO,不可与酸性清洁剂混用的原因是_____________________(用离子
NH 的体积比为___________(同温同压下)。
3
方程式表示)。工业上是将氯气通入30%的NaOH溶液中来制备NaClO溶液,若NaClO溶液中NaOH
的质量分数为1%,则生产1000kg该溶液需消耗氯气的质量为________kg(保留整数)。
17.党十九大报告中首次将树立和践行“绿水青山就是金山银山”的理念写入党代会报告,治理污染减少
排放具有十分重要的意义。回答下列问题:
第 4 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
化学假期作业(八)答题纸 16. (每空2分)
14.(每空2分)
(1) 。
(1)
(2) mol; 。
(2)
(3) (用离子方程式表示)。 kg(保留整数)。
(3)
17. (每空2分)
(4)
(1)
(5)
① 。
(6)
② 。
(7)
③ , 。
(8)
(2) g/L。
(9)
(3)
15.(除标注外每空2分)
① 。
(1) (1分), _。
② (同温同压下)。
(2) 。
(3) 。
(4) (填标号)。
(5) 。
(6) (用含n、m、V的代数式表示)。
第 5 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
衡水泰华中学决胜高考化学暑假必刷密卷第八套化学参考答案 C.双氧水与溶有二氧化硫的氯化钡溶液中的二氧化硫反应时,双氧水为反应的氧化剂,反应中被还
原为水,表现氧化性,故C不符合题意;
1.【答案】B
D.双氧水与盐酸酸化的氯化亚铁溶液中的氯化亚铁反应时,双氧水为反应的氧化剂,反应中被还原
【详解】
为水,表现氧化性,故D不符合题意;
反应物HCl中部分Cl元素化合价由-1价变成0价,化合价升高是还原剂;
故选A。
故选B。
4.【答案】C
2.【答案】A
【详解】
【详解】
A.金“虽被火亦未熟”是指金单质在空气中被火灼烧也不反应,反应金的化学性质很稳定,与其氧化
A.向FeCl 溶液中加入KSCN溶液,则FeCl 与KSCN反应生成血红色的FeSCN 络合物,与氧化
3 3 3
性无关,A不合题意;
还原反应无关,故A错误;
B.石灰(CaO):“以水沃之,即热蒸而解”是指CaO+H O=Ca(OH) ,反应放热,产生大量的水汽,而
2 2
B.铜丝加热后,Cu被氧化为黑色的CuO,伸入无水乙醇中后又重新变为红色,则黑色的CuO被还原
CaO由块状变为粉末状,未发生氧化还原反应,与其氧化性无关,B不合题意;
为Cu,则与氧化还原反应有关,故B正确;
Δ Δ Δ
C.石硫黄即S:“能化……银、铜、铁,奇物”是指2Ag+S Ag S、Fe+S FeS、2Cu+S Cu S,反
2 2
C.向酸性KMnO 溶液中加入乙醇,酸性高锰酸钾能将乙醇氧化为乙酸,自生被还原,从而使溶液的
4
应中S作氧化剂,与其氧化性有关,C符合题意;
紫色退去,则与氧化还原反应有关,故C正确;
D.石钟乳(CaCO ):“色黄,以苦酒(醋)洗刷则白”是指
3
D.向FeSO 溶液中加入NaOH溶液,先产生白色沉淀,则Fe2 2OH FeOH ,最终变成红褐
4 2
CaCO +2CH COOH=(CH COO) Ca+H O+CO ↑,未发生氧化还原反应,与其氧化性无关,D不合题
3 3 3 2 2 2
色,则4FeOH
2
O
2
2H
2
O=4FeOH
3
,与氧化还原反应有关,故D正确;
意;
答案选A。 故答案为:C。
3.【答案】A 5.【答案】B
【详解】 【分析】
A.双氧水与酸性高锰酸钾溶液反应时,双氧水为反应的还原剂,反应中被氧化为氧气,表现还原性, 配平两个反应为2K CuOH 2HBrO=2KCuO KBrKBrO5H O、
2 4 2 2
故A符合题意;
4KCuO 6H SO =O 4CuSO 6H O2K SO;
2 2 4 2 4 2 2 4
B.双氧水与淀粉碘化钾溶液中的碘化钾反应时,双氧水为反应的氧化剂,反应中被还原为水,表现
【详解】
氧化性,故B不符合题意;
第 6 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
A.反应①中HBrO→KBr中Br元素化合价降低,HbrO做氧化剂,K
2
CuOH
4
KCuO
2
中Cu 确;
C.②中K MnO 歧化生成KMnO 和MnO ,故其既体现氧化性又体现还原性,C说法不正确;
2 4 4 2
元素化合价升高,K CuOH 做还原剂,反应方程式为
2
4
D.根据化合价的变化分析,K MnO 歧化生成KMnO 和MnO 的物质的量之比为2:1,根据Mn元
2 4 4 2
2K 2 CuOH 4 2HBrO=2KCuO 2 KBrKBrO5H 2 O,则氧化剂和还原剂的物质的量之比为1:2, 素守恒可知,MnO 中的Mn元素只有 2 转化为KMnO ,因此,MnO 转化为KMnO 的理论转化率
2 4 2 4
3
A正确;
约为66.7%,D说法正确;
B.反应②反应方程式为4KCuO
2
6H
2
SO
4
=O
2
4CuSO
4
6H
2
O2K
2
SO
4
,生成1molO
2
转移4mol
综上所述,本题选D。
V 5.6L
电子,标况下生成5.6LO 即物质的量为n= = =0.25mol,转移电子
7.【答案】B
2 V 22.4L/mol
m
【分析】
0.25mol×4×N mol-1=N ,B错误;
A A
本题主要考查离子方程式的书写,侧重考查学生对基础知识的理解能力。
C.反应②反应方程式为4KCuO
2
6H
2
SO
4
=O
2
4CuSO
4
6H
2
O2K
2
SO
4
,Cu元素化合价升高,O
【详解】
元素化合价降低,KCuO 既做氧化剂也做还原剂,KCuO 既表现氧化性,又表现还原性,C正确;
A.Fe3+氧化性大于Cu2+,所以Fe先与Fe3+反应,即先发生的反应为:Fe+2Fe3+=3Fe2+,A项错误;
2 2
B.向Na S O 溶液中通入足量氯气,发生氧化还原反应,B正确;
D.由氧化剂的氧化性强于氧化产物,由①可得氧化性:HBrOKCuO ,由②可得氧化性:KCuO O , 2 2 3
2 2 2
C.向NH Al(SO ) 溶液中加入Ba(OH) 溶液至SO2-恰好沉淀完全,铵根离子结合氢氧根离子的能力大
则氧化性强弱顺序为:HBrOKCuO O ,D正确; 4 4 2 2 4
2 2
于氢氧化铝的,反应生成氢氧化铝沉淀和一水合氨,正确的离子方程式为
故选:B。
6.【答案】D NH+ 4 +Al3++2SO2 4 -+2Ba2++4OH-=Al(OH) 3 +NH 3 H 2 O+2BaSO 4 ,C项错误;
【分析】 D.用Cu电极电解硫酸铜溶液,阳极为Cu失电子生成Cu2+,阴极为Cu2+得电子生成Cu,D项错误;
由题中信息可知,高温下在熔融强碱性介质中用KClO 氧化 MnO 制备K MnO ,然后水溶后冷却调 故合理选项为B。
3 2 2 4
溶液pH至弱碱性使K MnO 歧化生成KMnO 和MnO ,Mn元素的化合价由+6变为+7和+4。 8. 【答案】D
2 4 4 2
【详解】 【详解】
A.①中高温下在熔融强碱性介质中用KClO 氧化 MnO 制备K MnO ,由于瓷坩埚易被强碱腐蚀, A.在原理① 中,NaClO 是氧化剂,HNO 是氧化产物,氧化性HNO