文档内容
衡水泰华决胜二三高考化学暑假必刷密卷新高考版
衡水泰华中学决胜高考化学暑假必刷密卷 第9套 C.反应的离子方程式:3ClO 2CNO H O=N 2HCO 3Cl
2 2 3
组编人:张云暖
做题时间:2022 年__月___日,__:__—__:__ 校对人: 贾美菁 D.每处理1molCNO转移3mole
审核人:王立明
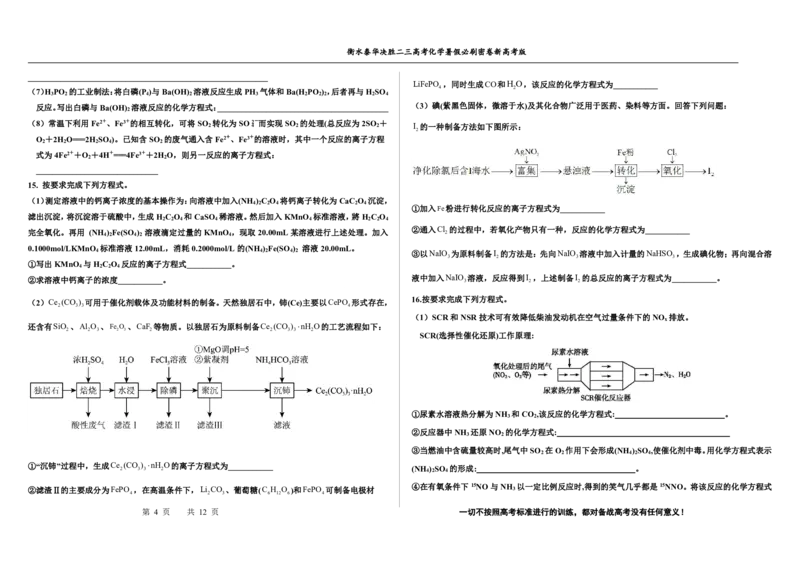
实际得分:____家长签字(严禁代签):______ 3.科学家发现某些生物酶体系可以促进H+和e-的转移(如a、b和c),能将海洋中的NO转化为N 进
2 2
励志格言:幸福不会从天而降,梦想不会自动成真。实现我们的奋斗目标,开创我们 入大气层,反应过程如图所示。
的美好未来,必须紧紧依靠人民、始终为了人民。——
本套亮点:汇集氧化还原反应和陌生方程式书写各地最新模拟题,有基础考查题,也有新
颖且有思维量的题目,充分利用,定能查漏补缺,收获满满。
注意事项:
1, 本套密卷满分100分,做题所需时间75分钟;
2, 请一律用0.5或以上的黑色中性签字笔在规定的答题纸上做答,注意书写规范;
3,做题不改错,等于没有做!做完之后,要求依照答案用红笔自判所有主客观题,并算 下列说法正确的是
出总得分,请家长签字确认,并在积累本进行认真的错题整改反思,并把本套题的主要收
获、主要不足和反思写到每套题所附的反思纸上,开学上交。 A.过程Ⅰ中NO发生氧化反应 B.a和b中转移的e-数目相等
2
一、 单项选择题本题共9小题,每小题3分,共27分。在每小题给出的四个选项中,只有一项是
符合题目要求的。
C.过程Ⅱ中参与反应的n(NO):n
NH
4
+
=1:4
1.下列过程不涉及氧化还原反应的是
D.过程Ⅰ→Ⅲ的总反应为NO-+NH+=N +2H O
2 4 2 2
A.古代用铜矿石、锡矿石冶炼铸造青铜器 B.出土后的青铜器大多数已受到锈蚀
4.用CuS、Cu S处理酸性废水中的Cr O2,发生的反应如下:
C.古代用明矾溶液清除青铜镜表面的锈斑 D.现代用双氧水去除青铜器上有害的CuCl 2 2 7
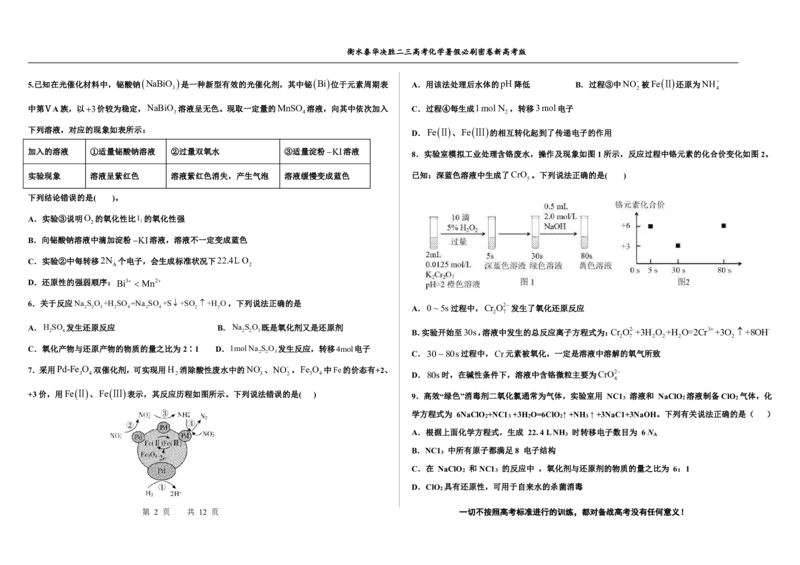
2. 处理某废水时,反应过程中部分离子浓度与反应进程关系如图,反应过程中主要存在N 2 、HCO 3 、 反应①:CuSCr 2 O 7 2 H Cu2 SO2 4 Cr3 H 2 O(未配平)
ClO、CNO(C+4价,N-3价)、Cl-等微粒。下列说法不正确的是 反应②:Cu
2
SCr
2
O
7
2 H Cu2 SO2
4
Cr3 H
2
O(未配平)
下列判断正确的是( )
A.反应①和②中各有2种元素的化合价发生变化
B.处理等物质的量的Cr O2时,反应①和②中消耗H的物质的量相等
2 7
C.反应①中还原剂与氧化剂的物质的量之比为3:4
D.相同质量的CuS和Cu S处理酸性废水中Cr O2时,Cu S消耗更多Cr O2
A.该废水呈强酸性 B.废水处理后转化为无害物质 2 2 7 2 2 7
第 1 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
5.已知在光催化材料中,铋酸钠 NaBiO 是一种新型有效的光催化剂,其中铋 Bi 位于元素周期表 A.用该法处理后水体的pH降低 B.过程③中NO- 被Fe Ⅱ 还原为NH+
3 2 4
中第ⅤA族,以3价较为稳定,NaBiO 溶液呈无色。现取一定量的MnSO 溶液,向其中依次加入 C.过程④每生成1molN ,转移3mol电子
3 4 2
下列溶液,对应的现象如表所示:
D.Fe
Ⅱ
、Fe
Ⅲ
的相互转化起到了传递电子的作用
加入的溶液 ①适量铋酸钠溶液 ②过量双氧水 ③适量淀粉KI溶液
8.实验室模拟工业处理含铬废水,操作及现象如图1所示,反应过程中铬元素的化合价变化如图2。
实验现象 溶液呈紫红色 溶液紫红色消失,产生气泡 溶液缓慢变成蓝色 已知:深蓝色溶液中生成了CrO 。下列说法正确的是( )
5
下列结论错误的是( )。
A.实验③说明O 的氧化性比I 的氧化性强
2 2
B.向铋酸钠溶液中滴加淀粉KI溶液,溶液不一定变成蓝色
C.实验②中每转移2N 个电子,会生成标准状况下22.4L O
A 2
D.还原性的强弱顺序:Bi3 Mn2
6.关于反应Na 2 S 2 O 3 +H 2 SO 4 =Na 2 SO 4 +S+SO 2 +H 2 O,下列说法正确的是 A.0~5s过程中,Cr O2发生了氧化还原反应
2 7
A.H
2
SO
4
发生还原反应 B.Na
2
S
2
O
3
既是氧化剂又是还原剂
B.实验开始至30s,溶液中发生的总反应离子方程式为:Cr O2-+3H O +H O=2Cr3++3O +8OH-
2 7 2 2 2 2
C.氧化产物与还原产物的物质的量之比为2∶1 D.1mol Na S O 发生反应,转移4mol电子
2 2 3 C.30~80s过程中,Cr元素被氧化,一定是溶液中溶解的氧气所致
7.采用Pd-Fe
3
O
4
双催化剂,可实现用H
2
消除酸性废水中的NO
3
-、NO-
2
,Fe
3
O
4
中Fe的价态有+2、
D.80s时,在碱性条件下,溶液中含铬微粒主要为CrO2
4
+3价,用Fe
Ⅱ
、Fe
Ⅲ
表示,其反应历程如图所示。下列说法错误的是( ) 9.高效“绿色”消毒剂二氧化氯通常为气体,实验室用 NC1 溶液和 NaClO 溶液制备ClO 气体,化
3 2 2
学方程式为 6NaClO +NC1 +3H O=6ClO ↑+NH ↑+3NaC1+3NaOH。下列有关说法正确的是( )
2 3 2 2 3
A.根据上面化学方程式,生成 22.4LNH 时转移电子数目为 6N
3 A
B.NC1 中所有原子都满足8 电子结构
3
C.在 NaClO 和NC1 的反应中 ,氧化剂与还原剂的物质的量之比为 6:1
2 3
D.ClO 具有还原性,可用于自来水的杀菌消毒
2
第 2 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
二.不定项选择题:本题共4小题,每小题4分,共16分。在每小题给出的四个选项中,有一项或两 A.脱硫过程中,需要控制温度
项符合题目要求。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项, B.氧化过程中,Se转化为H SeO 的反应中氧化剂和还原剂的物质的量之比为4:5
2 3
只选一个且正确得2分,选两个且都正确的得4分,但只要选错一个,该小题得0分。 C.滤液III中主要存在的金属离子有Na+、Zn2+、Fe3+、Cu2+
10.铅位于IVA族,PbO偏碱性,易溶于硝酸,PbO 2 偏酸性,难溶于硝酸。已知:PbS与稀HNO 3 D.还原过程中生成粗硒的离子方程式为:H SeO +2SO 2 =Se↓+2SO 2 +H O
2 3 3 4 2
发生反应I :3PbS+8HNO (稀)=3Pb(NO ) +3S↓+2NO↑+4H O;PbS与浓HNO 发生反应II:PbS
3 3 2 2 3 13.已知:As O 、锌和稀硫酸反应会生成AsH 、硫酸锌和水。现将4.0mg含As O 的试样和锌、稀硫
2 3 3 2 3
+8HNO (浓)=PbSO +8NO ↑+4H O。下列推断正确的是( )
3 4 2 2 酸混合恰好完全反应,将生成的AsH 缓慢通过热玻璃管中,AsH 完全分解冷却后得到3mg固体。下
3 3
A.Pb O 与HNO 溶液发生反应:Pb O +4H+=PbO +2Pb2++2H O
3 4 3 3 4 2 2 列有关说法不正确的是( )(As的相对原子质量为75)
B.由反应I、II可知,氧化性:HNO (浓)>HNO (稀)>PbO
3 3 2 A.试样中As O 的质量分数为99%
2 3
C.反应I若生成4.48LNO,转移0.6N 电子
A B.参与反应的锌失去的电子数为1.210-4N
A
Δ
D.S可以与浓硝酸反应:S+6HNO (浓) H SO +6NO ↑+2H O
C.分解产生的氢气在标准状况下体积为1.344mL
3 2 4 2 2
D.若硫酸的物质的量浓度为0.12mol/L,则消耗稀硫酸的体积为1mL
11.实验室中利用固体KMnO 进行如图实验,下列说法错误的是
4 三、非选择题:共57分,考生根据要求作答。
14.完成下列反应:
(1)利用石灰乳和硝酸工业的尾气(含NO、NO )反应,既能净化尾气,又能获得应用广泛的Ca(NO ) 。
2 2 2
生产中溶液需保持弱碱性,在酸性溶液中Ca(NO ) 会发生分解,产物之一是NO,反应的离子方程:
2 2
(2)生产硫化钠大多采用无水芒硝(Na SO )-碳粉还原法,若煅烧所得气体为等物质的量的CO和
A.G与H均为氧化产物 B.实验中KMnO 只作氧化剂 2 4
4
CO ,写出煅烧时发生反应的化学方程式:_____________________________
2
C.Mn元素至少参与了3个氧化还原反应 D.G与H的物质的量之和可能为0.25mol
(3)AgNO 光照易分解,生成 Ag 和红棕色气体等物质,其光照分解反应的化学方程式:
3
12.工业上以硫酸泥(主要含S、Se、Fe O 、CuO、ZnO、SiO 等)为原料提取硒,流程图如图所示。
2 3 2 _______________________________________________________________________。
下列说法错误的是( ) (4)废旧干电池中的MnO 与FeS在70℃的硫酸中浸取,生成MnSO 和Fe (SO ) 的化学方程式:
2 4 2 4 3
_____________________________________________________________
(5)当用CaSO 水悬浮液吸收经O 预处理的烟气时,清液(pH约为8)中SO2-将NO 转化为NO-,
3 3 3 2 2
其离子方程式:______________________________________________。
(6)CuSO 溶液能用作P 中毒的解毒剂,反应可生成P的最高价含氧酸和铜,该反应的化学方程式:
4 4
第 3 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
___________________________________________________________
LiFePO ,同时生成CO和H O,该反应的化学方程式为___________
(7)H PO 的工业制法:将白磷(P )与Ba(OH) 溶液反应生成PH 气体和Ba(H PO ) ,后者再与H SO 4 2
3 2 4 2 3 2 2 2 2 4
反应。写出白磷与Ba(OH) 溶液反应的化学方程式:__________________________________________ (3)碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。回答下列问题:
2
(8)常温下利用Fe2+、Fe3+的相互转化,可将SO
2
转化为SO2
4
-而实现SO
2
的处理(总反应为2SO
2
+
I 的一种制备方法如下图所示:
2
O +2H O===2H SO )。已知含SO 的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程
2 2 2 4 2
式为4Fe2++O +4H+===4Fe3++2H O,则另一反应的离子方程式:
2 2
______________________________
15. 按要求完成下列方程式。
(1)测定溶液中的钙离子浓度的基本操作为:向溶液中加入(NH ) C O 将钙离子转化为CaC O 沉淀,
4 2 2 4 2 4
①加入Fe粉进行转化反应的离子方程式为___________
滤出沉淀,将沉淀溶于硫酸中,生成H C O 和CaSO 稀溶液。然后加入KMnO 标准溶液,將H C O
2 2 4 4 4 2 2 4
完全氧化。再用 (NH 4 ) 2 Fe(SO 4 ) 2 溶液滴定过量的KMnO 4 ,现取20.00mL某溶液进行上述处理。加入
②通入Cl
2
的过程中,若氧化产物只有一种,反应的化学方程式为___________
0.1000mol/LKMnO 标准溶液12.00mL,消耗0.2000mol/L的(NH ) Fe(SO ) 溶液20.00mL。
4 4 2 4 2 ③以NaIO 为原料制备I 的方法是:先向NaIO 溶液中加入计量的NaHSO ,生成碘化物;再向混合溶
3 2 3 3
①写出KMnO 与H C O 反应的离子方程式___________。
4 2 2 4
②求溶液中钙离子的浓度___________。 液中加入NaIO
3
溶液,反应得到I
2
,上述制备I
2
的总反应的离子方程式为___________。
(2)Ce (CO ) 可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要以CePO 形式存在,
16.按要求完成下列方程式。
2 3 3 4
(1)SCR和NSR技术可有效降低柴油发动机在空气过量条件下的NO 排放。
x
还含有SiO 、Al O 、Fe O 、CaF 等物质。以独居石为原料制备Ce (CO ) nH O的工艺流程如下:
2 2 3 2 3 2 2 3 3 2
SCR(选择性催化还原)工作原理:
①尿素水溶液热分解为NH 和CO ,该反应的化学方程式: 。
3 2
②反应器中NH 还原NO 的化学方程式:
3 2
③当燃油中含硫量较高时,尾气中SO 在O 作用下会形成(NH ) SO ,使催化剂中毒。用化学方程式表示
2 2 4 2 4
①“沉铈”过程中,生成Ce
2
(CO
3
)
3
nH
2
O的离子方程式为___________
(NH 4 ) 2 SO 4 的形成: 。
②滤渣Ⅱ的主要成分为FePO ,在高温条件下,Li CO 、葡萄糖(C H O )和FePO 可制备电极材
④在有氧条件下15NO与NH
3
以一定比例反应时,得到的笑气几乎都是15NNO。将该反应的化学方程式
4 2 3 6 12 6 4
第 4 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
补充完整: NNO+ H O。
2
(2)SiHCl 在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成(HSiO) O等,写出该反应的
3 2
化学方程式________________________________________。
(3)用酸性(NH ) CO水溶液吸收NO ,吸收过程中存在HNO 与(NH ) CO生成N 和CO 的反应。
2 2 x 2 2 2 2 2
写出该反应的化学方程式:___________________________________。
(4)为实现燃煤脱硫,向煤中加入浆状Mg(OH) ,使燃烧产生的SO 转化为稳定的镁化合物,写出
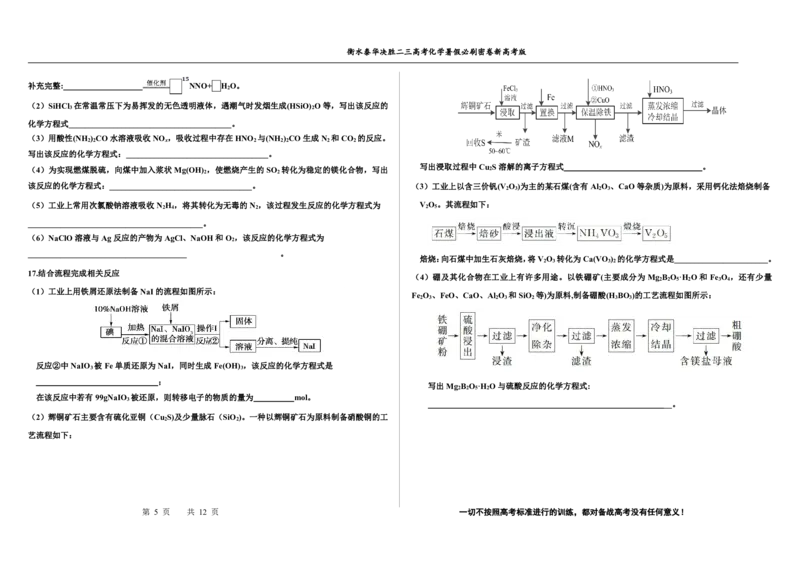
写出浸取过程中Cu
2
S溶解的离子方程式 。
2 2
该反应的化学方程式:___________________________________。 (3)工业上以含三价钒(V O )为主的某石煤(含有Al O 、CaO等杂质)为原料,采用钙化法焙烧制备
2 3 2 3
(5)工业上常用次氯酸钠溶液吸收N 2 H 4 ,将其转化为无毒的N 2 ,该过程发生反应的化学方程式为 V 2 O 5 。其流程如下:
___________________________________________。
(6)NaClO溶液与Ag反应的产物为AgCl、NaOH和O ,该反应的化学方程式为
2
_______________________________________ 。
焙烧:向石煤中加生石灰焙烧,将V O 转化为Ca(VO ) 的化学方程式是_______________________。
2 3 3 2
17.结合流程完成相关反应
(4)硼及其化合物在工业上有许多用途。以铁硼矿(主要成分为 Mg B O ·H O和 Fe O ,还有少量
2 2 5 2 3 4
(1)工业上用铁屑还原法制备NaI的流程如图所示:
Fe O 、FeO、CaO、Al O 和SiO 等)为原料,制备硼酸(H BO )的工艺流程如图所示:
2 3 2 3 2 3 3
反应②中NaIO 被Fe单质还原为NaI,同时生成Fe(OH) ,该反应的化学方程式是
3 3
;
写出Mg B O ·H O与硫酸反应的化学方程式:
2 2 5 2
在该反应中若有99gNaIO 被还原,则转移电子的物质的量为 mol。
3
__。
(2)辉铜矿石主要含有硫化亚铜(Cu S)及少量脉石(SiO )。一种以辉铜矿石为原料制备硝酸铜的工
2 2
艺流程如下:
第 5 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
化学假期作业(九)答题纸 16. (每空2分共18分)
14.(每空2分,共16分) (1)
(1) ① 。
(2) ②
(3) ③ 。
(4) ④ NNO+ H O。
2
(5) (2)
(3)
(6)
(4)___________________________________
(7)
(5)
(8)
(6) 。
15.(每空2分,共14分)
17. (除标注外每空2分,共9分)
(1) ① ②
(1) ; mol(1分)
(2) ①
(2) 。
②
(3)__________________ _____
(3) ①
(4) __。
②
③
第 6 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
衡水泰华中学决胜高考化学暑假必刷密卷第九套化学参考答案 A.由图示可知,过程I中NO- 转化为NO,氮元素化合价由+3价降低到+2价,NO- 作氧化剂,被还
2 2
1.【答案】C 原,发生还原反应,A错误;
【详解】
B.由图示可知,过程I为NO- 在酶1的作用下转化为NO和H O,依据得失电子守恒、电荷守恒和
2 2
A.古代用铜矿石、锡矿石冶炼铸造青铜器,Cu元素由化合态变为游离态,Cu元素的化合价降低,
酶1
原子守恒可知,反应的离子方程式为:NO-
2
+2H++e-=NO+H
2
O,生成1molNO,a过程转移1mole-,
属于氧化还原反应,故A不选;
B.出土后的青铜器大多数已受到锈蚀,锈蚀过程中Cu元素的化合价由0价升高到+2价,属于氧化 过程II为NO和NH+ 4 在酶2的作用下发生氧化还原反应生成H 2 O和N 2 H 4 ,依据得失电子守恒、电荷
还原反应,故B不选;
守恒和原子守恒可知,反应的离子方程式为:NO+NH+ 4 +3e-+2H+
酶
=
2
H 2 O+N 2 H 4 ,消耗1molNO,b过
C.明矾溶液显酸性,能与铜锈发生复分解反应,反应中没有元素的化合价变化,不涉及氧化还原反
程转移4mole-,转移电子数目不相等,B错误;
应,故C选;
酶2
C.由图示可知,过程 II 发生反应的参与反应的离子方程式为:NO+NH+ 4 +3e-+2H+ = H 2 O+N 2 H 4 ,
D.现代用双氧水去除青铜器上有害的CuCl,O元素的化合价降低,Cu元素的化合价升高,为氧化
还原反应,故D不选;
n(NO):n(NH+
4
)=1:1,C错误;
2.【答案】A
D.由图示可知,过程 I 的离子方程式为 NO - 2 +2H++e-
酶
=
1
NO+H 2 O,过程 II 的离子方程式为
【详解】
酶2 酶3
NO+NH+ 4 +3e-+2H+ = H 2 O+N 2 H 4 ,过程III的离子方程式为N 2 H 4 = N 2 ↑+4H++4e-,则过程Ⅰ→Ⅲ的总
A.废水中主要存在ClO-、CNO-,水解溶液呈碱性,故A错误;
反应为NO- +NH+=N ↑+2H O,D正确;
B.处理某废水后,产物为HCO、N 、Cl-都为无害物质,故B正确; 2 4 2 2
3 2
答案选D。
C.由图可知,ClO-浓度减小,HCO浓度增加,则还原反应为ClO-→Cl-,氧化反应为CNO-→N ,
3 2
4【答案】C
由电子、电荷守恒可知离子反应为3ClO 2CNO H
2
O=N
2
2HCO
3
3Cl,故C正确;
【分析】
D.由图可知,ClO-浓度减小,HCO浓度增加,则还原反应为ClO-→Cl-,氧化反应为CNO-(N化 对于反应①,铜元素化合价未变化,硫元素化合价由-2升高至+6,铬元素化合价由+6降低至+3,
3
氢元素和氧元素化合价未变化;根据得失电子守恒、电荷守恒、原子守恒配平可得:
合价为+3)→N (N化合价为0),每处理1molCNO-转移3mole-,故D正确。故选A。
2
3.【答案】D
3CuS+4Cr
2
O
7
2 +32H+=3Cu2++3SO 2 +8Cr3++16H
2
O;对于反应②,铜元素化合价由+1升高至+2,
4
【详解】 硫元素化合价由-2升高至+6,铬元素化合价由+6降低至+3,氢元素和氧元素化合价未变化。根据
得失电子守恒、电荷守恒、原子守恒配平可得:3Cu S+5Cr O2 +46H+=6Cu2++3SO 2 +10Cr3++23H O;
2 2 7 2
4
第 7 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
据以上分析进行解答。 6.【答案】B
【详解】 【解析】
A.反应①中硫元素价态由-2价升高到+6价,铬元素价态由+6价降低到+3价;反应②中铜元素由+1 【分析】
价升高到+2价,硫元素价态由-2价升高到+6价,铬元素价态由+6价降低到+3价,故A错误; Na S O +H SO =Na SO +S↓+SO ↑+H O,该反应的本质是硫代硫酸根离子在酸性条件下发上歧化反
2 2 3 2 4 2 4 2 2
B.结合以上分析可知,处理等物质的量的Cr O2时,反应①和②中消耗H+的物质的量不相等,故B 应生成硫和二氧化硫,化合价发生变化的只有S元素一种,硫酸的作用是提供酸性环境。
2 7
【详解】
错误;
A.H SO 转化为硫酸钠和水,其中所含元素的化合价均未发生变化,故其没有发生还原反应,A说法
2 4
C.结合以上分析可知,还原剂为CuS,氧化剂为Cr O2,还原剂与氧化剂的物质的量之比为3:4,
2 7
不正确;
故C正确;
B.Na S O 中的S的化合价为+2,其发生歧化反应生成S(0价)和SO (+4价),故其既是氧化剂又是还
2 2 3 2
160g 160g
D.假设质量均为160g,n(CuS)= =1.67mol,n(Cu S)= =1mol;根据反应方程
原剂,B说法正确;
2
96g/mol 160g/mol
C.该反应的氧化产物是SO ,还原产物为S,氧化产物与还原产物的物质的量之比为1:1,C说法不
2
4
式可知:3CuS~4 Cr 2 O 7 2 ,3Cu 2 S~5 Cr 2 O 7 2 ,所以 CuS 消耗 n( Cr 2 O 7 2 )= 3 ×1.67=2.2mol, 正确;
5
n(Cr O2 )=1× =1.7mol;所以CuS消耗的更多,故D错误; D.根据其中S元素的化合价变化情况可知,1molNa 2 S 2 O 3 发生反应,要转移2mol电子,D说法不
2 7 3
正确。
5【答案】A
综上所述,本题选B。
【详解】
7【答案】A
A.②中加入过量双氧水,再加入适量淀粉KI溶液,溶液缓慢变成蓝色,不一定是氧气氧化的I-,
【详解】
故A错误;
A . 根 据 图 示 , 该 方 法 的 总 反 应 为 2NO 5H 2H N 6H O 、
B.向铋酸钠溶液中滴加淀粉KI溶液,铋酸钠能把KI氧化成I ,但有可能进一步氧化成IO,所以 3 2 2 2
2 3
溶液不一定变成蓝色,故B正确;
2NO
2
3H
2
2H N
2
4H
2
O,反应消耗氢离子,用该法处理后水体的pH增大,故A错误;
C.根据得失电子守恒可知,实验②中每转移2个电子会生成1mol氧气,标准状况下氧气体积为22.4L, B.根据图示,过程③中NO- 被Fe Ⅱ 还原为NH+,故B正确;
2 4
故C正确;
C.过程④NO- 、NH+发生归中反应生成氮气,每生成1molN 转移3mol电子,故C正确;
2 4 2
D.结合实验①的现象,NaBiO 氧化了MnSO ,根据还原剂的还原性比还原产物的还原性强,可知
3 4
D.根据图示,Fe
Ⅱ
、Fe
Ⅲ
相互转化,把氢气失的电子传给了N原子,起到了传递电子的作用,
Bi3 Mn2,故D正确;故答案为A。
第 8 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
故D正确;答案选A。 10【答案】AD
8【答案】D 【详解】
【分析】 A.Pb O 中含有二价铅和四价铅,PbO偏碱性,易溶于硝酸,PbO 偏酸性,难溶于硝酸,则Pb O
3 4 2 3 4
对照图1和图2,0s~5s,Cr元素的化合价仍为+6价;5s~30s,Cr元素的化合价由+6价降为+3价;30s~80s, 与硝酸反应生成Pb(NO ) 和PbO ,发生反应离子方程式:Pb O +4H+═PbO +2Pb2++2H O,故A
3 2 2 3 4 2 2
Cr元素的化合价又由+3价升高为+6价。 正确;
【详解】 B.根据题意,硝酸不能把二价铅氧化为四价铅,说明硝酸的氧化性小于PbO ,故B错误;
2
A.0~5s过程中,Cr O2发生反应生成CrO ,Cr元素都呈+6价,发生非氧化还原反应,A错误; C.没有说明是否是标准状况,无法计算气体的物质的量,因而不能计算生成4.48LNO,转移的电子
2 7 5
数,故C错误;
B.由图2可知,实验开始至30s时,K Cr O 被还原为Cr3+,H O 被氧化生成O ,总反应离子方程
2 2 7 2 2 2
Δ
式为:Cr O2 +3H O +8H+=2Cr3++7H O+3O ↑,B错误; D.浓硝酸具有强氧化性,能把 S 氧化为硫酸,则 S 与浓硝酸反应:S +6HNO (浓) H SO
2 7 2 2 2 2 3 2 4
C.30s时,绿色溶液中主要含有Cr3+,80s时黄色溶液中主要含有CrO2
4
,所以30~80s过程中,Cr
+6NO 2 ↑+2H 2 O,故D正确;
元素被氧化,可能是剩余的H O 所致,C错误; 答案选AD。
2 2
D.Cr 2 O 7 2 +H 2 O 2CrO2 4 +2H+,80s时,在碱性条件下,平衡正向移动,溶液中含铬微粒主要 11.
【答案】BD
为CrO2,D正确;答案选D。
4
【分析】
9【答案】B
KMnO 固体受热分解生成K MnO 、MnO 、O ,K MnO 、MnO 均具有氧化性,在加热条件下能与
4 2 4 2 2 2 4 2
【详解】
浓盐酸发生氧化还原反应,反应过程中Cl-被氧化为Cl ,K MnO 、MnO 被还原为MnCl ,因此气体
2 2 4 2 2
A.缺标准状况,无法计算22.4LNH 的物质的量和反应转移电子的数目,故A错误;
3 单质G为O ,气体单质H为Cl 。
2 2
B.NC1 3 为共价化合物,电子式为 ,由电子式可知分子中中所有原子都满足8 电子结构,故C 【详解】
正确; A.加热KMnO 固体的反应中,O元素化合价由-2升高至0被氧化,加热K MnO 、MnO 与浓盐酸
4 2 4 2
C.由方程式可知,NaClO 中氯元素的化合价升高被氧化,NaClO 为反应的还原剂,NC1 中氮元素的 的反应中,Cl元素化合价由-1升高至0被氧化,因此O 和Cl 均为氧化产物,故A正确;
2 2 3 2 2
化合价降低被还原,NC1 为反应的氧化剂,则氧化剂与还原剂的物质的量之比为1:6,故C错误; B.KMnO 固体受热分解过程中,Mn元素化合价降低被还原,部分O元素化合价升高被氧化,因此
3 4
D.ClO 具有氧化性,可用于自来水的杀菌消毒,故D错误;故选B。 KMnO 既是氧化剂也是还原剂,故B错误
2 4
二、不定项选择题(每个小题有1-2个正确选项,共5小题,每题4分,部分分2分,共20分)
第 9 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
D.还原过程中生成粗硒的离子方程式为:H SeO +2SO 2 =Se↓+2SO 2 +H O,D项正确;
2 3 3 4 2
C.Mn元素在反应过程中物质及化合价变化为 ,Mn元
故选C。
13.
素至少参加了3个氧化还原反应,故C正确; 【答案】B
D.每生成1molO 转移4mol电子,每生成1molCl 转移2mol电子,若KMnO 转化为MnCl 过程 【分析】
2 2 4 2
中得到的电子全部是Cl-生成Cl 所失去的,则气体的物质的量最大,由 2KMnO ~5Cl 可知,n(气 根 据 题 目 所 给 信 息 可 知 , As O 、 锌 和 稀 硫 酸 反 应 的 方 程 式 为
2 4 2 2 3
体) max =0.25mol,但该气体中一定含有O 2 ,因此最终所得气体的物质的量小于0.25mol,故D错误; Δ
As O +6Zn+6H SO =2AsH +6ZnSO +3H O,AsH 分解的方程式为2AsH 2As+3H ↑,AsH 完全分
2 3 2 4 3 4 2 3 3 2 3
综上所述,说法错误的是BD,故答案为:BD。
198
12.
解 后 得 到 3mgAs , 则 4.0mg 试 样 中 含 As O 的 质 量 为 ×3mg=3.96mg ,
2 3
752
【答案】C
3.9610-3g
【分析】 n(As 2 O 3 )= =210-5mol,据此分析解答。
198g/mol
NaClO、稀HSO
硫酸泥中加煤油将S溶解,过滤后以滤液的形式除去,加入 3 2 4滤渣中的Se氧化成H 2 SeO 3 , 【详解】
过滤
同时Fe 2 O 3 、CuO、ZnO被硫酸溶解 滤渣II为SiO 2 ;滤液中主要含有Na+、Zn2+、Fe3+、Cu2+、 A.根据以上分析,试样中As O 的质量分数为 3.96mg 100%=99%,故A正确;
2 3
4.0mg
H 2 SeO 3 、SO 2 4 Na 2 SO 3 等 H 2 SeO 3 被还原成Se,Fe3+被还原为Fe2+,然后过滤使Na+、Zn2+、Fe2+、Cu2+
B.反应中As元素化合价由As O 中+3价降低为AsH 中-3价,Zn中锌元素化合价由0价升高为+2
2 3 3
等以滤液III的形式除去,得到粗硒。
价,根据得失电子守恒,锌失去电子的物质的量为2 10-5 2 6=2.4 10-4mol,故B错误;
【详解】
Δ 3
A.S溶于煤油,Se、Fe 2 O 3 、CuO、ZnO、SiO 2 等不溶于煤油,过滤可除去S和煤油,温度太低,硫 C.由方程式2AsH 2As+3H ↑可知,生成氢气的物质的量为2 10-5mol 2 =610-5mol,在标准状
3 2
2
在煤油中溶解度降低,温度太高,煤油挥发量大,均导致脱硫率低,A项正确;
B.氧化过程方程式为4NaClO +5Se+2H SO +3H O=2Na SO +2Cl ↑+5H SeO ,氧化剂和还原剂的比 况下体积为6 10-5mol 22.4L/mol=0.001344L=1.344mL,故C正确;
3 2 4 2 2 4 2 2 3
为4:5,B项正确; D . 由 方 程 式 As O +6Zn+6H SO =2AsH +6ZnSO +3H O 可 知 , 消 耗 硫 酸 的 物 质 的 量 为
2 3 2 4 3 4 2
C.由流程分析,滤渣II为SiO 2 ;加入Na 2 SO 3 、稀H 2 SO 4 ,H 2 SeO 3 被还原成Se,Fe3+被还原为Fe2+, 1.210-4mol
2 10-5mol 6=1.2 10-4mol,则消耗稀硫酸的体积为 =10-3L=1mL,故D正确;
滤液III中主要存在的金属离子有Na+、Zn2+、Fe2+、Cu2+,C项错误; 0.12mol/L
第 10 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
答案选B。
①HCO在水溶液中即有电离平衡,又有水解平衡,Ce3+结合HCO电离平衡产生的CO2及水分子形成
3 3 3
14. (1)3NO-+2H+===NO-+2NO↑+H O
2 3 2
高温
难溶的Ce
2
(CO
3
)
3
nH
2
O,使HCO
3
电离平衡正向移动,H+增多,又促使HCO
3
的水解平衡正向移动,
(2)2.3Na SO +8C=====3Na S+4CO↑+4CO ↑
2 4 2 2
光照 产生大量H 2 CO 3 ,H 2 CO 3 过饱和分解成H 2 O和CO 2 ,所以本问离子方程式应填
(3) 2AgNO =====2Ag+2NO ↑+O ↑
3 2 2
△ “6HCO-+2Ce3++(n-3)H O=Ce (CO ) nH O+3CO ↑”;
(4)9MnO +2FeS+10H SO =====9MnSO +Fe (SO ) +10H O 3 2 2 3 3 2 2
2 2 4 4 2 4 3 2
②根据题目所给信息可知,Fe元素由反应物中+3价变为生成物中的+2价,做氧化剂降价,C H O
(5)SO2-+2NO +2OH-===SO2-+2NO-+H O 6 12 6
3 2 4 2 2
做 还 原 剂 被 氧 化 成 CO , 根 据 得 失 电 子 守 恒 , 本 问 方 程 式 应 填
(6)10CuSO +P +16H O===4H PO +10Cu+10H SO
4 4 2 3 4 2 4
Li CO C H O FePO LiFePO
(7)2P 4 +3Ba(OH) 2 +6H 2 O===3Ba(H 2 PO 2 ) 2 +2PH 3 ↑ “6 2 3+ 6 12 6+12 4=12 4+6CO↑+6H 2 O+6CO 2 ↑”。
(8)2Fe3++SO +2H O===2Fe2++SO2-+4H+
2 2 4 (3)①2AgI+Fe=2Ag+Fe2++2I-②FeI +Cl =I +FeCl ③2IO-+5HSO-=I +5SO2-+3H++H O
2 2 2 2 3 3 2 4 2
15.(1)【答案】①2MnO -+5H C O +6H+=2Mn2++8H O+10CO ↑②0.05mol/L
4 2 2 4 2 2
【解析】
【解析】
①KMnO 与H C O 反应时,KMnO 会将H C O 氧化为CO ,自身被还原为Mn2+,根据电子守恒 【分析】
4 2 2 4 4 2 2 4 2
可 知 KMnO 与 H C O 的 系 数 比 为 2 : 5 , 再 结 合 元 素 守 恒 可 得 离 子 方 程 式 为 含碘的海水中加入硝酸银生成AgI沉淀,过滤后得到碘化银浊液,加入铁粉发生反应
4 2 2 4
2MnO4 +5H
2
C
2
O
4
+6H+=2Mn2++8H
2
O+10CO
2
↑; 2AgI+Fe=2Ag+Fe2++2I-,通入氯气氧化碘离子生成碘单质;
1 ①由流程图可知悬浊液中含AgI,AgI可与Fe反应生成FeI 和Ag,FeI 易溶于水,在离子方程式中
2 2
②根据电子守恒可知(NH ) Fe(SO ) 与KMnO 存在数量关系:n(KMnO )=5n[(NH ) Fe(SO ) ],所以
4 2 4 2 4 4 4 2 4 2 能拆,故加入Fe粉进行转化反应的离子方程式为2AgI+Fe=2Ag+Fe2++2I-;
1
②通入Cl 的过程中,因I-还原性强于Fe2+,Cl 先氧化还原性强的I-,若氧化产物只有一种,则该氧
与 草 酸 反 应 后 剩 余 的 n (KMnO )= 5 ×0.2000mol/L×0.02L=0.0008mol , 则 与 草 酸 反 应 的 2 2
1 4
化产物只能是I ,故反应的化学方程式为FeI +Cl =I +FeCl ;
5 2 2 2 2 2
n (KMnO )=0.1000mol/L×0.012L-0.0008mol=0.0004mol,所以 n(H C O )= 2 ×0.0004mol=0.001mol,
2 4 2 2 4 ③先向NaIO 溶液中加入计量的NaHSO ,生成碘化物即含I-的物质;再向混合溶液中(含I-)加入NaIO
3 3 3
0.001mol
n(Ca2+)=n(H 2 C 2 O 4 )=0.001mol,所以c(Ca2+)= 0.02L =0.05mol/L。 溶液,反应得到I 2 ,上述制备I 2 的两个反应中I-为中间产物,总反应为IO 3 与HSO 3 发生氧化还原反
应,生成SO2和I ,根据得失电子守恒、电荷守恒及元素守恒配平离子方程式即可得:
4 2
(2)【答案】①6HCO-+2Ce3++(n-3)H O=Ce (CO ) nH O+3CO ↑
3 2 2 3 3 2 2
2IO-+5HSO-=I +5SO2-+3H++H O,故答案为:2IO-+5HSO-=I +5SO2-+3H++H O。
3 3 2 4 2 3 3 2 4 2
②6Li CO +C H O +12FePO =12LiFePO +6CO↑+6H O+6CO ↑
2 3 6 12 6 4 4 2 2
【解析】
第 11 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
16(10分)
填表时间:2022年__月___日,__:__;反思人:___________家长签字:_____________
本套暴露的主要问题
(1)CO(NH 2 ) 2 +H 2 O CO 2 ↑+2NH 3 ↑ 8NH 3 +6NO 2 7N 2 +12H 2 O 板块 该板块失分 对每一分失分的原因反思
2SO +O +4NH +2H O=2(NH ) SO 415NO+4NH +3O 4 6
2 2 3 2 4 2 4 3 2
单项选 总分27分
(2)2SiHCl +3H O===(HSiO) O+6HCl
3 2 2
择题 丢了( )分
(3)2HNO +(NH ) CO===2N ↑+CO ↑+3H O
2 2 2 2 2 2 双选题 总分16分
(4)2Mg(OH) +2SO +O ===2MgSO +2H O 丢了( )分
2 2 2 4 2
(5)N H +2NaClO===2NaCl+N ↑+2H O
主观题 总分57分
2 4 2 2
丢了( )分
(6)4Ag+4NaClO+2H O===4AgCl+4NaOH+O ↑
2 2
本套题的主要收获
17.(1) 2Fe+NaIO +3H O===2Fe(OH) ↓+NaI, 3 知识上
3 2 3
的收获
(2)Cu S+4Fe3+=2Cu2++4Fe2++S
2
技巧上
(3)CaO+O +V O Ca(VO )
2 2 3 3 2
的收获
(4)Mg B O ·H O+2H SO ===2MgSO +2H BO 本套题的综合反思
2 2 5 2 2 4 4 3 3
做题状
态
做题结
果
自我提
醒
第( )套化学暑假必刷密卷专用反思表
第 12 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!