文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题03
1.为研究废旧电池的再利用,实验室利用旧电池的铜帽和锌皮(主要成分为Zn和Cu)回收Cu
并制备皓矾(ZnSO∙7HO)的部分实验过程如图所示。下列叙述错误的是
4 2
A.“溶解”操作中溶液温度不宜过高
B.溶解时铜发生的反应为Cu+HO+2H+=Cu2++2HO
2 2 2
C.加入NaOH溶液后,若pH过高会使海绵铜中混有氢氧化铜杂质
D.“过滤”操作后,将滤液蒸发浓缩、冷却结晶即可得到纯净的ZnSO∙7HO
4 2
2.下列离子方程式的书写正确的是
A. 将1molCl 通入含1molFeI 的溶液中:2Fe2++2I-+2Cl=2Fe3++4Cl-+I
2 2 2 2
B. 1mol·L-1的NaAlO 溶液和2.5mol·L-1的HCl溶液等体积均匀混合:2AlO+5H+=Al3++
2
Al(OH) ↓+HO
3 2
C. 过量SO 通入NaClO溶液中:SO +HO+ClO-=HClO+HSO
2 2 2
D.Mg(HCO ) 溶液与足量的NaOH溶液反应:Mg2++HCO OH-=MgCO ↓+HO
3 2 + 3 2
答案:B
3.在特定碱性条件下,过量HO 可将Cr(Ⅲ)完全氧化成Cr(Ⅵ),其反应为HO+CrO+
2 2 2 2
W↑→CrO+Y(未配平),下列有关说法错误的是
A. W为OH-
B. 上述反应中氧化剂和还原剂的物质的量之比为3∶2
C. 1mol H O 参加反应时,转移电子的物质的量为2mol
2 2
D. 在酸性条件下Cr O可以转化为CrO
2
4.通常超市里的商品在摆放到货架前会先进行分类,因此我们在超市能迅速找到所需商品。
下列关于物质的分类组合正确的是
选项 物质 类别
A 钠、液氯、铁、冰水混合物 纯净物
B 碘伏、生石灰、青铜、空气 混合物
C HSO 、HClO、稀盐酸、NaCl溶液 电解质
2 4 4
D 纯碱、NaOH、NH 、KOH 碱
3
5.已知:①Al(OH) 固体的熔点为300℃;②无水AlCl 晶体易升华;③熔融状态的HgCl 不
3 3 2能导电,稀溶液具有弱的导电能力且可作为手术刀的消毒液,下列关于Al(OH) 、AlCl 和HgCl 的
3 3 2
说法正确的是
A. 均为弱电解质
B. 均为离子化合物
C. HgCl 的水溶液导电能力很弱,说明其难溶于水
2
D. HgCl 在水中的电离方程式可能是HgCl HgCl++Cl-
2 2
6.下列离子方程式正确的是
A.澄清石灰水与过量CO 反应:CO+Ca2++2OH-=CaCO ↓+HO
2 2 3 2
B.Fe2+与HO 在酸性溶液中的反应:2Fe2++HO=2Fe3++2HO+2H+
2 2 2 2 2
C.向沸水中滴加饱和的FeCl 溶液制备Fe(OH) 胶体:Fe3++3HO=== Fe(OH) (胶体)+3H+
3 3 2 3
D.向碳酸氢铵溶液中加入足量石灰水:Ca2++HCO OH-=CaCO ↓+HO
+ 3 2
7.下列实验中,能够正确描述反应的离子方程式是
A. 磁性氧化铁溶于稀HNO:Fe O+12H++NO 3Fe3++NO↑+6HO
3 3 4 = 2
B. 海水提溴工艺中,用纯碱溶液富集Br :3Br +3CO 5Br-+BrO 3CO↑
2 2 = + 2
C. 用石灰乳制漂白粉:Ca2++2OH-+Cl=Ca2++Cl-+ClO-+HO
2 2
D. 用足量NaSO 的碱性溶液除去水中的Cl:4Cl+SO 5HO=10H++2SO+8Cl-
2 2 3 2 2 2 + 2
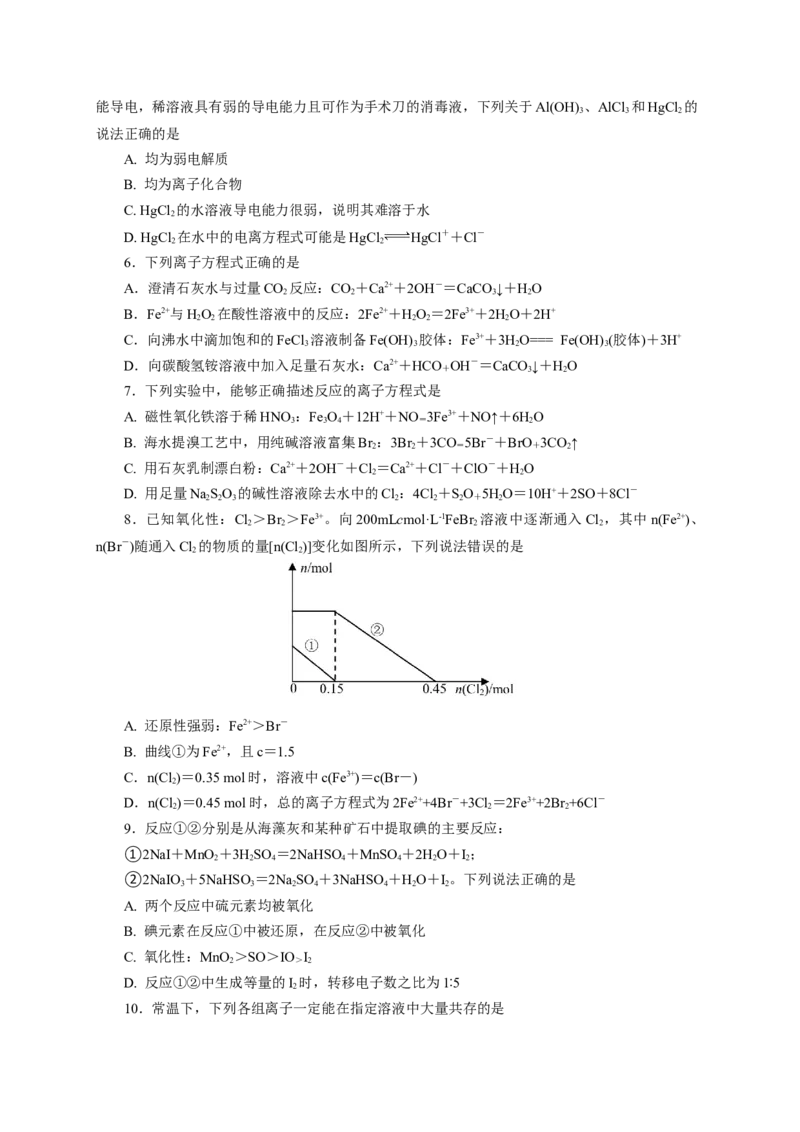
8.已知氧化性:Cl >Br >Fe3+。向200mLcmol·L-1FeBr 溶液中逐渐通入Cl ,其中n(Fe2+)、
2 2 2 2
n(Br-)随通入Cl 的物质的量[n(Cl )]变化如图所示,下列说法错误的是
2 2
A. 还原性强弱:Fe2+>Br-
B. 曲线①为Fe2+,且c=1.5
C.n(Cl )=0.35 mol时,溶液中c(Fe3+)=c(Br-)
2
D.n(Cl )=0.45 mol时,总的离子方程式为2Fe2++4Br-+3Cl=2Fe3++2Br +6Cl-
2 2 2
9.反应①②分别是从海藻灰和某种矿石中提取碘的主要反应:
①2NaI+MnO +3HSO =2NaHSO+MnSO +2HO+I;
2 2 4 4 4 2 2
②2NaIO +5NaHSO=2NaSO +3NaHSO+HO+I。下列说法正确的是
3 3 2 4 4 2 2
A. 两个反应中硫元素均被氧化
B. 碘元素在反应①中被还原,在反应②中被氧化
C. 氧化性:MnO >SO>IO I
2 > 2
D. 反应①②中生成等量的I 时,转移电子数之比为1∶5
2
10.常温下,下列各组离子一定能在指定溶液中大量共存的是A.在中性溶液中:Na+、Ba2+、SO、Cl-
B. 与Al反应能放出H 的溶液中:Fe2+、K+、NO
2 、SO
C.=1×10-13mol·L-1的溶液中:NH、Na+、Cl-、NO
D.水电离的c(H+)=1×10-13mol·L-1的溶液中:K+、Na+、AlO、CO
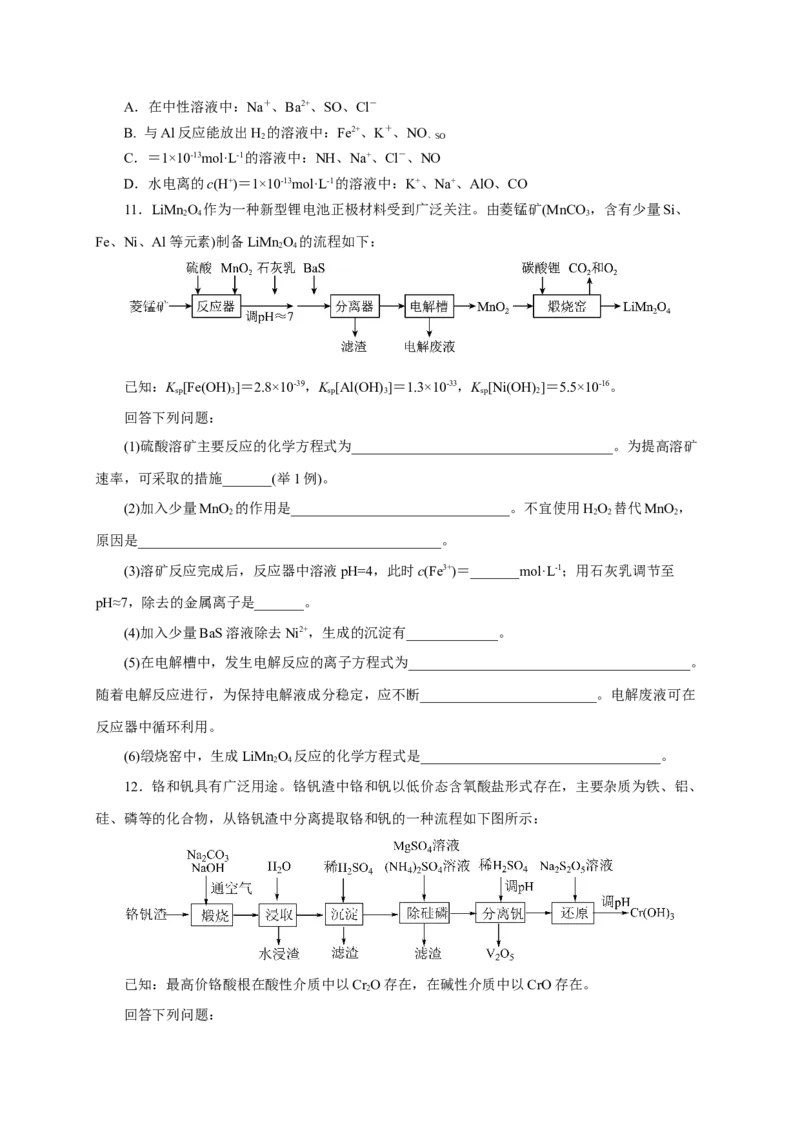
11.LiMn O 作为一种新型锂电池正极材料受到广泛关注。由菱锰矿(MnCO ,含有少量Si、
2 4 3
Fe、Ni、Al等元素)制备LiMn O 的流程如下:
2 4
已知:K [Fe(OH) ]=2.8×10-39,K [Al(OH) ]=1.3×10-33,K [Ni(OH) ]=5.5×10-16。
sp 3 sp 3 sp 2
回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为_____________________________________。为提高溶矿
速率,可采取的措施_______(举1例)。
(2)加入少量MnO 的作用是_______________________________。不宜使用HO 替代MnO ,
2 2 2 2
原因是___________________________________________。
(3)溶矿反应完成后,反应器中溶液pH=4,此时c(Fe3+)=_______mol·L-1;用石灰乳调节至
pH≈7,除去的金属离子是_______。
(4)加入少量BaS溶液除去Ni2+,生成的沉淀有_____________。
(5)在电解槽中,发生电解反应的离子方程式为________________________________________。
随着电解反应进行,为保持电解液成分稳定,应不断_________________________。电解废液可在
反应器中循环利用。
(6)缎烧窑中,生成LiMn O 反应的化学方程式是__________________________________。
2 4
12.铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、
硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示:
已知:最高价铬酸根在酸性介质中以Cr O存在,在碱性介质中以CrO存在。
2
回答下列问题:(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为_______(填化
学式)。
(2)水浸渣中主要有SiO 和______________。
2
(3)“沉淀”步骤调pH到弱碱性,主要除去的杂质是_______________。
(4)“除硅磷”步骤中,使硅、磷分别以MgSiO 和MgNH PO 的形式沉淀,该步需要控制溶液的
3 4 4
pH≈9以达到最好的除杂效果,若pH<9时,会导致_______________________________;pH>9时,
会导致_____________________________。
(5)“分离钒”步骤中,将溶液pH调到1.8左右得到VO 沉淀,VO 在pH<1时,溶解 为 VO或
2 5 2 5
VO3+在碱性条件下,溶解为VO或VO VO 具有_______(填标号)。
,上述性质说明 2 5
A.酸性 B.碱性 C.两性
(6)“还原”步骤中加入焦亚硫酸钠(NaSO)溶液,反应的离子方程式为_____________________。
2 2 5