文档内容
第 27 讲 氮及其化合物的转化关系
[复习目标] 1.能从物质类别、氮的化合价变化理解氮及其化合物的转化关系。2.能从含氮
物质的性质和转化的视角解释生产、生活中的相关现象。
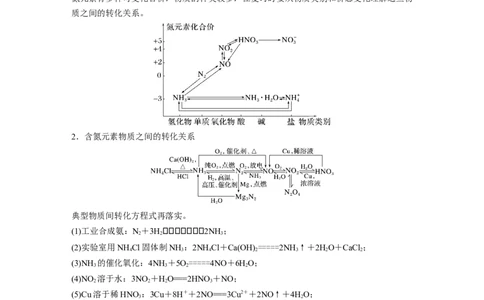
1.氮元素的“价—类”二维图
氮元素有多种可变化合价,物质的种类较多,在复习时要从物质类别和价态变化理解这些物
质之间的转化关系。
2.含氮元素物质之间的转化关系
典型物质间转化方程式再落实。
(1)工业合成氨:N+3H2NH ;
2 2 3
(2)实验室用NH Cl固体制NH :2NH Cl+Ca(OH) =====2NH ↑+2HO+CaCl ;
4 3 4 2 3 2 2
(3)NH 的催化氧化:4NH +5O=====4NO+6HO;
3 3 2 2
(4)NO 溶于水:3NO +HO===2HNO+NO;
2 2 2 3
(5)Cu溶于稀HNO:3Cu+8H++2NO===3Cu2++2NO↑+4HO;
3 2
(6)Cu溶于浓HNO:Cu+4H++2NO===Cu2++2NO ↑+2HO;
3 2 2
(7)炽热的炭在浓硝酸中燃烧:C+4HNO(浓)=====CO↑+4NO ↑+2HO;
3 2 2 2
(8)浓硝酸见光分解:4HNO=====4NO ↑+O↑+2HO。
3 2 2 2
一、氮在自然界中的循环
1.自然界中氮的循环如图所示。下列说法不正确的是( )A.工业合成氨属于人工固氮
B.雷电作用下N 与O 发生了化学反应
2 2
C.在氮的循环中不涉及氧化还原反应
D.含氮无机物与含氮有机化合物可相互转化
答案 C
解析 工业合成氨是氮气和氢气在高温、高压和催化剂条件下生成氨气,属于人工固氮,故
A正确;雷电作用下N 与O 发生反应生成NO,故B正确;在氮的循环中,工业合成氨、
2 2
雷电作用过程中N元素化合价改变,涉及氧化还原反应,故C错误;含氮无机物与含氮有
机化合物可相互转化,如氨气可合成尿素,故D正确。
2.(2022·石家庄高三模拟)下列关于自然界中氮循环(如图)的说法错误的是( )
A.①和②均属于氮的固定
B.氢、氧元素也参与了自然界中的氮循环
C.④中每生成1 mol NO,消耗2 mol O
2
D.③和⑤过程中氮元素分别被还原和氧化
答案 D
解析 反应①将N 转化为NO,属于氮的固定,反应②属于植物固氮,A正确;由图示知,
2
氮循环过程中涉及氢、氧元素,B正确;反应④是O 将NH 氧化为NO,N元素化合价由-
2 3
3价升高到+5价,即生成1 mol NO失去8 mol电子,根据得失电子守恒可知每生成 1 mol
NO需要消耗2 mol O ,C正确;反应③中NO被氧化为NO,反应⑤中NO被还原为N ,D
2 2
错误。二、氮及其化合物的转化与物质推断
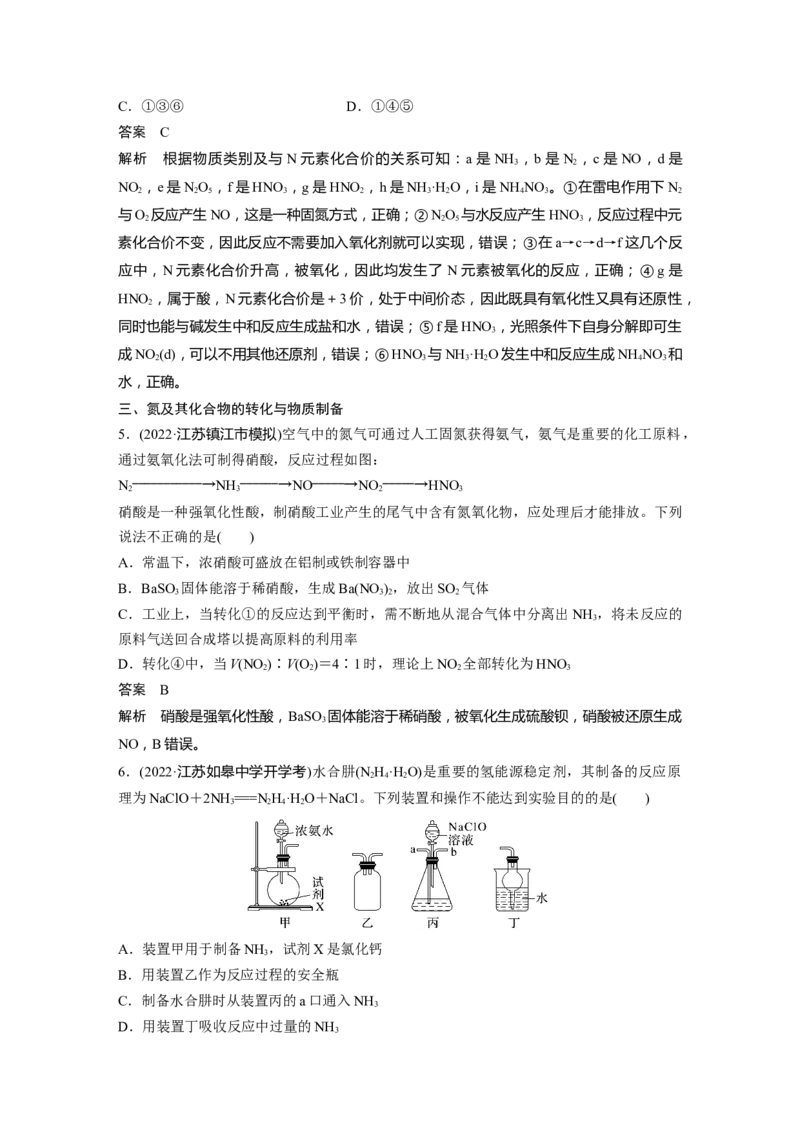
3.下列关系图中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。当X无论是强
酸还是强碱时都有如下转化关系(其他产物及反应所需条件均已略去),当X是强碱时,过量
的B跟Cl 反应除生成C外,另一产物是盐酸盐。
2
下列说法不正确的是( )
A.当X是强酸时,A、B、C、D、E、F中均含同一种元素,F可能是HSO
2 4
B.当X是强碱时,A、B、C、D、E、F中均含同一种元素,F是HNO
3
C.当X是强酸时,C在常温下是气态单质
D.B和Cl 的反应为氧化还原反应
2
答案 C
解析 当X是强碱时,和强碱反应产生的气态氢化物B可判断为NH ,则A为铵盐,过量
3
的B跟Cl 反应生成的盐酸盐是 NH Cl,则C为N ,由此判断D为NO、E为NO 、F为
2 4 2 2
HNO ;A和强酸反应生成的B能被Cl 氧化,且生成的C能被O 连续氧化,在常见的物质
3 2 2
中可考虑A为硫化物,所以,当X是强酸时,A、B、C、D、E、F可分别为(NH )S、
4 2
HS、S、SO 、SO 、HSO ,故A、B正确,C错误;B是氨气或硫化氢,氨气与Cl 反应生
2 2 3 2 4 2
成氯化铵和氮气,硫化氢和氯气反应生成硫单质和氯化氢,因此B与氯气的反应是氧化还
原反应,故D正确。
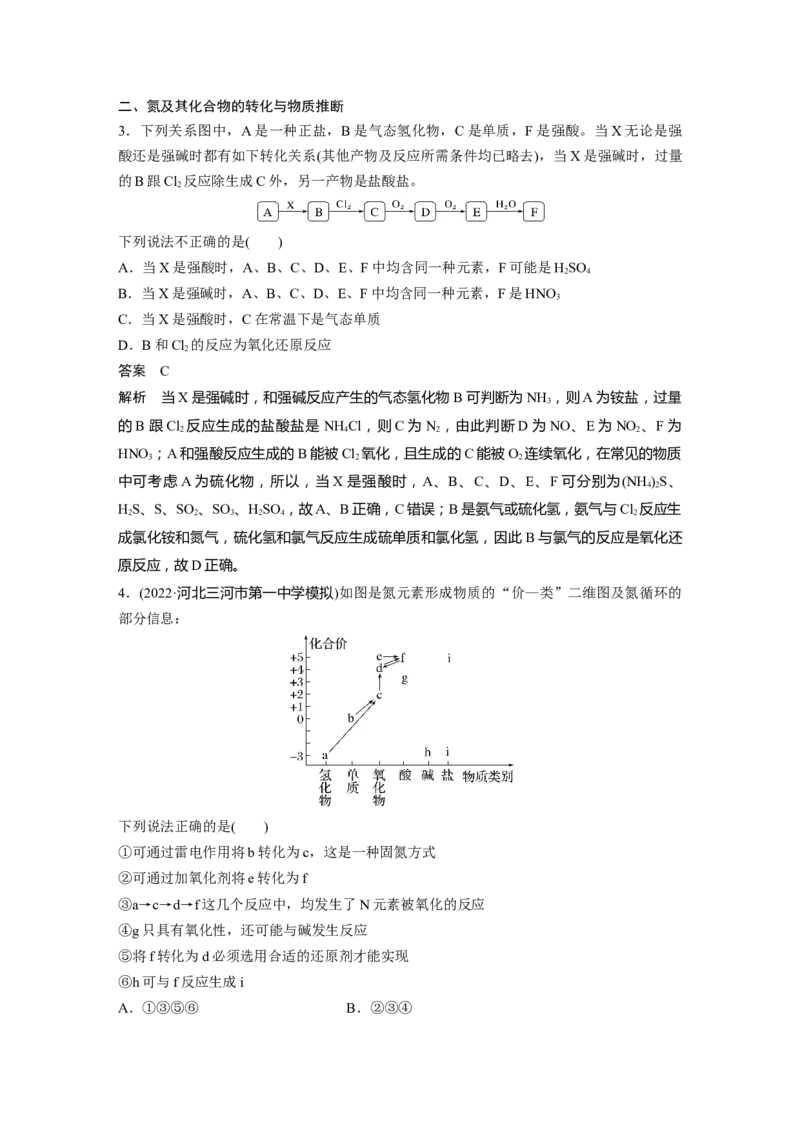
4.(2022·河北三河市第一中学模拟)如图是氮元素形成物质的“价—类”二维图及氮循环的
部分信息:
下列说法正确的是( )
①可通过雷电作用将b转化为c,这是一种固氮方式
②可通过加氧化剂将e转化为f
③a→c→d→f这几个反应中,均发生了N元素被氧化的反应
④g只具有氧化性,还可能与碱发生反应
⑤将f转化为d必须选用合适的还原剂才能实现
⑥h可与f反应生成i
A.①③⑤⑥ B.②③④C.①③⑥ D.①④⑤
答案 C
解析 根据物质类别及与N元素化合价的关系可知:a是NH ,b是N ,c是NO,d是
3 2
NO ,e是NO ,f是HNO ,g是HNO ,h是NH ·H O,i是NH NO 。①在雷电作用下N
2 2 5 3 2 3 2 4 3 2
与O 反应产生NO,这是一种固氮方式,正确;②NO 与水反应产生HNO,反应过程中元
2 2 5 3
素化合价不变,因此反应不需要加入氧化剂就可以实现,错误;③在a→c→d→f这几个反
应中,N元素化合价升高,被氧化,因此均发生了 N元素被氧化的反应,正确;④g是
HNO ,属于酸,N元素化合价是+3价,处于中间价态,因此既具有氧化性又具有还原性,
2
同时也能与碱发生中和反应生成盐和水,错误;⑤f是HNO ,光照条件下自身分解即可生
3
成NO (d),可以不用其他还原剂,错误;⑥HNO 与NH ·H O发生中和反应生成NH NO 和
2 3 3 2 4 3
水,正确。
三、氮及其化合物的转化与物质制备
5.(2022·江苏镇江市模拟)空气中的氮气可通过人工固氮获得氨气,氨气是重要的化工原料,
通过氨氧化法可制得硝酸,反应过程如图:
N―――――――――――→NH ――――――→NO―――――→NO ―――――→HNO
2 3 2 3
硝酸是一种强氧化性酸,制硝酸工业产生的尾气中含有氮氧化物,应处理后才能排放。下列
说法不正确的是( )
A.常温下,浓硝酸可盛放在铝制或铁制容器中
B.BaSO 固体能溶于稀硝酸,生成Ba(NO ),放出SO 气体
3 3 2 2
C.工业上,当转化①的反应达到平衡时,需不断地从混合气体中分离出NH ,将未反应的
3
原料气送回合成塔以提高原料的利用率
D.转化④中,当V(NO )∶V(O )=4∶1时,理论上NO 全部转化为HNO
2 2 2 3
答案 B
解析 硝酸是强氧化性酸,BaSO 固体能溶于稀硝酸,被氧化生成硫酸钡,硝酸被还原生成
3
NO,B错误。
6.(2022·江苏如皋中学开学考)水合肼(N H·H O)是重要的氢能源稳定剂,其制备的反应原
2 4 2
理为NaClO+2NH ===NH·H O+NaCl。下列装置和操作不能达到实验目的的是( )
3 2 4 2
A.装置甲用于制备NH ,试剂X是氯化钙
3
B.用装置乙作为反应过程的安全瓶
C.制备水合肼时从装置丙的a口通入NH
3
D.用装置丁吸收反应中过量的NH
3答案 A
解析 浓氨水需受热或加入碱性物质才能分解产生NH ,CaCl 不能使浓氨水分解,A项错
3 2
误;化学实验装置中的安全瓶的进气管和出气管均较短,B项正确;氨气密度比空气小,为
了利于氨气与NaClO溶液反应,应从装置丙的a口通入氨气,C项正确;氨气会污染环境,
用装置丁可吸收过量的NH ,并能防倒吸,D项正确。
3
7.(2022·山东淄博市模拟)氨基甲酸铵(NH COONH)易分解,易水解,难溶于CCl 。某小组
2 4 4
设计如图所示装置制备氨基甲酸铵。
已知:2NH (g)+ CO(g)NH COONH (s) ΔH<0
3 2 2 4
下列分析错误的是( )
A.A装置的优点是能够随时控制反应的发生和停止
B.装置B、C、E中试剂可分别为饱和碳酸氢钠溶液、浓硫酸、PO 固体
2 5
C.装置D使用冰水浴
D.装置F中所用试剂可为NH Cl与熟石灰
4
答案 B
解析 A装置为碳酸钙与盐酸反应制备CO 的简易装置,该装置的优点是能够随时控制反应
2
的发生和停止,A正确;氨基甲酸铵易水解,进入装置D的气体必须是干燥纯净气体,左
侧装置B、C试剂可分别为饱和碳酸氢钠溶液、浓硫酸,制备纯净干燥的CO ,装置F可用
2
NH Cl与熟石灰制备氨气,E中试剂需干燥氨气,可以选用碱石灰,但不能选用 PO 固体,
4 2 5
B错误、D正确;制备氨基甲酸铵的反应为放热反应,制得的物质易分解,所以装置D需降
温,使用冰水浴,C正确。
四、氮及其化合物的转化与典型物质性质探究
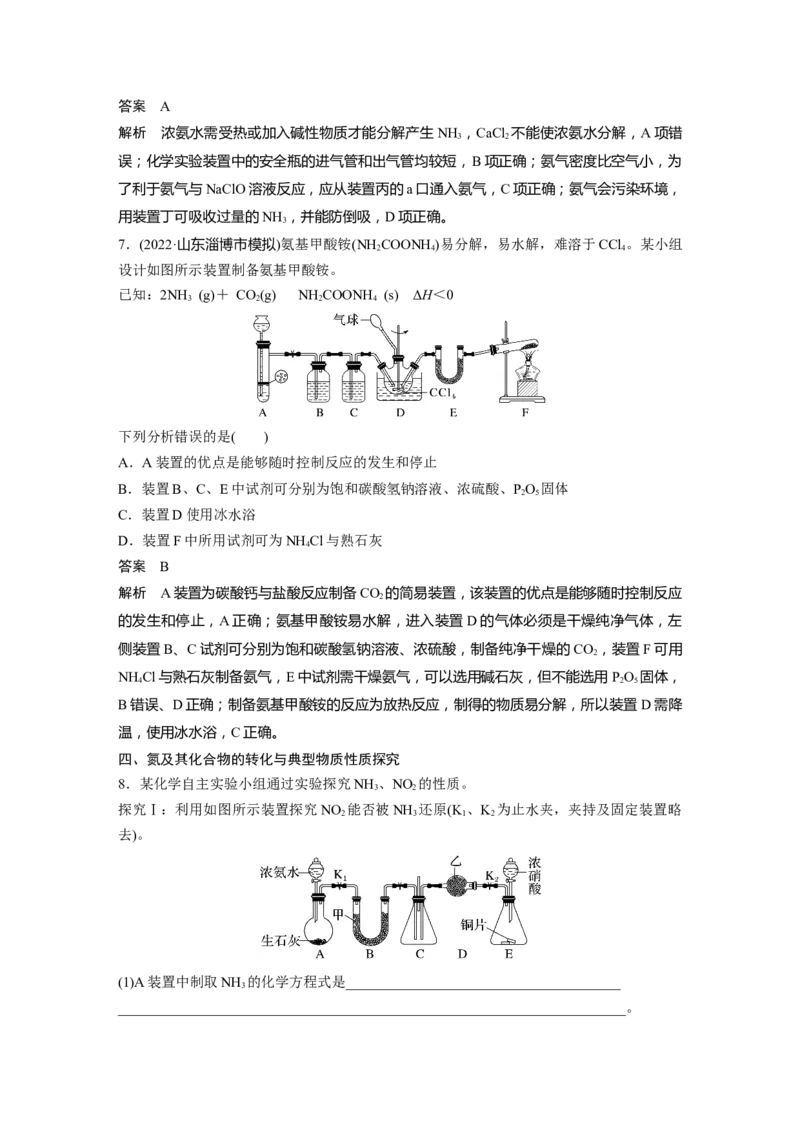
8.某化学自主实验小组通过实验探究NH 、NO 的性质。
3 2
探究Ⅰ:利用如图所示装置探究NO 能否被NH 还原(K 、K 为止水夹,夹持及固定装置略
2 3 1 2
去)。
(1)A装置中制取NH 的化学方程式是_______________________________________
3
________________________________________________________________________。(2)甲、乙分别是________(填字母)。
a.浓硫酸、碱石灰
b.碱石灰、碱石灰
c.碱石灰、无水氯化钙
d.五氧化二磷、五氧化二磷
(3)若NO 能够被NH 还原,预期C装置中能观察到的现象是__________________________。
2 3
(4)此实验装置存在一个明显的缺陷是_______________________________________
________________________________________________________________________。
探究Ⅱ:探究NO 、O 混合气体的喷泉实验。
2 2
(5)请在G装置中的虚线上描出导管实线图。
(6)G装置中浓硫酸有三种作用:混合NO 、O 气体;干燥NO 、O; __________。
2 2 2 2
(7)将G装置上面的圆底烧瓶收集满气体(标准状况下)进行喷泉实验,若混合气体全部被吸收,
则所得溶液物质的量浓度为______ mol·L-1(结果保留两位有效数字)。
答案 (1)NH ·H O+CaO===NH ↑+Ca(OH) (2)c (3)C装置中混合气体颜色变浅
3 2 3 2
(4)缺少尾气处理装置 (5) (进气管短,出气管长) (6)观察气泡的速率,控制混合气体
的比例
(7)0.036
解析 (7)烧瓶中充满溶液,则恰好发生反应4NO +O+2HO===4HNO,HNO 的物质的量
2 2 2 3 3
是恰好完全反应的NO 和O(体积比4∶1)总物质的量的,溶液体积等于烧瓶体积,设烧瓶
2 2
体 积 为 V L , 则 溶 液 的 物 质 的 量 浓 度 为 = × mol·L - 1≈0.036 mol·L - 1 。
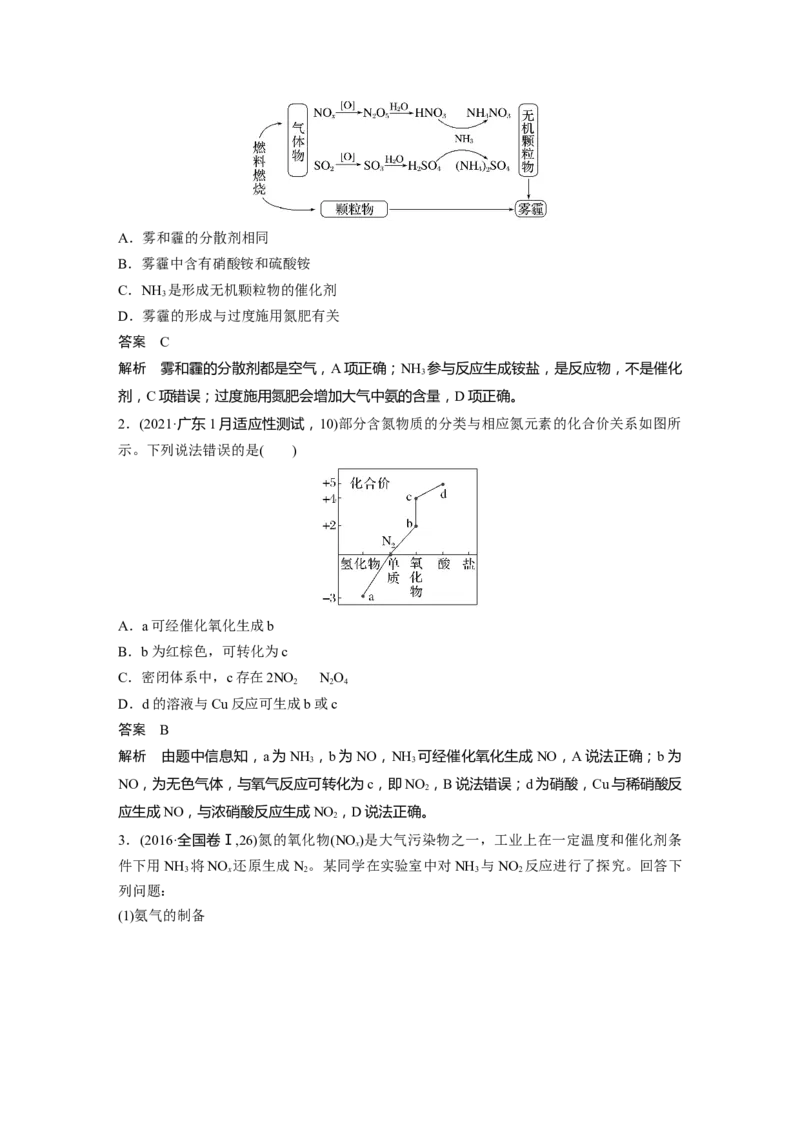
1.(2018·全国卷Ⅱ,8)研究表明,氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关(如下
图所示)。下列叙述错误的是( )A.雾和霾的分散剂相同
B.雾霾中含有硝酸铵和硫酸铵
C.NH 是形成无机颗粒物的催化剂
3
D.雾霾的形成与过度施用氮肥有关
答案 C
解析 雾和霾的分散剂都是空气,A项正确;NH 参与反应生成铵盐,是反应物,不是催化
3
剂,C项错误;过度施用氮肥会增加大气中氨的含量,D项正确。
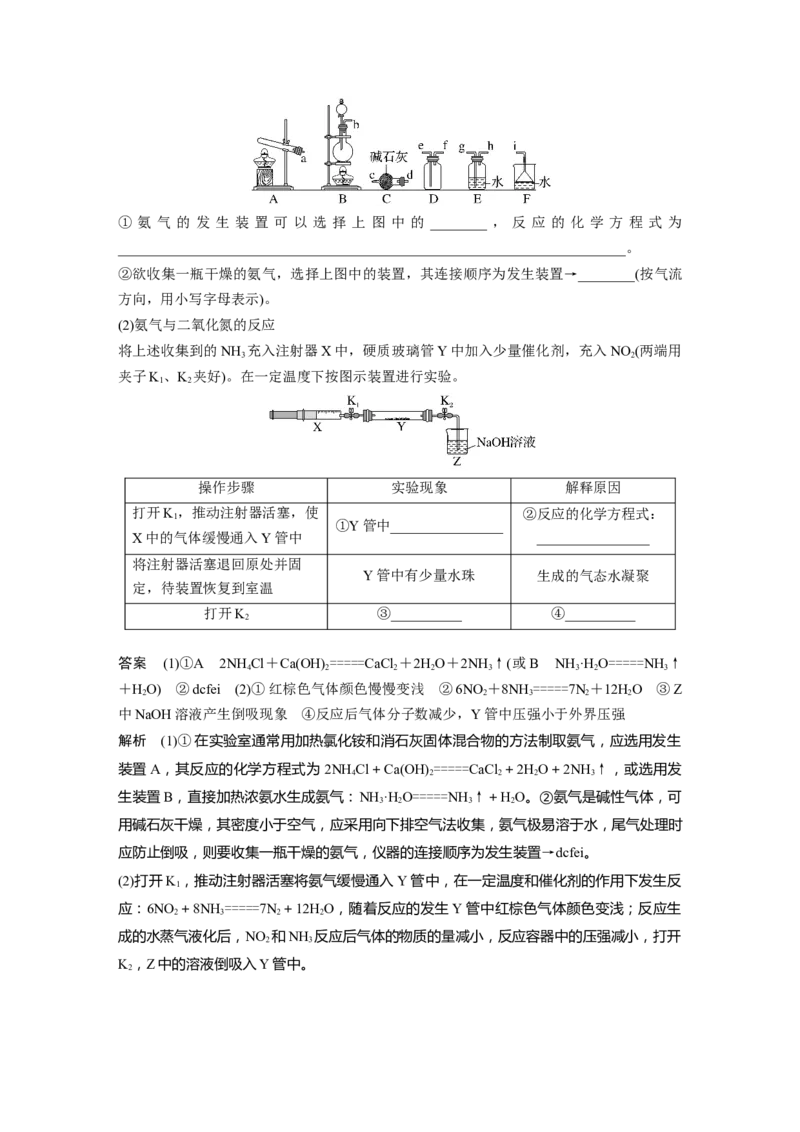
2.(2021·广东1月适应性测试,10)部分含氮物质的分类与相应氮元素的化合价关系如图所
示。下列说法错误的是( )
A.a可经催化氧化生成b
B.b为红棕色,可转化为c
C.密闭体系中,c存在2NO NO
2 2 4
D.d的溶液与Cu反应可生成b或c
答案 B
解析 由题中信息知,a为NH ,b为NO,NH 可经催化氧化生成NO,A说法正确;b为
3 3
NO,为无色气体,与氧气反应可转化为c,即NO ,B说法错误;d为硝酸,Cu与稀硝酸反
2
应生成NO,与浓硝酸反应生成NO ,D说法正确。
2
3.(2016·全国卷Ⅰ,26)氮的氧化物(NO)是大气污染物之一,工业上在一定温度和催化剂条
x
件下用NH 将NO 还原生成N 。某同学在实验室中对NH 与NO 反应进行了探究。回答下
3 x 2 3 2
列问题:
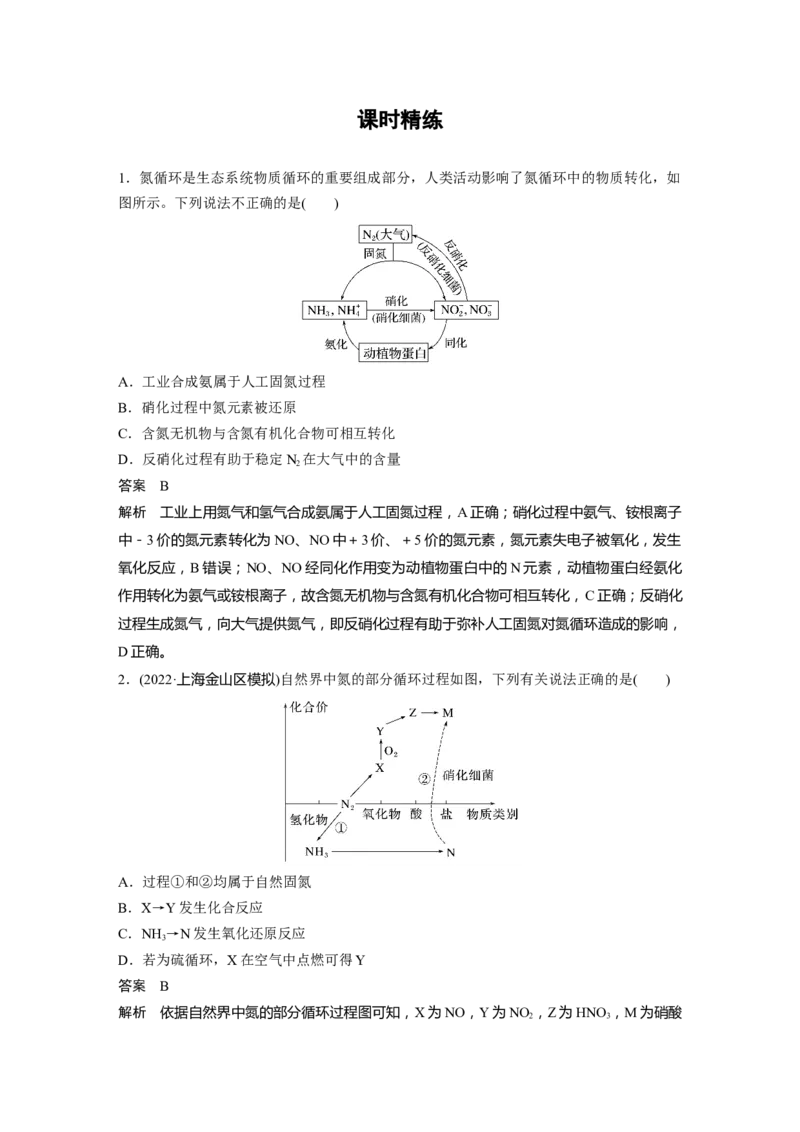
(1)氨气的制备① 氨 气 的 发 生 装 置 可 以 选 择 上 图 中 的 ________ , 反 应 的 化 学 方 程 式 为
________________________________________________________________________。
②欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为发生装置→________(按气流
方向,用小写字母表示)。
(2)氨气与二氧化氮的反应
将上述收集到的NH 充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO (两端用
3 2
夹子K、K 夹好)。在一定温度下按图示装置进行实验。
1 2
操作步骤 实验现象 解释原因
打开K,推动注射器活塞,使 ②反应的化学方程式:
1
①Y管中________________
X中的气体缓慢通入Y管中 ________________
将注射器活塞退回原处并固
Y管中有少量水珠 生成的气态水凝聚
定,待装置恢复到室温
打开K ③__________ ④__________
2
答案 (1)①A 2NH Cl+Ca(OH) =====CaCl +2HO+2NH ↑(或B NH ·H O=====NH ↑
4 2 2 2 3 3 2 3
+HO) ②dcfei (2)①红棕色气体颜色慢慢变浅 ②6NO +8NH =====7N +12HO ③Z
2 2 3 2 2
中NaOH溶液产生倒吸现象 ④反应后气体分子数减少,Y管中压强小于外界压强
解析 (1)①在实验室通常用加热氯化铵和消石灰固体混合物的方法制取氨气,应选用发生
装置A,其反应的化学方程式为2NH Cl+Ca(OH) =====CaCl +2HO+2NH ↑,或选用发
4 2 2 2 3
生装置B,直接加热浓氨水生成氨气:NH ·H O=====NH ↑+HO。②氨气是碱性气体,可
3 2 3 2
用碱石灰干燥,其密度小于空气,应采用向下排空气法收集,氨气极易溶于水,尾气处理时
应防止倒吸,则要收集一瓶干燥的氨气,仪器的连接顺序为发生装置→dcfei。
(2)打开K ,推动注射器活塞将氨气缓慢通入Y管中,在一定温度和催化剂的作用下发生反
1
应:6NO +8NH =====7N +12HO,随着反应的发生Y管中红棕色气体颜色变浅;反应生
2 3 2 2
成的水蒸气液化后,NO 和NH 反应后气体的物质的量减小,反应容器中的压强减小,打开
2 3
K,Z中的溶液倒吸入Y管中。
2课时精练
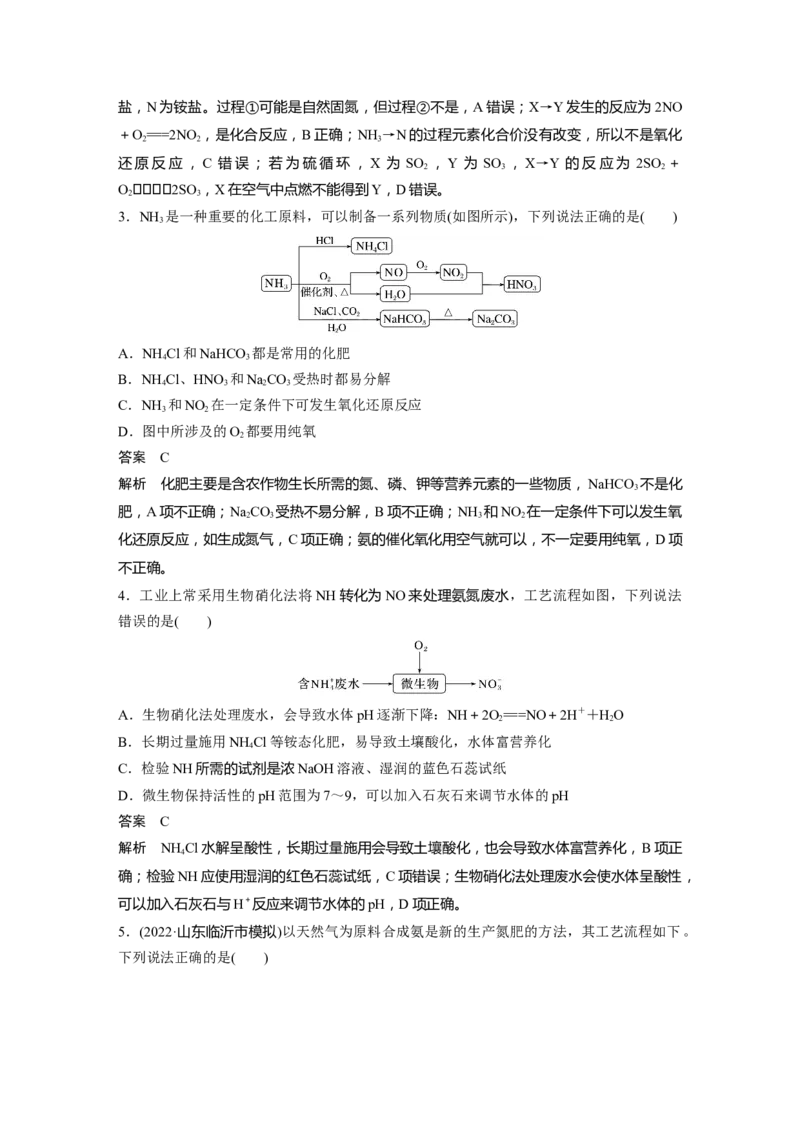
1.氮循环是生态系统物质循环的重要组成部分,人类活动影响了氮循环中的物质转化,如
图所示。下列说法不正确的是( )
A.工业合成氨属于人工固氮过程
B.硝化过程中氮元素被还原
C.含氮无机物与含氮有机化合物可相互转化
D.反硝化过程有助于稳定N 在大气中的含量
2
答案 B
解析 工业上用氮气和氢气合成氨属于人工固氮过程,A正确;硝化过程中氨气、铵根离子
中-3价的氮元素转化为NO、NO中+3价、+5价的氮元素,氮元素失电子被氧化,发生
氧化反应,B错误;NO、NO经同化作用变为动植物蛋白中的N元素,动植物蛋白经氨化
作用转化为氨气或铵根离子,故含氮无机物与含氮有机化合物可相互转化,C正确;反硝化
过程生成氮气,向大气提供氮气,即反硝化过程有助于弥补人工固氮对氮循环造成的影响,
D正确。
2.(2022·上海金山区模拟)自然界中氮的部分循环过程如图,下列有关说法正确的是( )
A.过程①和②均属于自然固氮
B.X→Y发生化合反应
C.NH →N发生氧化还原反应
3
D.若为硫循环,X在空气中点燃可得Y
答案 B
解析 依据自然界中氮的部分循环过程图可知,X为NO,Y为NO ,Z为HNO,M为硝酸
2 3盐,N为铵盐。过程①可能是自然固氮,但过程②不是,A错误;X→Y发生的反应为2NO
+O===2NO ,是化合反应,B正确;NH →N的过程元素化合价没有改变,所以不是氧化
2 2 3
还原反应,C 错误;若为硫循环,X 为 SO ,Y 为 SO ,X→Y 的反应为 2SO +
2 3 2
O2SO ,X在空气中点燃不能得到Y,D错误。
2 3
3.NH 是一种重要的化工原料,可以制备一系列物质(如图所示),下列说法正确的是( )
3
A.NH Cl和NaHCO 都是常用的化肥
4 3
B.NH Cl、HNO 和NaCO 受热时都易分解
4 3 2 3
C.NH 和NO 在一定条件下可发生氧化还原反应
3 2
D.图中所涉及的O 都要用纯氧
2
答案 C
解析 化肥主要是含农作物生长所需的氮、磷、钾等营养元素的一些物质,NaHCO 不是化
3
肥,A项不正确;NaCO 受热不易分解,B项不正确;NH 和NO 在一定条件下可以发生氧
2 3 3 2
化还原反应,如生成氮气,C项正确;氨的催化氧化用空气就可以,不一定要用纯氧,D项
不正确。
4.工业上常采用生物硝化法将NH转化为NO来处理氨氮废水,工艺流程如图,下列说法
错误的是( )
A.生物硝化法处理废水,会导致水体pH逐渐下降:NH+2O===NO+2H++HO
2 2
B.长期过量施用NH Cl等铵态化肥,易导致土壤酸化,水体富营养化
4
C.检验NH所需的试剂是浓NaOH溶液、湿润的蓝色石蕊试纸
D.微生物保持活性的pH范围为7~9,可以加入石灰石来调节水体的pH
答案 C
解析 NH Cl水解呈酸性,长期过量施用会导致土壤酸化,也会导致水体富营养化,B项正
4
确;检验NH应使用湿润的红色石蕊试纸,C项错误;生物硝化法处理废水会使水体呈酸性,
可以加入石灰石与H+反应来调节水体的pH,D项正确。
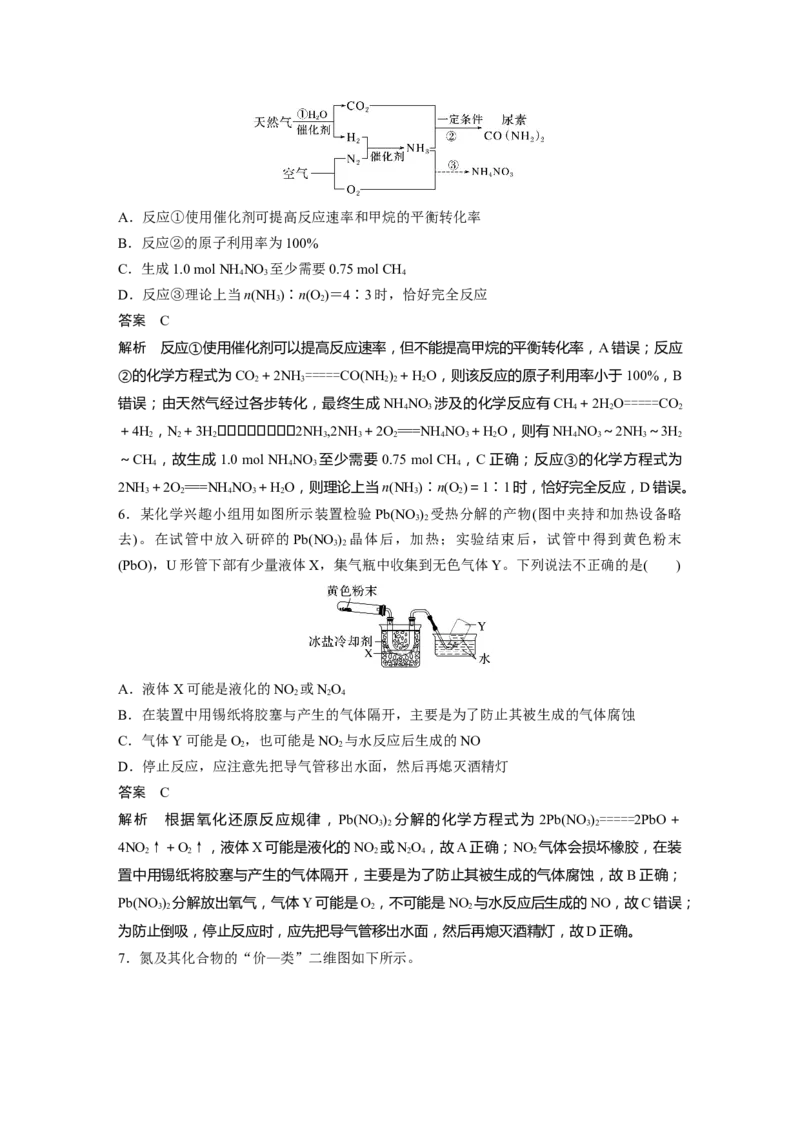
5.(2022·山东临沂市模拟)以天然气为原料合成氨是新的生产氮肥的方法,其工艺流程如下。
下列说法正确的是( )A.反应①使用催化剂可提高反应速率和甲烷的平衡转化率
B.反应②的原子利用率为100%
C.生成1.0 mol NH NO 至少需要0.75 mol CH
4 3 4
D.反应③理论上当n(NH )∶n(O )=4∶3时,恰好完全反应
3 2
答案 C
解析 反应①使用催化剂可以提高反应速率,但不能提高甲烷的平衡转化率,A错误;反应
②的化学方程式为CO +2NH =====CO(NH) +HO,则该反应的原子利用率小于100%,B
2 3 2 2 2
错误;由天然气经过各步转化,最终生成NH NO 涉及的化学反应有CH +2HO=====CO
4 3 4 2 2
+4H,N+3H2NH ,2NH+2O===NH NO +HO,则有NH NO ~2NH ~3H
2 2 2 3 3 2 4 3 2 4 3 3 2
~CH ,故生成1.0 mol NH NO 至少需要0.75 mol CH ,C正确;反应③的化学方程式为
4 4 3 4
2NH +2O===NH NO +HO,则理论上当n(NH )∶n(O )=1∶1时,恰好完全反应,D错误。
3 2 4 3 2 3 2
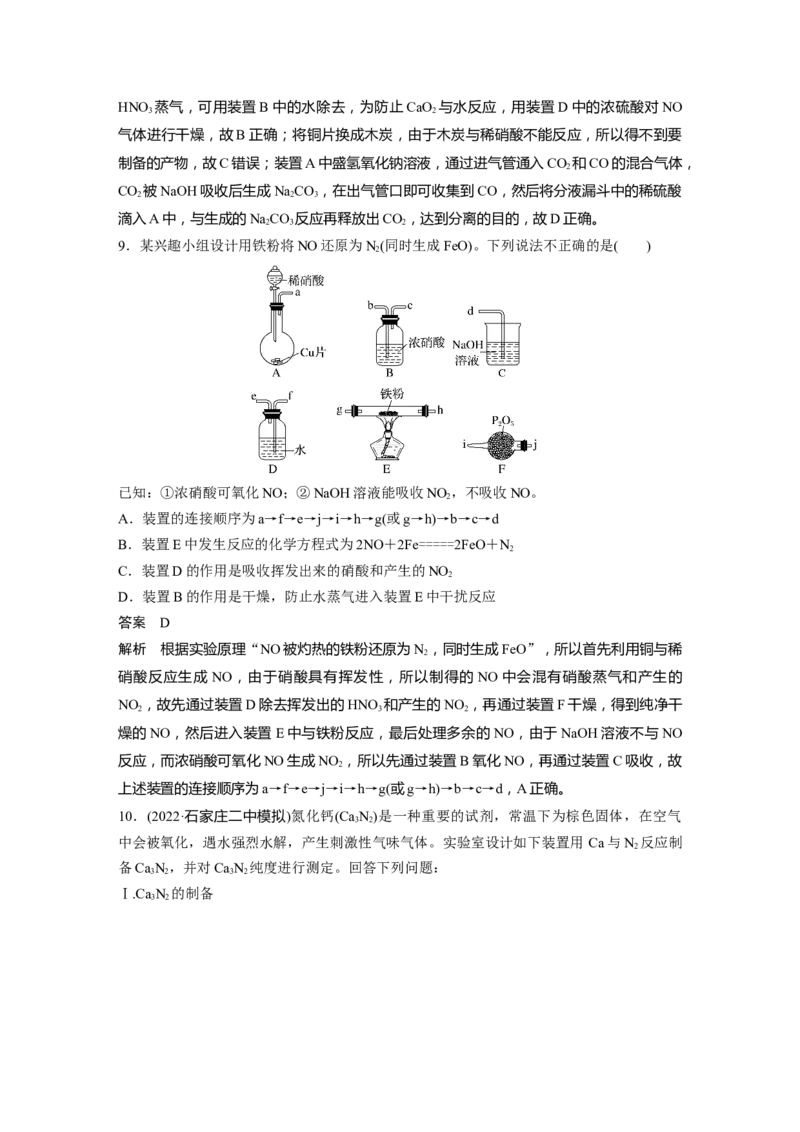
6.某化学兴趣小组用如图所示装置检验Pb(NO ) 受热分解的产物(图中夹持和加热设备略
3 2
去)。在试管中放入研碎的Pb(NO ) 晶体后,加热;实验结束后,试管中得到黄色粉末
3 2
(PbO),U形管下部有少量液体X,集气瓶中收集到无色气体Y。下列说法不正确的是( )
A.液体X可能是液化的NO 或NO
2 2 4
B.在装置中用锡纸将胶塞与产生的气体隔开,主要是为了防止其被生成的气体腐蚀
C.气体Y可能是O,也可能是NO 与水反应后生成的NO
2 2
D.停止反应,应注意先把导气管移出水面,然后再熄灭酒精灯
答案 C
解析 根据氧化还原反应规律,Pb(NO ) 分解的化学方程式为 2Pb(NO )=====2PbO+
3 2 3 2
4NO ↑+O↑,液体X可能是液化的NO 或NO ,故A正确;NO 气体会损坏橡胶,在装
2 2 2 2 4 2
置中用锡纸将胶塞与产生的气体隔开,主要是为了防止其被生成的气体腐蚀,故B正确;
Pb(NO ) 分解放出氧气,气体Y可能是O,不可能是NO 与水反应后生成的NO,故C错误;
3 2 2 2
为防止倒吸,停止反应时,应先把导气管移出水面,然后再熄灭酒精灯,故D正确。
7.氮及其化合物的“价—类”二维图如下所示。下列说法正确的是( )
A.X可通过加热氯化铵固体制取
B.从物质类别角度分析,P和Z都属于酸性氧化物
C.将X转化为 Q的过程,属于氮的固定
D.3.2 g Cu与10 mol·L-1的Y溶液恰好反应,生成NO、NO 混合气体1.12 L(标准状况),
2
则 Y 溶液的体积为 15 mL
答案 D
解析 X是NH ,加热氯化铵固体生成的NH 和HCl遇冷重新生成NH Cl,不能制取NH ,
3 3 4 3
A错误;P是NO ,Z是NO 或NO ,NO 、NO 不是酸性氧化物,B错误;Q是NO,氨
2 5 2 2 4 2 2 4
气转化为NO不属于氮的固定,C错误;Y是HNO ,3.2 g Cu为0.05 mol,与HNO 反应生
3 3
成0.05 mol Cu(NO ) ,生成NO、NO 混合气体1.12 L(标准状况),则气体总物质的量为0.05
3 2 2
mol,据N原子守恒可知原硝酸中n(HNO)=0.05 mol×2+0.05 mol=0.15 mol,故硝酸溶液
3
的体积为=0.015 L=15 mL,D正确。
8.(2023·郑州检测)某学习小组设计实验制备Ca(NO ) ,实验装置如图所示(夹持装置已略
2 2
去)。已知:2NO+CaO===Ca(NO ) ;2NO +CaO===Ca(NO ) 。下列说法不正确的是(
2 2 2 2 2 3 2
)
A.通入N 是为了排尽装置中的空气
2
B.装置B、D中的试剂可分别为水和浓硫酸
C.将铜片换成木炭也可以制备纯净的亚硝酸钙
D.借助装置A及氢氧化钠溶液和稀硫酸可以分离CO 和CO
2
答案 C
解析 装置内的空气会将NO氧化为NO ,影响产物的产量,所以通入N 是为了排尽装置
2 2
中的空气,故A正确;由于硝酸具有挥发性,所以在A中生成的NO气体中会含有少量HNO 蒸气,可用装置B中的水除去,为防止CaO 与水反应,用装置D中的浓硫酸对NO
3 2
气体进行干燥,故B正确;将铜片换成木炭,由于木炭与稀硝酸不能反应,所以得不到要
制备的产物,故C错误;装置A中盛氢氧化钠溶液,通过进气管通入CO 和CO的混合气体,
2
CO 被NaOH吸收后生成NaCO ,在出气管口即可收集到CO,然后将分液漏斗中的稀硫酸
2 2 3
滴入A中,与生成的NaCO 反应再释放出CO,达到分离的目的,故D正确。
2 3 2
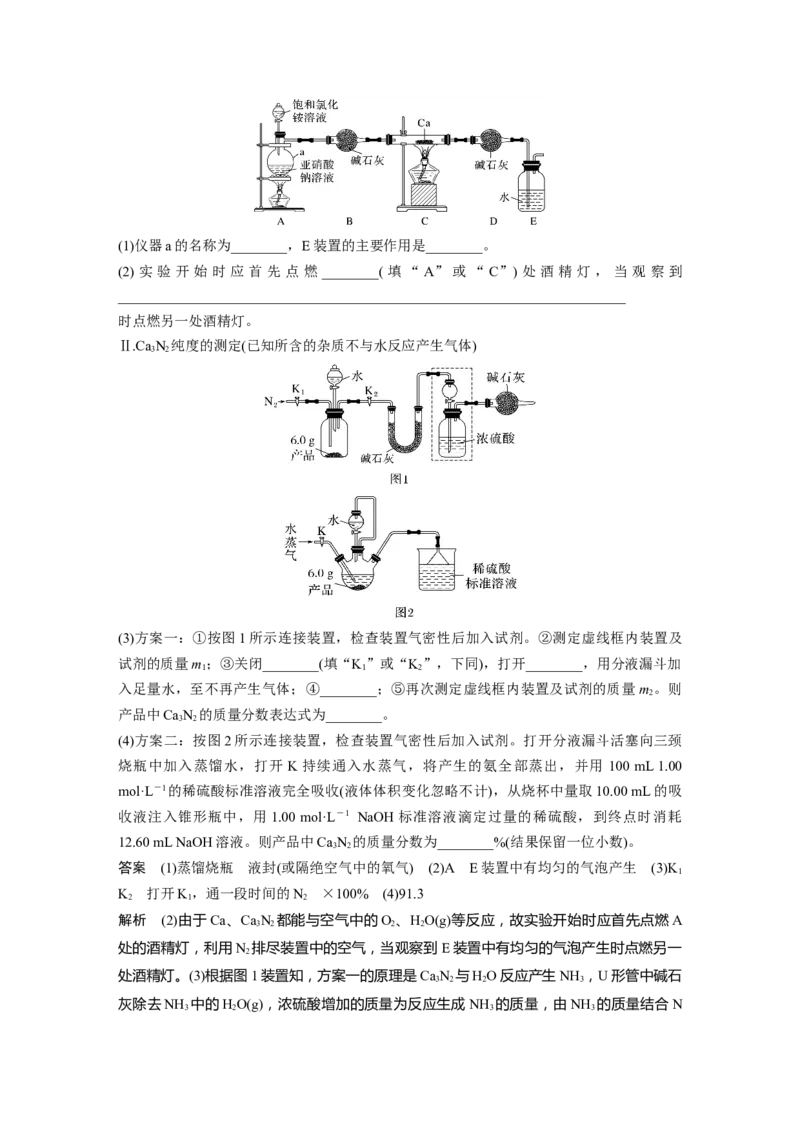
9.某兴趣小组设计用铁粉将NO还原为N(同时生成FeO)。下列说法不正确的是( )
2
已知:①浓硝酸可氧化NO;②NaOH溶液能吸收NO ,不吸收NO。
2
A.装置的连接顺序为a→f→e→j→i→h→g(或g→h)→b→c→d
B.装置E中发生反应的化学方程式为2NO+2Fe=====2FeO+N
2
C.装置D的作用是吸收挥发出来的硝酸和产生的NO
2
D.装置B的作用是干燥,防止水蒸气进入装置E中干扰反应
答案 D
解析 根据实验原理“NO被灼热的铁粉还原为N ,同时生成FeO”,所以首先利用铜与稀
2
硝酸反应生成NO,由于硝酸具有挥发性,所以制得的 NO中会混有硝酸蒸气和产生的
NO ,故先通过装置D除去挥发出的HNO 和产生的NO ,再通过装置F干燥,得到纯净干
2 3 2
燥的NO,然后进入装置E中与铁粉反应,最后处理多余的NO,由于NaOH溶液不与NO
反应,而浓硝酸可氧化NO生成NO ,所以先通过装置B氧化NO,再通过装置C吸收,故
2
上述装置的连接顺序为a→f→e→j→i→h→g(或g→h)→b→c→d,A正确。
10.(2022·石家庄二中模拟)氮化钙(Ca N)是一种重要的试剂,常温下为棕色固体,在空气
3 2
中会被氧化,遇水强烈水解,产生刺激性气味气体。实验室设计如下装置用 Ca与N 反应制
2
备Ca N,并对Ca N 纯度进行测定。回答下列问题:
3 2 3 2
Ⅰ.Ca N 的制备
3 2(1)仪器a的名称为________,E装置的主要作用是________。
(2) 实 验 开 始 时 应 首 先 点 燃 ________( 填 “ A” 或 “ C”) 处 酒 精 灯 , 当 观 察 到
________________________________________________________________________
时点燃另一处酒精灯。
Ⅱ.Ca N 纯度的测定(已知所含的杂质不与水反应产生气体)
3 2
(3)方案一:①按图1所示连接装置,检查装置气密性后加入试剂。②测定虚线框内装置及
试剂的质量m;③关闭________(填“K”或“K”,下同),打开________,用分液漏斗加
1 1 2
入足量水,至不再产生气体;④________;⑤再次测定虚线框内装置及试剂的质量m 。则
2
产品中Ca N 的质量分数表达式为________。
3 2
(4)方案二:按图2所示连接装置,检查装置气密性后加入试剂。打开分液漏斗活塞向三颈
烧瓶中加入蒸馏水,打开 K持续通入水蒸气,将产生的氨全部蒸出,并用 100 mL 1.00
mol·L-1的稀硫酸标准溶液完全吸收(液体体积变化忽略不计),从烧杯中量取10.00 mL的吸
收液注入锥形瓶中,用 1.00 mol·L-1 NaOH标准溶液滴定过量的稀硫酸,到终点时消耗
12.60 mL NaOH溶液。则产品中Ca N 的质量分数为________%(结果保留一位小数)。
3 2
答案 (1)蒸馏烧瓶 液封(或隔绝空气中的氧气) (2)A E装置中有均匀的气泡产生 (3)K
1
K 打开K,通一段时间的N ×100% (4)91.3
2 1 2
解析 (2)由于Ca、Ca N 都能与空气中的O 、HO(g)等反应,故实验开始时应首先点燃A
3 2 2 2
处的酒精灯,利用N 排尽装置中的空气,当观察到E装置中有均匀的气泡产生时点燃另一
2
处酒精灯。(3)根据图1装置知,方案一的原理是Ca N 与HO反应产生NH ,U形管中碱石
3 2 2 3
灰除去NH 中的HO(g),浓硫酸增加的质量为反应生成NH 的质量,由NH 的质量结合N
3 2 3 3元素守恒测定Ca N 的纯度。反应生成NH 的质量为(m -m) g,根据N元素守恒,Ca N 的
3 2 3 2 1 3 2
质量为××148 g·mol-1= g,产品中Ca N 的质量分数为×100%=×100%。(4)方案二的原
3 2
理是Ca N 与HO反应产生NH ,打开K持续通入水蒸气,将产生的氨全部蒸出,NH 完全
3 2 2 3 3
被稀硫酸标准溶液吸收,然后用NaOH标准溶液滴定过量的稀硫酸,则10.00 mL溶液中过
量硫酸的物质的量n (H SO )=
过量 2 4
n(NaOH)=×1.00 mol·L-1×0.012 60 L=0.006 3 mol,与NH 反应的硫酸的物质的量为
3
1.00 mol·L-1×0.1 L-0.006 3 mol×=0.037 mol,根据反应2NH +HSO ===(NH )SO 以及
3 2 4 4 2 4
N 元素守恒可知,Ca N 的物质的量为 0.037 mol,产品中 Ca N 的质量分数为
3 2 3 2
×100%≈91.3%。
11.某处工厂排出的烟道气中含氮氧化物(主要为NO、NO )、粉尘和少量水蒸气。课外兴趣
2
活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图所示:
(1)装置A中放置无碱玻璃棉,其目的是除去______________________________________。
为保证检测的准确性,装置C中盛放的化学试剂可以是________(填字母,下同)。
a.碱石灰
b.浓硫酸
c.五水合硫酸铜(CuSO ·5H O)
4 2
(2)装置 D 中主要发生:2NaOH+2NO ===NaNO +NaNO +HO;2NaOH+NO+
2 2 3 2
NO ===2NaNO +HO
2 2 2
①若反应后尾气无残留,则参加反应的NO 、NO物质的量的比值________。
2
a.≥1 b.≤1 c.任意值
②可使用适量酸性HO 溶液,将溶液中的NO全部氧化为NO,发生反应的离子方程式是
2 2
________________________________________________________________________
________________________________________________________________________。
(3)溶液中NO直接排放在水体中也会造成污染,现用活泼金属将溶液中的NO转化为N ,
2
实现氮元素的脱除,具体步骤如下:
步骤一 取适量(2)中HO 处理后的溶液,调节pH至中性,蒸发浓缩,得到c(NO)为
2 2
0.100 mol·L-1的溶液甲。
步骤二 取三份50 mL溶液甲,分别用金属铝、金属铁和铝铁合金在45 ℃、惰性气体氛围
中对溶液甲进行氮脱除。
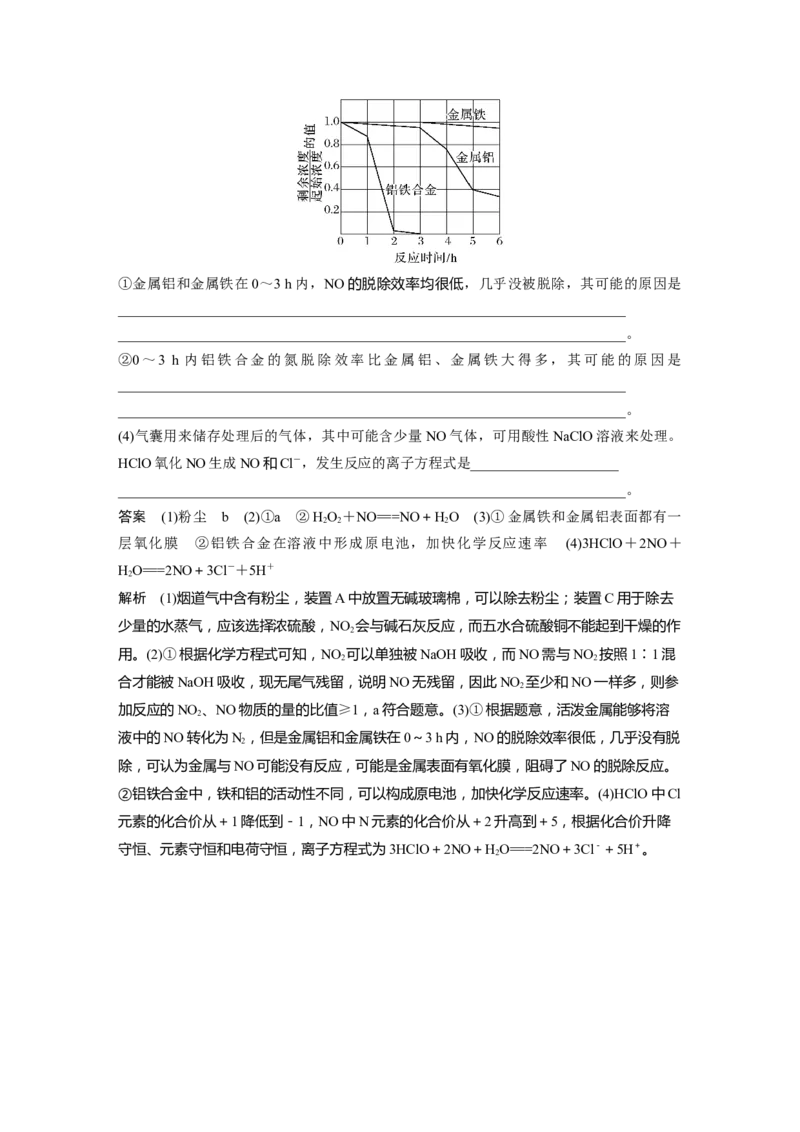
步骤三 重复实验2~3次,溶液中NO的残留情况与反应时间的关系如图所示。①金属铝和金属铁在0~3 h内,NO的脱除效率均很低,几乎没被脱除,其可能的原因是
________________________________________________________________________
________________________________________________________________________。
②0~3 h 内铝铁合金的氮脱除效率比金属铝、金属铁大得多,其可能的原因是
________________________________________________________________________
________________________________________________________________________。
(4)气囊用来储存处理后的气体,其中可能含少量NO气体,可用酸性NaClO溶液来处理。
HClO氧化NO生成NO和Cl-,发生反应的离子方程式是_____________________
________________________________________________________________________。
答案 (1)粉尘 b (2)①a ②HO +NO===NO+HO (3)①金属铁和金属铝表面都有一
2 2 2
层氧化膜 ②铝铁合金在溶液中形成原电池,加快化学反应速率 (4)3HClO+2NO+
HO===2NO+3Cl-+5H+
2
解析 (1)烟道气中含有粉尘,装置A中放置无碱玻璃棉,可以除去粉尘;装置C用于除去
少量的水蒸气,应该选择浓硫酸,NO 会与碱石灰反应,而五水合硫酸铜不能起到干燥的作
2
用。(2)①根据化学方程式可知,NO 可以单独被NaOH吸收,而NO需与NO 按照1∶1混
2 2
合才能被NaOH吸收,现无尾气残留,说明NO无残留,因此NO 至少和NO一样多,则参
2
加反应的NO 、NO物质的量的比值≥1,a符合题意。(3)①根据题意,活泼金属能够将溶
2
液中的NO转化为N,但是金属铝和金属铁在0~3 h内,NO的脱除效率很低,几乎没有脱
2
除,可认为金属与NO可能没有反应,可能是金属表面有氧化膜,阻碍了NO的脱除反应。
②铝铁合金中,铁和铝的活动性不同,可以构成原电池,加快化学反应速率。(4)HClO中Cl
元素的化合价从+1降低到-1,NO中N元素的化合价从+2升高到+5,根据化合价升降
守恒、元素守恒和电荷守恒,离子方程式为3HClO+2NO+HO===2NO+3Cl-+5H+。
2