文档内容
课时检测(七十二) 性质探究型综合实验
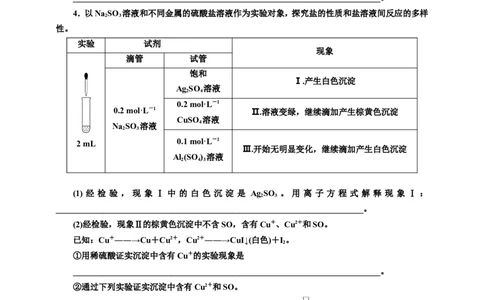
1.某学习小组通过下列装置探究MnO 与FeCl·6HO能否反应产生Cl 。
2 3 2 2
资料:FeCl 是一种共价化合物,熔点306 ℃,沸点315 ℃。
3
Ⅰ.实验操作和现象:
操作 现象
i.A中部分固体溶解,上方出现白雾;
点燃酒精灯,加热 ii.稍后,产生黄色气体,管壁附着黄色液滴;
iii.B中溶液变蓝
Ⅱ.分析现象的成因:
(1)现象 i 中的白雾是________,用化学方程式和必要的文字说明白雾的形成原因:
________________________________________________________________________
________________________________________________________________________。
(2)分析现象ii,该小组探究黄色气体的成分,实验如下:
a.直接加热FeCl·6HO,产生白雾和黄色气体。
3 2
b.将现象ii和a中的黄色气体通入KSCN溶液中,溶液均变红。
通过该实验说明现象ii中的黄色气体中含有________。
(3)除了氯气可使B中溶液变蓝外,该小组还提出其他两种可能的原因:
可能原因①:实验b检出的气体使之变蓝;
反应的离子方程式是________________________________________________。
可能原因②:_______________________________________________________;
反应的离子方程式是_________________________________________________。
(4)为进一步确认黄色气体中是否含有Cl ,小组提出两种方案,均证实了Cl 的存在。
2 2
在A、B间增加盛有某种试剂的洗气瓶
方案1 B中溶液变为蓝色
C
将B中KI淀粉溶液替换为NaBr溶液;
方案2 B中溶液呈浅橙红色;未检出Fe2+
检验Fe2+
①方案 1 洗气瓶 C 中盛放的试剂是__________,从化学平衡原理的角度加以解释:
________________________________________________________________________
________________________________________________________________________。
② 方 案 2 中 检 验 Fe2 + 的 最 佳 试 剂 是 __________ , 若 存 在 Fe2 + , 则 现 象 是
________________________________________________________________________。
③ 综 合 方 案 1 、 2 的 现 象 , 说 明 方 案 2 中 选 择 NaBr 溶 液 的 依 据 :
________________________________________________________________________。
(5) 将 A 中 产 物 分 离 得 到 FeO 和 MnCl , 则 A 中 产 生 Cl 的 化 学 方 程 式 是
2 3 2 2________________________________________________________________________
________________________________________________________________________。
2.过二硫酸钾(K SO)易潮解,易分解,是一种重要的氧化剂。某学习小组设计实验探究过二硫酸
2 2 8
钾的性质。
实验(一) 探究过二硫酸钾的强氧化性。
(1)用KSO 溶液与KI溶液反应,实验操作与现象如表所示:
2 2 8
实验 操作 现象
在10 mL 0.1 mol·L-1含淀粉的KI溶液中滴加4
Ⅰ 一段时间后,溶液缓慢变蓝色
mL 0.1 mol·L-1 KSO 溶液
2 2 8
在10 mL 0.1 mol·L-1含淀粉的KI溶液中先滴几
Ⅱ 滴0.1 mol·L-1 FeSO 溶液,再滴加4 mL 0.1 溶液迅速变蓝色
4
mol·L-1 KSO 溶液
2 2 8
① 根 据 碰 撞 理 论 分 析 , 实 验 Ⅰ 中 KSO 和 KI 反 应 很 慢 的 主 要 原 因 :
2 2 8
________________________________________________________________________。
②实验Ⅱ中Fe2+起催化作用,总反应分两步进行:
(ⅰ)2Fe2+ +SO===2Fe3++2SO;
2
(ⅱ)__________________________________________________。
请 你 补 充 反 应 (ⅱ) , 并 设 计 实 验 证 明 实 验 Ⅱ 反 应 后 的 溶 液 中 含 有 Fe3 + :
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(2)查阅文献知,氧化性:SO>MnO。在稀硫酸酸化的MnSO 溶液中滴加1滴催化剂AgNO 溶液,
2 4 3
再滴加KSO 溶液,实验现象是____________________________________,该反应的离子方程式为
2 2 8
_____________________________________________________
________________________________________________________________________。
实验(二) 探究过二硫酸钾的不稳定性。
已知几种物质的熔、沸点如表所示:
物质 SO SO O
3 2 2
熔点/℃ 16.8 -72.7 -218.4
沸点/℃ 44.8 10 -182.9
取适量的KSO 装入硬质玻璃管中,加热,将分解产物依次通过装置B、C、D,实验中发现B中U
2 2 8
形管内产生无色液体,接着无色液体慢慢变成固体,C中溶液颜色无明显变化,D中溶液逐渐变蓝色。
(3)加热前,先通入一段时间N,当观察到D装置中__________________________(填实验现象)时,
2
点燃酒精灯。
(4)B装置的U形管中收集到的物质是__________(填化学式)。(5)当A装置的硬质玻璃管中固体完全分解时,停止加热。冷却至室温,然后取少量残留固体于试
管中,加入蒸馏水,溶解后滴加BaCl 溶液和盐酸,产生白色沉淀。写出A装置中KSO 发生分解的化
2 2 2 8
学方程式:__________________________________________。
3.FeCl 为中学化学中经常使用的物质,某化学实验小组为探究FeCl 的性质,进行了如下实验。
3 3
(1)学习小组A向FeCl 溶液中分别加入Na CO 溶液和Na SO 溶液,发现有如图所示实验现象:
3 2 3 2 3
对于②中的实验现象,学习小组A的同学们有诸多猜测,继续进行实验:小明取少许②中的红棕
色溶液于试管中,滴入盐酸酸化的BaCl 溶液,产生白色沉淀。
2
小 明 得 出 结 论 : FeCl 与 Na SO 发 生 了 氧 化 还 原 反 应 , 反 应 的 离 子 方 程 式 是
3 2 3
__________________________________。
小红认为小明的实验不严谨,重新设计实验方案并进行实验,证实了小明的结论是正确的。实验
方案及现象:_______________________________________________
________________________________________________________________________。
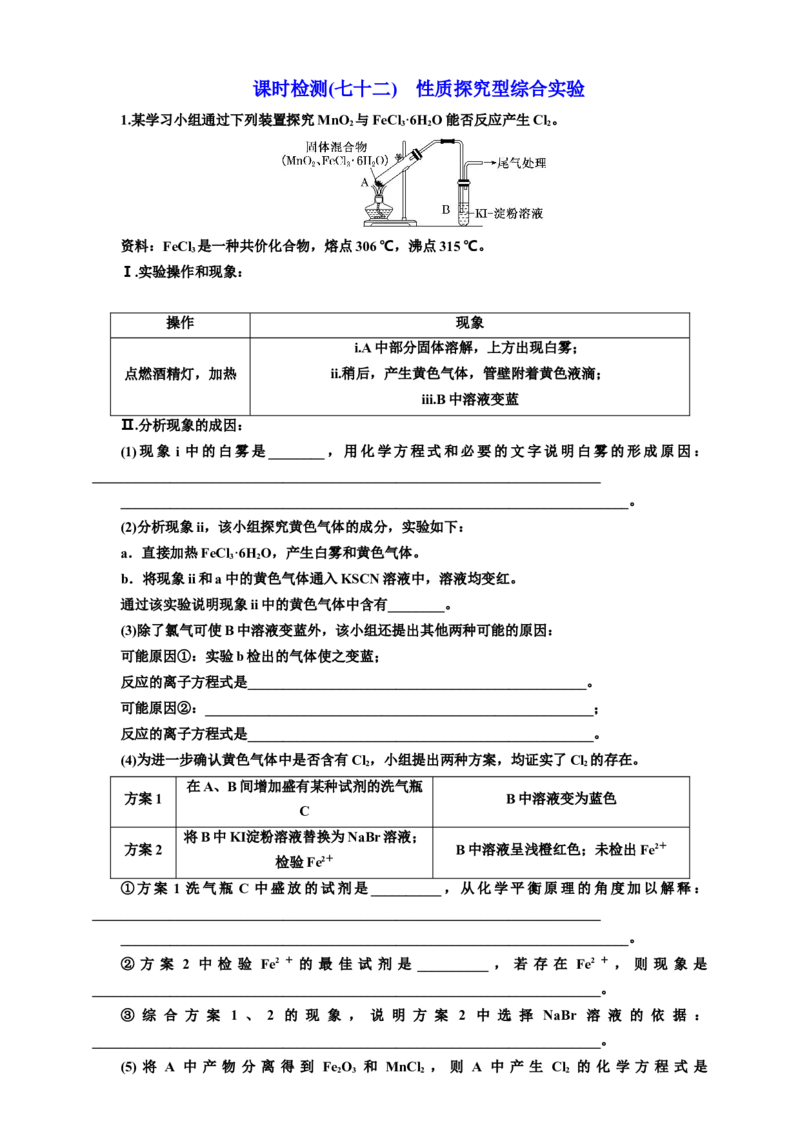
(2)学习小组B进一步探究FeCl 溶液与足量锌粉的反应。实验操作及实验现象如表所示:
3
实验操作 实验现象
配制100 mL 1.0 mol·L-1 FeCl 溶液,测其pH
3
—
约为0.7[即c(H+)≈0.2 mol·L-1]
溶液温度迅速上升,稍后出现红褐色沉淀,同
向反应瓶中加入6.5 g锌粉,然后加入50 mL
时出现少量气泡;反应一段时间后静置,上层
1.0 mol·L-1 FeCl 溶液,搅拌
3
溶液为浅绿色,反应瓶底部有黑色固体
收集并检验反应过程中产生的气体 集气管口靠近火焰,有爆鸣声
已知:Zn的化学性质与Al相似,能发生反应Zn+2HO+2NaOH===Na [Zn(OH) ]+H↑。
2 2 4 2
①结合实验现象和平衡移动原理解释出现红褐色沉淀的原因:_______________
________________________________________________________________________
________________________________________________________________________。
②分离出黑色固体,经下列实验证实了其中含有的主要物质成分。
ⅰ.黑色固体可以被磁铁吸引;
ⅱ.向黑色固体中加入足量的NaOH溶液,产生气泡;
ⅲ.将ⅱ中剩余固体用蒸馏水洗涤后,加入稀盐酸,产生大量气泡;
ⅳ.向ⅲ反应后的溶液中滴加KSCN溶液,无变化。
a.黑色固体中一定含有的物质是_______________________________________。
b.学习小组 B 的同学认为上述实验无法确定黑色固体中是否含有 FeO ,理由是
3 4
________________________________________________________________________
________________________________________________________________________________________________________________________________________________。
(3)为进一步探究1.0 mol·L-1 FeCl 溶液中Fe3+和H+氧化性的相对强弱,学习小组B补充实验并
3
观察到反应开始时的实验现象如表所示:
实验操作 实验现象
将5 mL 1.0 mol·L-1 FeCl 溶液与0.65 g锌粉 溶液温度迅速上升,开始时几乎没有气泡产
3
混合 生
将________与0.65 g锌粉混合 立即产生大量气泡
学习小组B得出结论:在1.0 mol·L-1 FeCl 溶液中,Fe3+的氧化性比H+的强。则表格中横线处应
3
填___________________________________________________________
________________________________________________________________________。
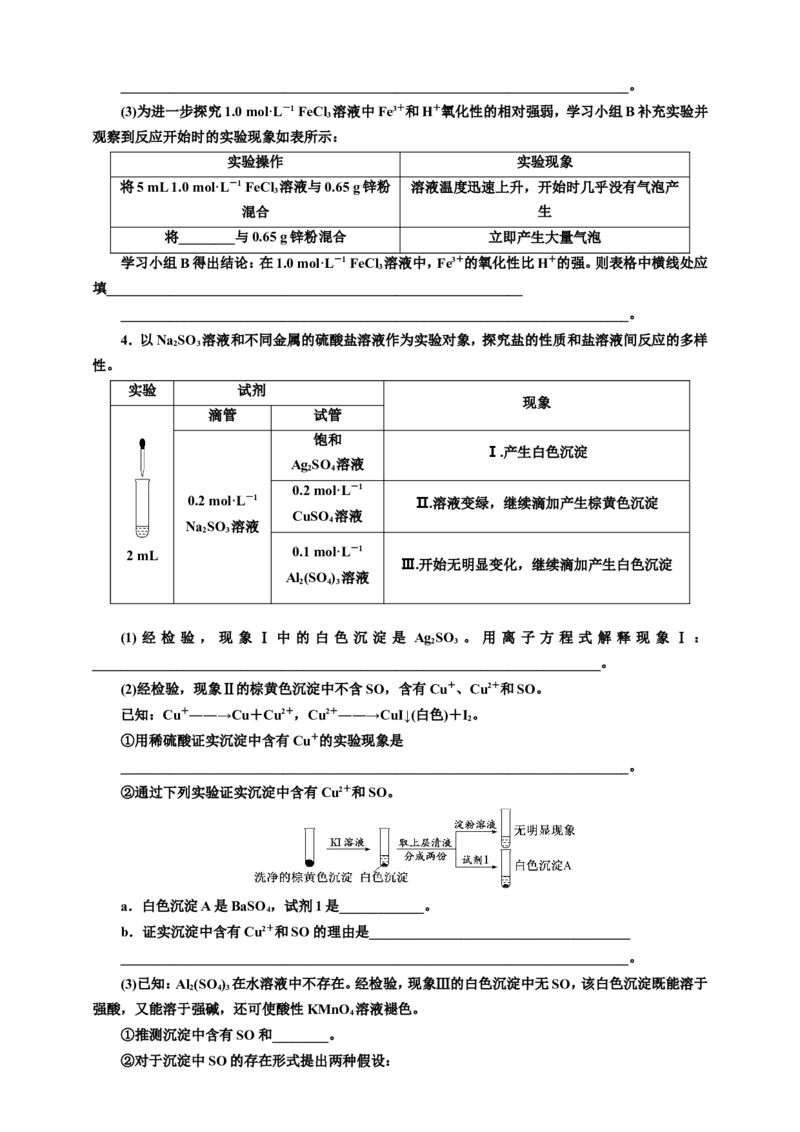
4.以Na SO 溶液和不同金属的硫酸盐溶液作为实验对象,探究盐的性质和盐溶液间反应的多样
2 3
性。
实验 试剂
现象
滴管 试管
饱和
Ⅰ.产生白色沉淀
Ag SO 溶液
2 4
0.2 mol·L-1
0.2 mol·L-1 Ⅱ.溶液变绿,继续滴加产生棕黄色沉淀
CuSO 溶液
Na SO 溶液 4
2 3
2 mL 0.1 mol·L-1
Ⅲ.开始无明显变化,继续滴加产生白色沉淀
Al (SO ) 溶液
2 4 3
(1) 经 检 验 , 现 象 Ⅰ 中 的 白 色 沉 淀 是 Ag SO 。 用 离 子 方 程 式 解 释 现 象 Ⅰ :
2 3
________________________________________________________________________。
(2)经检验,现象Ⅱ的棕黄色沉淀中不含SO,含有Cu+、Cu2+和SO。
已知:Cu+――→Cu+Cu2+,Cu2+――→CuI↓(白色)+I。
2
①用稀硫酸证实沉淀中含有Cu+的实验现象是
________________________________________________________________________。
②通过下列实验证实沉淀中含有Cu2+和SO。
a.白色沉淀A是BaSO ,试剂1是____________。
4
b.证实沉淀中含有Cu2+和SO的理由是_____________________________________
________________________________________________________________________。
(3)已知:Al (SO ) 在水溶液中不存在。经检验,现象Ⅲ的白色沉淀中无SO,该白色沉淀既能溶于
2 4 3
强酸,又能溶于强碱,还可使酸性KMnO 溶液褪色。
4
①推测沉淀中含有SO和________。
②对于沉淀中SO的存在形式提出两种假设:ⅰ.被Al(OH) 所吸附;ⅱ.存在于铝的碱式盐中。
3
对假设ⅱ设计了对比实验,证实了假设ⅱ成立。
a.将对比实验方案补充完整。
步骤一:
步骤二(按上图形式呈现):
(4)根据实验,亚硫酸盐的性质有_______________________________________。
盐溶液间反应的多样性与_____________________________________________
________________________________________________________________________有关。
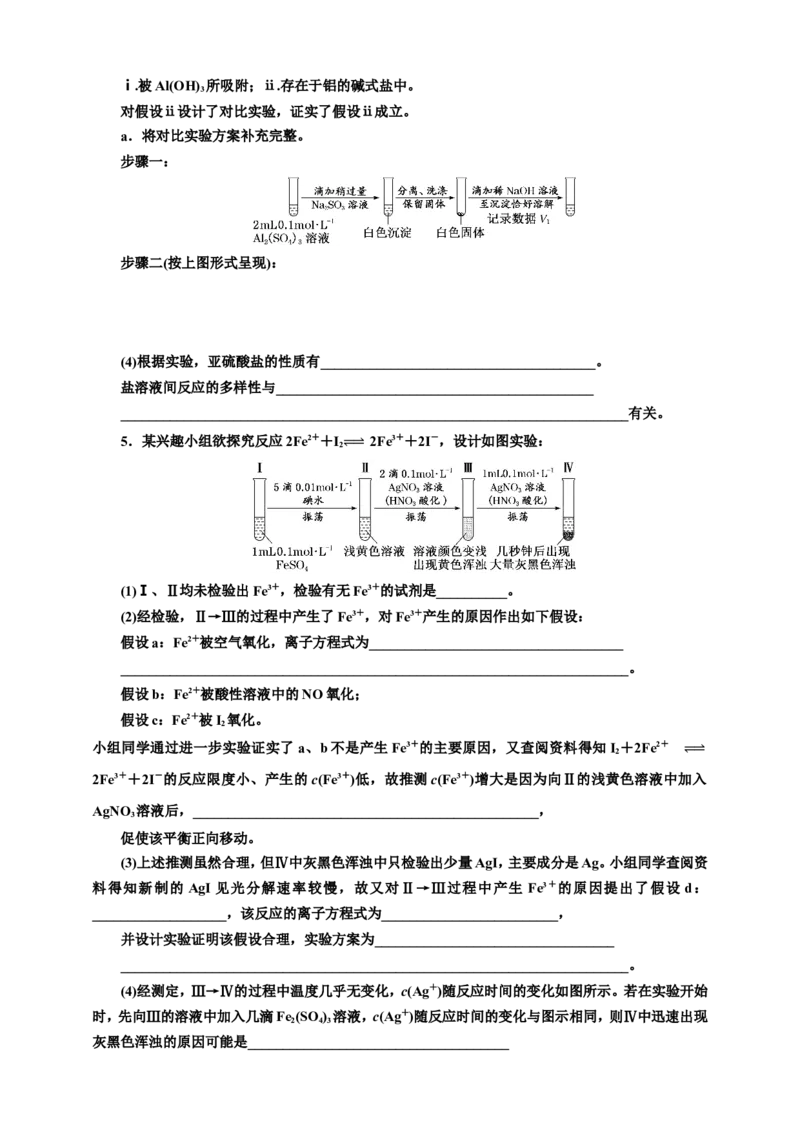
5.某兴趣小组欲探究反应2Fe2++I 2Fe3++2I-,设计如图实验:
2
⥫⥬
(1)Ⅰ、Ⅱ均未检验出Fe3+,检验有无Fe3+的试剂是__________。
(2)经检验,Ⅱ→Ⅲ的过程中产生了Fe3+,对Fe3+产生的原因作出如下假设:
假设a:Fe2+被空气氧化,离子方程式为____________________________________
________________________________________________________________________。
假设b:Fe2+被酸性溶液中的NO氧化;
假设c:Fe2+被I 氧化。
2
小组同学通过进一步实验证实了a、b不是产生Fe3+的主要原因,又查阅资料得知I +2Fe2+⥫⥬
2
2Fe3++2I-的反应限度小、产生的c(Fe3+)低,故推测c(Fe3+)增大是因为向Ⅱ的浅黄色溶液中加入
AgNO 溶液后,_________________________________________________,
3
促使该平衡正向移动。
(3)上述推测虽然合理,但Ⅳ中灰黑色浑浊中只检验出少量AgI,主要成分是Ag。小组同学查阅资
料得知新制的 AgI 见光分解速率较慢,故又对Ⅱ→Ⅲ过程中产生 Fe3+的原因提出了假设 d:
___________________,该反应的离子方程式为_________________________,
并设计实验证明该假设合理,实验方案为__________________________________
________________________________________________________________________。
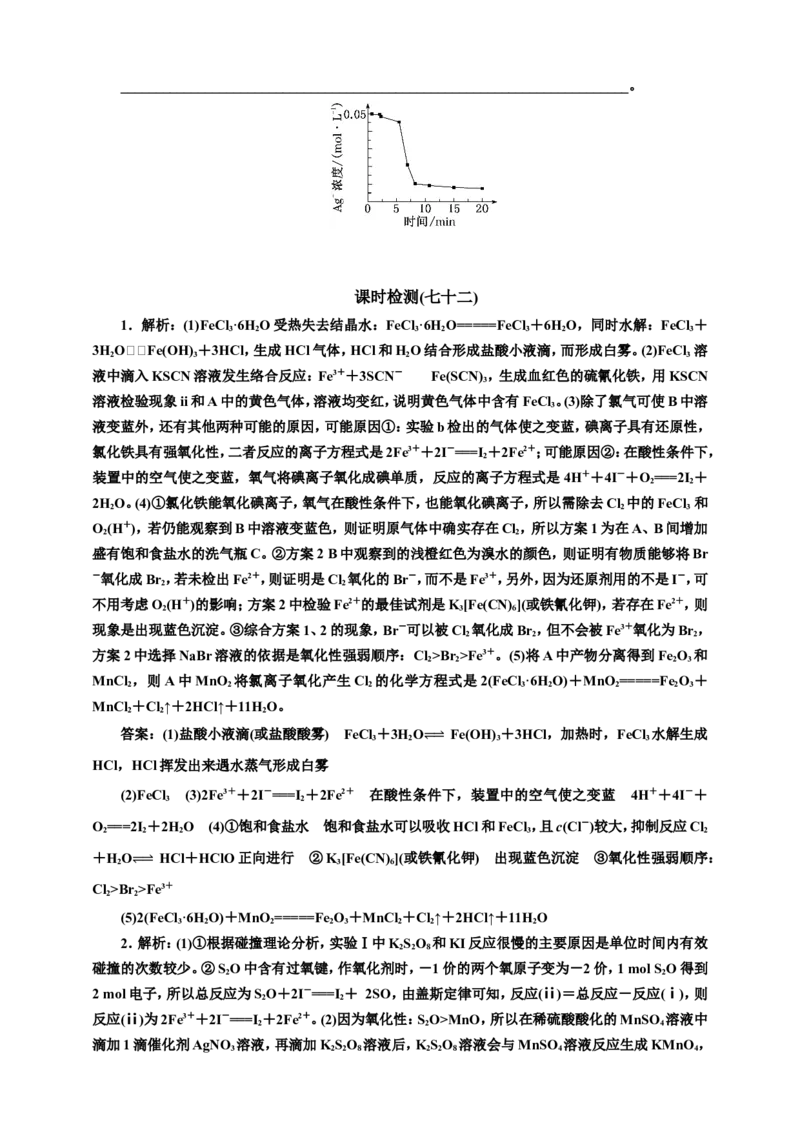
(4)经测定,Ⅲ→Ⅳ的过程中温度几乎无变化,c(Ag+)随反应时间的变化如图所示。若在实验开始
时,先向Ⅲ的溶液中加入几滴Fe(SO ) 溶液,c(Ag+)随反应时间的变化与图示相同,则Ⅳ中迅速出现
2 4 3
灰黑色浑浊的原因可能是_____________________________________________________________________________________________________________。
课时检测(七十二)
1.解析:(1)FeCl ·6HO受热失去结晶水:FeCl·6HO=====FeCl+6HO,同时水解:FeCl+
3 2 3 2 3 2 3
3HOFe(OH) +3HCl,生成HCl气体,HCl和HO结合形成盐酸小液滴,而形成白雾。(2)FeCl 溶
2 3 2 3
液中滴入KSCN溶液发生络合反应:Fe3++3SCN-Fe(SCN) ,生成血红色的硫氰化铁,用KSCN
3
溶液检验现象ii和A 中的黄色气体,溶液均变红,说明黄色气体中含有FeCl。(3)除了氯气可使B中溶
3
液变蓝外,还有其他两种可能的原因,可能原因①:实验b检出的气体使之变蓝,碘离子具有还原性,
氯化铁具有强氧化性,二者反应的离子方程式是2Fe3++2I-===I +2Fe2+;可能原因②:在酸性条件下,
2
装置中的空气使之变蓝,氧气将碘离子氧化成碘单质,反应的离子方程式是4H++4I-+O===2I +
2 2
2HO。(4)①氯化铁能氧化碘离子,氧气在酸性条件下,也能氧化碘离子,所以需除去Cl 中的FeCl 和
2 2 3
O(H+),若仍能观察到B中溶液变蓝色,则证明原气体中确实存在Cl ,所以方案1为在A、B间增加
2 2
盛有饱和食盐水的洗气瓶C。②方案2 B中观察到的浅橙红色为溴水的颜色,则证明有物质能够将Br
-氧化成Br ,若未检出Fe2+,则证明是Cl 氧化的Br-,而不是Fe3+,另外,因为还原剂用的不是I-,可
2 2
不用考虑O(H+)的影响;方案2中检验Fe2+的最佳试剂是K[Fe(CN) ](或铁氰化钾),若存在Fe2+,则
2 3 6
现象是出现蓝色沉淀。③综合方案1、2的现象,Br-可以被Cl 氧化成Br ,但不会被Fe3+氧化为Br ,
2 2 2
方案2中选择NaBr溶液的依据是氧化性强弱顺序:Cl >Br >Fe3+。(5)将A中产物分离得到FeO 和
2 2 2 3
MnCl ,则A中MnO 将氯离子氧化产生Cl 的化学方程式是2(FeCl ·6HO)+MnO =====FeO +
2 2 2 3 2 2 2 3
MnCl +Cl ↑+2HCl↑+11HO。
2 2 2
答案:(1)盐酸小液滴(或盐酸酸雾) FeCl+3HO Fe(OH) +3HCl,加热时,FeCl 水解生成
3 2 3 3
HCl,HCl挥发出来遇水蒸气形成白雾 ⥫⥬
(2)FeCl (3)2Fe3++2I-===I +2Fe2+ 在酸性条件下,装置中的空气使之变蓝 4H++4I-+
3 2
O===2I +2HO (4)①饱和食盐水 饱和食盐水可以吸收HCl和FeCl,且c(Cl-)较大,抑制反应Cl
2 2 2 3 2
+HO HCl+HClO正向进行 ②K[Fe(CN) ](或铁氰化钾) 出现蓝色沉淀 ③氧化性强弱顺序:
2 3 6
Cl >Br⥫>⥬Fe3+
2 2
(5)2(FeCl ·6HO)+MnO =====FeO+MnCl +Cl ↑+2HCl↑+11HO
3 2 2 2 3 2 2 2
2.解析:(1)①根据碰撞理论分析,实验Ⅰ中KSO 和KI反应很慢的主要原因是单位时间内有效
2 2 8
碰撞的次数较少。②SO中含有过氧键,作氧化剂时,-1价的两个氧原子变为-2价,1 mol S O得到
2 2
2 mol电子,所以总反应为SO+2I-===I + 2SO,由盖斯定律可知,反应(ⅱ)=总反应-反应(ⅰ),则
2 2
反应(ⅱ)为2Fe3++2I-===I +2Fe2+。(2)因为氧化性:SO>MnO,所以在稀硫酸酸化的MnSO 溶液中
2 2 4
滴加1滴催化剂AgNO 溶液,再滴加KSO 溶液后,KSO 溶液会与MnSO 溶液反应生成KMnO ,
3 2 2 8 2 2 8 4 4则实验现象是无色溶液变为紫红色。(3)加热前,先通入一段时间N,当观察到D装置中出现连续气泡
2
时,说明装置中空气排尽,则开始点燃酒精灯。(4)实验中发现B中U形管内产生无色液体,接着无色
液体慢慢变成固体,根据物质的熔、沸点信息可知产物为SO 。(5)残留固体溶解后滴加BaCl 溶液和盐
3 2
酸,产生白色沉淀,说明含有硫酸根离子,根据分析知分解产物为硫酸钾、三氧化硫和氧气,其分解的
化学方程式为2KSO△,2KSO +2SO ↑+O↑。
2 2 8 2 4 3 2
答案:(1)①单位时间内有效碰撞的次数较少 ②2Fe3++2I-===I +2Fe2+ 取实验Ⅱ反应后的溶
2
液于试管中,向其中滴入KSCN溶液,溶液变为血红色 (2)无色溶液变为紫红色 5SO+2Mn2++
2
8HO===2MnO+10SO+16H+ (3)出现连续气泡
2
(4)SO (5)2K SO=====2KSO +2SO ↑+O↑
3 2 2 8 2 4 3 2
3.解析:(1)取少许②中的红棕色溶液于试管中,滴入盐酸酸化的BaCl 溶液,产生白色沉淀。
2
FeCl 与Na SO 发生了氧化还原反应,离子方程式是2Fe3++SO+HO===2Fe2++SO+2H+;为体现
3 2 3 2
实验的严谨性,还应检验Fe2+的存在。(2)①溶液温度升高,反应过程中生成H 使溶液中的c(H+)减小 ,
2
Fe3++3HO Fe(OH) +3H+平衡正向移动,使溶液中出现红褐色的氢氧化铁沉淀。②因为Zn的化
2 3
学性质与Al⥫相⥬似,能与NaOH溶液发生反应放出氢气,根据向黑色固体中加入足量的NaOH溶液,产
生气泡,说明有Zn存在,且ⅱ中剩余固体用蒸馏水洗涤后,加入稀盐酸,产生大量气泡,说明含有金属
Fe;向ⅲ反应后的溶液中滴加KSCN溶液无变化,说明溶液不含Fe3+,故无法确定是否有FeO,因为
3 4
Fe3+可与铁继续反应生成Fe2+,导致ⅳ中检测不到Fe3+。所以黑色固体中一定含有的物质是Fe和
Zn。(3)本实验的目的是探究1.0 mol·L-1 FeCl 溶液中Fe3+和H+氧化性的相对强弱,应保证盐酸和
3
FeCl 溶液中c(H+)相同,且两溶液的体积也相等,所以应该选择5 mL 0.2 mol·L-1盐酸。
3
答案:(1)2Fe3++SO+HO===2Fe2++SO+2H+ 取少许②中红棕色溶液于试管中,滴加铁氰化
2
钾溶液,出现蓝色沉淀(其他合理答案也可) (2)①溶液温度升高,反应过程中生成H 使溶液中的c(H
2
+)减小,Fe3++3HO Fe(OH) +3H+平衡正向移动,使溶液中出现红褐色的氢氧化铁沉淀 ②a.Fe
2 3
和Zn b.若存在Fe⥫O⥬,稀盐酸和FeO 反应,产生的Fe3+可与铁继续反应生成Fe2+,导致ⅳ中检测
3 4 3 4
不到Fe3+,与不含有FeO 得到的ⅳ中现象相同 (3)5 mL 0.2 mol·L-1盐酸
3 4
4.解析:(1)0.2 mol·L-1Na SO 溶液滴入饱和Ag SO 溶液中,Ag SO 饱和溶液被稀释,因此不可
2 3 2 4 2 4
能是Ag SO 沉淀,溶液中SO浓度较大,因此推断白色沉淀为Ag SO ,反应的离子方程式为2Ag++
2 4 2 3
SO===Ag SO ↓。(2)①已知:Cu+――→Cu+Cu2+,若沉淀中含有Cu+,加入稀硫酸会发生歧化反应生
2 3
成铜单质,实验现象是有红色固体生成。②a.分析实验流程可知实验原理为2Cu2++4I-===2CuI+I、
2
I+SO+HO===SO+2I-+2H+、SO+Ba2+===BaSO ↓,根据白色沉淀A是BaSO 可知,加入的试剂
2 2 4 4
为含Ba2+的化合物,可以选用盐酸酸化的BaCl 溶液。b.由白色沉淀A为BaSO 可知,原沉淀中的SO
2 4
被氧化为SO,则加入KI时反应生成了I,说明原沉淀中有Cu2+,即加入KI时Cu2+与I-反应生成白
2
色沉淀CuI和I,I 又与SO反应生成SO与I-,所以加入淀粉无明显现象。(3)①根据题意知,现象Ⅲ
2 2
的白色沉淀中无SO,该白色沉淀既能溶于强酸,又能溶于强碱,结合元素守恒可知沉淀中应含有Al3+
和OH-,可使酸性KMnO 溶液褪色是因为存在有还原性的SO。②根据假设可知实验的目的是证明
4
产生的沉淀是Al(OH) 还是铝的碱式盐,给定实验首先制备出现象Ⅲ中的沉淀,然后滴加NaOH溶液,
3
因此对比实验也要首先制备出Al(OH) 沉淀,然后滴加NaOH溶液,若二者消耗的NaOH体积相同,
3则现象Ⅲ中的沉淀就是Al(OH) 沉淀,若二者消耗的NaOH体积不同,则现象Ⅲ中的沉淀为铝的碱式
3
盐,步骤二见答案中图片。(4)I 被还原,酸性KMnO 溶液褪色,均显示了亚硫酸盐的还原性,亚硫酸盐
2 4
与Al3+发生相互促进的水解反应生成氢氧化铝,证明了亚硫酸盐在水溶液中水解而体现了碱性,根据
实验流程及现象可知,盐溶液间反应的多样性和盐的性质及反应条件有关。
答案:(1)2Ag++SO===Ag SO ↓ (2)①加入稀硫酸后有红色固体生成 ②HCl和BaCl 溶液
2 3 2
在I-的作用下,Cu2+转化为白色沉淀CuI,SO转化为SO
(3)①Al3+、OH-
②
INCLUDEPICTURE "C:\\Users\\Administrator\\Desktop\\7\\25HXCXYL8-61.TIF" \*
MERGEFORMATINET
(4)还原性、水解溶液显碱性 两种盐溶液中阴阳离子的性质和反应条件
5.解析:(1)检验Fe3+的试剂可以为KSCN溶液。(2)Ⅱ→Ⅲ的过程中产生了Fe3+,若是亚铁离子
被空气中的氧气氧化,则对应的离子方程式为4Fe2++O+4H+===4Fe3++2HO;Ⅱ中存在反应I+
2 2 2
2Fe2+⥫⥬ 2Fe3++2I-,加入AgNO 溶液后,Ag+与I-反应产生黄色沉淀,I-浓度降低,使上述平衡正
3
向移动。(3)Ⅳ中灰黑色浑浊中只检验出少量AgI,主要成分是Ag,说明银离子被还原,则一定有微粒
被氧化,故产生Fe3+的原因可能是银离子将亚铁离子氧化,反应的离子方程式为Fe2++Ag+===Fe3+
+Ag↓。(4)Ⅲ→Ⅳ的过程中,温度几乎不变,发生反应Fe2++Ag+===Fe3++Ag↓,实验开始时,向Ⅲ中
加入几滴Fe(SO ) 溶液,仍能迅速出现灰黑色沉淀,且c(Ag+)变化图像与未加Fe(SO ) 溶液相 同,
2 4 3 2 4 3
说明Fe3+不能催化该反应,则单质银为该反应的催化剂,反应一段时间后,催化剂是影响反应速率的
主要因素。
答案:(1)KSCN溶液 (2)4Fe2++O+4H+===4Fe3++2HO Ag+与I-结合生成了AgI沉淀,溶
2 2
液中I-浓度降低 (3)Fe2+被Ag+氧化 Fe2++Ag+===Fe3++Ag↓ 向1 mL 0.1 mol·L-1FeSO 溶液中
4
滴加1 mL 0.1 mol·L-1AgNO 溶液,出现灰黑色固体后,取上层清液于试管中,再向上层清液中滴加
3
KSCN溶液,若溶液立即变红,则证明假设成立 (4)反应生成的Ag作催化剂,加快了Fe2++Ag+
===Fe3++Ag↓的反应速率