文档内容
课时检测(七) 氧化还原反应的计算与方程式的配平
1.一定条件下,PbO 与Cr3+反应的产物是CrO和Pb2+,则与1 mol Cr3+反应所需PbO 的物质
2 2 2
的量为( )
A.3.0 mol B.1.5 mol
C.1.0 mol D.0.75 mol
2.关于反应2Fe(CO) +7NO===2FeO+14NO+10CO ,下列说法正确的是( )
5 2 4 2 2
A.NO 发生氧化反应
2 4
B.生成1 mol CO ,转移2 mol电子
2
C.氧化产物与还原产物的物质的量之比为5∶7
D.FeO 可以和Fe反应生成FeO
2 2 3
3.(2023·浙江校联考三模)关于反应2KMnO +10HF+2KF+3HO===2K MnF +3O↑+8HO,
4 2 2 2 6 2 2
下列说法正确的是( )
A.HO 既是氧化剂又是还原剂
2 2
B.KMnF 是氧化产物
2 6
C.氧化剂与还原剂物质的量之比为2∶3
D.生成1 mol O ,转移4 mol电子
2
4.(2023·山东淄博校联考二模)用FeS、Cu S处理酸性废水中的CrO,发生的反应如下:
2 2
反应Ⅰ:FeS+CrO+H+―→Fe3++SO+Cr3++HO(未配平)
2 2
反应Ⅱ:Cu S+CrO+H+―→Cu2++SO+Cr3++HO(未配平)
2 2 2
下列说法错误的是( )
A.反应Ⅰ中还原剂与还原产物的物质的量之比为1∶3
B.处理等物质的量CrO时,消耗Cu S的物质的量更多
2 2
C.处理等物质的量CrO时,反应Ⅱ消耗H+更多
2
D.用FeS除去废水中CrO的同时,还有利于吸附悬浮杂质
2
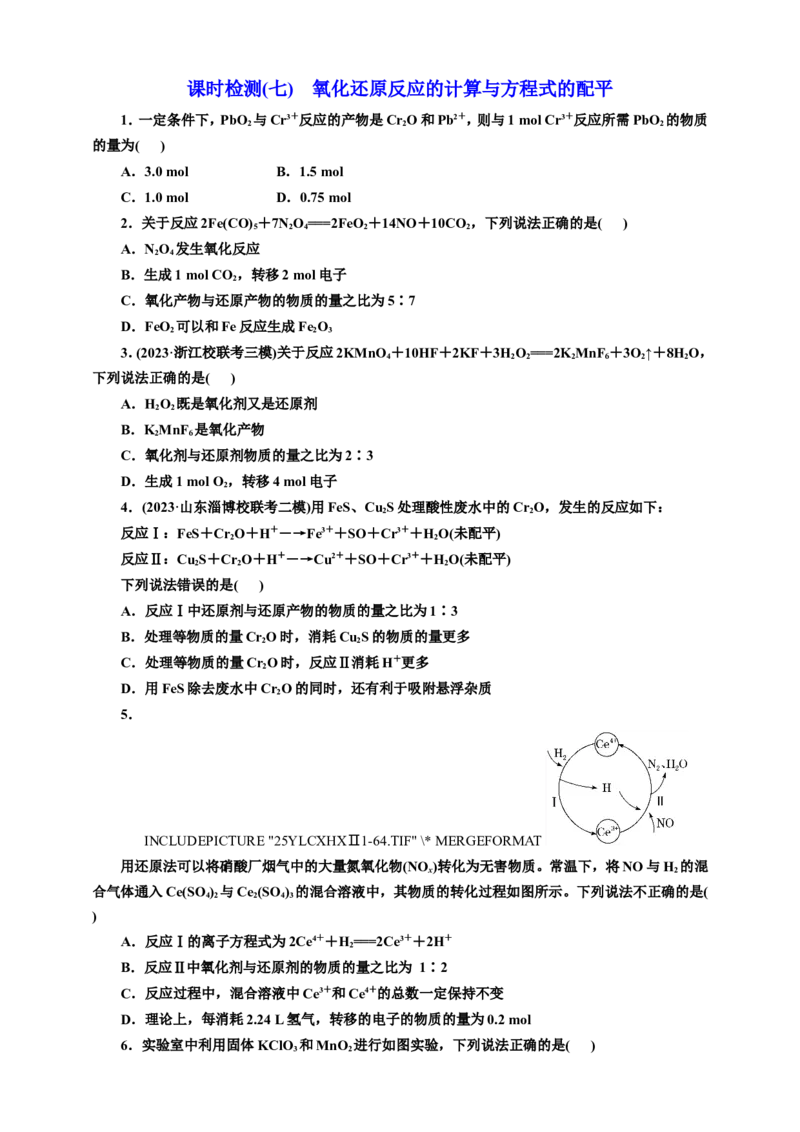
5.
INCLUDEPICTURE "25YLCXHXⅡ1-64.TIF" \* MERGEFORMAT
用还原法可以将硝酸厂烟气中的大量氮氧化物(NO)转化为无害物质。常温下,将NO与H 的混
x 2
合气体通入Ce(SO ) 与Ce(SO ) 的混合溶液中,其物质的转化过程如图所示。下列说法不正确的是(
4 2 2 4 3
)
A.反应Ⅰ的离子方程式为2Ce4++H===2Ce3++2H+
2
B.反应Ⅱ中氧化剂与还原剂的物质的量之比为 1∶2
C.反应过程中,混合溶液中Ce3+和Ce4+的总数一定保持不变
D.理论上,每消耗2.24 L氢气,转移的电子的物质的量为0.2 mol
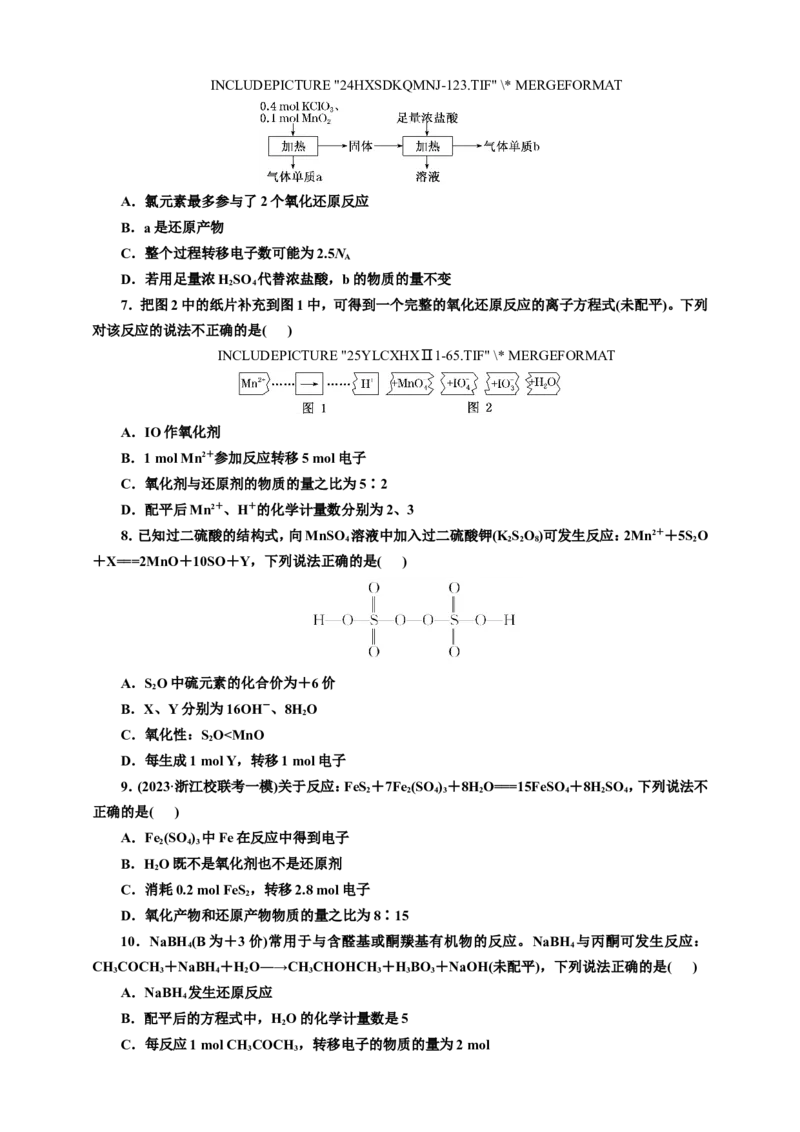
6.实验室中利用固体KClO 和MnO 进行如图实验,下列说法正确的是( )
3 2INCLUDEPICTURE "24HXSDKQMNJ-123.TIF" \* MERGEFORMAT
A.氯元素最多参与了2个氧化还原反应
B.a是还原产物
C.整个过程转移电子数可能为2.5N
A
D.若用足量浓HSO 代替浓盐酸,b的物质的量不变
2 4
7.把图2中的纸片补充到图1中,可得到一个完整的氧化还原反应的离子方程式(未配平)。下列
对该反应的说法不正确的是( )
INCLUDEPICTURE "25YLCXHXⅡ1-65.TIF" \* MERGEFORMAT
A.IO作氧化剂
B.1 mol Mn2+参加反应转移5 mol电子
C.氧化剂与还原剂的物质的量之比为5∶2
D.配平后Mn2+、H+的化学计量数分别为2、3
8.已知过二硫酸的结构式,向MnSO 溶液中加入过二硫酸钾(K SO)可发生反应:2Mn2++5SO
4 2 2 8 2
+X===2MnO+10SO+Y,下列说法正确的是( )
A.SO中硫元素的化合价为+6价
2
B.X、Y分别为16OH-、8HO
2
C.氧化性:SOMnO,B、C项错误;每生成16 mol H+,转移10 mol电子,故每生成1 mol H+,转移0.625 mol电
2
子,D项错误。
9.D Fe(SO ) 中Fe元素的化合价降低,在反应中得到电子被还原,A项正确;HO中H、O元素
2 4 3 2
的化合价都没有变化,HO既不是氧化剂也不是还原剂,B项正确;反应中,S元素的化合价由FeS 中
2 2
的-1价升至SO中的+6价,1 mol FeS 参与反应转移14 mol电子,则消耗0.2 mol FeS 转移电子的
2 2
物质的量为0.2 mol×14=2.8 mol,C项正确;反应中,Fe元素的化合价由Fe(SO ) 中的+3价降至
2 4 3
FeSO 中的+2价,Fe(SO ) 是氧化剂,FeSO 是还原产物,1 mol Fe (SO ) 参与反应得到2 mol电子生
4 2 4 3 4 2 4 3
成2 mol FeSO ,S元素的化合价由FeS 中的-1价升至SO中的+6价,FeS 是还原剂,SO是氧化产
4 2 2
物,1 mol FeS 参与反应失去14 mol电子生成2 mol SO,根据得失电子守恒,氧化产物与还原产物物
2
质的量之比为1∶7,D项错误。
10.BC 由升降法配平可得硼氢化钠与丙酮反应的化学方程式为 4CH COCH +NaBH +
3 3 4
4HO===4CHCHOHCH +HBO+NaOH,丙酮中碳元素的化合价降低被还原,是反应的氧化剂,发
2 3 3 3 3
生还原反应,硼氢化钠中氢元素的化合价升高被氧化,是反应的还原剂,发生氧化反应。硼氢化钠是反
应的还原剂,发生氧化反应,故A错误;配平后的方程式中,水的化学计量数是4,故B正确;每反应4
mol 丙酮,转移电子的物质的量为8 mol,则每反应1 mol丙酮,转移电子的物质的量为2 mol,故C正
确;丙酮是反应的氧化剂,发生还原反应,则将丙酮换成乙醛,所得有机产物为乙醇,故D错误。11.(1)5 2 14 H+ 5 5 2 MnO 7 HO
2
(2)28 5 24 KOH 28 3 2 12 HO
2
12.解析:(1)反应中,Fe元素的化合价由+3价升为+6价,每生成1 mol K FeO,反应过程中转
2 4
移3 mol电子,则生成0.1 mol K FeO 转移电子的物质的量为0.3 mol。(2)反应中,Ce元素的化合价降
2 4
低,得到电子被还原,故在该反应中,HO 作还原剂,失去电子被氧化生成O,故每有1 mol H O 参加
2 2 2 2 2
反应,转移电子的物质的量为2 mol。(3)根据化学方程式2LiBH ===2LiH+2B+3H↑可知,每生成3
4 2
mol H ,反应过程中转移6 mol电子,则生成标准状况下22.4 L即1 mol H 时,转移电子的物质的量为
2 2
2 mol。(4)反应消耗KMnO 的物质的量为0.50 mol·L-1×0.04 L=0.020 mol,根据氧化还原反应中电子
4
转移数目相等,可知反应消耗HO 的物质的量为×0.020 mol=0.050 mol,则此双氧水中HO 的质量
2 2 2 2
为0.050 mol×34 g·mol-1=1.7 g。(5)n(KI)=0.2 mol·L-1×0.3 L=0.06 mol,其与一定量的酸性KMnO
4
溶液恰好反应生成等物质的量的I 和KIO ,则n(I )=n(KIO )=0.02 mol,失去电子的物质的量为
2 3 2 3
0.02 mol×2+0.02 mol×6=0.16 mol,根据氧化还原反应中电子转移数目相等,可知反应消耗 KMnO
4
的物质的量为=0.032 mol。
答案:(1)0.3 (2)还原 2 mol (3)2 (4)1.7 (5)0.032
13.解析:(2)①由NO、NO及其对应的化学计量数并结合得失电子守恒、电荷守恒、元素守恒配平
离子方程式为4NO+10MnO+14OH-===NO+3NO+10MnO+7HO。②由①分析知分离反应后的
2
混合溶液可获得氮肥,A项正确;由化学式KMnO 可知,n(Mn)=n(K),所以反应后的混合溶液中:
4
c(MnO)+c(MnO)=c(K+),B项错误;酸性条件下,KMnO 的还原产物为Mn2+,碱性条件下,KMnO
4 4
的还原产物为MnO,C项正确。③KMnO →KMnO 得1个电子,NO→NO失3个电子,根据得失电
4 2 4
子守恒可得关系式:3KMnO ~NO,则n(KMnO )=3n(NO)=3×=3 mol,m(KMnO )=3 mol×158
4 4 4
g·mol-1=474 g。(3)②由题图可知,PI端NO失去电子发生氧化反应生成 NO :NO+HO-2e-
2 2
===NO+2H+,最终NO 和HO 发生氧化还原反应生成硝酸:2NO +HO===2HNO 。
2 2 2 2 2 2 2 3
答案:(1)形成酸雨(或形成光化学烟雾、破坏臭氧层等)
(2)①4 10 14 OH- 10 7 HO ②AC ③474
2
(3)①化学 ②NO+HO-2e-===NO+2H+
2 2
2NO +HO===2HNO
2 2 2 3