文档内容
课时检测(三十二) 原子结构、核外电子排布的基本知能评价
1.下列选项中的现象与电子的跃迁无关的是( )
A.燃放焰火 B.霓虹灯广告
C.燃烧蜡烛 D.平面镜成像
2.下列表示氮原子结构的化学用语中,对核外电子运动状态描述正确且能据此确定电子能级的
是( )
A. B.
C.1s22s22p3 D.
3. (2024年1月·九省联考吉林、黑龙江卷)电解重水(D O)是制取氘气(D )的一种方法。设N 为阿
2 2 A
伏加德罗常数的值。下列说法错误的是( )
A.DO分子间存在氢键
2
B.DO的熔、沸点比HO高
2 2
C.2 g DO含中子数目为N
A
D.制取11.2 L D 转移的电子数目为N
2 A
4.(2023·安徽省滁州市二模)高能粒子Se是第一个成功观测到双β衰变现象的原子核,其双β衰
变的方程式为 Se―→Kr+2e。下列说法正确的是( )
A.Se和Kr互为同位素
B.Se和Kr的中子数相等
C.Kr次外层电子数为8
D.双β衰变放出能量
5.Co的衰变方程为Co―→Ni++e+ν,其中ν 是反中微子,它的电荷数为0,静止质量可认为是
e e
0。下列说法错误的是( )
A.衰变产物Ni的质量数是60
B.Co的基态原子中,成单电子数为3
C.Co与Ni的基态原子核外电子占据的轨道数不同
D.基态原子Ni的价层电子排布为3d84s2
6.检验微量砷的原理为2AsH +12AgNO +3HO===As O↓+12HNO +12Ag↓。已知AsH 在常
3 3 2 2 3 3 3
温下为无色气体。下列说法正确的是( )
A.基态原子As的核外电子排布式为[Ar]4s24p3
B.NO的空间构型为平面三角形
C.固态AsH 属于共价晶体
3
D.HNO 既含离子键又含共价键
3
7.A、B为两短周期元素,A元素原子的L层比B元素原子的L层少3个电子,B原子核外电子总
数比A原子核外电子总数多5,则A和B形成化合物的化学式为( )
A.AB B.BA
2 3 2
C.AB D.B A
4 3 2
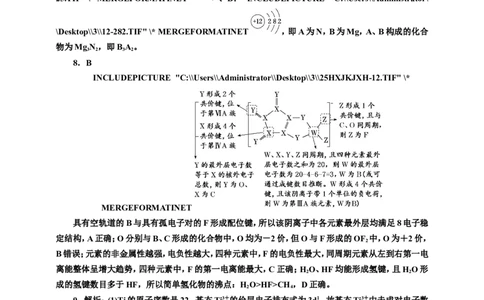
8.(2024·湖北襄阳模拟)LDFCB是锂离子电池常用的一种离子导体,其阴离子由同周期元素W、
X、Y、Z构成(如图),Y的最外层电子数等于X的核外电子总数,四种元素最外层电子数之和为20,下列说法错误的是( )
A.该阴离子中,各元素最外层均满足8电子稳定结构
B.Y分别与W、X、Z形成的化合物中,Y的价态相同
C.四种元素中,Z的电负性和第一电离能均最大
D.简单氢化物的沸点:Y>Z>X
9.(1)基态Ti3+中未成对电子数有________个;与Ti同族相邻的元素Zr的基态原子价层电子排布
式为________。与钛同周期元素的基态原子中,未成对电子数与钛相同的元素有________种。
(2)血红蛋白中的铁处于基态时,其最高能级中的单电子数为________。
(3)Cr与Ni的基态原子核外未成对电子数之比为________。
(4)第四周期中未成对电子数最多的基态原子的价层电子轨道表示式为______________________。
(5)2023年,中国航天可谓异彩纷呈。全年完成宇航发射的次数将逼近70次,成为中国航天新的里
程碑。航天器的制作材料中包含了Al、Cr、Cu、C、N、O、Si等多种元素。上述元素中基态原子未成对电
子数与Al相同的有________。
(6) 氨硼烷(NHBH)的制备是当今科学研究的重要课题,可用反应B(OCH )+NH Cl+
3 3 3 3 4
LiAlH ===NHBH+Al(OCH )+LiCl+H↑进行制备。反应中涉及元素的基态原子中含1个未成对
4 3 3 3 3 2
电子的有________种。
课时检测(三十二)
1.D 平面镜成像是光线反射的结果,与电子跃迁无关,霓虹灯广告、燃烧蜡烛、节日里燃放的焰
火是原子的发射光谱,与原子核外电子发生跃迁有关。
2.D A是N的原子结构示意图,只能看出原子核外各个电子层上含有电子数的多少,不能描述
核外电子的运动状态,错误。B是N的电子式,可以得出原子的最外电子层上有5个电子,不能描述核
外电子的运动状态,错误。C是N的核外电子排布式,可以得出原子核外有几个电子层,还可以得出各
个能级上有几个电子,但不能描述核外电子的运动状态,错误。D是基态原子N的核外电子排布图,包
含了电子层数、能级数以及轨道内电子的自旋状态等信息,正确。
3.D O原子电负性较大,DO分子间存在氢键,故A正确;DO和HO分子间都能形成氢键,但
2 2 2
DO相对分子质量大于HO,范德华力较大,熔沸点较高,故B正确;DO中含有10个中子,2 g DO的
2 2
物质的量为=0.1 mol,含中子数目为N ,故C正确;未说明气体所处的温度和压强,无法计算11.2 L
A
D 的物质的量,故D错误。
2
4.D 同位素是指具有相同质子数、不同中子数的原子,Se和Kr质子数不同,二者不互为同位素,
A错误;质量数-质子数=中子数,二者质量数相同,质子数不同,所以中子数也不相同,B错误;氪是
36号元素,次外层电子数为18,C错误;衰变过程释放能量,故双β衰变放出能量,D正确。
5.C 衰变过程遵守质子和中子守恒,则Ni的质子数为28,质量数为60,故A正确; Co的核外
电子排布式为 1s22s22p63s23p63d74s2,成单电子数为 3,基态原子 Ni 的核外电子排布式为1s22s22p63s23p63d84s2,Co与Ni的基态原子核外电子占据的轨道数均为15,故B正确,C错误;基态原
子Ni的价层电子排布为3d84s2,D正确。
6.B 基态原子As的核外电子排布式为3d104s24p3,A错误;NO中心原子N的价层电子对数为
3,无孤电子对,中心原子N的杂化类型为sp2,故NO的空间构型为平面三角形,B正确;固态AsH 属
3
于分子晶体,C错误;HNO 只含共价键,D错误。
3
7.D A元素原子的L层比B元素原子的L层少3个电子,A原子核外电子总数比B原子核外电
子总数少5,那么肯定是B元素原子M层上多了2个电子,而且A元素原子的L层未排满,所以二者
的原子结构示意图分别为 A: INCLUDEPICTURE "C:\\Users\\Administrator\\Desktop\\3\\7-
25.TIF" \* MERGEFORMATINET 、B: INCLUDEPICTURE "C:\\Users\\Administrator\
\Desktop\\3\\12-282.TIF" \* MERGEFORMATINET ,即A为N,B为Mg,A、B构成的化合
物为MgN,即B A。
3 2 3 2
8.B
INCLUDEPICTURE "C:\\Users\\Administrator\\Desktop\\3\\25HXJKJXH-12.TIF" \*
MERGEFORMATINET
具有空轨道的B与具有孤电子对的F形成配位键,所以该阴离子中各元素最外层均满足8电子稳
定结构,A正确;O分别与B、C形成的化合物中,O均为-2价,但O与F形成的OF 中,O为+2价,
2
B错误;元素的非金属性越强,电负性越大,四种元素中,F的电负性最大,同周期元素从左到右第一电
离能整体呈增大趋势,四种元素中,F的第一电离能最大,C正确;HO、HF均能形成氢键,且HO形
2 2
成的氢键数目多于HF,所以简单氢化物的沸点:HO>HF>CH ,D正确。
2 4
9.解析:(1)Ti的原子序数是22,基态Ti3+的价层电子排布式为3d1,故基态Ti3+中未成对电子数
为1。与Ti同族相邻的元素Zr的原子序数为40,Zr的基态原子价层电子排布式为4d25s2。基态钛原子
的价层电子排布式为3d24s2,未成对电子数是2,与钛同周期的所有元素的基态原子中,未成对电子数
与钛相同的元素为Ni(3d84s2)、Ge(4s24p2)、Se(4s24p4),共3种。(2)血红蛋白中的铁是+2价亚铁,处于基
态时,其最高能级的电子排布式为3d6,单电子数为4。(3)基态铬原子价层电子排布式为3d54s1,核外有
6个未成对电子,基态镍原子价层电子排布式为3d84s2,核外有2个未成对电子,则铬与镍的基态原子
核外未成对电子数之比为3∶1。(4)第四周期元素中,含有的未成对电子数最多的基态原子的价层电子
排布式为3d54s1,为铬元素,其基态原子的价层电子轨道表示式为 。(5)Al的价层
电子排布式为3s23p1,有1个未成对电子,Cr、Cu、C、N、O、Si中只有Cu(价层电子排布:3d104s1)基态
原子未成对电子数与Al相同。(6)该反应中涉及的元素有B、O、C、H、N、Cl、Li、Al,B的价层电子排布式为2s22p1,O的价层电子排布式为2s22p4,C的价层电子排布式为2s22p2,H的价层电子排布式为
1s1,N的价层电子排布式为2s22p3,Cl的价层电子排布式为3s23p5,Li的价层电子排布式为2s1,Al的
价层电子排布式为3s23p1,含1个未成对电子的元素是H、B、Cl、Li、Al,共5种。
答案:(1)1 4d25s2 3 (2)4 (3)3∶1
(4) (5)Cu (6)5