文档内容
课时检测(二十三) 硫及其化合物的基本知能评价
1《. 天工开物》中篇·燔石中记载:“凡烧硫黄石,与煤矿石同形……石精感受火神,化出黄光飞
走,遇盂掩住不能上飞,则化成汁液靠着盂底,其液流入弦袋之中,其弦又透小眼流入冷道灰槽小池,
则凝结而成硫黄矣。”下列说法错误的是( )
A.描述制取硫的过程中涉及氧化还原反应、气化、液化、凝固
B.硫元素全部以化合态存在于自然界中
C.硫难溶于水,微溶于酒精,易溶于二硫化碳
D.用硫粉可以处理洒落在地上的金属汞
2.(2024·舟山市高三模拟)下列有关硫单质性质的叙述中,正确的是( )
A.硫与金属或非金属反应时均作氧化剂
B.自然界中在富氧环境中的含硫化合物,硫通常显+4价或+6价
C.硫燃烧时,硫过量时燃烧的产物是SO ,氧气过量时燃烧的产物是SO
2 3
D.硫在空气中的燃烧产物是SO ,在纯氧中的燃烧产物也是SO
2 2
3.下列说法正确的是( )
A.SO 和SO 都是酸性氧化物,二者的水溶液都是强酸
2 3
B.将铜片放入浓硫酸中,无明显现象是因为铜片发生了钝化
C.富含硫黄的矿物在工业上可用于制造硫酸
D.鉴别SO 与HS不能用滴有淀粉溶液的碘水
2 2
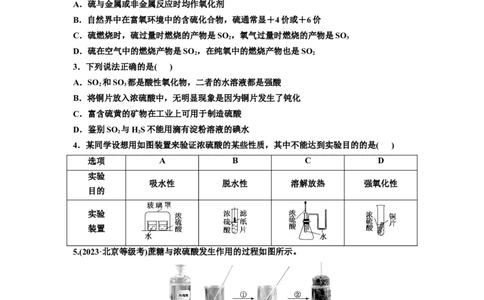
4.某同学设想用如图装置来验证浓硫酸的某些性质,其中不能达到实验目的的是( )
选项 A B C D
实验
吸水性 脱水性 溶解放热 强氧化性
目的
实验
装置
5.(2023·北京等级考)蔗糖与浓硫酸发生作用的过程如图所示。
下列关于该过程的分析不正确的是( )
A.过程①白色固体变黑,主要体现了浓硫酸的脱水性
B.过程②固体体积膨胀,与产生的大量气体有关
C.过程中产生能使品红溶液褪色的气体,体现了浓硫酸的酸性
D.过程中蔗糖分子发生了化学键的断裂
6.(2024·威海市一中统考)向酸化的KI溶液中通入SO ,溶液变黄并出现浑浊,发生反应Ⅰ:SO
2 2
+4H++4I-===2I +S↓+2HO,继续通入SO ,溶液变为无色,发生反应Ⅱ:I+SO +2HO===SO+
2 2 2 2 2 2
4H++2I-。下列说法错误的是( )A.SO 、I 的氧化性强弱与外界条件有关
2 2
B.每生成0.1 mol SO,整个过程中转移 0.4 mol 电子,同时消耗0.2 mol KI
C.该过程的总反应为3SO +2HO===2SO+S↓+4H+
2 2
D.该反应过程中KI作催化剂
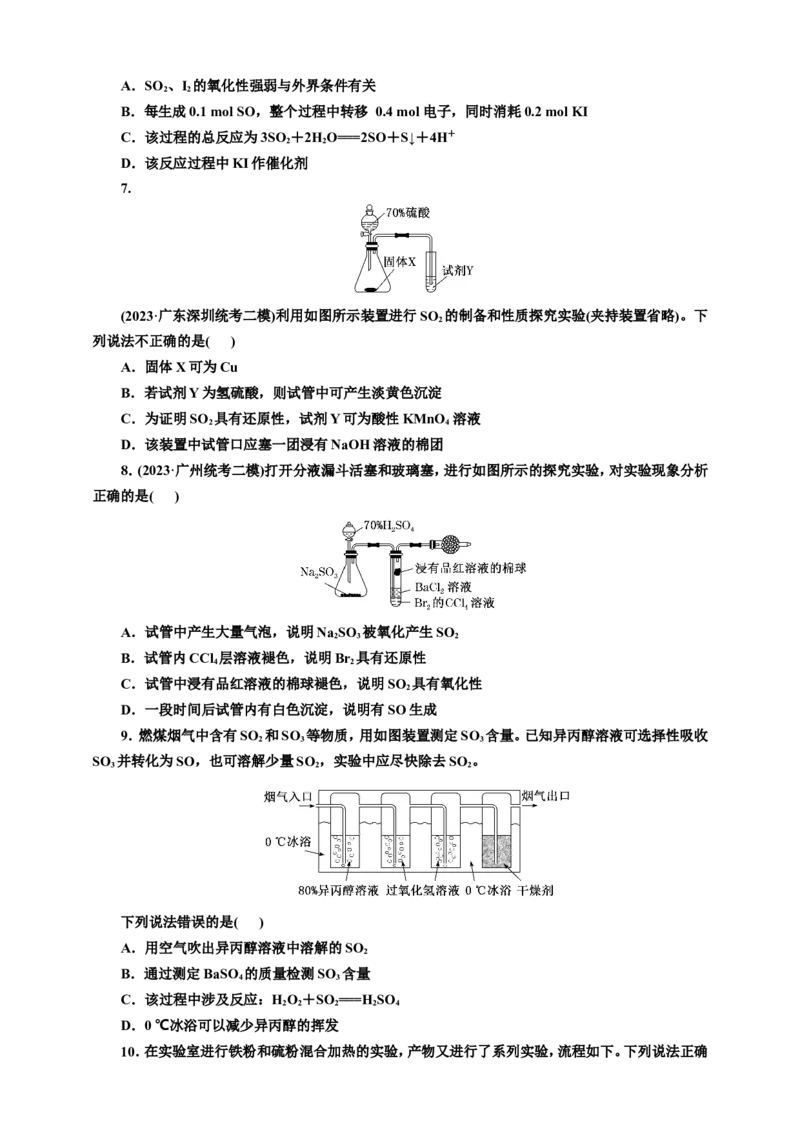
7.
(2023·广东深圳统考二模)利用如图所示装置进行SO 的制备和性质探究实验(夹持装置省略)。下
2
列说法不正确的是( )
A.固体X可为Cu
B.若试剂Y为氢硫酸,则试管中可产生淡黄色沉淀
C.为证明SO 具有还原性,试剂Y可为酸性KMnO 溶液
2 4
D.该装置中试管口应塞一团浸有NaOH溶液的棉团
8.(2023·广州统考二模)打开分液漏斗活塞和玻璃塞,进行如图所示的探究实验,对实验现象分析
正确的是( )
A.试管中产生大量气泡,说明Na SO 被氧化产生SO
2 3 2
B.试管内CCl 层溶液褪色,说明Br 具有还原性
4 2
C.试管中浸有品红溶液的棉球褪色,说明SO 具有氧化性
2
D.一段时间后试管内有白色沉淀,说明有SO生成
9.燃煤烟气中含有SO 和SO 等物质,用如图装置测定SO 含量。已知异丙醇溶液可选择性吸收
2 3 3
SO 并转化为SO,也可溶解少量SO ,实验中应尽快除去SO 。
3 2 2
下列说法错误的是( )
A.用空气吹出异丙醇溶液中溶解的SO
2
B.通过测定BaSO 的质量检测SO 含量
4 3
C.该过程中涉及反应:HO+SO ===H SO
2 2 2 2 4
D.0 ℃冰浴可以减少异丙醇的挥发
10.在实验室进行铁粉和硫粉混合加热的实验,产物又进行了系列实验,流程如下。下列说法正确的是 ( )
A.气体A和D含有同一物质,且均为氧化产物
B.硫元素一共参加了2个氧化还原反应
C.沉淀F可以和NaOH溶液在加热的条件下反应
D.若固体B中加浓硫酸,发生反应时被氧化的和被还原的均为同一种元素
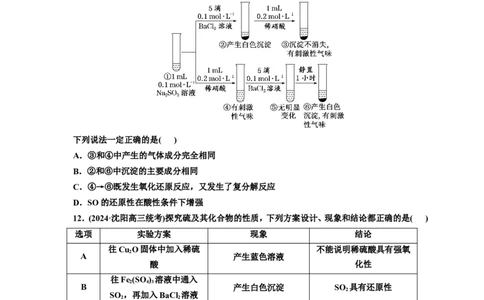
11.为探究Na SO 的性质,实验小组同学进行了如下实验:
2 3
下列说法一定正确的是( )
A.③和④中产生的气体成分完全相同
B.②和⑥中沉淀的主要成分相同
C.④→⑥既发生氧化还原反应,又发生了复分解反应
D.SO的还原性在酸性条件下增强
12.(2024·沈阳高三统考)探究硫及其化合物的性质,下列方案设计、现象和结论都正确的是( )
选项 实验方案 现象 结论
往Cu O固体中加入稀硫 不能说明稀硫酸具有强氧
2
A 产生蓝色溶液
酸 化性
往Fe(SO ) 溶液中通入
2 4 3
B 产生白色沉淀 SO 具有还原性
2
SO ,再加入BaCl 溶液
2 2
C 往CuSO 溶液中通入HS 产生黑色沉淀 HS酸性强于HSO
4 2 2 2 4
往紫色石蕊溶液中通入
D 石蕊溶液先变红后褪色 SO 具有漂白性
2
SO
2
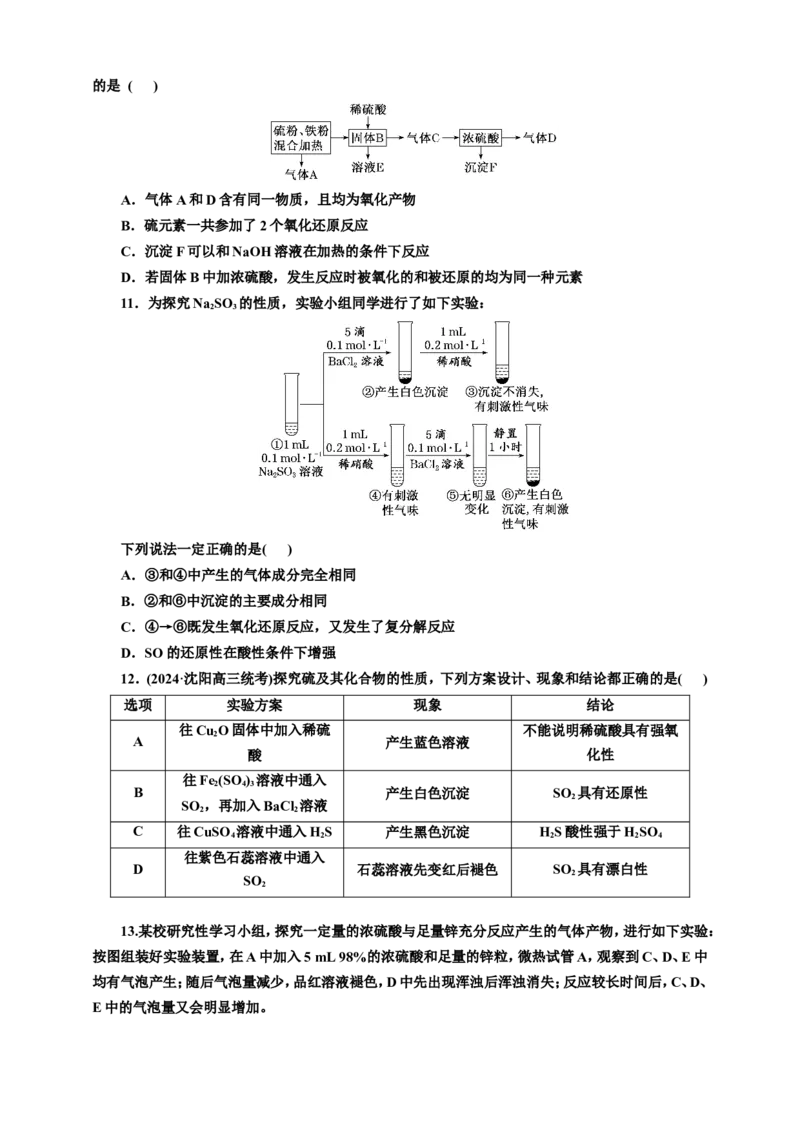
13.某校研究性学习小组,探究一定量的浓硫酸与足量锌充分反应产生的气体产物,进行如下实验:
按图组装好实验装置,在A中加入5 mL 98%的浓硫酸和足量的锌粒,微热试管A,观察到C、D、E中
均有气泡产生;随后气泡量减少,品红溶液褪色,D中先出现浑浊后浑浊消失;反应较长时间后,C、D、
E中的气泡量又会明显增加。试回答:
(1) 写 出 A 中 从 反 应 开 始 到 停 止 可 能 发 生 反 应 的 化 学 方 程 式 :
________________________________________________________________________
________________________________________________________________________。
(2)从甲、乙中选择合适的装置填入B、C中,并进行正确连接,a接________、________接b,c接
________、________接d。
(3)能证明浓硫酸具有强氧化性的实验现象为_______________________________
________________________________________________________________________。
(4)D中浑浊消失,反应的离子方程式为___________________________________
________________________________________________________________________。
(5)D、E两支试管中CCl 的作用是________________________________________。
4
(6)若A中Zn足量,充分反应后得到气体的成分是__________。
课时检测(二十三)
1.B 由硫黄石加热,发生氧化还原反应得硫蒸气,冷凝为液态流入“弦袋之中”,再凝固为固态,
A选项正确;硫元素既有单质存在于火山喷发口附近及地壳的岩层中,又有化合态存在于自然界,B选
项错误;硫难溶于水,微溶于酒精,易溶于二硫化碳,C选项正确;常温下S可以与Hg直接化合成固态
的HgS,D选项正确。
2.D 硫单质为零价,是中间价态,与金属反应时作氧化剂,与非金属性比它强的非金属(如氧、氯、
氟等)反应时作还原剂,A错误;+4价硫有较强的还原性,在富氧环境中容易被氧化成+6价,主要以
+6价存在,B错误;硫在过量氧气中燃烧也只生成二氧化硫,C错误;硫在空气中或者纯氧中的燃烧
产物只能是SO ,D正确。
2
3.C SO 和SO 都是酸性氧化物,SO 溶于水反应产生的HSO 是弱酸,SO 溶于水反应产生的
2 3 2 2 3 3
HSO 是强酸,A错误;将铜片放入浓硫酸中,无明显现象是因为不具备反应所需的温度,B错误;根据
2 4
化学反应过程中各种元素守恒可知,富含硫黄的矿物在工业上可用于制造硫酸,C正确;SO 与碘水反
2
应产生HSO 、HI,使含有淀粉的溶液蓝色褪去,而HS与I 反应产生S、HI,产生淡黄色沉淀,二者现
2 4 2 2
象不同,可以用滴有淀粉溶液的碘水进行鉴别,D错误。
4.D A项中玻璃罩内空气中的水蒸气不断地被浓HSO 吸收,导致左侧烧杯中的水不断减少,
2 4
右侧烧杯内液体量增多;B项中滤纸片沾上浓硫酸后,很快会因脱水而变黑;C项中浓硫酸滴到小试管
内的水中,放出的热量会使锥形瓶内压强增大,U形管内液面出现左低右高的现象;D项中因常温下铜
片与浓硫酸不反应,无法判断浓硫酸是否表现出强氧化性。
5.C 浓硫酸具有脱水性,能将有机物中的H原子和O原子按2∶1的比例脱除,蔗糖中加入浓
硫酸,白色固体变黑,体现浓硫酸的脱水性,A项正确;浓硫酸脱水过程中释放大量的热,此时发生反应C+2HSO (浓)=====CO ↑+2SO ↑+2HO,产生大量气体,使固体体积膨胀,B项正确;结合选项
2 4 2 2 2
B可知,浓硫酸脱水过程中生成的SO 能使品红溶液褪色,体现浓硫酸的强氧化性,C项错误;该过程
2
中,蔗糖发生化学反应,发生了化学键的断裂,D项正确。
6.B 由反应Ⅰ可知,SO 的氧化性强于I,由反应Ⅱ可知,I 的氧化性强于SO ,故可说明SO 、I
2 2 2 2 2 2
的氧化性强弱与外界条件有关,A正确;由反应ⅡI+SO +2HO===SO+4H++2I-可知,每生成0.1
2 2 2
mol SO,转移0.2 mol电子,同时生成0.2 mol I-,反应 0.1 mol I ,由反应ⅠSO +4H++4I-===2I +
2 2 2
S↓+2HO可知,每生成0.1 mol I ,转移0.2 mol电子,反应0.2 mol I-,故整个过程中转移0.4 mol电
2 2
子,不消耗KI,B错误;由盖斯定律,反应Ⅰ+2×反应Ⅱ可得该过程的总反应为3SO +2HO===2SO
2 2
+S↓+4H+,C正确;由C项分析可知,该反应过程中KI作催化剂,D正确。
7.A 铜和浓硫酸在加热条件下反应生成硫酸铜、二氧化硫和水,因此固体X不可能是Cu,故A
错误;若试剂Y为氢硫酸,二氧化硫和氢硫酸反应生成硫单质和水,则试管中可产生淡黄色沉淀,故B
正确;酸性高锰酸钾溶液具有强氧化性,为证明SO 具有还原性,试剂Y可为酸性KMnO 溶液,其现
2 4
象是溶液褪色,故C正确;二氧化硫会污染环境,因此该装置中试管口应塞一团浸有NaOH溶液的棉
团,故D正确。
8.D Na SO 与硫酸中S元素的化合价为相邻价态,不能发生氧化还原反应,Na SO 与70%的硫
2 3 2 3
酸发生复分解反应生成 SO ,故 A 错误;试管内 CCl 层溶液褪色,发生反应 SO +Br +
2 4 2 2
2HO===H SO +2HBr,说明Br 具有氧化性,故B错误;试管中浸有品红溶液的棉球褪色,说明SO
2 2 4 2 2
具有漂白性,故C错误;CCl 层发生反应SO +Br +2HO===H SO +2HBr,硫酸与氯化钡反应生成
4 2 2 2 2 4
白色沉淀硫酸钡,说明有SO生成,故D正确。
9.A 空气中的氧气能将溶解的SO 氧化为SO,不能用空气吹出异丙醇溶液中溶解的SO ,A错
2 2
误;根据S原子守恒,可通过测定BaSO 的质量计算SO 的质量,从而检测SO 含量,B正确;未被异
4 3 3
丙醇溶液吸收的SO 和过氧化氢发生氧化还原反应,反应的化学方程式为HO+SO ===H SO ,C正
2 2 2 2 2 4
确;异丙醇易挥发,0 ℃冰浴温度较低,可减少异丙醇的挥发,D正确。
10.C 首先铁粉和硫粉反应生成FeS,S和O 反应生成SO ,FeS与稀硫酸反应生成FeSO 和
2 2 4
HS,HS和HSO (浓)反应生成S、SO 和HO。由以上分析可知,气体A中SO 是氧化产物,气体D
2 2 2 4 2 2 2
中SO 是还原产物,A错误;铁粉和硫粉反应生成FeS,S和O 反应生成SO ,HS 和HSO (浓)反应生
2 2 2 2 2 4
成S、SO 和HO,反应中S元素化合价都发生改变,故硫元素一共参加了3个氧化还原反应,B错误;
2 2
沉淀F是S,S与NaOH在加热条件下反应生成Na S、Na SO 和HO,C正确;固体B为FeS,FeS和
2 2 3 2
浓硫酸反应生成Fe(SO )、S、SO 和HO,其中被氧化的元素为Fe和S,被还原的元素为S,故发生反
2 4 3 2 2
应时被氧化的和被还原的不为同一种元素,D错误。
11.C ①→③依次发生反应:Na SO +BaCl ===BaSO ↓+2NaCl、BaSO 与HNO 反应、过量的
2 3 2 3 3 3
Na SO 与HNO 反应,而①→④则是Na SO 与HNO 反应生成NO和SO ,可知③和④中产生的气体
2 3 3 2 3 3 2
成分不一定完全相同,NO和SO 的多少可能不同,A不符合题意;沉淀②的主要成分是BaSO ,而⑥
2 3
中沉淀是先加入稀硝酸后再加入BaCl ,硝酸具有强氧化性,将亚硫酸钠氧化为Na SO ,然后再与
2 2 4
BaCl 反应生成BaSO 沉淀,故二者的主要成分不同,B不符合题意;④→⑥是HSO先被氧化为SO,
2 4
SO再与Ba2+结合,既发生了复分解反应又发生了氧化还原反应,C符合题意;由题干信息可知,
②→③时的酸性比①→④的酸性弱,但②→③转化生成的硫酸根反而更多,①中SO浓度比②中的也
更大,不能说明SO的还原性在酸性条件下增强,D不符合题意。
12.A 在该反应过程中,+1价铜发生歧化反应生成+2价铜离子和单质铜,硫酸中元素化合价未发生变化,不能表现稀硫酸的氧化性,A正确;硫酸铁中含有硫酸根离子,再和钡离子反应生成硫酸
钡沉淀,不能体现二氧化硫的还原性,B错误;硫化铜难溶于水和酸,故CuSO 和硫化氢反应可以生成
4
硫化铜和硫酸,不能证明酸性的强弱,C错误;二氧化硫不能漂白指示剂,D错误。
13.解析:(1)开始阶段,浓硫酸与锌反应产生SO 气体:Zn+2HSO (浓)=====ZnSO +SO ↑+
2 2 4 4 2
2HO,随着反应的进行,浓硫酸逐渐被消耗,浓硫酸变为稀硫酸,与Zn发生置换反应生成H:Zn+
2 2
HSO ===ZnSO +H↑。(2)从题图看,C装置应是检验SO 气体的,应选择甲装置,则B处需接一安全
2 4 4 2 2
装置乙。(3)浓硫酸的强氧化性表现在SO被还原生成SO 的反应。(4)D中浑浊消失是因为过量的SO
2 2
与CaSO 反应生成Ca(HSO )。(5)SO 不溶于CCl ,故CCl 可以防倒吸。(6)Zn足量,后期Zn与稀硫
3 3 2 2 4 4
酸反应生成H。
2
答案:(1)Zn+2HSO (浓)=====ZnSO +SO ↑+2HO、Zn+HSO ===ZnSO +H↑
2 4 4 2 2 2 4 4 2
(2)3(或4) 4(或3) 2 1
(3)C中品红溶液褪色 (4)SO +HO+CaSO ===Ca2++2HSO
2 2 3
(5)防倒吸 (6)SO 、H
2 2