文档内容
课时检测(十八) 镁铝制取工艺
1.类推是化学学习和研究常用的重要思维方法,但所得结论要经过实践的检验才能确定其正确
与否。根据你所掌握的知识,判断下列类推结论正确的是( )
A.Mg燃烧不能用CO 灭火,故Na燃烧也不能用CO 灭火
2 2
B.Al在O 中燃烧生成Al O,故Fe在O 中燃烧生成FeO
2 2 3 2 2 3
C.CO 与Na O 反应生成Na CO 和O,故SO 与Na O 反应生成Na SO 和O
2 2 2 2 3 2 2 2 2 2 3 2
D.Al与NaOH溶液反应生成H,故Mg与NaOH溶液反应也生成H
2 2
2.镁、铝单质的化学性质以相似性为主,但也存在某些较大差异性,下列物质能证明二者存在较
大差异性的是( )
①CO ②盐酸 ③NaOH溶液 ④醋酸
2
A.①④ B.②③ C.①③ D.②③④
3.下列离子方程式书写不正确的是( )
A.向硝酸铝溶液中通入过量氨气:
4NH +Al3++4HO===[Al(OH) ]-+4NH
3 2 4
B.将铝片打磨后置于NaOH溶液中:
2Al+2OH-+6HO===2[Al(OH) ]-+3H↑
2 4 2
C.向明矾溶液中加入过量的Ba(OH) 溶液:
2
Al3++2SO+2Ba2++4OH-===2BaSO ↓+[Al(OH) ]-
4 4
D.向Na[Al(OH) ]溶液中通入足量CO :
4 2
[Al(OH) ]-+CO ===Al(OH) ↓+HCO
4 2 3
4.(2024年1月·九省联考安徽卷)研究发现由铝原子构成的Al、Al和Al团簇阴离子都能与水自发
反应产生氢气。下列说法正确的是( )
A.Al、Al和Al互为同位素
B.Al与水反应时作还原剂
C.Al是由铝原子通过离子键结合而成
D.1 mol的Al含6.02×1023个电子
5.明矾[KAl(SO )·12HO]是一种复盐,在造纸等方面应用广泛。采用废易拉罐制备明矾的过程如
4 2 2
图所示。下列叙述错误的是( )
A.合理处理废易拉罐有利于环境保护和资源再利用
B.从废易拉罐中可回收的金属元素有Al和Fe
C.“沉淀”中的金属离子为Fe3+
D.上述流程中可用NaHSO 代替NaHCO
4 3
6.从铝土矿(主要成分为Al O)中提取铝的工艺流程如图。下列说法不正确的是( )
2 3
A.从Na[Al(OH) ]→Al(OH) →Al O 的转化过程中涉及的反应均为非氧化还原反应
4 3 2 3
B.Al O 与NaOH溶液反应的化学方程式:
2 3Al O+2NaOH+3HO===2Na[Al(OH) ]
2 3 2 4
C.Na[Al(OH) ]生成Al(OH) 的离子方程式:
4 3
[Al(OH) ]-+CO ===Al(OH) ↓+HCO
4 2 3
D.电解熔融Al O 阳极的电极反应式:
2 3
Al3++3e-===Al
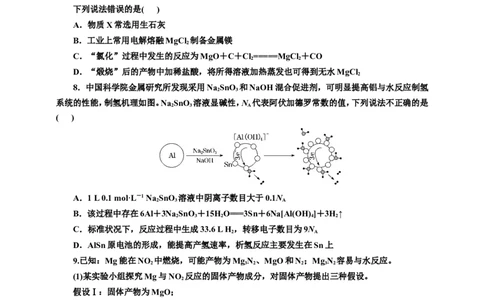
7.一种工业制备无水氯化镁的工艺流程如下:
下列说法错误的是( )
A.物质X常选用生石灰
B.工业上常用电解熔融MgCl 制备金属镁
2
C.“氯化”过程中发生的反应为MgO+C+Cl =====MgCl +CO
2 2
D.“煅烧”后的产物中加稀盐酸,将所得溶液加热蒸发也可得到无水MgCl
2
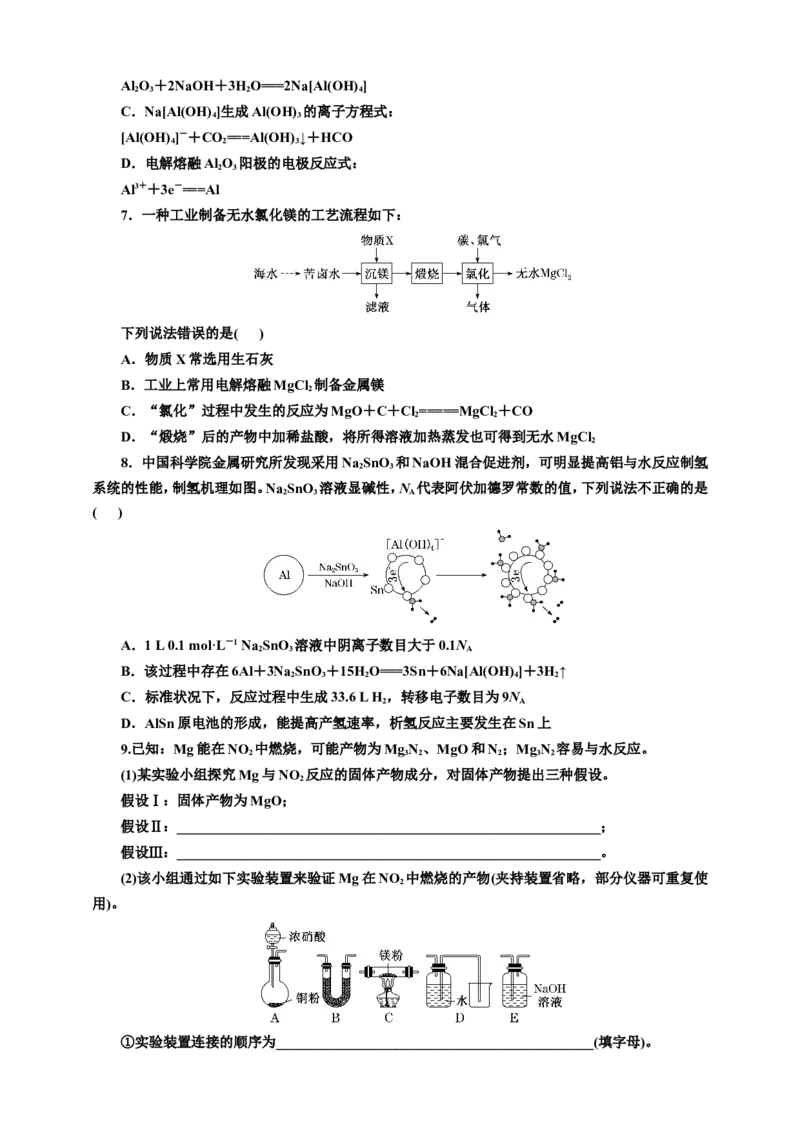
8.中国科学院金属研究所发现采用Na SnO 和NaOH混合促进剂,可明显提高铝与水反应制氢
2 3
系统的性能,制氢机理如图。Na SnO 溶液显碱性,N 代表阿伏加德罗常数的值,下列说法不正确的是
2 3 A
( )
A.1 L 0.1 mol·L-1 Na SnO 溶液中阴离子数目大于0.1N
2 3 A
B.该过程中存在6Al+3Na SnO +15HO===3Sn+6Na[Al(OH) ]+3H↑
2 3 2 4 2
C.标准状况下,反应过程中生成33.6 L H ,转移电子数目为9N
2 A
D.AlSn原电池的形成,能提高产氢速率,析氢反应主要发生在Sn上
9.已知:Mg能在NO 中燃烧,可能产物为MgN、MgO和N;MgN 容易与水反应。
2 3 2 2 3 2
(1)某实验小组探究Mg与NO 反应的固体产物成分,对固体产物提出三种假设。
2
假设Ⅰ:固体产物为MgO;
假设Ⅱ:____________________________________________________________;
假设Ⅲ:____________________________________________________________。
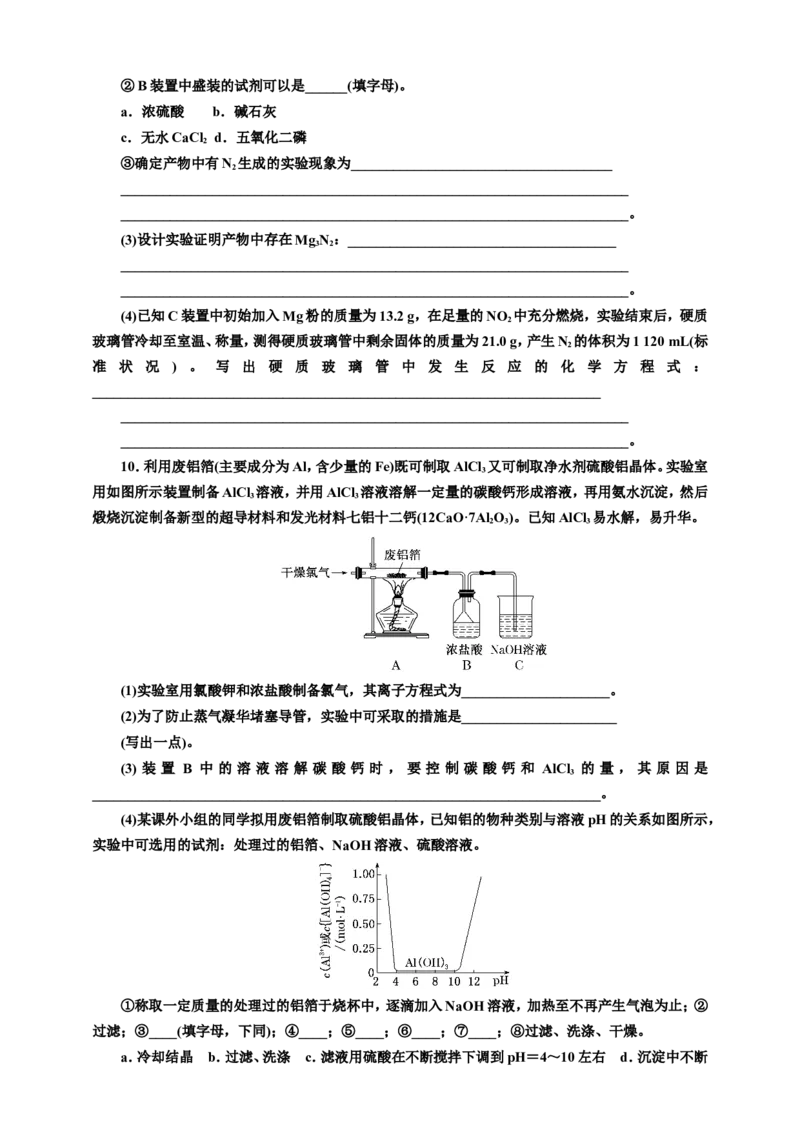
(2)该小组通过如下实验装置来验证Mg在NO 中燃烧的产物(夹持装置省略,部分仪器可重复使
2
用)。
①实验装置连接的顺序为_____________________________________________(填字母)。②B装置中盛装的试剂可以是______(填字母)。
a.浓硫酸 b.碱石灰
c.无水CaCl d.五氧化二磷
2
③确定产物中有N 生成的实验现象为_____________________________________
2
________________________________________________________________________
________________________________________________________________________。
(3)设计实验证明产物中存在MgN:______________________________________
3 2
________________________________________________________________________
________________________________________________________________________。
(4)已知C装置中初始加入Mg粉的质量为13.2 g,在足量的NO 中充分燃烧,实验结束后,硬质
2
玻璃管冷却至室温、称量,测得硬质玻璃管中剩余固体的质量为21.0 g,产生N 的体积为1 120 mL(标
2
准 状 况 ) 。 写 出 硬 质 玻 璃 管 中 发 生 反 应 的 化 学 方 程 式 :
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
10.利用废铝箔(主要成分为Al,含少量的Fe)既可制取AlCl 又可制取净水剂硫酸铝晶体。实验室
3
用如图所示装置制备AlCl 溶液,并用AlCl 溶液溶解一定量的碳酸钙形成溶液,再用氨水沉淀,然后
3 3
煅烧沉淀制备新型的超导材料和发光材料七铝十二钙(12CaO·7Al O)。已知AlCl 易水解,易升华。
2 3 3
(1)实验室用氯酸钾和浓盐酸制备氯气,其离子方程式为_____________________。
(2)为了防止蒸气凝华堵塞导管,实验中可采取的措施是______________________
(写出一点)。
(3) 装 置 B 中 的 溶 液 溶 解 碳 酸 钙 时 , 要 控 制 碳 酸 钙 和 AlCl 的 量 , 其 原 因 是
3
________________________________________________________________________。
(4)某课外小组的同学拟用废铝箔制取硫酸铝晶体,已知铝的物种类别与溶液pH的关系如图所示,
实验中可选用的试剂:处理过的铝箔、NaOH溶液、硫酸溶液。
①称取一定质量的处理过的铝箔于烧杯中,逐滴加入NaOH溶液,加热至不再产生气泡为止;②
过滤;③____(填字母,下同);④____;⑤____;⑥____;⑦____;⑧过滤、洗涤、干燥。
a.冷却结晶 b.过滤、洗涤 c.滤液用硫酸在不断搅拌下调到pH=4~10左右 d.沉淀中不断加入硫酸,至恰好溶解 e.蒸发浓缩
(5)为了分析废铝箔中铁元素的含量,某同学称取5.000 g 废铝箔,先将其预处理使铁元素还原为
Fe2+,并在容量瓶中配制成100 mL溶液;然后移取25.00 mL试样溶液,用1.000×10-2mol·L-1
KMnO 标准溶液滴定,消耗20.00 mL标准溶液。判断滴定终点的依据是
4
_______________________________________________________________________________________
废铝箔中铁元素的质量分数为________。
课时检测(十八)
1.A 由于钠比镁活泼,镁能与CO 反应,则钠也能与CO 反应,Mg燃烧不能用CO 灭火,故Na
2 2 2
燃烧也不能用CO 灭火,A项正确;Fe在O 中燃烧生成FeO ,B项错误;SO 与Na O 反应生成
2 2 3 4 2 2 2
Na SO ,C项错误;Al具有两性,能和NaOH溶液反应生成Na[Al(OH) ]和H,而Mg不具有两性,不
2 4 4 2
能和NaOH溶液反应,D项错误。
2.C 镁能与CO 反应而铝不能;铝能与NaOH溶液反应而镁不能。
2
3. A 硝酸铝与过量氨气、水反应生成氢氧化铝沉淀和硝酸铵,故A错误;向Na[Al(OH) ]溶液中
4
通入足量CO 生成氢氧化铝沉淀和碳酸氢钠,故D正确。
2
4. B 同位素是指同一元素不同核素的关系,该三者团簇阴离子是多原子聚集体,A错误;Al与
水反应产生氢气,则Al作还原剂,B正确;团簇是原子、分子或离子通过物理或化学结合力组成的,不
是简单的由铝原子通过离子键结合而成,C错误;1 mol的Al所含电子数是(13×18+1)×6.02×1023,D
错误。
5.D 废易拉罐作为可再生资源,其回收再利用对提高经济效益、社会效益、保护环境有着巨大
的促进作用,A正确;由题意可知,废易拉罐中主要含有Al和Fe,因此可从废易拉罐中回收的金属元
素有Al和Fe,B正确;“沉淀”的主要成分是Fe(OH) ,C正确;铝离子与碳酸氢根离子发生相互促进
3
的水解反应,生成氢氧化铝沉淀,硫酸氢根离子是强酸的酸式酸根,不能与铝离子反应,D错误。
6.D 向Na[Al(OH) ]溶液中通入CO 气体,发生反应生成Al(OH) ,Al(OH) 不稳定,受热分解生
4 2 3 3
成Al O,在该转化过程中无元素化合价的变化,因此涉及的反应均为非氧化还原反应,A正确;Al O
2 3 2 3
是两性氧化物,与NaOH溶液反应生成Na[Al(OH) ]和水,B正确;酸性:HCO >Al(OH) ,向
4 2 3 3
Na[Al(OH) ]溶液中通入过量CO 气体,发生反应的离子方程式为[Al(OH) ]-+CO ===Al(OH) ↓+
4 2 4 2 3
HCO,C正确;电解熔融Al O 时,阳极上O2-失去电子变为O,电极反应式为2O2--4e-===O ↑,D
2 3 2 2
错误。
7.D 物质 X 的作用是使 Mg2+转化为 Mg(OH) ,工业上常选用 CaO,发生反应 CaO+
2
HO===Ca(OH) ,Ca(OH) +Mg2+===Mg(OH) +Ca2+,A正确;Mg是较活泼金属,工业上常用电解
2 2 2 2
熔融MgCl 制备金属镁,B正确;由题图可知,“氯化”过程的反应物为MgO、氯气、C,生成物之一为
2
MgCl ,另一产物为CO而不是CO ,因C在高温下能将CO 还原为CO,化学方程式为MgO+C+
2 2 2
Cl =====MgCl +CO,C正确;“煅烧”后得到MgO,MgO和盐酸反应得到MgCl 溶液,由于MgCl
2 2 2 2
在溶液中水解为氢氧化镁和HCl,将所得溶液加热蒸发,HCl会逸出,MgCl 水解平衡正向移动,得到
2
氢氧化镁,得不到无水MgCl ,D错误。
2
8.C 图示中Al可以与Na SnO 和NaOH反应,Al与Na SnO 发生反应的化学方程式为6Al+
2 3 2 3
3Na SnO +15HO===3Sn+6Na[Al(OH) ]+3H↑(1),与 NaOH 发生反应的化学方程式为 2Al+
2 3 2 4 2
2NaOH+6HO===2Na[Al(OH) ]+3H↑(2),随着反应的进行,生成的Sn和氢气的量也逐渐增多。
2 4 2Na SnO 溶液显碱性,SnO会发生水解生成HSnO和OH-,阴离子个数增多,1 L 0.1 mol·L-1 Na SnO
2 3 2 3
溶液中阴离子数目大于0.1N ,A正确;根据前面的分析,发生反应(1)(2),B正确;在整个过程中,当
A
33.6 L氢气全部是反应(1)生成时,转移的电子数为9N ,当33.6 L氢气全部是反应(2)生成时,转移的
A
电子数为3N ,故转移电子数目介于3N 与9N 之间,C错误;形成AlSn 原电池可以加快反应速率,Al
A A A
活泼作负极,故Sn作正极,析氢反应主要发生在Sn上,D正确。
9.解析:(1)根据已知Mg在NO 中燃烧产物的可能性分析判断,假设Ⅰ:固体产物为MgO;假设
2
Ⅱ:固体产物为MgN;假设Ⅲ:固体产物为MgO和MgN 的混合物。(2)①A装置中铜与浓硝酸反应
3 2 3 2
产生二氧化氮,用B装置中的干燥剂干燥后,通入C装置硬质玻璃管中与镁粉反应,用E装置中的
NaOH溶液除去多余的二氧化氮,最后用D装置收集氮气(排水法),为确保C装置中无水蒸气,应在C
装置和E装置之间连接干燥装置,故装置的连接顺序为ABCBED。②二氧化氮不能用碱性干燥剂干燥,
U形管中盛装的是固体干燥剂,故B装置中盛装的试剂可以是无水氯化钙或五氧化二磷,选c、d。③从
C装置中导出的气体通过NaOH溶液吸收后,仍有气体将D装置广口瓶中的水压入烧杯中,则确定产
物中有N 生成。(3)Mg N 能与水反应生成具有刺激性气味的碱性气体,所以取少量反应后的固体产物,
2 3 2
加入水中产生有刺激性气味的气体,该气体能使湿润的红色石蕊试纸变蓝,则证明产物中存在
MgN。(4)13.2 g 镁的物质的量为 0.55 mol,设生成MgN 的物质的量为x mol,生成MgO的物质的
3 2 3 2
量为y mol,根据镁原子守恒得①3x+y=0.55 mol,根据反应完后剩余固体的质量得②100x+40y=
21.0 g,联立①②解得x=0.05,y=0.4;氮气的物质的量为1.12 L÷22.4 L·mol-1=0.05 mol;综上分析,
反应物为Mg和NO ,生成物为MgN、MgO和N,且物质的量之比为1∶8∶1,所以发生反应的化学
2 3 2 2
方程式为11Mg+4NO =====MgN+8MgO+N。
2 3 2 2
答案:(1)固体产物为MgN 固体产物为MgO和MgN 的混合物 (2)①ABCBED ②cd
3 2 3 2
③D装置中广口瓶中的水被气体压入烧杯中 (3)取少量C装置中反应后的固体产物,加入水中产
生有刺激性气味的气体,该气体可使湿润的红色石蕊试纸变蓝
(4)11Mg+4NO =====MgN+8MgO+N
2 3 2 2
10.解析:(2)由题意可知,氯化铝蒸气凝华易堵塞导管,则加粗导管、缩短导管长度、加热导管可
以防止蒸气凝华堵塞导管。(3)装置B中的氯化铝溶液溶解碳酸钙时,要控制碳酸钙和AlCl 的量,否则
3
钙离子会与氨水反应生成微溶的、不易分解的氢氧化钙,影响七铝十二钙的产率。(4)由题意可知,制备
硫酸铝晶体的操作为称取一定质量的处理过的铝箔于烧杯中,逐滴加入NaOH溶液,加热至不再产生
气泡为止,过滤,向滤液中加入硫酸,调节pH在4~10时生成氢氧化铝沉淀,再过滤、洗涤,向沉淀中
加入硫酸,至恰好溶解,蒸发浓缩、冷却结晶,再进行过滤、洗涤、干燥得到硫酸铝晶体。(5)由题意可知,
亚铁离子与酸性高锰酸钾溶液完全反应时,再滴入标准溶液,溶液会变为浅紫色,则判断滴定终点的
依据是滴入最后半滴高锰酸钾溶液时,溶液出现浅紫色且半分钟内不褪色;由得失电子守恒可得5Fe2
+~MnO,由滴定消耗20.00 mL 1.000×10-2 mol·L-1 KMnO 标准溶液可知,废铝箔中铁元素的质量分
4
数为
×100%=4.480%。
答案:(1)ClO+5Cl-+6H+===3Cl↑+3HO
2 2
(2)加粗导管、缩短导管长度、加热导管(写出一点即可)
(3)生成微溶于水的氢氧化钙使产率降低 (4)c b d e a
(5)滴入最后半滴高锰酸钾溶液时,溶液出现浅紫色且半分钟内不褪色 4.480%