文档内容
一、选择题
1《. 新修本草》是我国古代中药学著作之一,记载药物844种,其中有关于“青矾”的描
述为“本来绿色,新出窟未见风者,正如琉璃…烧之赤色…”。据此推测,“青矾”的主要成
分为( )
A.CuSO ·5H O B.FeSO ·7H O
4 2 4 2
C.KAl(SO )·12H O D.Fe (SO )·9H O
4 2 2 2 4 3 2
解析:选B。描述中为“本来绿色”,由此推断应选B。
2.铁是日常生活中使用最广泛的金属。下列关于铁的一些说法正确的是( )
A.常温下浓硫酸与铁不反应,故常温下可用铁制容器贮藏贮运浓硫酸
B.铁是较活泼的金属,它与卤素单质(X )反应的生成物均为FeX
2 3
C.Fe(OH) 易被氧化成Fe(OH) ,说明稳定性:Fe(OH) <Fe(OH)
2 3 2 3
D.Fe O 溶解于盐酸既有FeCl 又有FeCl 生成,故Fe O 属于混合物
3 4 2 3 3 4
解析:选C。A项,常温下铁在浓硫酸中钝化,钝化是化学变化,错误;B项,铁与碘化合
生成FeI,错误;D项,四氧化三铁是纯净物,错误。
2
3.(2019·包头高三检测)某同学欲探究铁及其化合物的性质,下列实验方案可行的是(
)
A.将铁粉加入热的浓硫酸中:探究铁的活泼性
B.将热的NaOH溶液滴入FeCl 溶液中:制备Fe(OH) 胶体
3 3
C.在蒸发皿中加热蒸干FeSO 溶液:制备FeSO ·6H O晶体
4 4 2
D.将铜粉加入FeCl 溶液中:验证Fe3+的氧化性强于Cu2+
3
解析:选D。由于浓硫酸具有强氧化性,铁与其反应生成Fe (SO ) 和SO ,无法说明铁的
2 4 3 2
活泼性,故A项方案不可行;将NaOH加入FeCl 溶液中,得到Fe(OH) 沉淀,无法得到
3 3
Fe(OH) 胶体,故B项方案不可行;在蒸发皿中加热蒸干FeSO 溶液,一方面氧气可将FeSO
3 4 4
氧化,另一方面会得到不含结晶水的化合物,故C项方案不可行;将铜粉加入FeCl 溶液中,
3
发生发应:Cu+2Fe3+===Cu2++2Fe2+,该反应说明Fe3+的氧化性强于Cu2+,故D项方案可
行。
4.(2019·济南测试)证明某溶液只含有Fe2+而不含有Fe3+的最佳实验方法是( )
A.先滴加氯水,再滴加KSCN溶液后显红色
B.先滴加KSCN溶液,不显红色,再滴加氯水后显红色
C.滴加NaOH溶液,先产生白色沉淀,后变为灰绿色,最后呈红褐色
D.只需滴加KSCN溶液
解析:选B。Fe2+和Fe3+的检验方法是常考的热点。实验设计的步骤:先加KSCN溶液,
无现象,可证明溶液中不含Fe3+,然后再滴加氯水,若溶液呈红色,说明溶液中含有Fe2+,故
B项正确;若含少量Fe3+,滴入NaOH溶液后生成的大量白色沉淀可覆盖极少量的红褐色沉
淀,不能确定是否含Fe3+,故C项不正确。
5.在浅绿色的Fe(NO ) 溶液中逐滴加入稀盐酸时,溶液颜色变化应是( )
3 2
A.颜色变浅 B.逐渐变深绿
C.没有改变 D.变棕黄色
解析:选D。Fe(NO ) 溶液中加入稀盐酸时发生反应:3Fe2++4H++NO===3Fe3++NO↑
3 2
+2HO,有棕黄色的Fe3+生成。
2
6(. 2019·湖北八校一联)为了探究铁、铜及其化合物的性质,某同学设计并进行了下列实
验。下列说法错误的是( )A.高温加热装置中发生的反应为3Fe(s)+4HO(g)=====Fe O(s)+4H(g)
2 3 4 2
B.虚线框处宜选择的装置是甲
C.实验时将螺旋状铜丝加热变黑后再趁热迅速伸入试管中,可观察到铜丝由黑色变为红
色
D.实验后,可用铝粉在高温下还原玻璃管中的固体获得铁单质
解析:选B。高温加热装置中铁粉与水蒸气反应生成四氧化三铁与氢气,化学方程式为
3Fe(s)+4HO(g)=====Fe O(s)+4H(g),A正确。氢气的密度比空气的密度小,所以用向
2 3 4 2
下排空气法通入H,应选择装置乙,B错误。铜丝加热变黑是发生反应2Cu+O=====2CuO,
2 2
氧化铜与氢气反应生成铜和水是发生反应CuO+H=====Cu+HO,所以铜丝由黑色变为红
2 2
色,C正确。实验后,玻璃管中的固体中含有Fe O,铝粉与Fe O 发生铝热反应生成氧化铝
3 4 3 4
和铁单质,D正确。
7.(2019·广东五校协作体第一次联考)下列实验的现象与对应结论均正确的是( )
选项 操作 现象 结论
向某溶液中加入CCl ,振
A 4 液体分层,下层呈紫红色 该溶液中存在I-
荡后静置
Al (SO ) 溶液中滴加过量
B 2 4 3 生成白色胶状物质 Al(OH) 溶于氨水
氨水 3
FeSO 溶液中滴入酸性高
C 4 紫色褪去 Fe2+有还原性
锰酸钾溶液
D SO 通入溴水中 溶液褪色 SO 有漂白性
2 2
解析:选C。向某溶液中加入CCl ,振荡后静置,分层,下层呈紫红色,说明含碘单质,A
4
项错误;Al (SO ) 溶液中滴加过量氨水,反应生成氢氧化铝白色沉淀,可知Al(OH) 不溶于氨
2 4 3 3
水,B项错误;FeSO 溶液中滴入酸性高锰酸钾溶液,发生氧化还原反应生成铁离子,紫色褪
4
去,说明Fe2+有还原性,C项正确;SO 通入溴水中,发生氧化还原反应,生成HSO 和HBr,
2 2 4
说明SO 有还原性,D项错误。
2
8.下列有关物质的检验方法不合理的是( )
A.向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含
有Fe2+
B.用酸性KMnO 溶液检验Fe (SO ) 溶液中是否含有FeSO
4 2 4 3 4
C.检验Fe(NO ) 是否已氧化变质,可将Fe(NO ) 溶于稀HSO 后滴加KSCN溶液,再观
3 2 3 2 2 4
察溶液是否变红
D.向某溶液中加入NaOH溶液产生红褐色沉淀,说明溶液中含有Fe3+
解析:选C。酸性条件下Fe2+被NO氧化成Fe3+,不能检验Fe(NO ) 是否已氧化变质,C
3 2
项不合理。
9.下列各组物质中,X是主体物质,Y是少量杂质,Z是为除去杂质所要加入的试剂,其
中所加试剂正确的一组是( )
选项 A B C D
X FeCl 溶液 FeCl 溶液 Fe FeSO 溶液
2 3 4
Y FeCl CuCl Al Fe (SO )
3 2 2 4 3Z Cl Fe NaOH溶液 Cu
2
解析:选C。Cl 与FeCl 反应,A错误;Fe与FeCl 、CuCl 均反应,B错误;D项中有新的
2 2 3 2
杂质CuSO 生成,D错误。
4
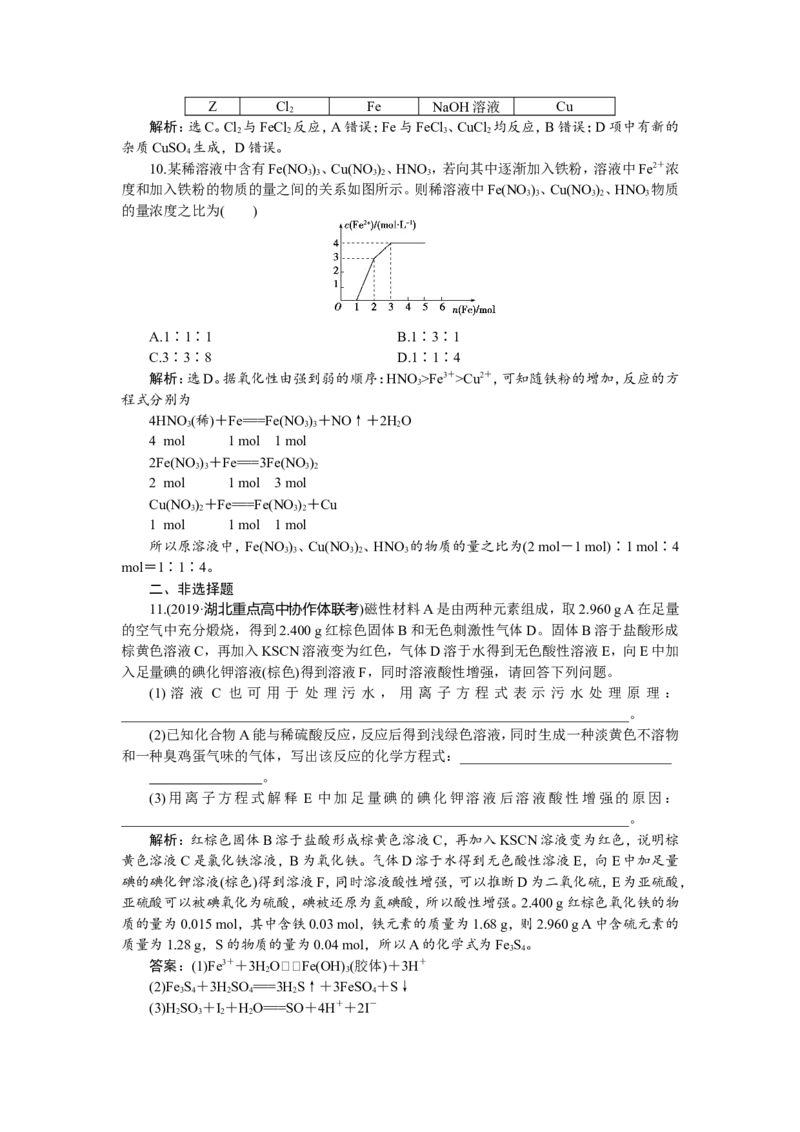
10.某稀溶液中含有Fe(NO )、Cu(NO )、HNO,若向其中逐渐加入铁粉,溶液中Fe2+浓
3 3 3 2 3
度和加入铁粉的物质的量之间的关系如图所示。则稀溶液中Fe(NO )、Cu(NO )、HNO 物质
3 3 3 2 3
的量浓度之比为( )
A.1∶1∶1 B.1∶3∶1
C.3∶3∶8 D.1∶1∶4
解析:选D。据氧化性由强到弱的顺序:HNO>Fe3+>Cu2+,可知随铁粉的增加,反应的方
3
程式分别为
4HNO(稀)+Fe===Fe(NO)+NO↑+2HO
3 3 3 2
4 mol 1 mol 1 mol
2Fe(NO )+Fe===3Fe(NO)
3 3 3 2
2 mol 1 mol 3 mol
Cu(NO )+Fe===Fe(NO)+Cu
3 2 3 2
1 mol 1 mol 1 mol
所以原溶液中,Fe(NO )、Cu(NO )、HNO 的物质的量之比为(2 mol-1 mol)∶1 mol∶4
3 3 3 2 3
mol=1∶1∶4。
二、非选择题
11.(2019·湖北重点高中协作体联考)磁性材料A是由两种元素组成,取2.960 g A在足量
的空气中充分煅烧,得到2.400 g红棕色固体B和无色刺激性气体D。固体B溶于盐酸形成
棕黄色溶液C,再加入KSCN溶液变为红色,气体D溶于水得到无色酸性溶液E,向E中加
入足量碘的碘化钾溶液(棕色)得到溶液F,同时溶液酸性增强,请回答下列问题。
(1) 溶 液 C 也 可 用 于 处 理 污 水 , 用 离 子 方 程 式 表 示 污 水 处 理 原 理 :
________________________________________________________________________。
(2)已知化合物A能与稀硫酸反应,反应后得到浅绿色溶液,同时生成一种淡黄色不溶物
和一种臭鸡蛋气味的气体,写出该反应的化学方程式:______________________________
。
(3)用离子方程式解释 E 中加足量碘的碘化钾溶液后溶液酸性增强的原因:
________________________________________________________________________。
解析:红棕色固体B溶于盐酸形成棕黄色溶液C,再加入KSCN溶液变为红色,说明棕
黄色溶液C是氯化铁溶液,B为氧化铁。气体D溶于水得到无色酸性溶液E,向E中加足量
碘的碘化钾溶液(棕色)得到溶液F,同时溶液酸性增强,可以推断D为二氧化硫,E为亚硫酸,
亚硫酸可以被碘氧化为硫酸,碘被还原为氢碘酸,所以酸性增强。2.400 g红棕色氧化铁的物
质的量为0.015 mol,其中含铁0.03 mol,铁元素的质量为1.68 g,则2.960 g A中含硫元素的
质量为1.28 g,S的物质的量为0.04 mol,所以A的化学式为Fe S。
3 4
答案:(1)Fe3++3HOFe(OH) (胶体)+3H+
2 3
(2)Fe S+3HSO ===3H S↑+3FeSO +S↓
3 4 2 4 2 4
(3)H SO +I+HO===SO+4H++2I-
2 3 2 212.绿矾被广泛用于医药和工业领域,工业上两种制备绿矾(FeSO ·7H O)的流程如图所
4 2
示,根据题意回答下列问题:
方法一:利用黄铜矿粉(主要成分为CuFeS)制取绿矾
2
(1)试剂a和试剂b分别是 ,操作1的名称是 。
(2)有一种细菌在有氧气存在的稀硫酸中,可以将CuFeS 氧化成硫酸盐,写出该反应的
2
化学方程式:________________________________________________________
________________________________________________________________________。
方法二:利用工业废铁屑制取绿矾
(3)加入适量NaCO 溶液的作用是________________________________________。
2 3
(4)操作Ⅰ需要用到的玻璃仪器名称有____________________________________。
(5)通过检验CO来判断操作Ⅰ是否洗涤干净,检验的方法是__________________
________________________________________________________________________
________________________________________________________________________。
答案:(1)稀HSO 、铁粉 过滤
2 4
(2)4CuFeS +17O+2HSO =====4CuSO +2Fe (SO )+2HO
2 2 2 4 4 2 4 3 2
(3)除去油污
(4)烧杯、玻璃棒、漏斗
(5)取少量最后一次的洗涤液于试管中,滴加BaCl 溶液,若无白色沉淀生成,则已经洗
2
涤干净;若有白色沉淀生成,则未洗涤干净
13.铁矿石是工业炼铁的主要原料之一,其主要成分为铁的氧化物(设杂质中不含铁元素
和氧元素,且杂质不与HSO 反应)。某研究性学习小组对某铁矿石中铁的氧化物的化学式进
2 4
行探究。
(Ⅰ)铁矿石中含氧量的测定
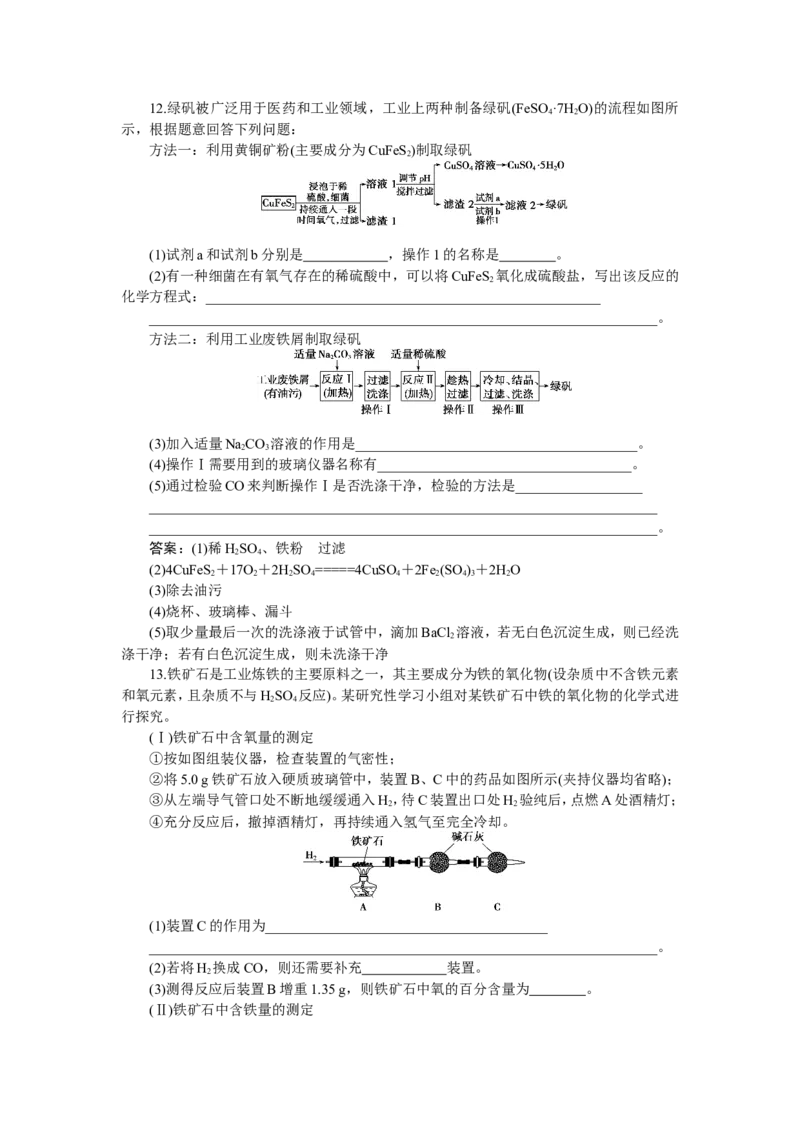
①按如图组装仪器,检查装置的气密性;
②将5.0 g铁矿石放入硬质玻璃管中,装置B、C中的药品如图所示(夹持仪器均省略);
③从左端导气管口处不断地缓缓通入H,待C装置出口处H 验纯后,点燃A处酒精灯;
2 2
④充分反应后,撤掉酒精灯,再持续通入氢气至完全冷却。
(1)装置C的作用为________________________________________
________________________________________________________________________。
(2)若将H 换成CO,则还需要补充 装置。
2
(3)测得反应后装置B增重1.35 g,则铁矿石中氧的百分含量为 。
(Ⅱ)铁矿石中含铁量的测定(1)步骤④中加热煮沸的作用是________________________________________________
________________________________________________________________________。
(2)步骤⑤中用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、 。
(3)下列有关步骤⑥的操作中说法正确的是 。
a.因为碘水为黄色,所以滴定过程中不需加指示剂
b.滴定过程中可利用淀粉溶液作为指示剂
c.滴定管用蒸馏水洗涤后可以直接装液
d.锥形瓶不需要用待测液润洗
e.滴定过程中,眼睛注视滴定管中液面变化
f.滴定结束后,30 s内溶液不恢复原来的颜色,再读数
(4)若滴定过程中消耗0.500 0 mol·L-1的KI溶液20.00 mL,则铁矿石中铁的百分含量为
。
(Ⅲ)由(Ⅰ)(Ⅱ)可以推算出该铁矿石中铁的氧化物的化学式为 。
答案:(Ⅰ)(1)防止空气中的水蒸气和CO 进入B中,影响测定结果
2
(2)尾气处理
(3)24%
(Ⅱ)(1)赶走溶液中溶解的过量Cl
2
(2)250 mL容量瓶
(3)df
(4)70%
(Ⅲ)Fe O
5 6