文档内容
备战2024年高考化学考前手感保温训练(新高考卷)
专练10 14道选择题+主观实验题
完卷时间:40分钟
答案速查
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 B D A D D B C B C B A C D C
一、选择题(共42分,只有1个正确选项)
1.中华文化源远流长,化学与文化传承密不可分。下列叙述错误的是
A.江西博物馆中“《论语》竹简”中竹简的主要成分是纤维素
B.安徽古代科学家方以智在其《物理小识》“有硇水者,剪银块投之,则旋而为水”,其
中的“硇水”指醋酸
C.甘肃出土的春秋早期秦国的铜柄铁剑中,铁元素有化合态和游离态两种存在形式
D.广西壮锦的主要原料是蚕丝等,蚕丝属于有机高分子化合物
【答案】B
【解析】A.竹简由竹子做成,主要成分是纤维素,A正确;B.硇水可以溶解银块,醋酸
不能溶解银块,所以硇水是硝酸,B不正确;C.铁剑中部分铁生锈生成氧化铁,故铁剑中
铁元素有化合态和游离态两种存在形式,C正确;D.蚕丝属于蛋白质,是有机高分子化合
物,D正确;答案选B。
2.下列化学事实不符合“量变引起质变”的哲学观点的是
A.Fe与稀硫酸反应生成H,但与浓硫酸发生钝化
2
B.向NaAlO 溶液中滴入盐酸先产生沉淀后沉淀消失
2
C.NaSO 溶液中滴入少量稀盐酸生成NaHSO,但滴入过量稀盐酸生成SO
2 3 3 2
D.葡萄糖(单糖)能发生银镜反应,但纤维素(多糖)不能发生银镜反应
【答案】D
【解析】A.Fe是比较活泼金属,能够与稀硫酸发生置换反应产生FeSO、H,但浓硫酸主
4 2
要以酸分子形式存在,具有强氧化性,在室温下遇到浓硫酸会发生钝化而不能进一步发生
反应,符合“量变引起质变”的哲学观点,A不符合题意;B.向NaAlO 溶液中滴入盐酸先
2
发生反应:NaAlO+HCl+HO=NaCl+Al(OH)↓,反应产生Al(OH) 白色沉淀,该物质是两性氢
2 2 3 3氧化物,当盐酸过量时,又发生反应:Al(OH)+3HCl=AlCl+3HO,因此看到反应产生的沉
3 3 2
淀又逐步溶解,直至沉淀消失,符合“量变引起质变”的哲学观点,B不符合题意;C.
HSO 是二元弱酸,向NaSO 溶液中滴入少量稀盐酸,发生反应:NaSO+HCl=NaHSO+NaCl,
2 3 2 3 2 3 3
生成了NaHSO;但当滴入过量稀盐酸时,又发生反应:NaHSO+HCl=NaCl+HO+SO↑,因此
3 3 2 2
又生成SO 气体。HCl的量不同,反应产物不同,符合“量变引起质变”的哲学观点,C不
2
符合题意;D.葡萄糖(单糖)的分子中含有醛基,能被弱氧化剂银氨溶液氧化而能发生银镜
反应,但纤维素(多糖)分子中无醛基,不能发生银镜反应,因此不符合“量变引起质变”
的哲学观点,D符合题意;故合理选项是D。
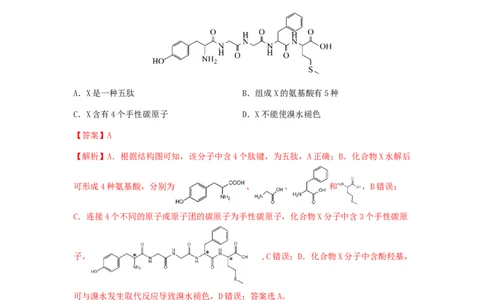
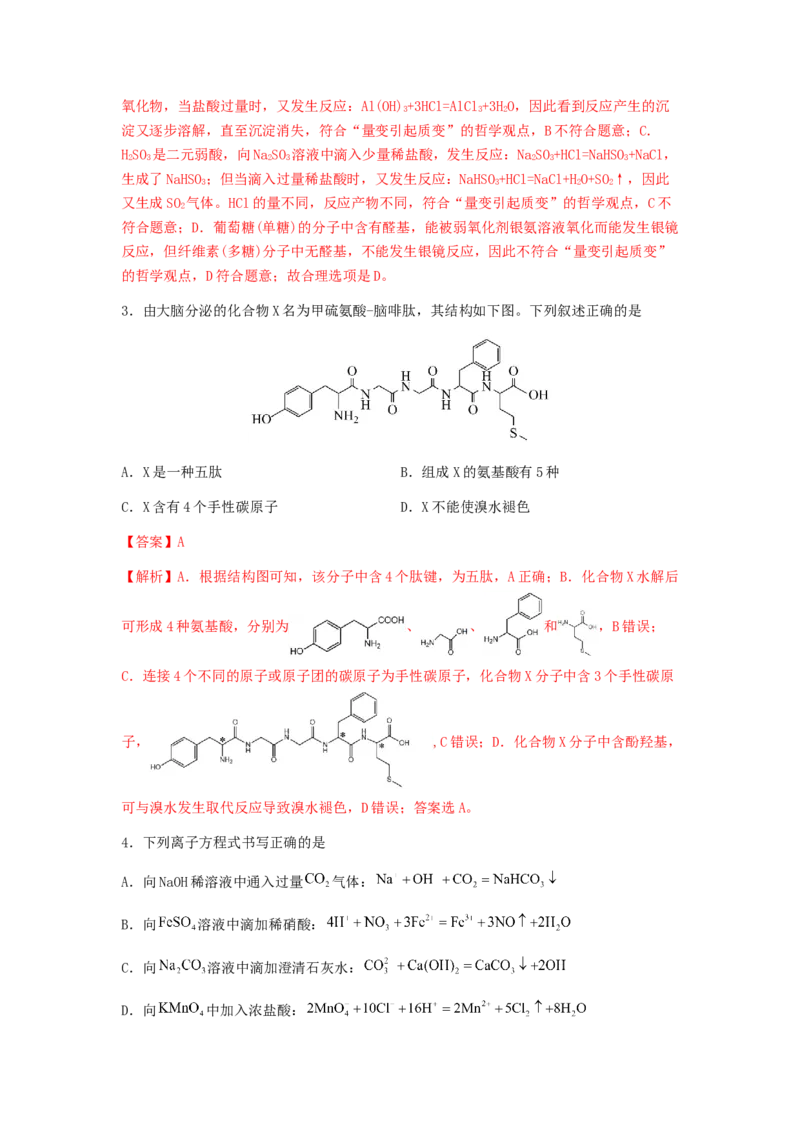
3.由大脑分泌的化合物X名为甲硫氨酸-脑啡肽,其结构如下图。下列叙述正确的是
A.X是一种五肽 B.组成X的氨基酸有5种
C.X含有4个手性碳原子 D.X不能使溴水褪色
【答案】A
【解析】A.根据结构图可知,该分子中含4个肽键,为五肽,A正确;B.化合物X水解后
可形成4种氨基酸,分别为 、 、 和 ,B错误;
C.连接4个不同的原子或原子团的碳原子为手性碳原子,化合物X分子中含3个手性碳原
子, ,C错误;D.化合物X分子中含酚羟基,
可与溴水发生取代反应导致溴水褪色,D错误;答案选A。
4.下列离子方程式书写正确的是
A.向NaOH稀溶液中通入过量 气体:
B.向 溶液中滴加稀硝酸:
C.向 溶液中滴加澄清石灰水:
D.向 中加入浓盐酸:【答案】D
【解析】A.向NaOH稀溶液中通入过量 气体生成碳酸氢钠: ,A错
误;B.电荷不守恒,应该为 ,B错误;C.澄清石
灰水在写离子方程式时拆成离子形式,即 ,C错误;D.高锰酸钾和
浓盐酸反应: ,D正确。答案选D。
5.下列有关物质的结构与性质说法正确的是
A.第二、三周期B、Al的第一电离能高于相邻元素,N、P的第一电离能低于相邻元素
B.键能:F-F大于Cl-Cl
C.O 是极性分子,它在水中溶解度高于在四氯化碳的溶解度
3
D.甲醇分子间的氢键键能大于水分子间的氢键键能
【答案】D
【解析】A.处于全满、半满轨道的电子稳定性强,因此第二、三周期B、Al的第一电离能
低于相邻元素,N、P的第一电离能高于相邻元素,A错误;B.由于F-F的键长短,使两
核间的斥力及电子层间斥力增大,使F-F的键能减小,F-F的键能小于Cl-Cl的键能,实
际F-F的键能为157kJ/mol,Cl-Cl的键能为242.7kJ/mol,B错误;C.虽然O 是极性分
3
子,但它在水中溶解度低于在四氯化碳的溶解度,C错误;D.CHOH分子中CH-是推电子
3 3
基团,分子中O原子的电负性最大,整个分子负电和主要集中在O原子周围,因此甲醇分
子中O原子带上明显负电,而水分子中O原子周围的负电荷密度则相对小些,因此甲醇分
子间氢键键能更大,例如甲醇分子的氢键键能为25.9kJ/mol,而水分子间的氢键键能为
18.8kJ/mol,D正确;答案选D。
6.下列有关实验现象和解释或结论都正确的是
选
实验操作 现象 解释或结论
项
向盛有2mL0.1mol/LNaOH溶液的试管中滴加4滴 先有白色沉
Ksp[Cu(OH)]HClO
2 2 2 3
产生
A.A B.B C.C D.D
【答案】B
【解析】A.反应中NaOH过量,再加4滴0.1mol/LCuSO 溶液生成氢氧化铜沉淀,不能证明
4
发生沉淀转化,A错误;B.实验中变量为温度,30℃条件下出现蓝色的时间较短,说明其
他条件相同时,温度越高,反应速率越大,B正确;C.挥发的乙醇也会使得酸性高锰酸钾
溶液褪色,不能说明1-溴丁烷发生消去反应生成1-丁烯,C错误;D.次氯酸具有氧化性,
把二氧化硫氧化为硫酸,硫酸根离子与钙离子形成沉淀,不能确定二者的酸性强弱,D错
误;故选B。
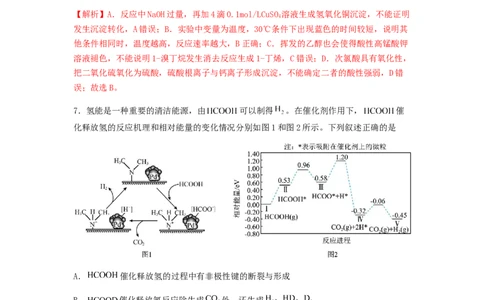
7.氢能是一种重要的清洁能源,由 可以制得 。在催化剂作用下, 催
化释放氢的反应机理和相对能量的变化情况分别如图1和图2所示。下列叙述正确的是
A. 催化释放氢的过程中有非极性键的断裂与形成
B. 催化释放氢反应除生成 外,还生成
C.在催化剂表面解离 键比解离 键难
D. 催化释放氢的热化学方程式为:
【答案】C
【解析】A.转化涉及到N-H键的断裂和形成、O-H键的断裂以及H-H键的形成,没有非极
性键的断裂,A错误;B.若用HCOOD代替HCOOH,反应为HCOOD分解,除生成CO 外,还生
2
成HD,没有H、D,B错误;C.由图可知,II→III过程中断裂O-H键,III→IV过程中断
2 2裂C-H键,III→IV的活化能大于II→III的,故在催化剂表面解离C−H键比解离O−H键
难,C正确;D.图2表示1分子HCOOH(g)生成CO(g)和H(g)时放出能量0.45eV,而热化
2 2
学方程式中ΔH为1mol反应的热量变化,故D错误;本题选C。
8.氮化钛(TiN)是新型耐热材料,其制备原理为6TiO+8NH 6TiN+12HO+N,实验装置
2 3 2 2
如图所示(夹持装置省略)。下列说法错误的是
A.试剂X可以是碱石灰或生石灰
B.装置的连接顺序为I→III→II→IV
C.先打开恒压分液漏斗旋塞,再打开管式炉加热开关
D.棉花的作用是防止固体进入导管,使导管堵塞
【答案】B
【分析】装置Ⅰ制备氨气,装置Ⅱ是发生装置,装置Ⅲ吸收尾气同时防止空气中的水蒸气
进入装置Ⅱ中,装置Ⅳ干燥氨气,据此解答。
【解析】A.浓氨水中加入氧化钙、氢氧化钠或碱石灰可以产生氨气,因此试剂X可以是碱
石灰或生石灰,A正确;B.氯化钙能吸收氨气,不能干燥氨气,所以装置的连接顺序为
I→IV→II→III,B错误;C.需要利用氨气排尽装置中的空气,所以先打开恒压分液漏斗
旋塞,再打开管式炉加热开关,C正确;D.由于气体的气流也可能把固体小颗粒插入导管
中,所以棉花的作用是防止固体进入导管,使导管堵塞,D正确;答案选B。
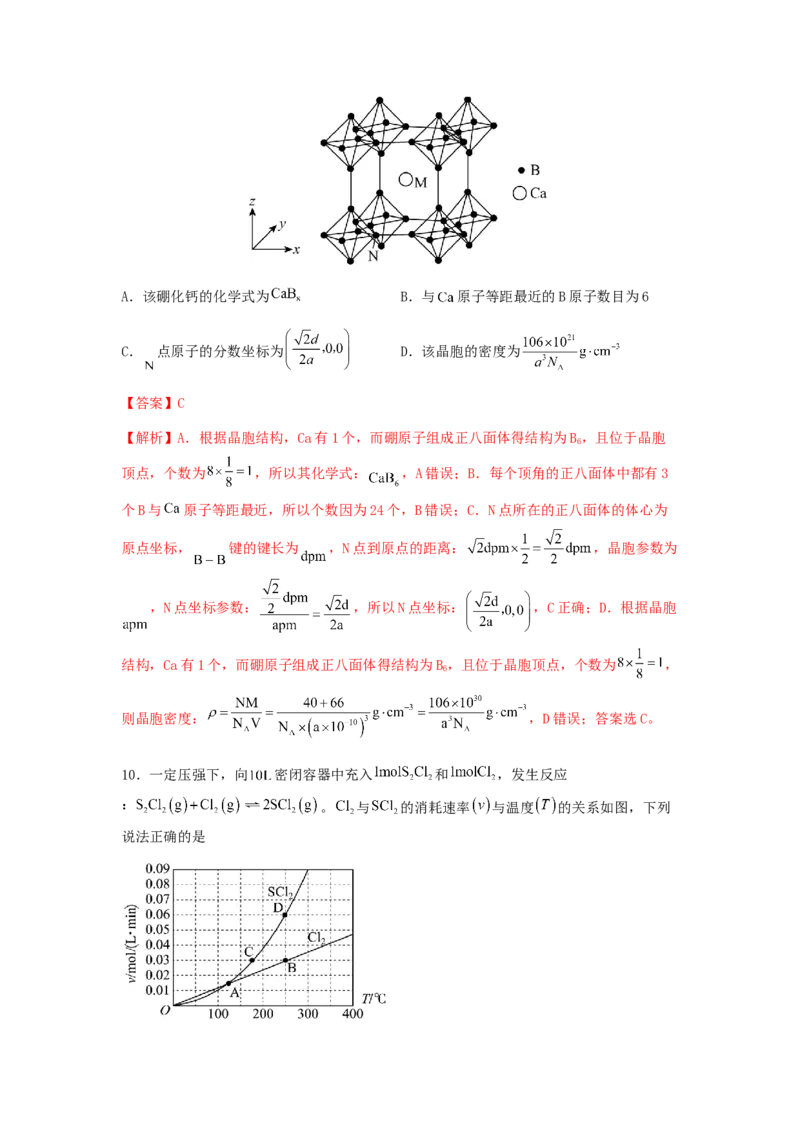
9.制造硼合金的原料硼化钙晶胞结构如图所示。硼原子组成正八面体,各个顶点通过
键互相连接成三维骨架。已知该晶体晶胞参数为 ,硼八面体中 键的键长为
,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分
数坐标,如 点原子的分数坐标为 。设 为阿伏加德罗常数的值,下列说法正
确的是A.该硼化钙的化学式为 B.与 原子等距最近的B原子数目为6
C. 点原子的分数坐标为 D.该晶胞的密度为
【答案】C
【解析】A.根据晶胞结构,Ca有1个,而硼原子组成正八面体得结构为B,且位于晶胞
6
顶点,个数为 ,所以其化学式: ,A错误;B.每个顶角的正八面体中都有3
个B与 原子等距最近,所以个数因为24个,B错误;C.N点所在的正八面体的体心为
原点坐标, 键的键长为 ,N点到原点的距离: ,晶胞参数为
,N点坐标参数: ,所以N点坐标: ,C正确;D.根据晶胞
结构,Ca有1个,而硼原子组成正八面体得结构为B,且位于晶胞顶点,个数为 ,
6
则晶胞密度: ,D错误;答案选C。
10.一定压强下,向 密闭容器中充入 和 ,发生反应
。 与 的消耗速率 与温度 的关系如图,下列
说法正确的是A. 四点中只有 点达到平衡状态
B.正反应的活化能小于逆反应的活化能
C.
D. ,反应达平衡后缩小容器体积,各物质浓度不变
【答案】B
【分析】Cl 的消耗速率表示正反应速率,SCl 的消耗速率表示逆反应速率,当
2 2
时,说明正逆反应速率相等,反应到达平衡,所以图像的平衡点应为
B和D点。
【解析】A. A点 ,未达到平衡,故A错误;B.随着温度升高,SCl
2
的消耗速率大于Cl 的消耗速率的二倍,则逆反应速率大于正反应速率,说明温度升高,
2
平衡逆向移动,是放热反应,则正反应的活化能小于逆反应的活化能,故B正确;C.该反
应为放热反应,温度升高,K减小,由图可知,C点温度最低,则K最大,故
,故C错误;D.300℃时,反应达平衡后缩小容器体积,平衡不移动,
但是体积缩小,各组分浓度均增加,故D错误。故选B。
11.配位化合物广泛应用于物质分离、定量测定、医药、催化等方面。利用氧化法可制备
某些配位化合物,如 。设
是阿伏加德罗常数的值,下列叙述正确的是
A. 中含有 键的数目为
B. 和 的VSEPR模型完全相同
C. 与足量 在催化剂作用下合成氨,生成的 分子数为
D. 质量分数为 的 溶液中,氧原子总数为
【答案】A
【解析】A. 中含有 键的数目为 ,故A正确;
B. 和 的中心原子的杂化方式相同,但是孤电子对数不同,故VSEPR模型不完全
相同,故B错误;C.合成氨是可逆反应,生成 的分子数小于 ,故C错误;D.
中氧原子总数为 ,水中还含有氧原子,则氧原子总数大于
,故D错误 ;答案选A。12.为检测某品牌银耳中添加剂亚硫酸盐的含量,取 银耳样品和 蒸馏水放入
三颈瓶中;取 碘标准溶液和 淀粉溶液加入锥形瓶中,并加入适量蒸
馏水搅拌,部分装置如图。向三颈瓶中通氮气,再加入过量磷酸,加热并保持微沸,同时
用 碘标准溶液滴定,至终点时滴定消耗了 碘标准液。另做空白实验,消
耗 碘标准溶液。下列说法错误的是
A.选择的三颈瓶规格为1000mL
B.滴定终点溶液变为蓝色,读数时应单手持滴定管
C.“不通氮气”或者“先加磷酸再通氮气”,这两种做法都会使测定结果偏高
D.银耳样品中亚硫酸盐的百分含量(以 质量计)为
【答案】C
【解析】A.三颈烧瓶所盛液体体积通常占其容积的1/3~2/3,则本实验应选择的三颈烧瓶规格为
,A正确;B.将SO 消耗完后,过量的碘单质与淀粉反应使溶液显蓝色,读数时应单手持滴定管,
2
B正确;C.开始通入氮气的目的是将装置中的空气排出,防止空气中的氧气将亚硫酸盐部分氧化成硫酸
盐而影响实验,若“不通氮气”或者“先加磷酸再通氮气”,反应生成的SO 量较少,消耗的标准碘液也
2
少,所测结果偏低,C错误;D.反应中消耗I 的体积为0.4 mL +1.0mL-0.2mL=1.2mL,n(I)=1.2×10-
2 2
3L×0.01mol/L=1.2×10-5mol,根据关系式I~ SO 知,n(SO)= 1.2×10-5 mol,
2 2 2
m(SO)=64g/mol×1.2×10-5mol=7.68×10-4g=0.000768g,样品为10.00g,因此SO 的含量为
2 2
,D正确;答案选C。
13.利用双极膜电解含有 的溶液,使 转化成碳燃料,实现了 还原流动。电
解池如下图所示,双极膜中水电离的 和 在电场作用下可以向两极迁移。下列说法
不正确的是A.银网电极与电源负极相连
B.双极膜b侧应该用质子交换膜
C.阴极电极反应为:
D.双极膜中有0.1mol 电离,则阳极附近理论上产生0.05mol
【答案】D
【分析】根据示意图,右侧 生成CO,发生还原反应,为阴极区,即Ag网为阴极,与
电源的负极相连,阴极的反应式为: ;Ni网为阳极,电极
反应式为: ,双极膜中H+向右侧移动,即b为质子膜,OH-向左侧
移动,a为阴离子膜。
【解析】A.由上述分析可知,银网电极为阴极,与电源负极相连,故A正确;B.双极膜
中H+向右侧移动,即b为质子膜,故B正确;C.阴极的电极反应式为:
,故C正确;D.根据阳极反应式 ,
产生0.05mol 会消耗0.2molOH-,双极膜中有0.2mol 电离,故D错误。答案选D。
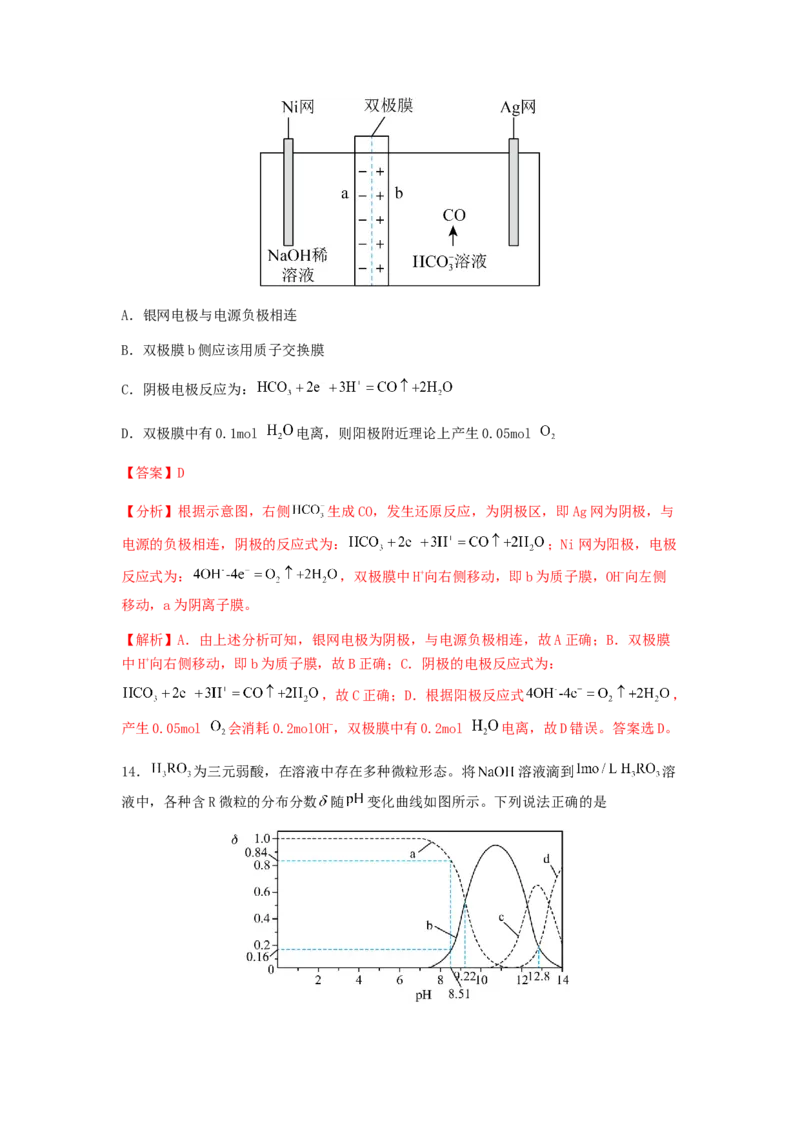
14. 为三元弱酸,在溶液中存在多种微粒形态。将 溶液滴到 溶
液中,各种含R微粒的分布分数 随 变化曲线如图所示。下列说法正确的是A. 的
B.当 调至11~12时发生反应的离子方程式为:
C. 时,溶液中
D. 时,溶液中
【答案】C
【分析】因为HRO 为三元弱酸,电离过程分步进行,则图中a、b、c、d分别表示HRO、
3 3 3 3
、 、 分布分数随pH变化曲线,据此解答。
【解析】A.图中pH=9.22时, ,则HRO 的 ,故A错误;
3 3
B.由图可知,当pH调至11~12时, 迅速减小, 迅速增大,则 与
OH−反应生成 ,发生反应的离子方程式为: ,故B错误;
C.pH=12.8时,溶液中由电荷守恒得:
,且 ,
则 ,故C正确;D.pH=14时,
c(OH−)=1mol/L,且由图可知: ,且各种含R微粒的浓度
都小于1mol/L,则溶液中 ,故D错误;故选
C。
二、主观题
16.(14分)无水四氯化锡 是一种重要的工业原料,其在常温下
为无色液体,沸点114℃,在空气中极易水解生成 ,液态四氯化锡对很多非极
性分子有一定的溶解度。实验室可选用以下装置用熔融的锡与氯气反应制备无水 ,
请回答有关问题:(1)四氯化锡分子的空间结构为 。
(2)A中盛放 晶体的仪器名称为 ,在其中发生反应的化学方程式是 。
(3)整个实验装置的连接顺序是A→ →B→C→ (装置可重复选用),若缺少装
置F,则收集器C中发生反应的化学方程式为 。
(4)收集器C中收集到的液体略显黄色,原因是 ,C中上方冷水的作用是 。
(5)除氯后测定最后产品的纯度。量取 ,ag/mL的样品,置于已称重含20mL水的称量
瓶中,混合后,移入锥形瓶,加入200mL水和2滴1%甲基橙指示液,用b mol/L的NaOH标
准液滴定,消耗标准液 (接近终点时,每滴加一滴标准液须待沉淀沉降后观察澄清
液体的颜色)。滴定到达终点的实验现象为 ,产品的纯度为 %。
【答案】(1)正四面体形(1分)
(2)圆底烧瓶 (1分) (2分)
(3)E→F (1分) F→D(1分) (2分)
(4)有氯气溶在了液态四氯化锡里(1分) 冷凝 (1分)
(5)滴入最后半滴NaOH标准液,溶液由红色变为黄色,且半分钟内不褪色(2分)
(2分)
【分析】装置 A 中KClO 与浓盐酸反应生成 KCl 、Cl、HO,混有 HCl 和水蒸气的Cl 进
3 2 2 2
入装置 E (盛装饱和食盐水)中,除去氯气中的 HCl 气体,再将气体通入装置 F (盛装
浓硫酸)中,除去水蒸气,再将干燥的 Cl 通入装置 B 中,与 Sn 在加热的条件下反应,
2
生成SnCl,再通过装置 C 对SnCl 蒸汽进行冷凝回流,多余的尾气经过 F 干燥装置,再
4 4
用装置 D 中 NaOH 溶液吸收处理,同时浓硫酸还起着防止水蒸气进入装置 C 的作用;
【解析】(1) 中心原子价电子数为 ,无孤电子对,分子空间构型为正四面体形;
(2)由装置图可知,A中盛放 晶体的仪器名称为圆底烧瓶,发生的反应方程式为:
;
(3)根据分析可得,整个实验装置的连接顺序是A→E→F→B→C→F→D;故答案为:
E→F;F→D;若缺少装置F,则收集器C中发生反应的化学方程式为:
;
(4)根据题干液态四氯化锡对很多非极性分子有一定的溶解度,氯气可溶于 ,收集
器C中收集到的溶解了氯气,使液体略显黄色;常温时 为无色液体,沸点(114℃)较
低,C中上方的冷水的作用是冷凝;(5)量取 ,ag/mL的样品,置于已称重含20mL
水的称量瓶中,混合后,移入锥形瓶,加入200mL水和2滴1%甲基橙指示液,发生反应
,溶液为红色,用b mol/L的NaOH标准液滴定,反应
为 ,消耗标准液 ,溶液滴定完后为碱性,滴定达到终点的实
验现象为滴入最后半滴NaOH溶液,溶液由红色变为黄色,且半分钟内不褪色,根据反应过
程的关系式为 ,产品的纯度为
。