文档内容
备战2024年高考化学考前手感保温训练(新高考卷)
专练13 14道选择题+主观流程题
完卷时间:40分钟
答案速查
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 C B B D A B B D D D B D C D
可能用到的相对原子质量:O 16 Cu 64 Ba 137 Hg 201
一、选择题(共42分,只有1个正确选项)
1.化学促进了科技进步和社会发展。下列有关说法错误的是
A.高性能聚酰亚胺薄膜是有机高分子材料制成的
B.电动车的模块化电池放电时化学能转化成电能
C.软磁铁氧体磁芯的制作材料属于合金
D.双低超净(超低 、CO)高效节能燃烧技术的应用有利于环保
【答案】C
【解析】A.高性能聚酰亚胺薄膜是当前世界上性能最好的有机高分子绝缘薄膜材料之一,
也被称为“黄金薄膜”,故A正确;B.电动车的模块化电池属于原电池,放电时化学能转
化成电能,故B正确;C.软磁铁氧体磁芯的制作材料为氧化铁,不是合金,故C错误;
D.双低超净(超低NO、CO)高效节能燃烧技术的应用可以减少氮氧化物的排放,有利于环
x
保,故D正确。故选C。
2.下列化学用语或表述正确的是
A.丙炔的键线式:
B.顺-2-丁烯的分子结构模型:
C. 的空间结构:V形
D.基态碳原子的轨道表示式:【答案】B
【解析】A. 碳碳三键呈直线,丙炔中三个碳原子在一条直线上,则丙炔的键线式:
,A错误;B. 顺-2-丁烯的球棍模型: ,B正确;C.
中B原子不含孤电子对,价层电子对数为:3+0=3,分子呈平面三角形结构,C错误;D.
基态碳原子的核外电子排布式为,根据洪特规则,2p轨道上的2个电子应该分别在2个轨
道上,且自旋方向相同,轨道表示式: ,D错误;选B。
3.实验室中,关于下列仪器使用的说法正确的是
A.①和③可用于配制10%的NaCl溶液
B.③和④可用于分离苯酚和水
C.②可用于量取酸性高锰酸钾溶液
D.瓷材质的⑤可用于煅烧石灰石
【答案】B
【解析】A.配制一定质量分数的溶液需要计算、称量、溶解,需托盘天平、药匙、量筒、
烧杯、玻璃棒,A错误;B.③和④可用于分液分离苯酚和水,B正确;C.量取酸性高锰酸
钾溶液应该使用酸式滴定管,C错误;D.瓷材质会和碱性物质反应,⑤不可用于煅烧石灰
石,D错误;故选B。
4.下列有关物质结构与性质的说法错误的是
A.简单氢化物分子间形成的氢键越多,物质的熔、沸点越高
B.超分子具有分子识别和自组装的重要特征
C.通过X射线衍射实验可区分晶体 和非晶体
D.离子晶体中阴、阳离子有配位数说明离子键有饱和性【答案】D
【解析】A.分子间氢键使分子之间的相互作用更为紧密牢固,因而需要更高的能量使它们
具有良好的自由性,故熔沸点升高,分子间形成的氢键越多,物质的熔、沸点越高,A正
确;B.超分子是由两种或两种以上的分子通过分子间相互作用形成的分子聚集体,超分子
的重要特征是分子识别与自组装,B正确;C.当X射线通过晶体时,会在记录仪上看到分
立的斑点或谱线,而非晶体则没有,所以X射线衍射实验是区分晶体与非晶体最可靠的方
法,C正确;D.离子键是没有方向性和饱和性的,只要空间允许,一个阳离子周围都尽可
能多地排列阴离子,D错误;故选D。
5.周期表中ⅢA族单质及其化合物应用广泛。 极易水解生成 ( 在水溶液中完
全电离为 和 )和硼酸( ),硼酸是一元弱酸,能溶于水;硼酸和甲醇在浓硫酸
存在下生成挥发性的硼酸甲酯 ; 是一种重要还原剂,其与热水反应生
成 和硼酸钠( );高温下 和焦炭在氯气的氛围中反应,生成 及一种剧
毒气体;GaN是第三代半导体研究的热点。下列化学反应表示正确的是
A. 与热水反应:
B. 溶液与NaOH溶液反应:
C.用石墨作电极电解 制备Al的阴极反应式:
D.高温下 、焦炭在氯气中反应:
【答案】A
【解析】A.由题干信息可知, 是一种重要还原剂,其与热水反应生成 和硼酸钠
( ),则 与热水反应的化学方程式为: ,A正
确;B.由题干信息可知, 在水溶液中完全电离为 和 ,则 溶液与NaOH溶
液反应的离子方程式为:H++OH-=HO,B错误;C.电解时阴极发生还原反应,故用石墨作
2
电极电解 制备Al的阴极反应式为:Al3++3e-=Al,阳极反应式才是 ,
C错误;D.由题干信息可知,高温下 和焦炭在氯气的氛围中反应,生成 及一种
剧毒气体,根据元素守恒可推知该气体为CO,则高温下 、焦炭在氯气中反应方程式
为: ,D错误;故答案为:A。6.X、Y、Z、M、Q五种短周期主族元素,原子序数依次增大。X、Y、Z位于同一周期,且
互不相邻,三者的最外层电子数之和为15,基态Y原子的价电子层中有3个未成对电子,Z
与Q同主族,M原子在同周期中原子半径最大,下列说法不正确的是
A.化学键中离子键成分的百分数:MZ>MQ
B.键角:XZNaCl,故A正
确;B.BF 中B价电子对数为3,无孤电子对,空间构型为平面三角形,NCl 中N原子价电
3 3
子对数为4,有1个孤电子对,空间构型为三角锥形,所以键角:BF>NCl,故B错误;
3 3
C.电子层数越多半径越大,电子层数相同,质子数越多半径越小,F、Na、Cl原子形成稀
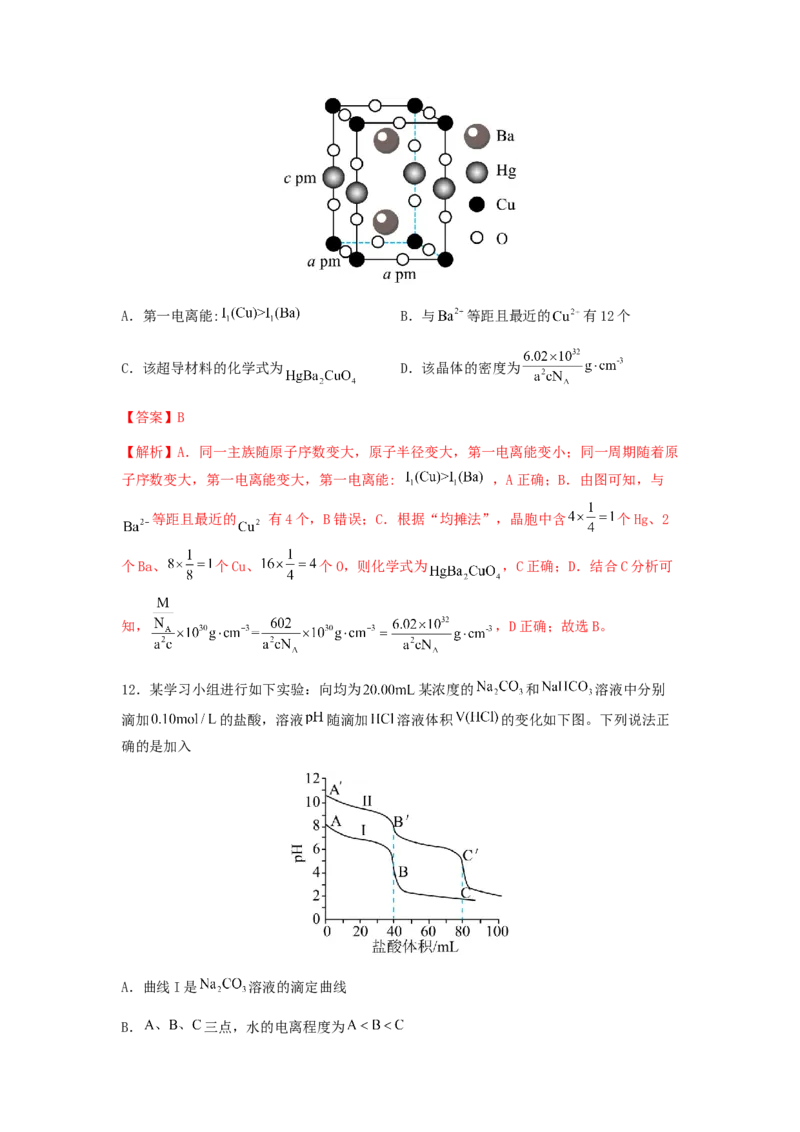
有气体电子构型的简单离子的半径:Na+K ,故相同浓度的碳酸钠和碳酸氢钠,碳酸钠水解的程度更大,因
2 3 a1 a2
此碳酸钠的碱性更强,应为曲线II,A错误;B.图I中A点溶质为碳酸氢钠,碳酸氢根离
子水解,促进水的电离,B点溶质为氯化钠,不影响水的电离,C点溶质为氯化钠和稀盐酸,
盐酸抑制水的电离,故A>B>C ,B错误;C. 点溶质为碳酸氢钠,根据质子守恒可知,微
粒满足关系式为 ,C错误;D.根据图像可知一开
始碳酸钠的浓度为 ,钠离子浓度为 ,而根据物料守恒可知
,
,D正确;故选D。
13.利用下图电池装置可验证不同化合价铁元素的相关性质。
已知:电池装置中,盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率
(如下表)应尽可能地相近;两烧杯中溶液体积相等。
离子 Li+ Na+ Ca2+ K+ Cl-
4.07 5.19 6.59 7.62 4.61 7.40 7.91 8.27
下列说法正确的是
A.根据上表数据,盐桥中应选择KNO 作为电解质
3
B.石墨电极上对应的电极反应式为:
C.反应一段时间后,当右池中 时,左池中
D.盐桥中的阴离子进入石墨电极一侧溶液中【答案】C
【分析】由题意和图知,铁电极为负极,电极反应式为 ,石墨电极为正极,
电极反应式为 ,由此回答。
【解析】A.Fe2+、Fe3+能与 反应,Ca2+与 不能大量共存,FeSO、Fe(SO) 都属
4 2 4 3
于强酸弱碱盐,水溶液呈酸性,酸性条件下 能与Fe2+反应,根据题意“盐桥中阴、阳
离子不与溶液中的物质发生化学反应”,盐桥中阴离子不可以选择 、 ,阳离子
不可以选择Ca2+,盐桥中阴、阳离子的迁移率(u∞)应尽可能地相近,根据表中数据,
盐桥中应选择KCl作为电解质,A错误;B.由分析知,石墨电极为正极,电极反应式为
,B错误;C.由图知,右池中原 ,发生反应为
,现 ,即 ,在此过程中
增加了0.10mol/L,转移的电子数为0.10mol/L,则由负极反应式 知,
左池中 增加了0.05mol/L,即左池中 ,C正确;D.盐桥中的阴
离子流向负极,由分析知,进入铁电极一侧溶液中,D错误;故选C。
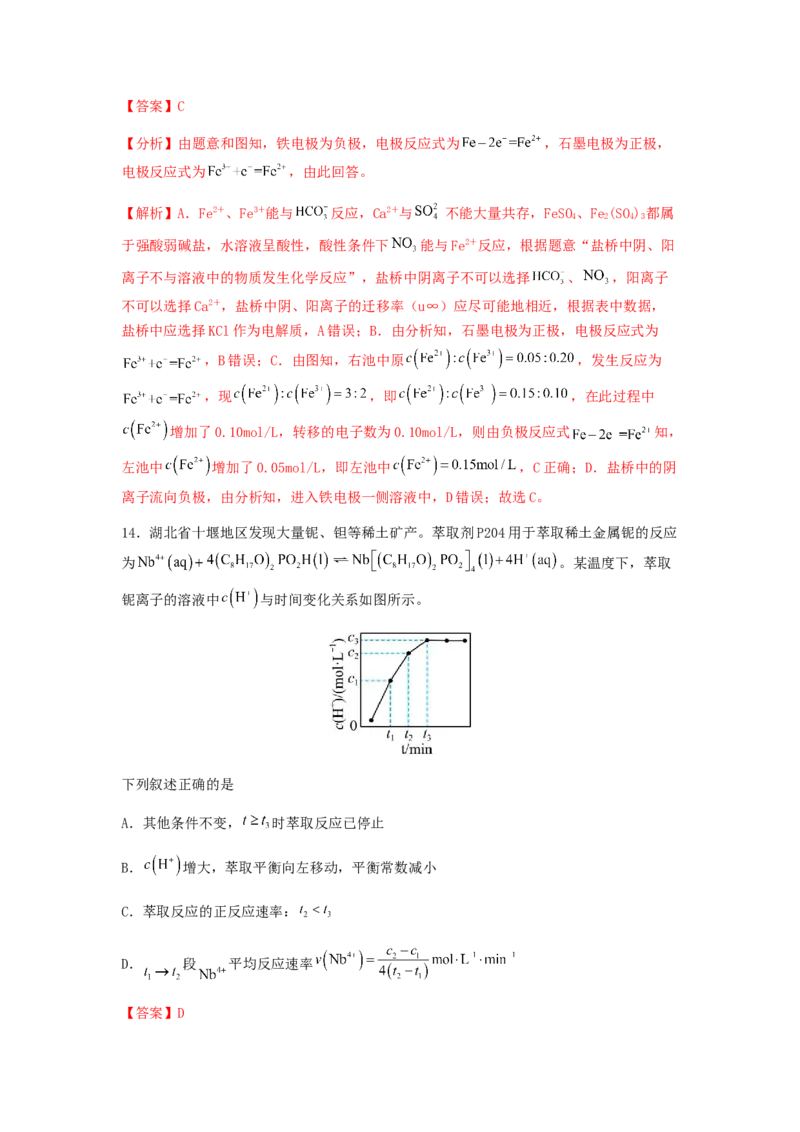
14.湖北省十堰地区发现大量铌、钽等稀土矿产。萃取剂P204用于萃取稀土金属铌的反应
为 。某温度下,萃取
铌离子的溶液中 与时间变化关系如图所示。
下列叙述正确的是
A.其他条件不变, 时萃取反应已停止
B. 增大,萃取平衡向左移动,平衡常数减小
C.萃取反应的正反应速率:
D. 段 平均反应速率
【答案】D【解析】A.平衡时正反应、逆反应不断进行,只是正、逆反应速率相等,A项错误;B.
平衡常数只与温度有关,温度不变,K不变,B项错误;C.萃取反应发生后,正反应速率
由大到小至不变时达到平衡, 时正反应速率大于 ,C项错误;D.根据萃取反应式,铌
离子消耗速率是氢离子生成速率的四分之一, ,D项正
确;故选:D。
二、主观题
15.(14分)草酸镍( )是一种不溶于水的浅绿色粉末,常用于制镍催化剂和镍粉
等。以铜镍合金废料(主要成分为镍和铜,含有一定量的铁和硅)为原料生产草酸镍的工艺
流程如图:
已知:①“浸出”液含有的离子主要有 、 、 、 、 、 ;②pH增
大, 被氧化的速率加快,同时生成的 水解形成的胶体能吸附 ;③草酸的
, 。
回答下列问题:
(1)Ni在元素周期表中的位置是 。
(2)生产时为提高合金废料浸出率,下列措施可行的是 (填字母)。
A.适当延长浸出时间 B.高温浸出 C.分批加入混酸浸取并搅拌
(3)“萃取”步骤中萃取除去的主要金属阳离子是 。
(4)“氧化”过程中,控制70℃、pH小于3的条件下进行。
①“氧化”过程的离子方程式为 ;②若pH大于3镍的回收率降低的原因是
。
(5)“过滤”后的滤液中加入 溶液反应得到草酸镍,过滤得到的草酸镍需要用
蒸馏水洗涤,检验晶体是否洗涤干净的方法是 ;已知常温下
,当溶液 时, 沉淀完全[ 认为完全沉淀],则此时溶液中草酸的浓度 (保留两位有效数字)。
(6)在空气中加热二水合草酸镍得到NiO,该反应的化学方程式为 。
【答案】(1)第4周期Ⅷ族(1分)
(2)ac(2分)
(3)Cu2+(1分)
(4)① (2分) ②pH过高,Fe3+生成氢氧化铁胶体
吸附大量Ni2+,导致镍回收率降低(2分)
(5)取最后一次的洗涤液少许于试管中,先加盐酸酸化,再加氯化钡溶液,若无沉淀生成,
则证明洗涤干净(2分) (2分)
(6) (2分)
【分析】由已知信息可知,合金废料中加入混酸浸取液浸取后,得到的溶液中含有的离子
有H+、Ni2+、Cu2+、Fe3+、 、 ,向溶液中加入萃取剂,用萃取剂除去溶液中的
Cu2+,向萃取后的溶液中加入还原剂,将Fe3+还原为Fe2+,然后加入HO,将Fe2+氧化为
2 2
FeOOH沉淀,除去溶液中的铁元素;过滤后,向滤液中加入,(NH)CO 溶液反应得到
4 2 2 4
NiCO。
2 4
【解析】(1)Ni为28号元素,位于周期表中第4周期Ⅷ族;
(2)a.适当延长浸出时间可以使反应更充分,提高浸出率,a项选;b.高温条件下可以
加快反应速率,但是在高温条件下硝酸会挥发,故不能用高温浸出,b项不选;c.分批加
入混酸浸取并搅拌能使反应物混合更均匀,更充分,提高浸出率,c项选;答案选ac;
(3)由流程分析可知,后续的操作不能除去Cu2+,故只能在萃取步骤中除去Cu2+;
(4)①由题意可知,氧化过程是在70℃、pH小于3的条件下进行,过氧化氢与亚铁离子
发生氧化还原反应生成FeOOH沉淀,反应的离子方程式为
;②由题给信息可知,溶液pH增大,Fe2+被氧化的速率
加快,同时生成的Fe3+水解形成更多的胶体能吸附Ni2+,导致镍回收率降低;
(5)由流程可知,草酸镍晶体表面附有可溶的硫酸铵和硝酸铵,检验晶体是否洗涤干净实
际上就是检验洗涤液中是否存在硫酸根,则检验方法为取最后一次的洗涤液少许于试管中,
先加盐酸酸化,再加氯化钡溶液,若无沉淀生成,则证明洗涤干净;常温下
K [NiCO]=1.70×10-17,当溶液pH=2时,Ni2+沉淀完全,假设Ni2+浓度为1×10-
sp 2 45mol·L-1,则 ,溶液pH=2,
c(H+)=1×10-2 mol·L-1,草酸的K = ,则
a2
,K = ,则=
a1
;
(6)在空气中加热二水合草酸镍得到NiO,该反应的化学方程式为
。