文档内容
专练 36 化学平衡的移动及影响因素
一、单项选择题
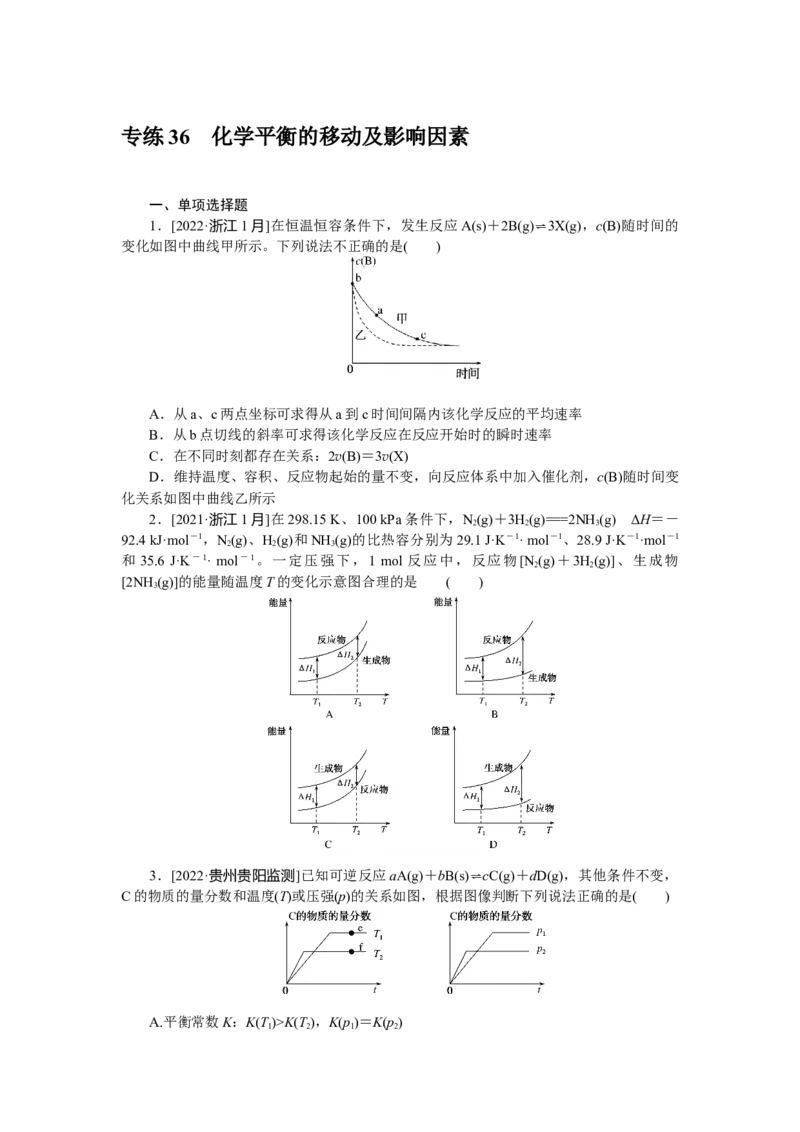
1.[2022·浙江1月]在恒温恒容条件下,发生反应A(s)+2B(g)⇌3X(g),c(B)随时间的
变化如图中曲线甲所示。下列说法不正确的是( )
A.从a、c两点坐标可求得从a到c时间间隔内该化学反应的平均速率
B.从b点切线的斜率可求得该化学反应在反应开始时的瞬时速率
C.在不同时刻都存在关系:2v(B)=3v(X)
D.维持温度、容积、反应物起始的量不变,向反应体系中加入催化剂,c(B)随时间变
化关系如图中曲线乙所示
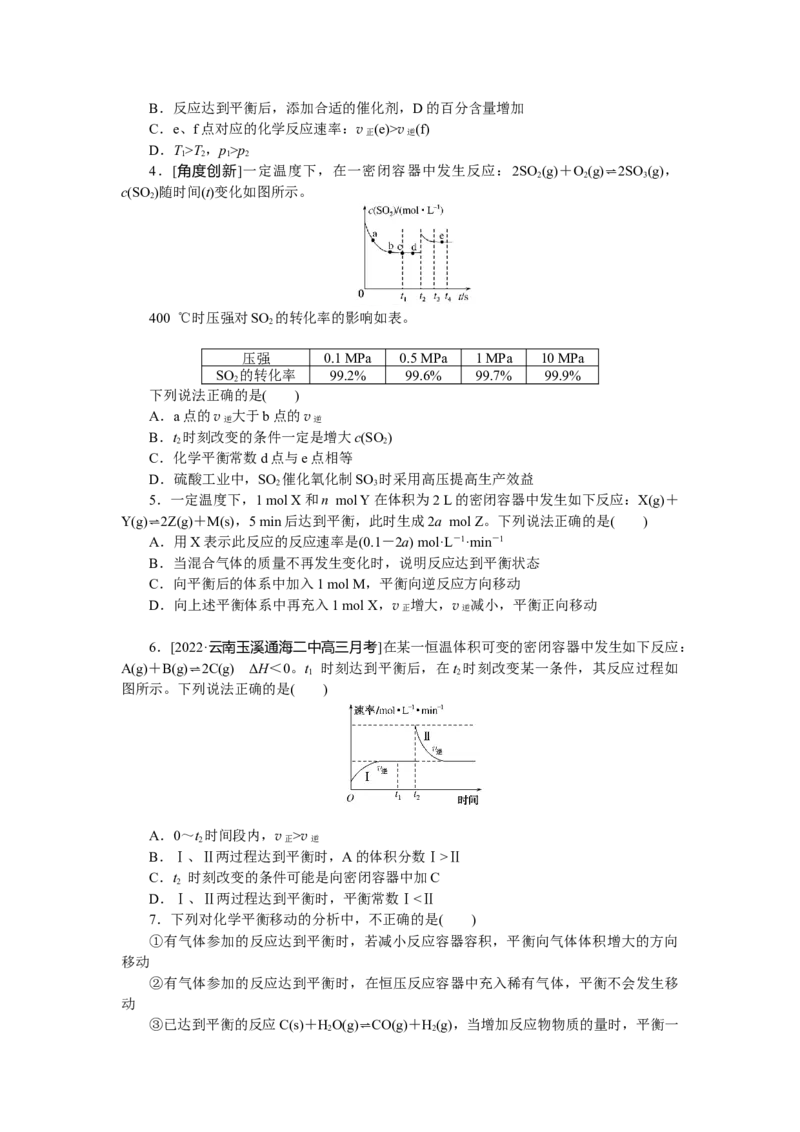
2.[2021·浙江1月]在298.15 K、100 kPa条件下,N(g)+3H(g)===2NH(g) ΔH=-
2 2 3
92.4 kJ·mol-1,N(g)、H(g)和NH (g)的比热容分别为29.1 J·K-1· mol-1、28.9 J·K-1·mol-1
2 2 3
和 35.6 J·K-1· mol-1。一定压强下,1 mol 反应中,反应物[N (g)+3H(g)]、生成物
2 2
[2NH (g)]的能量随温度T的变化示意图合理的是 ( )
3
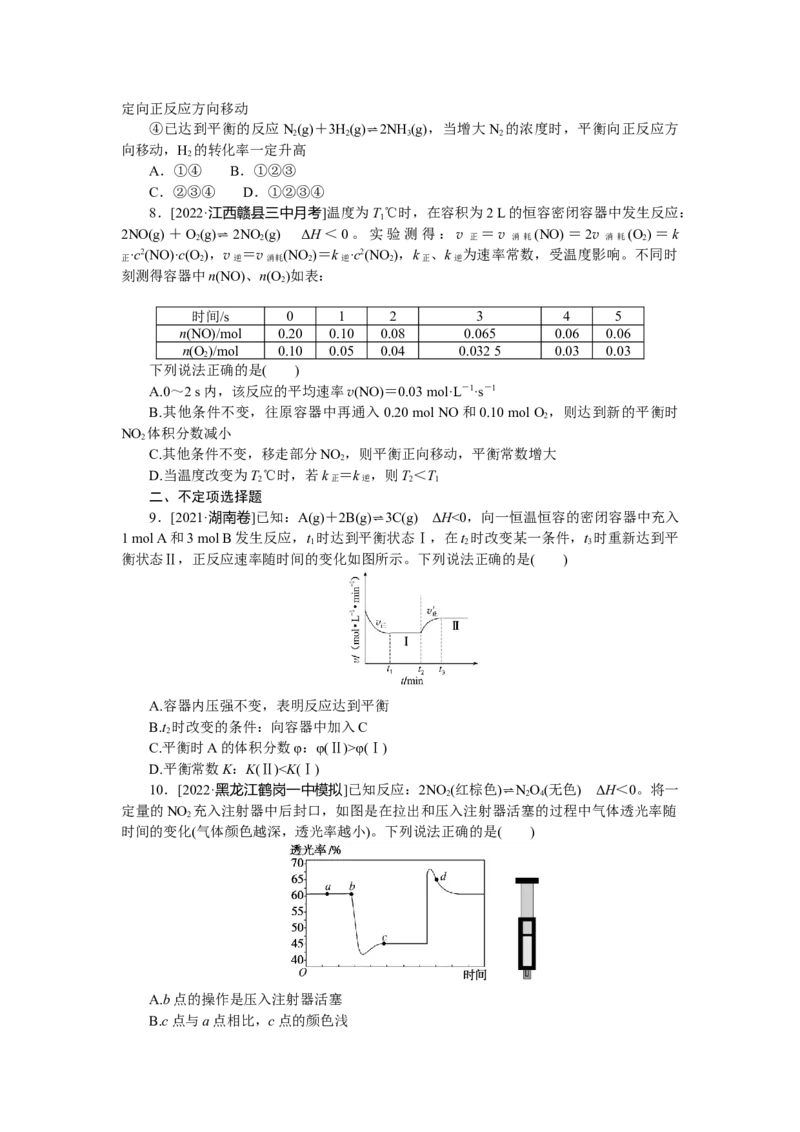
3.[2022·贵州贵阳监测]已知可逆反应aA(g)+bB(s)⇌cC(g)+dD(g),其他条件不变,
C的物质的量分数和温度(T)或压强(p)的关系如图,根据图像判断下列说法正确的是( )
A.平衡常数K:K(T)>K(T),K(p)=K(p)
1 2 1 2B.反应达到平衡后,添加合适的催化剂,D的百分含量增加
C.e、f点对应的化学反应速率:v正 (e)>v逆 (f)
D.T>T,p>p
1 2 1 2
4.[角度创新]一定温度下,在一密闭容器中发生反应:2SO
2
(g)+O
2
(g)⇌2SO
3
(g),
c(SO )随时间(t)变化如图所示。
2
400 ℃时压强对SO 的转化率的影响如表。
2
压强 0.1 MPa 0.5 MPa 1 MPa 10 MPa
SO 的转化率 99.2% 99.6% 99.7% 99.9%
2
下列说法正确的是( )
A.a点的v逆 大于b点的v逆
B.t 时刻改变的条件一定是增大c(SO )
2 2
C.化学平衡常数d点与e点相等
D.硫酸工业中,SO 催化氧化制SO 时采用高压提高生产效益
2 3
5.一定温度下,1 mol X和n mol Y在体积为2 L的密闭容器中发生如下反应:X(g)+
Y(g)⇌2Z(g)+M(s),5 min后达到平衡,此时生成2a mol Z。下列说法正确的是( )
A.用X表示此反应的反应速率是(0.1-2a) mol·L-1·min-1
B.当混合气体的质量不再发生变化时,说明反应达到平衡状态
C.向平衡后的体系中加入1 mol M,平衡向逆反应方向移动
D.向上述平衡体系中再充入1 mol X,v正 增大,v逆 减小,平衡正向移动
6.[2022·云南玉溪通海二中高三月考]在某一恒温体积可变的密闭容器中发生如下反应:
A(g)+B(g)⇌2C(g) ΔH<0。t
1
时刻达到平衡后,在t
2
时刻改变某一条件,其反应过程如
图所示。下列说法正确的是( )
A.0~t
2
时间段内,v正 >v逆
B.Ⅰ、Ⅱ两过程达到平衡时,A的体积分数Ⅰ>Ⅱ
C.t 时刻改变的条件可能是向密闭容器中加C
2
D.Ⅰ、Ⅱ两过程达到平衡时,平衡常数Ⅰ<Ⅱ
7.下列对化学平衡移动的分析中,不正确的是( )
①有气体参加的反应达到平衡时,若减小反应容器容积,平衡向气体体积增大的方向
移动
②有气体参加的反应达到平衡时,在恒压反应容器中充入稀有气体,平衡不会发生移
动
③已达到平衡的反应C(s)+H
2
O(g)⇌CO(g)+H
2
(g),当增加反应物物质的量时,平衡一定向正反应方向移动
④已达到平衡的反应N
2
(g)+3H
2
(g)⇌2NH
3
(g),当增大N
2
的浓度时,平衡向正反应方
向移动,H 的转化率一定升高
2
A.①④ B.①②③
C.②③④ D.①②③④
8.[2022·江西赣县三中月考]温度为T℃时,在容积为2 L的恒容密闭容器中发生反应:
1
2NO(g)+O
2
(g)⇌2NO
2
(g) ΔH<0。实验测得:v
正
=v
消耗
(NO)=2v
消耗
(O
2
)=k
正
·c2(NO)·c(O
2
),v逆 =v消耗 (NO
2
)=k
逆
·c2(NO
2
),k
正
、k
逆
为速率常数,受温度影响。不同时
刻测得容器中n(NO)、n(O )如表:
2
时间/s 0 1 2 3 4 5
n(NO)/mol 0.20 0.10 0.08 0.065 0.06 0.06
n(O )/mol 0.10 0.05 0.04 0.032 5 0.03 0.03
2
下列说法正确的是( )
A.0~2 s内,该反应的平均速率v(NO)=0.03 mol·L-1·s-1
B.其他条件不变,往原容器中再通入0.20 mol NO和0.10 mol O ,则达到新的平衡时
2
NO 体积分数减小
2
C.其他条件不变,移走部分NO ,则平衡正向移动,平衡常数增大
2
D.当温度改变为T℃时,若k =k ,则T<T
2 正 逆 2 1
二、不定项选择题
9.[2021·湖南卷]已知:A(g)+2B(g)⇌3C(g) ΔH<0,向一恒温恒容的密闭容器中充入
1 mol A和3 mol B发生反应,t 时达到平衡状态Ⅰ,在t 时改变某一条件,t 时重新达到平
1 2 3
衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是( )
A.容器内压强不变,表明反应达到平衡
B.t 时改变的条件:向容器中加入C
2
C.平衡时A的体积分数φ:φ(Ⅱ)>φ(Ⅰ)
D.平衡常数K:K(Ⅱ)”“=”或“<”)。
②平衡常数K 的表达式为K =________。
2 2
③氯气在水中的溶解度(以物质的量浓度表示)为c,则c=________。(用平衡压强p和上述平衡常数表示,忽略HClO的电离)
(4)工业上,常采用“加碳氯化”的方法以高钛渣(主要成分为TiO)为原料生产TiCl ,
2 4
相应的化学方程式为:
Ⅰ.TiO
2
(s)+2Cl
2
(g)⇌TiCl
4
(g)+O
2
(g) ΔH
Ⅰ
=181 kJ·mol-1,K
Ⅰ
=3.4×10-29
Ⅱ.2C(s)+O
2
(g)⇌2CO(g)
ΔH =-221 kJ·mol-1,K =1.2×1048
Ⅱ Ⅱ
结 合 数 据 说 明 氯 化 过 程 中 加 碳 的 理 由 :
_______________________________________________________________________________
_______________________________________________________________________________
__________________________________________________________。
(5)在一定温度下,以I 为催化剂,氯苯和Cl 在CS 中发生平行反应,分别生成邻二氯
2 2 2
苯和对二氯苯,两产物浓度之比与反应时间无关。反应物起始浓度均为 0.5 mol·L-1,反应
30 min测得氯苯15%转化为邻二氯苯,25%转化为对二氯苯。保持其他条件不变,若要提
高产物中邻二氯苯的比例,可采用的措施是________。
A.适当提高反应温度
B.改变催化剂
C.适当降低反应温度
D.改变反应物浓度