文档内容
专项训练 晶胞中的配位数选择题(解析版)
一、单选题
1.某物质W(摩尔质量为 )的晶胞结构如图所示。下列有关说法中正确的是
A.W的化学式为 B.熔融状态下W一定能导电
C.每个晶胞的质量为 D.X、Y配位数分别为2、4
【答案】C
【详解】A.由图知X位于顶点与面上,Y位于晶胞内,由均摊法可求出一个晶胞中
含有4个X、4个Y,化学式为 (或 ),选项A错误:
B.根据题中信息不能确定W是离子晶体,选项B错误:
C.晶胞中 ,故 ,选项C正确;
D.由晶胞图知,每个Y周围存在四个等距离且最近的X,即Y的配位数是4,故X
的配位数也是4,选项D错误;
答案选C。
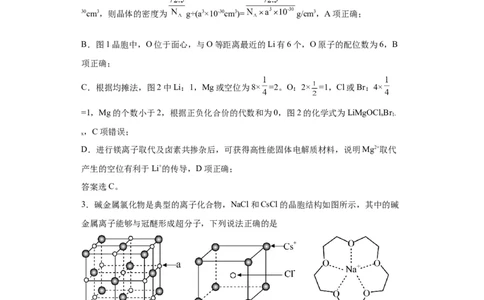
2.晶体结构的缺陷美与对称美同样受关注。某富锂超离子导体的晶胞是立方体(图
1),进行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料(图2)。下列说法
错误的是
A.图1晶体密度为 gcm-3 B.图1中O原子的配位数为6
∙
资料收集整理【淘宝店铺:向阳百分百】C.图2表示的化学式为 D. 取代产生的空位有利于 传导
【答案】C
【详解】A.根据均摊法,图1的晶胞中含Li:8× +1=3,O:2× =1,Cl:4×
=1,1个晶胞的质量为 g= g,晶胞的体积为(a×10-10cm)3=a3×10-
30cm3,则晶体的密度为 g÷(a3×10-30cm3)= g/cm3,A项正确;
B.图1晶胞中,O位于面心,与O等距离最近的Li有6个,O原子的配位数为6,B
项正确;
C.根据均摊法,图2中Li:1,Mg或空位为8× =2。O:2× =1,Cl或Br:4×
=1,Mg的个数小于2,根据正负化合价的代数和为0,图2的化学式为LiMgOCl Br
x 1-
,C项错误;
x
D.进行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料,说明Mg2+取代
产生的空位有利于Li+的传导,D项正确;
答案选C。
3.碱金属氯化物是典型的离子化合物,NaCl和CsCl的晶胞结构如图所示,其中的碱
金属离子能够与冠醚形成超分子,下列说法正确的是
A.NaCl晶体中a离子的配位数为12
B.每个CsCl晶胞中含有个1个CsCl分子
C.碱金属离子与冠醚通过离子键形成超分子
D.不同空穴尺寸的冠醚可识别不同的碱金属离子
【答案】D
资料收集整理【淘宝店铺:向阳百分百】【详解】A.钠离子的离子半径小于氯离子,因此氯化钠晶胞中a为离子半径较小的钠
离子,每个钠离子同时吸引6个氯离子,钠离子的配位数为6,A项错误;
B.每个CsCl晶胞中含有8个 和8个 ,因此每个CsCl晶胞中含有8个CsCl分
子,B项错误;
C.碱金属离子与冠醚通过配位键形成超分子,C项错误;
D.冠醚与金属阳离子通过配位作用相结合,不同大小的冠醚可以识别不同大小的碱
金属离子,D项正确;
答案选D。
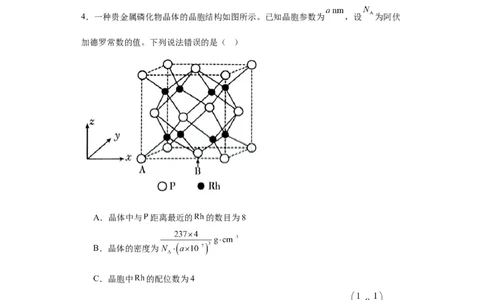
4.一种贵金属磷化物晶体的晶胞结构如图所示。已知晶胞参数为 ,设 为阿伏
加德罗常数的值。下列说法错误的是( )
A.晶体中与 距离最近的 的数目为8
B.晶体的密度为
C.晶胞中 的配位数为4
D.晶胞中,若 处原子分数坐标为 ,则 处原子分数坐标为
【答案】D
【详解】A.结合晶胞结构图,可知与 距离最近的 的数目为8,故A正确;
B.利用均摊法,可计算出晶胞中P原子个数 ,Rh原子个数8,可得化学
式Rh P,结合晶胞密度的计算公式,带入数据 ,故B正确;
2
资料收集整理【淘宝店铺:向阳百分百】C.晶胞中与Rh直接相连的P与、有4个,所以配位数为4,故C正确;
D.B原子位于底面的面心,所以坐标应为 ,故D错误;
答案选D。
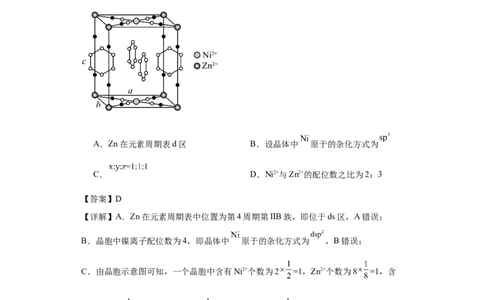
5.化学式为 的笼形包合物四方晶胞结构如图所示(H原子
未画出),晶胞中N原子均参与形成配位键,每个苯环只有一半属于该晶胞。晶胞参数
为a=b≠c, 则下列叙述正确的是
A.Zn在元素周期表d区 B.设晶体中 原于的杂化方式为
C. D.Ni2+与Zn2+的配位数之比为2:3
【答案】D
【详解】A.Zn在元素周期表中位置为第4周期第IIB族,即位于ds区,A错误;
B.晶胞中镍离子配位数为4,即晶体中 原于的杂化方式为 ,B错误;
C.由晶胞示意图可知,一个晶胞中含有Ni2+个数为2 =1,Zn2+个数为8 =1,含
有CN-为8 =4,NH 个数为8 =2,苯环个数为4 =2,则该晶胞的化学式为
3
,则x:y:z=4:2:2=2:1:1,C错误;
D.晶胞中每个N原子均参与形成配位键,Ni2+周围形成的配位键数目为4,Zn2+周围
形成的配位键数目为6,则Ni2+与Zn2+的配位数之比为4:6=2:3,D正确;
故选D。
6.Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻。能量密度大等优
良性能,得到广泛应用。下列有关锂化合物的说法中错误的是
资料收集整理【淘宝店铺:向阳百分百】A. 晶胞如图2所示。已知晶胞参数为0.4665nm,阿伏伽德罗常数的值为 ,
则 的密度为
B. 是离子晶体,其晶格能是
C. 晶胞中O的配位数是8
D. 中阴离子的空间结构是三角锥形
【答案】D
【详解】A. 晶胞如图2所示,则晶胞中有8个Li原子,氧原子个数为
,已知晶胞参数为0.4665nm,阿伏加德罗常数的值为 ,则 的密
度为 ,故A正确;
B. 含有锂离子和氧离子, 是离子晶体,晶格能是指气态离子形成1mol形体
释放的能量,晶格能用正号表示,因此 晶格能是 ,故B正确;
C.以右侧面面心的氧离子分析,与O离子结合的有8个锂离子,因此 晶胞中O
的配位数是8,故C正确;
D. 中阴离子价层电子对数为 ,其空间结构是正四
面体形,故D错误。
资料收集整理【淘宝店铺:向阳百分百】综上所述,答案为D。
7. 晶体是制备氟代硼铍酸钾晶体的原料之一,其晶胞结构与 类似,下列说法
中不正确的是
A.Be原子的配位数是12
B.若原子a、b的坐标分别为 、 ,则原子c的坐标为
C.沿晶胞面对角线投影,所得的投影结果是
D.设O与Be的最近距离为 ,用 表示阿伏加德罗常数的值,则 晶体的
密度为
【答案】A
【详解】A.由晶胞结构可知Be位于O原子构成的四面体的体心,Be原子的配位数是
4,A错误;
B.由 的晶胞结构可知,每个Be处于晶胞体对角线的 处,结合原子a、b的坐
标可知原子c的坐标为 ,B正确;
C.沿面对角线进行投影,可知所得的投影结果是 ,C正确;
D.若O与Be的最近距离为 ,则题中a、c之间的距离为 ,又因为a、c之间
资料收集整理【淘宝店铺:向阳百分百】的距离为晶胞体对角线长的 ,则晶胞体对角线长为 ,故晶胞棱长为 ,
晶胞内Be的个数为4,O的个数为 ,则根据晶胞质量=晶胞密度×晶胞体
积可得,晶胞密度为 ,D正确;
故选:A。
8.纳米 可催化 的分解,其晶胞结构如图所示。关于 的说法正确的是
A. 的配位数是4
B. 与 间最短距离为
C.若A离子的坐标为 ,则B原子的坐标为
D.若晶体密度为 ,则晶胞参数
【答案】C
【详解】A.根据晶胞图可知,Ce4+的配位数为8,故A错误;
B.把晶胞平均分成8个小立方体,O2-位于小立方体的中心,即Ce4+与O2-最短距离是
体对角线的 ,最短距离是 nm,故B错误;
C.若A的坐标为(0, , ),A点位于面心,根据B选项分析,则B的坐标为( ,
资料收集整理【淘宝店铺:向阳百分百】, ),故C正确;
D.Ce4+位于顶点和面心,个数为 =4,O2-位于晶胞内部,个数为8,化学式
为CeO,则晶胞的质量为 g,根据密度的定义,晶胞的参数为
2
nm= nm,故D错误;
答案为C。
9.钡在氧气中燃烧时得到一种钡的氧化物晶体,其晶胞的结构如图所示,下列说法中
正确的是
A.该晶体中只含有离子键属于离子晶体
B.Ba2+的配位数与O 的配位数之比为1:1
C.晶体的化学式为Ba O
2 2
D.该晶体的晶胞结构与CsCl相似
【答案】B
【详解】A.根据晶胞图可知,该化合物是由阴阳离子组成,即该化合物为离子晶体,
Ba2+与O 之间存在离子键,两个氧原子之间存在共价键,故A错误;
B.根据晶胞图可知,与Ba2+等距离且最近的O 有6个,同理与O 等距离最近的
Ba2+有6个,因此两个配位数之比为1∶1,故B正确;
C.Ba2+位于顶点和面心,个数为 =4,O 位于棱上和体心,个数为
资料收集整理【淘宝店铺:向阳百分百】=4,化学式为BaO,故C错误;
2
D.BaO 与NaCl的晶胞图相似,CsCl的晶胞图 ,该晶胞图与CsCl不相似,
2
故D错误;
答案为B。
10.几种晶体的晶胞结构如图所示。已知: 、 均为立方晶胞。下列说法错
误的是
A.相同条件下,熔点:
B.另一种 晶胞结构中,当 处于体心时,则 处于棱心
C. 晶胞中a点原子坐标参数为 ,则b点原子坐标参数为
D.三种晶体中,Ca的配位数均为8
【答案】D
【详解】A. 半径小于 , 的离子键强于 的, 熔点更高,A项正确;
B.另一种 晶胞结构中,当 处于体心时, 处于顶角、O处于棱心,B项正
确;
C.由 晶胞结构及a点原子坐标参数为 ,可知 点原子坐标参数为,
,C项正确;
资料收集整理【淘宝店铺:向阳百分百】D. 中 的配位数为12,D项错误;
故答案为:D。
11.某卤化物可用于制作激光基质材料,其立方晶胞结构如图所示,已知:晶胞参数
为 , 为阿伏加德罗常数的值。下列有关该晶体的说法正确的是
A.化学式为 B.K的配位数为6
C.若K位于晶胞的体心,则F位于面心D.密度为
【答案】A
【详解】A. 晶胞中,钾原子位于顶点,个数为 ,镁原子位于体心,个
数为1,氟原子位于面心,个数为 ,则晶胞中K、Mg、F的原子个数比为
1:1:3,化学式为 ,A项正确;
B.与K等距且最近的F位于面心,共有12个,所以K的配位数为12,B项错误;
C.晶体中若K位于晶胞的体心,则F位于棱心,Mg位于顶点,C项错误;
D.该晶体的密度 ,D项错误;
故选A。
12.氧化锌(ZnO)的透明度高,具有优异的常温发光性能。氧化锌的两种晶胞结构如图
所示。下列说法错误的是
资料收集整理【淘宝店铺:向阳百分百】A.甲、乙两种晶体类型的晶胞内 数目之比为2∶1
B.甲中 位于 形成的四面体空隙中,空隙填充率为50%
C.乙的晶胞沿z轴的二维投影图如图丙所示
D.两种晶胞中 的配位数均为4
【答案】C
【详解】A.甲类型的晶胞中有4个Zn2+位于晶胞内,则甲晶胞有4个Zn2+;乙晶胞有
4个Zn2+位于晶胞棱上,1个Zn2+位于晶胞内,则乙晶胞共 个Zn2+,甲、乙
两种晶体类型的晶胞内Zn2+数目之比为2 : 1,故A正确;
B.甲晶胞中O2-形成8个空隙,Zn2+占据4个空隙,则空隙填充率为50%,故B正确;
C.乙的晶胞沿z轴的二维投影图如图 ,故C错误;
D.O2-的配位数即为晶胞中距离O2-最近的离子个数,观察甲乙两晶胞,可知距离O2-
最近的离子个数均为4个Zn2+,则两种晶胞中O2-的配位数均为4,故D正确;
故选C。
13.具有光催化活性的TiO 可通过氮掺杂生成TiO N 后,在光照下的输出稳定性更
2 2-a b
好,其晶胞结构如图,已知原子1、原子2的分数坐标为(0,0, )和(1,0,0),设阿
伏加德罗常数的值为N ,下列说法正确的是
A
A.氮掺杂生成的TiO N 中,a= ,b=
2-a b
B.原子3的分数坐标为(1,0, )
C.TiO 晶体中,Ti的配位数为8
2
资料收集整理【淘宝店铺:向阳百分百】D.TiO 的密度为 g·cm-3
2
【答案】A
【详解】A.由TiO N 晶体结构可知,氮掺杂反应后有3个氧空穴,O原子6个在棱
2-a b
上、6个在后面,1个在体内,O原子个数为 ,N原子1个在棱上、
1个在面,N原子个数为 ,Ti原子8个在顶点、4个在面心,1个在体内,
Ti原子个数为 , , ,
,A正确;
B.原子1、2的坐标分别为 ,由TiO2的晶胞结构可知,原子3的坐
标为 ,B错误;
C.钛离子形成体心四方点阵,氧离子形成八面体,八面体嵌入体心四方点阵中,每个
钛离子周围有6个氧离子,Ti的配位数为8,C错误;
D. Ti原子在晶胞的8个顶点、4个面心和1个在体内,Ti原子的个数为
,O原子在8个棱上、8个面上,2个在体内,O原子个数为
,则1mol晶胞的质量 ,一个晶胞的质量为
,体积为 ,则TiO2的密度为
,D错误;
故答案为:A。
资料收集整理【淘宝店铺:向阳百分百】14.锑---钾合金可用作钾离子电池的电极材料,图a为其晶胞结构,图b为晶胞的一
部分,下列有关说法正确的是
A.晶胞密度为 g·cm-3
B.Sb原子的配位数为6
C.最邻近的Sb原子构成的最小空间结构为正四面体
D.从电子排布推断,K的第一电离能比Sb大
【答案】C
【详解】A.根据“均摊法”,晶胞中含 个Sb、 个K,则
晶体密度为 ,A错误;
B.以底面Sb原子为例,距其等距且最近的K原子上下层各有4个,故配位数为8,B
错误;
C.由图b可知,最邻近的Sb原子构成的最小空间结构为正四面体,C正确;
D.同一周期随着原子序数变大,第一电离能变大,K的第一电离能比Sb小,D错误;
故选C。
15.硒化锌是一种重要的半导体材料;其晶胞结构如图甲所示,已知晶胞参数为p
nm,图乙为晶胞的俯视图,下列说法正确的是
资料收集整理【淘宝店铺:向阳百分百】A.晶胞中硒原子的配位数为8
B.晶胞中d点原子分数坐标为( , , )
C.Zn位于元素周期表的d区
D.Zn和Se的最短距离为 p nm
【答案】D
【详解】A.该晶胞中Zn原子位于Se围成的正四面体空隙内,Zn原子的配位数是4,
Se原子位于顶点和面心,个数为:4,Zn原子位于体内个数为:4,则该晶胞对应的化
学式为ZnSe,晶胞中Se原子的配位数也是4,A错误;
B.该晶胞中a点坐标为(0,0,0),a原子位于坐标原点,由图乙可知d原子在坐标轴
正方向空间内,且到x轴、y轴、z轴的距离分别为 、 、 ,即d原子的坐标为( ,
, ),B错误;
C.Zn为30号元素位于ds区,C错误;
D.Zn、Se的最短距离为体对角线的 ,即为 p nm ,D正确;
故选:D。
16.铁是应用最广泛的金属,在不同条件下能形成不同的晶体结构,分别称为α-
Fe,γ-Fe,δ-Fe,其晶胞如图所示,下列说法错误的是
A.晶胞参数最长的是δ-Fe B.密度最小的是α-Fe
C.铁原子配位数最大的是,γ-Fe D.上述三种铁之间的转化是化学变化
【答案】A
【详解】A.根据图示,晶胞参数最长的为γ-Fe,因其晶胞面心有Fe,A错误;
B.根据均摊法可知,γ-Fe中Fe个数, ;δ-Fe中Fe个数,
;α-Fe中Fe个数, ,三者晶胞参数相差不大,则体积相差不大,
资料收集整理【淘宝店铺:向阳百分百】晶胞中所含Fe原子个数越少,晶胞密度越小,则α-Fe晶胞密度最小,B正确;
C.α-Fe的配位数6,γ-Fe的配位数为12,δ-Fe的配位数为8,C正确;
D.因为三者的结构不同,故三种铁之间的转化为化学变化,D正确;
故答案为:A。
17.几种离子晶体的晶胞如图所示,则下列说法错误的是
A.在 晶胞中距离 最近且等距的 在空间构成的几何构型为正八面体
B.在 晶胞中,距离 最近且等距的 数目为8
C.上述三种晶胞中,其阳离子的配位数大小关系为
D.若 的晶胞边长为 ,则 与 之间最近距离为
【答案】C
【详解】A.NaCl晶体种,Na+周围距离最近的Cl-有6个,构成正八面体,A正确;
B.在CsCl晶体中,Cs+为体心,距离 Cs+ 最近且等距的 Cl−数目为8,B正确;
C.由图可知,在NaCl晶胞中,钠离子的配位数为6,在CsCl晶胞中,铯离子的配位
数为8,在ZnS晶胞中,Zn2+的配位数为4,所以阳离子的配位数为ZnS<NaCl<
CsCl,C错误;
D.由图可知,Zn2+与S2-之间的最近距离为体对角线的 ,若ZnS的晶胞边长为apm,
则体对角线为 ,所以Zn2+与S2-之间的最近距离为 ,D正确;
故答案为:C。
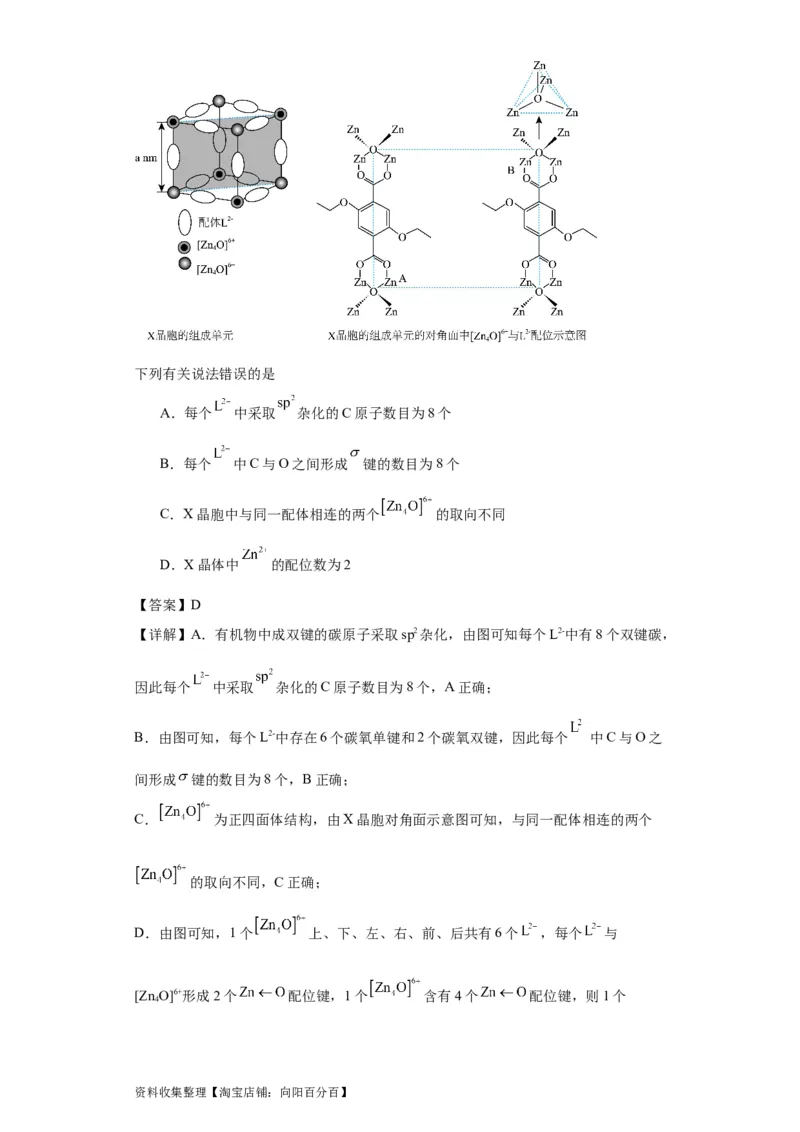
18.配位化合物X由配体 和具有正四面体结构的 组成。化合物X晶体具有
面心立方结构,其晶胞由8个结构相似的组成单元(如图)构成。
资料收集整理【淘宝店铺:向阳百分百】下列有关说法错误的是
A.每个 中采取 杂化的C原子数目为8个
B.每个 中C与O之间形成 键的数目为8个
C.X晶胞中与同一配体相连的两个 的取向不同
D.X晶体中 的配位数为2
【答案】D
【详解】A.有机物中成双键的碳原子采取sp2杂化,由图可知每个L2-中有8个双键碳,
因此每个 中采取 杂化的C原子数目为8个,A正确;
B.由图可知,每个L2-中存在6个碳氧单键和2个碳氧双键,因此每个 中C与O之
间形成 键的数目为8个,B正确;
C. 为正四面体结构,由X晶胞对角面示意图可知,与同一配体相连的两个
的取向不同,C正确;
D.由图可知,1个 上、下、左、右、前、后共有6个 ,每个 与
[Zn O]6+形成2个 配位键,1个 含有4个 配位键,则1个
4
资料收集整理【淘宝店铺:向阳百分百】中 形成的配位键数目为 ,1个 的配位数为4,D正确;
故选D。
19.已知γ-AgI晶体属立方晶系,其晶胞截面如图所示(晶胞参数为620pm,设阿伏伽
德罗常数的值为N ),则下列关于γ-AgI晶胞的描述错误的是
A
A. 与 的配位数均为4
B.与 距离最近且相等的 有12个
C. 填充在 构成的四面体空隙中,其空隙填充率为50%
D.该晶体的摩尔体积
【答案】D
【分析】由晶胞截面图可知,晶胞中碘离子位于顶点和面心,则碘离子个数为8×
+6× =4,碘离子构成8个四面体,银离子交替填充在碘离子构成的四面体的体心,则
位于体内的银离子个数为4。
【详解】A.由分析可知,银离子交替填充在碘离子构成的四面体的体心,则银离子
的配位数为4,由化学式可知,碘离子的配位数也为4,故A正确;
B.由分析可知,银离子交替填充在碘离子构成的四面体的体心,则与银离子距离最近
且相等的银离子有12个,故B正确;
C.由分析可知,碘离子构成8个四面体,银离子交替填充在碘离子构成的四面体的体
心,则空隙填充率为 ×100%=50%,故C正确;
D.由晶胞参数可知,晶体的摩尔体积V = = m3/mol,
m
故D错误;
故选D。
资料收集整理【淘宝店铺:向阳百分百】20.某立方卤化物可用于制作光电材料,其晶胞结构如图所示。下列说法正确的是
A.Ca2+的配位数为14 B.与F-距离最近的是K+
C.该物质的化学式为KCaF D.若F-换为Cl-,则晶胞棱长不变
3
【答案】C
【详解】A.从图中可以看出,中心Ca2+与距离最近的6个F-构成正八面体结构,则
Ca2+的配位数为6,A不正确;
B.与F-距离最近的K+距离为棱长的 倍,与F-距离最近的Ca2+距离为棱长的 ,则
与F-距离最近的是Ca2+,B不正确;
C.晶胞中,含有K+数目为 =1,含有F-数目为 =3,含有Ca2+数目为1,则该物
质的化学式为KCaF ,C正确;
3
D.若F-换为Cl-,由于Cl-半径大于F-半径,则晶胞棱长将发生改变,D不正确;
故选C。
资料收集整理【淘宝店铺:向阳百分百】